文档内容
微考点 8 氧化还原反应的概念和规律、应用
题点(一)基本概念与实质
1.(2022·北京卷)下列物质混合后,因发生氧化还原反应使溶液 减小的是( )
A.向 溶液中加入少量 溶液,生成白色沉淀
B.向 和 的悬浊液中通入空气,生成红褐色沉淀
C.向 溶液中加入少量 溶液,生成蓝绿色沉淀
D.向 溶液中通入氯气,生成黄色沉淀
1.D A.向NaHSO 中加入少量BaCl 溶液,实际参与反应的只有硫酸根离子和钡离子,忽略体积变化,
4 2
H+的浓度不变,其pH不变,A错误;B.向 NaOH 和 Fe(OH) 的悬浊液中通入空气,虽然有氢氧化亚铁被
2
氧化成了红褐色的氢氧化铁,其方程式为 ,该过和中会消耗水,则增大
了氢氧根离子的浓度,pH会变大,B错误;C.向 NaHCO 溶液中加入少量 CuSO 溶液,生成蓝绿色沉淀
3 4
[Cu (OH) CO ],其中没有元素的化合价发生变化,故没有氧化还原反应,C错误;D.向H S中通入氯气生
2 2 3 2
成HCl和单质硫沉淀,这个氧化还原反应增大了H+的浓度,pH减小,D正确。故选D。
2.(2021· 天津卷)关于反应 所涉及的物质,下列说法错误的是(
)
A. H SO 在该反应中为氧化剂 B. Na SO 容易被空气中的O 氧化变质
2 4 2 3 2
C. Na SO 是含有共价键的离子化合物 D. SO 是导致酸雨的主要有害污染物
2 4 2
2.A A. 中无化合价的变化,不属于氧化还原反应,所以该反应中
无氧化剂,故A错误;B.Na SO 不稳定,容易被空气中的O 氧化成硫酸钠变质,故B正确;C.Na SO 含
2 3 2 2 4
有阴阳离子,存在离子键,硫酸根中含有共价键,故C正确;
D.SO 在空去中会转化成硫酸,形成酸雨,所以二氧化硫是导致酸雨的主要有害污染物,故D正确;故选
2
A。3.(2021·江苏卷)黑火药是中国古代四大发明之一,其爆炸反应为2KNO +S+3C=K S+N ↑+3CO ↑。下列
3 2 2 2
说法正确的是()
A.黑火药中含有两种单质 B.爆炸时吸收热量
C.反应中S作还原剂 D.反应为置换反应
3.A A.黑火药中含有S、C两种单质,A正确;B.爆炸反应为放热反应,B错误;
C.该反应中S元素化合价降低,作氧化剂,C错误;D.该反应不符合“单质+化合物=另一种单质+另一种
化合物”的形式,不是置换反应,D错误;综上所述答案为A。
4.(2022·洛阳市第一高级中学高三检测)下列叙述不涉及氧化还原反应的是( )
A.使用酸性重铬酸钾溶液检验是否酒驾
B.葡萄糖被人体吸收利用提供能量
C.锻打铁制品时将红热的铁制品投入水中淬火
D.明矾作净水剂处理饮用水
4.D A.酸性重铬酸钾溶液具有强氧化性,能和乙醇发生氧化还原反应,使用酸性重铬酸钾溶液检验是
否酒驾涉及氧化还原反应,A错误;B.葡萄糖在人体内被氧化生成二氧化碳和水释放出能量,涉及氧化还
原反应,B错误;C.红热的铁和水生成氢气和四氧化三铁,涉及氧化还原反应,C错误;D.明矾作净水
剂处理饮用水是因为铝离子水解生成氢氧化铝吸附杂质,没有涉及氧化还原反应,D正确;故选D。
5.(2022·浙江·马寅初中学高三阶段练习)“氯酸钾氧化法”制备KIO 第一步反应为:6I +11KClO +3H O
3 2 3 2
6KH(IO ) +5KCl+3Cl ↑。下列关于该反应说法正确的是( )
3 2 2
A.I 发生还原反应
2
B.KClO 既是氧化剂又是还原剂
3
C.氧化产物与还原产物的物质的量之比为2:1
D.生成22.4L(标准状况)Cl 时,反应转移20mole-
2
5. D A.I 中I化合价升高,失去电子,发生氧化反应,故A错误;B.KClO 中Cl化合价降低,因此
2 3
KClO 作氧化剂,故B错误;C.反应中KH(IO ) 为氧化产物,KCl、Cl 为还原产物,因此氧化产物与还原产
3 3 2 2
物的物质的量之比为6:8=3:4,故C错误;D.根据反应方程式分析,转移60mol电子,生成3mol氯气,因
此生成22.4LCl (标准状况物质的量为1mol)时,反应转移20mole-,故D正确。综上所述,答案为D。
2
6.(双选)(2022·枣庄市第三中学高三开学考试)次磷酸 与足量的氢氧化钠溶液反应生成溶液, 可以用于镀铜,发生反应的离子方程式为
。下列说法正确的是( )
A. 中P元素的化合价为 价 B. 属于正盐
C.还原性: D.若反应生成1molCu,转移
6. BC A.利用元素化合价代数和为0,计算H PO 中P元素的化合价为+1价,故A错误;
3 2
B.次磷酸与足量的氢氧化钠溶液反应生成NaH PO 溶液,因此NaH PO 属于正盐,故B正确;C.还原剂
2 2 2 2
H PO -的还原性强于还原产物Cu的还原性,故C正确;D.依据Cu由+2价降低为0价,若反应生成
2 2
1molCu,转移2mole-,故D错误;答案选BC。
题点(二)基本规律及应用
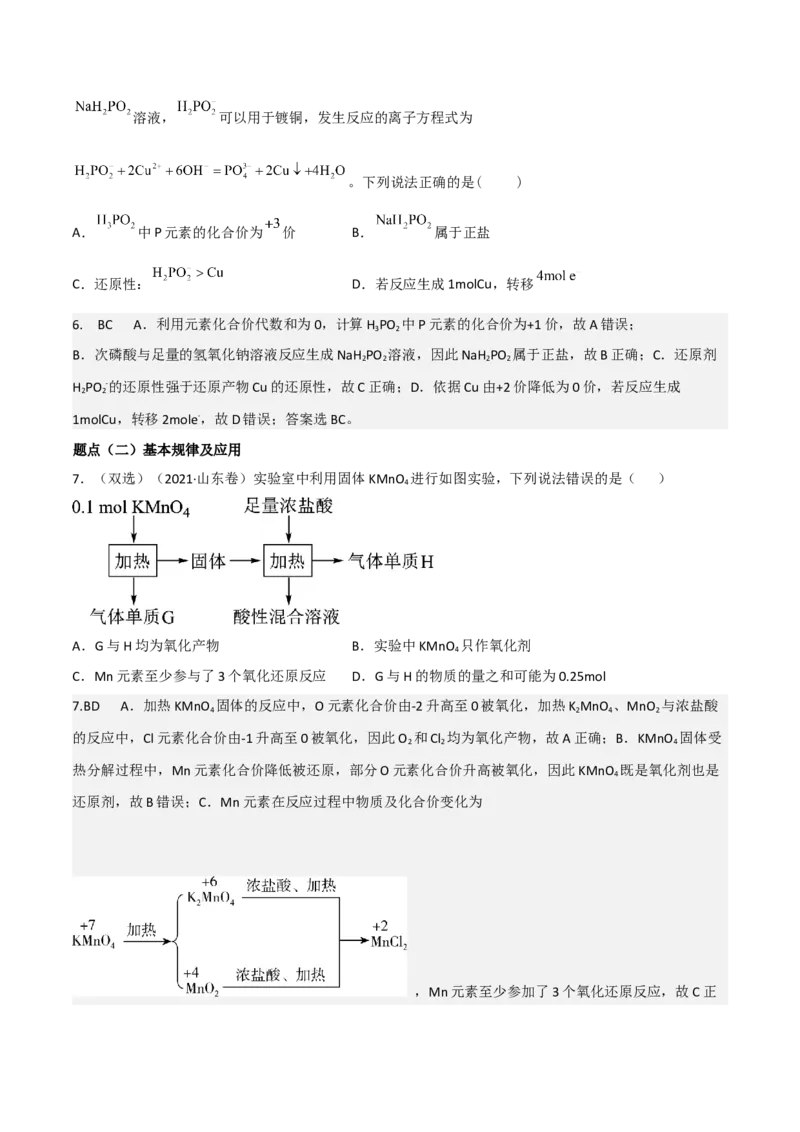
7.(双选)(2021·山东卷)实验室中利用固体KMnO 进行如图实验,下列说法错误的是( )
4
A.G与H均为氧化产物 B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为0.25mol
7.BD A.加热KMnO 固体的反应中,O元素化合价由-2升高至0被氧化,加热K MnO 、MnO 与浓盐酸
4 2 4 2
的反应中,Cl元素化合价由-1升高至0被氧化,因此O 和Cl 均为氧化产物,故A正确;B.KMnO 固体受
2 2 4
热分解过程中,Mn元素化合价降低被还原,部分O元素化合价升高被氧化,因此KMnO 既是氧化剂也是
4
还原剂,故B错误;C.Mn元素在反应过程中物质及化合价变化为
,Mn元素至少参加了3个氧化还原反应,故C正确;D.每生成1mol O 转移4mol电子,每生成1mol Cl 转移2mol电子,若KMnO 转化为MnCl 过程中得
2 2 4 2
到的电子全部是Cl-生成Cl 所失去的,则气体的物质的量最大,由2KMnO ~5Cl 可知,n(气
2 4 2
体) =0.25mol,但该气体中一定含有O ,因此最终所得气体的物质的量小于0.25mol,故D错误;综上所
max 2
述,说法错误的是BD,故答案为:BD。
8.(2021·吉林松原高三期中)已知四种物质的氧化能力W >Z >X >Y ,下列说法不正确的是()
2 2 2 2
A.还原性:Y->Z->W-
B.2NaW + Y =2NaY + W 可以发生
2 2
C.Z 与X-在水溶液中不能大量共存
2
D.W 通入NaX和NaY的混合溶液中:W 先氧化Y-
2 2
8. B A.因为氧化能力是W >Z >X >Y ,所以还原性:Y->Z->W-,故A正确;
2 2 2 2
B.因为氧化性W >Y ,所以Y 不能置换出W ,即反应2NaW+Y =2NaY+W 不能发生,故B错误;C.因为
2 2 2 2 2 2
Z >X ,所以Z 能置换出X ,则Z 与X-在水溶液中不能大量共存,故C正确;D.因为氧化能力是W >Z
2 2 2 2 2 2 2
>X >Y ,所以还原性:Y->X->Z->W-,则W 通入到NaX和NaY的混合溶液中:W 优先氧化Y-,故D
2 2 2 2
正确;故选B。
9.(2022·江西金溪一中高三阶段练习)实验室中为研究不同物质之间的反应进行如图实验。下列说法正
确的是( )
A.丙为还原产物,丁为氧化产物
B.每生成标准状况下5.6L气体丙,消耗0.2molKMnO
4
C.上述有4个氧化还原反应
D.若0.1molNaSO 完全反应,转移0.15mol电子
2 3
9.D A.在KMnO(H+)溶液与双氧水反应中,HO 是还原剂,则丙(O)为氧化产物,丁(S)为HS(还原剂)与
4 2 2 2 2
O 反应的产物,是氧化产物,D不正确;B.KMnO(H+)溶液与双氧水混合反应,可建立如下有关系式:
2 4
2KMnO——5O,则每生成标准状况下5.6L(0.25mol)气体丙(O),消耗0.1molKMnO,B不正确;C.由分析
4 2 2 4
可知,上述发生的4个反应中,有3个属于氧化还原反应,C不正确;D.由反应可得出如下关系式:
4NaSO——6e-,若0.1molNaSO 完全反应,转移 =0.15mol电子,D正确;故选D。
2 3 2 310.(2022·广东模拟预测)实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中含有
和白色物质X,下列说法正确的是( )
A.X溶液显无色 B.NO和Y均为还原产物
C.浓硫酸在反应中表现出氧化性和酸性 D.NO与Y的物质的量之和可能为2mol
10.C A.据分析,白色物质X为CuSO ,溶液为蓝色,故A错误;B.Cu S和白色物质CuSO 加稀硫酸和稀
4 2 4
硝酸时溶解,存在反应:3Cu S+16H++4NO =6Cu2++3S↓+4NO↑+8H O,Y为S单质,则NO为还原产物、Y
2 2
为氧化产物,故B错误;C.由5Cu+4H SO (浓) 3CuSO +Cu S+4H O可知,硫元素从+6价降低到-2价时
2 4 4 2 2
表现氧化性,有硫酸铜生成表现出酸性,故C正确;
D.由5Cu+4H SO (浓) 3CuSO +Cu S+4H O知,3molCu生成0.6molCu S,0.6molCu S发生反应
2 4 4 2 2 2 2
3Cu S+16H++4NO =6Cu2++3S↓+4NO↑+8H O得到0.8mol NO与0.6mol S,NO与S物质的量之和为1.4mol,
2 2
故D错误;故选C。