文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷01
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.下列“一带一路”特色贸易商品中,主要有机成分不属于糖类的是
A.吉尔吉斯坦蜂蜜 B.内蒙古羊绒 C.新疆棉花 D.俄罗斯大列巴
2.2023年10月24日,新修订的海洋保护法获得通过。以下过程未涉及氧化还原反应的是
A.量子点技术应用于深海探测与光学传感 B.高铁酸钠(NaFeO)处理水
2 4
C.利用风电技术对海水进行原位电解制氢 D.热空气吹出法从海水中提溴
3.下列有关 和 的性质,叙述错误的是
A.鉴别等物质的量浓度的 溶液和 溶液可以用盐酸
B.向等体积等物质的量浓度两种溶液中分别滴加等量酚酞溶液, 溶液红色较深
C.小苏打是发酵粉的主要成分之一
D.除去 溶液并混有的少量 ,用加热法
4.下列有关物质的性质与用途不相对应的是选
性质 用途
项
A 二氧化硅硬度大,耐腐蚀 作光导纤维
B 液氨汽化时要吸收大量的热 作制冷剂
C 氧化钙能与水反应 作干燥剂
D 二氧化硫具有还原性 作抗氧化剂
5.下列关系错误的是
A.沸点:CO>N B.第一电离能:Si<P<S
2
C.在水中的溶解度:SO >CO D.还原性:稀盐酸<浓盐酸
2 2
6.四氯化碳是常用的不燃溶剂,由如下反应制备: 。下列说法正确的是
A.CS 的熔沸点比CO 的低 B.CCl 的热稳定性比CF 的高
2 2 4 4
C.该制备反应是熵增过程 D.CS 的键角大于CCl 的键角
2 4
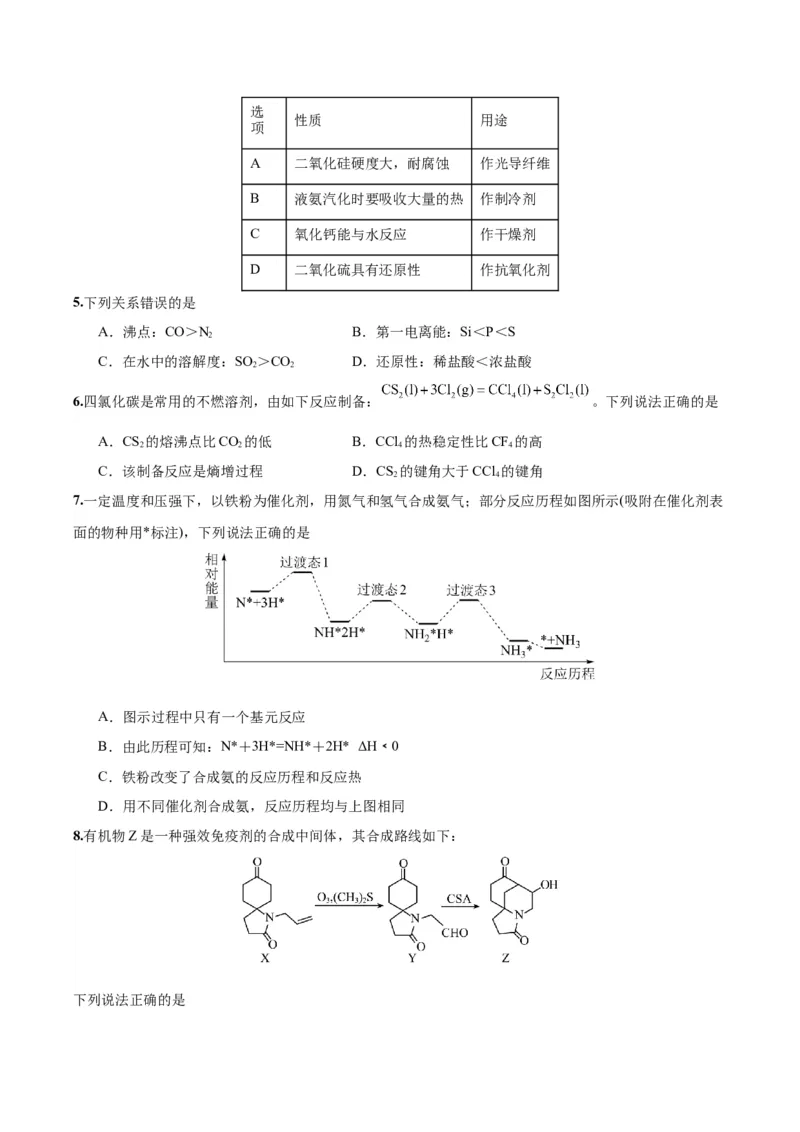
7.一定温度和压强下,以铁粉为催化剂,用氮气和氢气合成氨气;部分反应历程如图所示(吸附在催化剂表
面的物种用*标注),下列说法正确的是
A.图示过程中只有一个基元反应
B.由此历程可知:N*+3H*=NH*+2H* ΔH﹤0
C.铁粉改变了合成氨的反应历程和反应热
D.用不同催化剂合成氨,反应历程均与上图相同
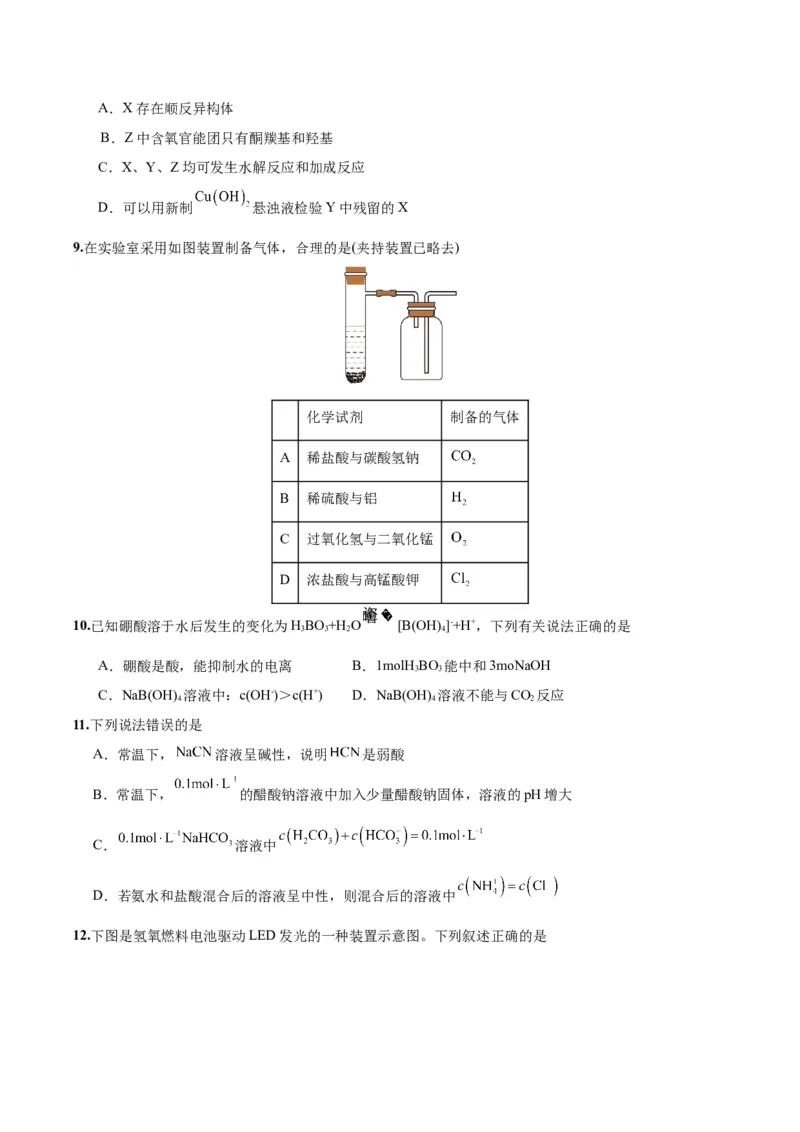
8.有机物Z是一种强效免疫剂的合成中间体,其合成路线如下:
下列说法正确的是A.X存在顺反异构体
B.Z中含氧官能团只有酮羰基和羟基
C.X、Y、Z均可发生水解反应和加成反应
D.可以用新制 悬浊液检验Y中残留的X
9.在实验室采用如图装置制备气体,合理的是(夹持装置已略去)
化学试剂 制备的气体
A 稀盐酸与碳酸氢钠
B 稀硫酸与铝
C 过氧化氢与二氧化锰
D 浓盐酸与高锰酸钾
10.已知硼酸溶于水后发生的变化为HBO+H O [B(OH) ]-+H+,下列有关说法正确的是
3 3 2 4
A.硼酸是酸,能抑制水的电离 B.1molH BO 能中和3moNaOH
3 3
C.NaB(OH) 溶液中:c(OH-)>c(H+) D.NaB(OH) 溶液不能与CO 反应
4 4 2
11.下列说法错误的是
A.常温下, 溶液呈碱性,说明 是弱酸
B.常温下, 的醋酸钠溶液中加入少量醋酸钠固体,溶液的pH增大
C. 溶液中
D.若氨水和盐酸混合后的溶液呈中性,则混合后的溶液中
12.下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列叙述正确的是A.装置最终实现化学能转化为电能 B.电解质溶液pH变大
C.导线中每通过1mole-,需要消耗11.2 LO (标况) D.b为正极
2
二、非选择题:本题共4小题,共64分。
13.(15分)氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。回答下
列问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为 。
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,
它可通过环硼氮烷、 与 进行合成。
① 中涉及的元素H、B、N电负性最大的是 。
②键角: (填“>”、“<”或“=”),原因是 。
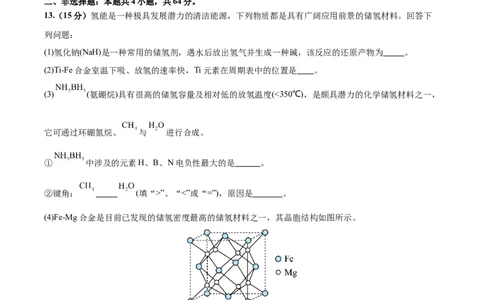
(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
①距离Mg原子最近的Fe原子个数是 。
②若该晶胞的棱长为anm,阿伏加德罗常数的值为 ,则该合金的密度为 。
③若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的
体积约为 L。
14.(18分)A为重要的有机化工原料,B分子的核磁共振氢谱图中只有一个吸收峰,下列是合成防火材料聚碳酸酯(PC)和有广泛用途的内酯 的路线:
已知:i: ( 、 为氢原子或烃基)
ii: (R、 、 代表烃基)
请回答下列问题:
(1)A的名称为 。
(2)反应①的反应类型为 。
(3)C分子含有的官能团是 。
(4)化合物甲的分子式为 。
(5)反应④的方程式为 。
(6)E分子内含有六元环,可发生水解反应,其结构简式是 。
(7)X是 的同分异构体,符合下列条件的 的结构简式是 。
① 能与足量银氨溶液生成 ;
② 中核磁共振氢谱中出现3组吸收峰,峰面积比为 。
(8)以物质B为原料选用必要的无机试剂经过以下3步反应合成 。
B CHOCH CH(CH )
3 2 3 2
写出中间产物1和中间产物2的结构简式:中间产物1 、中间产物2 。
15.(14分)某同学制备HSO ,再用HSO 制备C H,并检验产物。
2 4 2 4 2 4
I.制备HSO 的重要一步是制SO
2 4 3
(1)某同学在实验室中根据2SO (g)+O(g) 2SO (g),设计如图1所示实验装置来制备SO 固体。
2 2 3 3①在A装置中加入NaSO 固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是 。
2 3
②装置D盛放的是 溶液,其作用是 。
③实验开始时的操作顺序为 。
a.先点燃E处的酒精灯后将混合气体通入E
b.先将混合气体通入E后点燃E处的酒精灯
II.制取乙烯
图2是实验室制乙烯的发生装置,根据图示回答下列问题:
(2)图2中仪器①、②的名称分别为 。
(3)反应前在②中放入几块碎瓷片的目的是 。
III.检验产物
(4)为检验上述实验收集到的产物,该小组同学进行了如表实验并得出相应结论。
实验序号 检验试剂和反应条件 现象 结论
① 酸性KMnO 溶液 紫红色褪去 产物含有乙烯
4
② 澄清Ca(OH) 溶液. 变浑浊 产物含有CO
2 2
③ 通过品红溶液 红色褪去 产物含有SO
2
实验①~③中的结论不合理的是 (填序号),原因是 。
16.(17分)我国科学家在“碳中和”项目上进行了如图相关深入研究,并取得一定效果。请回答下列问
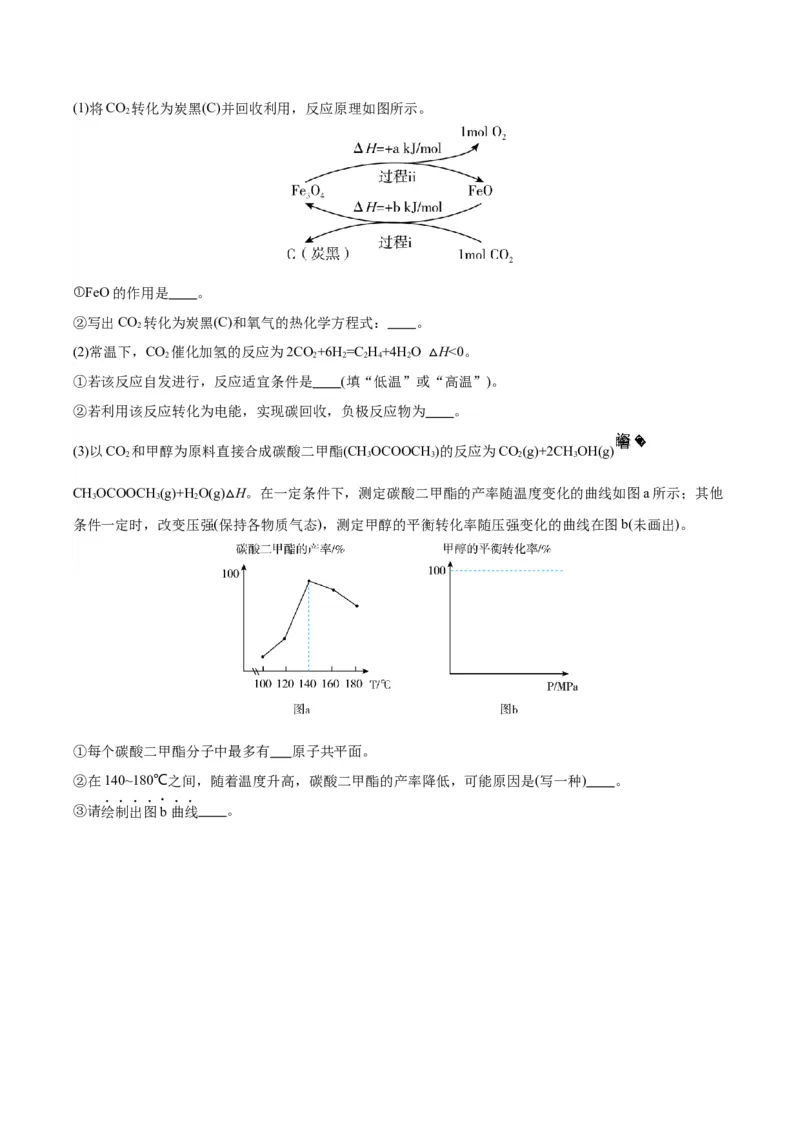
题:(1)将CO 转化为炭黑(C)并回收利用,反应原理如图所示。
2
①FeO的作用是 。
②写出CO 转化为炭黑(C)和氧气的热化学方程式: 。
2
(2)常温下,CO 催化加氢的反应为2CO+6H =C H+4H O H<0。
2 2 2 2 4 2
①若该反应自发进行,反应适宜条件是 (填“低温”或△“高温”)。
②若利用该反应转化为电能,实现碳回收,负极反应物为 。
(3)以CO 和甲醇为原料直接合成碳酸二甲酯(CHOCOOCH )的反应为CO(g)+2CH OH(g)
2 3 3 2 3
CHOCOOCH (g)+HO(g) H。在一定条件下,测定碳酸二甲酯的产率随温度变化的曲线如图a所示;其他
3 3 2
条件一定时,改变压强(保△持各物质气态),测定甲醇的平衡转化率随压强变化的曲线在图b(未画出)。
①每个碳酸二甲酯分子中最多有 原子共平面。
②在140~180℃之间,随着温度升高,碳酸二甲酯的产率降低,可能原因是(写一种) 。
③请绘制出图b曲线 。