文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷04(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 Cl-35.5 O-16 Si-28 Ca-40
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.2023年第19届杭州亚运会上出现了很多新材料,其中用到天然有机高分子材料的是
A.竞赛自行车整体车架采用高模量碳纤维
B.运动员房间的漱口杯、衣架采用麦秸秆材质
C.白色棚罩“云之翼”的顶部覆盖了带二氧化钛涂层的PTFE(聚四氟乙烯)膜
D.亚运火炬“薪火”的金属部分采用1070铝合金旋压成型
2.过氧化钠常用作供氧剂: 。下列说法正确的是
A. 为非极性分子 B. 的电子式:
C. 与 互为同素异形体 D.NaOH属于离子化合物,不含有共价键
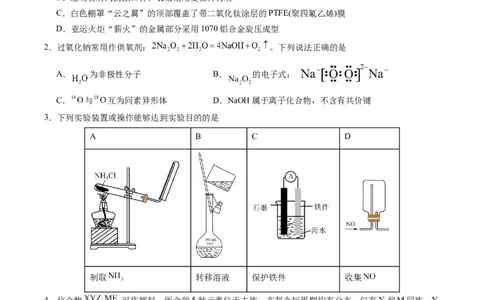
3.下列实验装置或操作能够达到实验目的的是
A B C D
制取 转移溶液 保护铁件 收集
4.化合物 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y
的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最
多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
5.下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是 ):B.食醋去除水垢中的 :
C.利用覆铜板制作印刷电路板:
D. 去除废水中的 :
6. 和 均可发生水解反应,其中 的水解机理示意图如下:
下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化
C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
7.室温下,下列实验探究方案能达到探究目的的是
选
实验目的 实验方案
项
将溴乙烷、乙醇和烧碱的混合物加热,产生的气体通入溴的 溶
A 证明溴乙烷发生了消去反应
液中,观察溶液颜色变化
B 证明 向NaCl、NaI混合溶液中滴加少量 溶液,观察沉淀的颜色
检验NaCl溶液中是否存在 用洁净的铂丝蘸取该溶液,在酒精灯外焰上灼烧,观察火焰是否出
C
KCl杂质 现紫色
比较 和HClO的酸 相同条件下,分别用pH试纸测定0.1 mol/L 溶液、0.1
D
性强弱 mol/L NaClO溶液的pH,观察pH试纸颜色
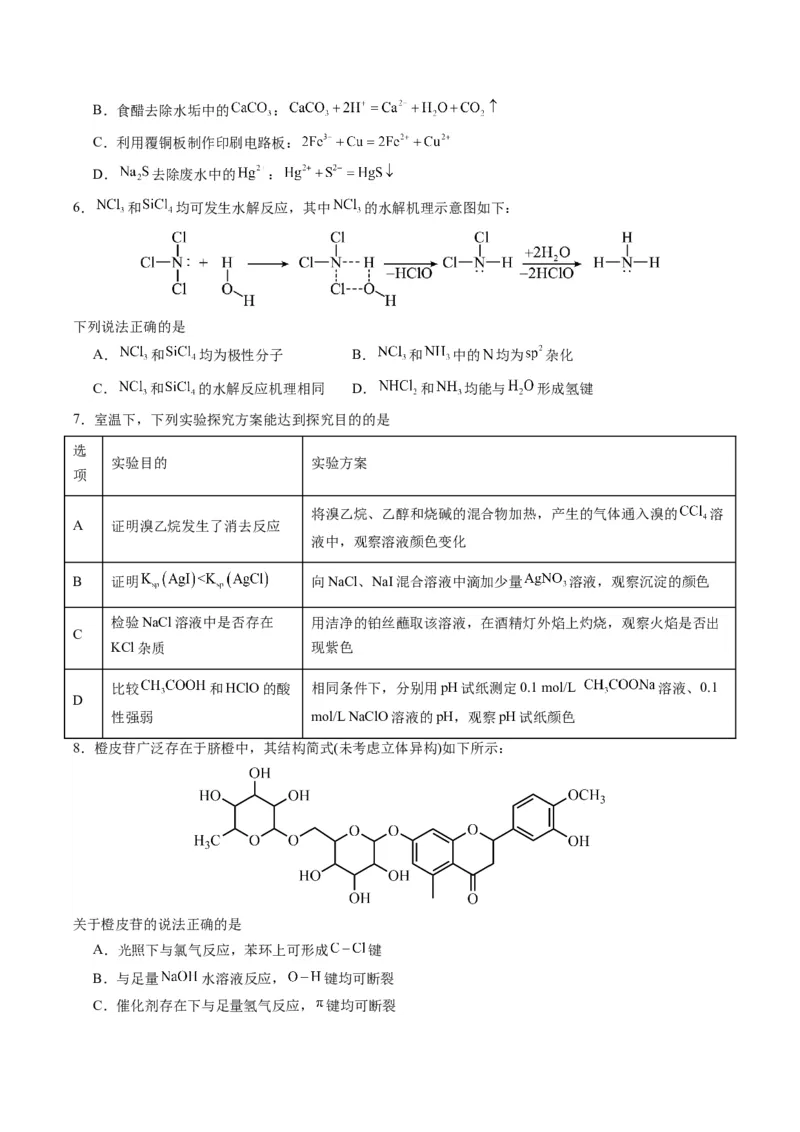
8.橙皮苷广泛存在于脐橙中,其结构简式(未考虑立体异构)如下所示:
关于橙皮苷的说法正确的是
A.光照下与氯气反应,苯环上可形成 键
B.与足量 水溶液反应, 键均可断裂
C.催化剂存在下与足量氢气反应, 键均可断裂D.与 醇溶液反应,多羟基六元环上可形成 键
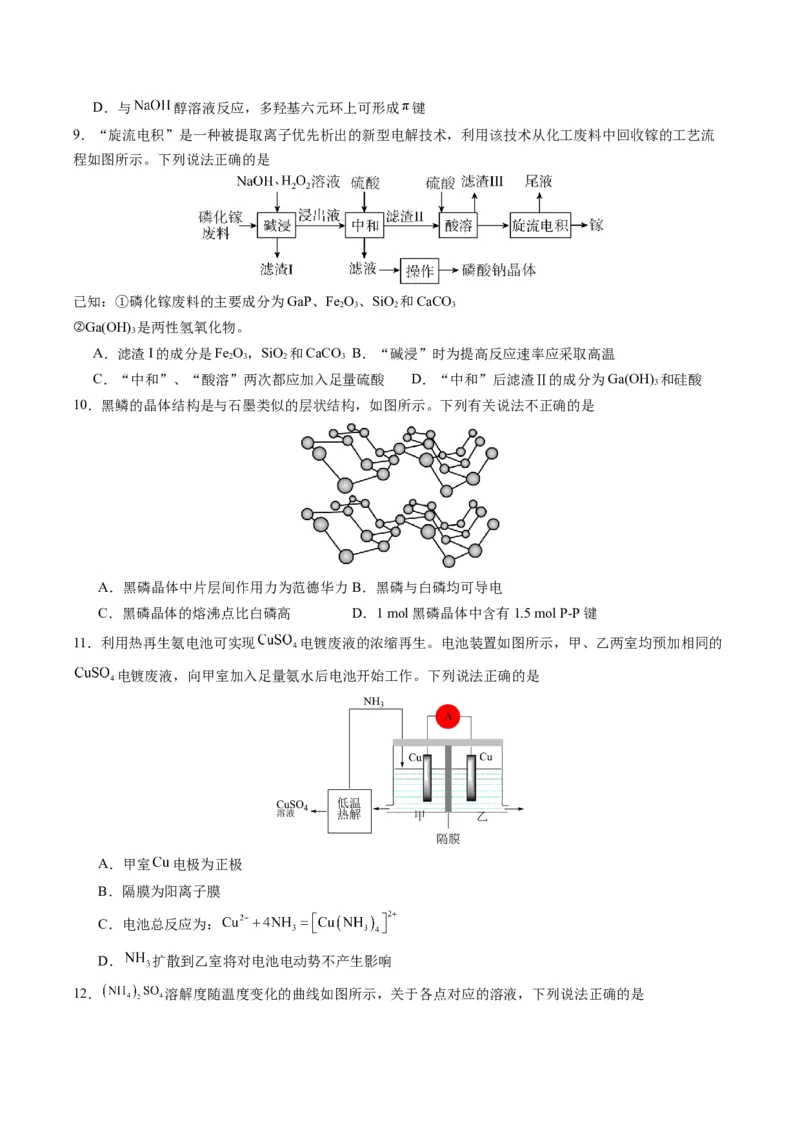
9.“旋流电积”是一种被提取离子优先析出的新型电解技术,利用该技术从化工废料中回收镓的工艺流
程如图所示。下列说法正确的是
已知:①磷化镓废料的主要成分为GaP、Fe O、SiO 和CaCO
2 3 2 3
②Ga(OH) 是两性氢氧化物。
3
A.滤渣I的成分是Fe O,SiO 和CaCO B.“碱浸”时为提高反应速率应采取高温
2 3 2 3
C.“中和”、“酸溶”两次都应加入足量硫酸 D.“中和”后滤渣Ⅱ的成分为Ga(OH) 和硅酸
3
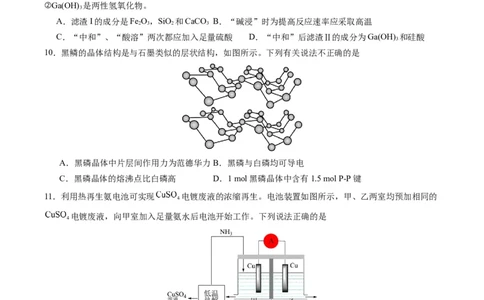
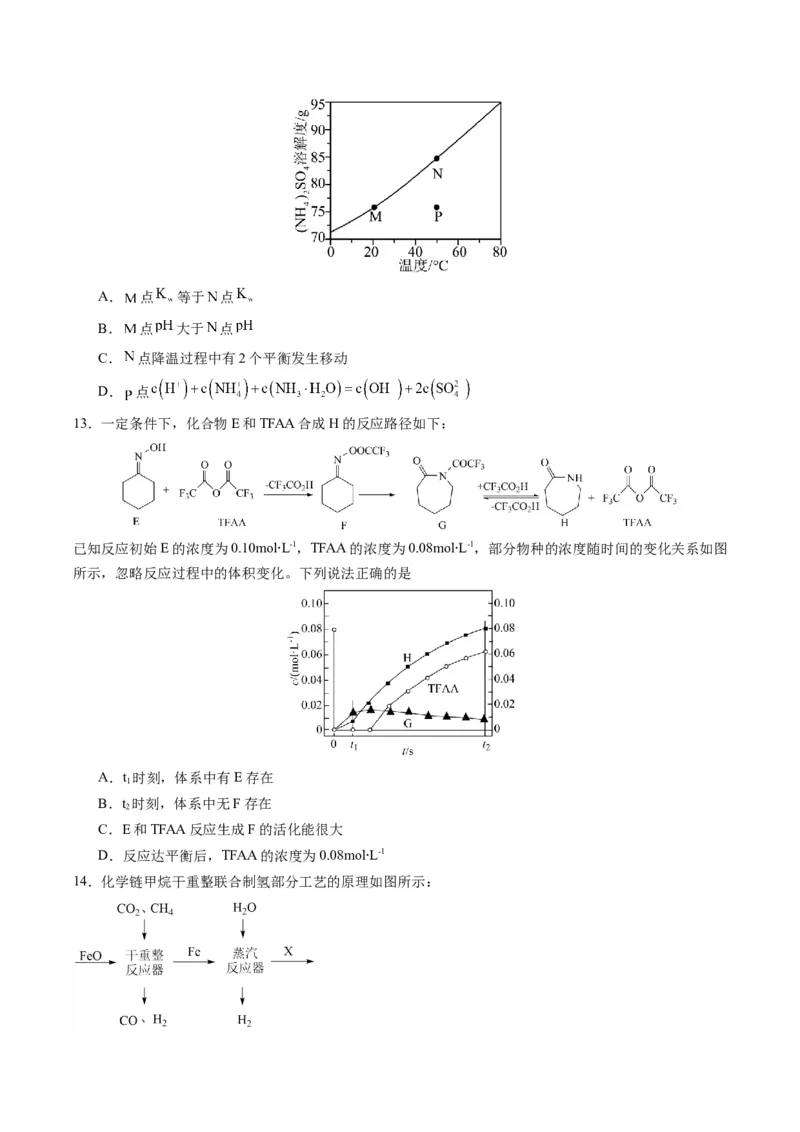
10.黑鳞的晶体结构是与石墨类似的层状结构,如图所示。下列有关说法不正确的是
A.黑磷晶体中片层间作用力为范德华力B.黑磷与白磷均可导电
C.黑磷晶体的熔沸点比白磷高 D.1 mol黑磷晶体中含有1.5 mol P-P键
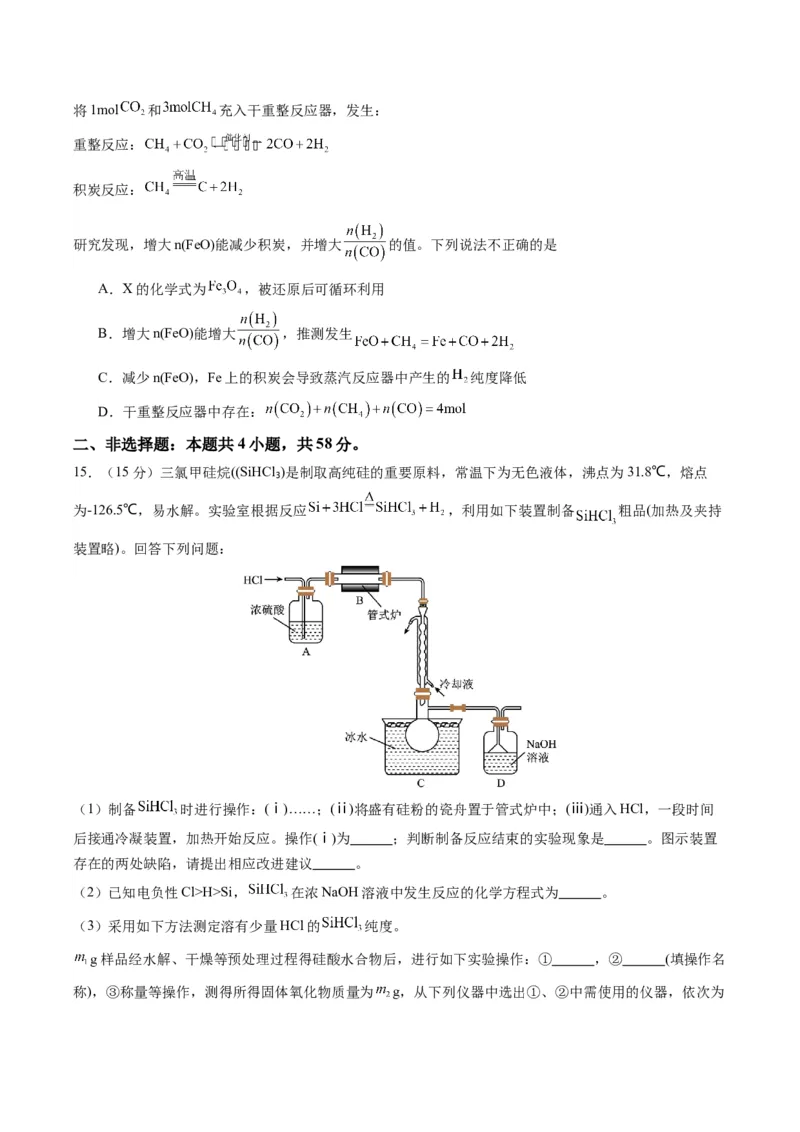
11.利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的
电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势不产生影响
12. 溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列说法正确的是A. 点 等于 点
B. 点 大于 点
C. 点降温过程中有2个平衡发生移动
D. 点
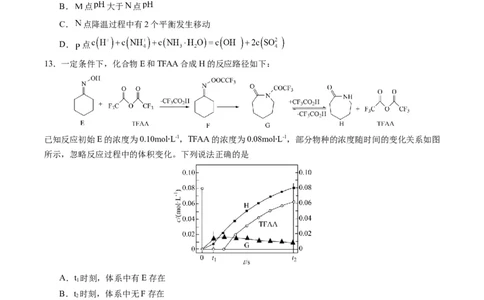
13.一定条件下,化合物E和TFAA合成H的反应路径如下:
已知反应初始E的浓度为0.10molL-1,TFAA的浓度为0.08molL-1,部分物种的浓度随时间的变化关系如图
所示,忽略反应过程中的体积变化。下列说法正确的是
∙ ∙
A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很大
D.反应达平衡后,TFAA的浓度为0.08molL-1
14.化学链甲烷干重整联合制氢部分工艺的原理如图所示:
∙将1mol 和 充入干重整反应器,发生:
重整反应:
积炭反应:
研究发现,增大n(FeO)能减少积炭,并增大 的值。下列说法不正确的是
A.X的化学式为 ,被还原后可循环利用
B.增大n(FeO)能增大 ,推测发生
C.减少n(FeO),Fe上的积炭会导致蒸汽反应器中产生的 纯度降低
D.干重整反应器中存在:
二、非选择题:本题共4小题,共58分。
15.(15分)三氯甲硅烷((SiHCl₃)是制取高纯硅的重要原料,常温下为无色液体,沸点为31.8℃,熔点
为-126.5℃,易水解。实验室根据反应 ,利用如下装置制备 粗品(加热及夹持
装置略)。回答下列问题:
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间
后接通冷凝装置,加热开始反应。操作(ⅰ)为 ;判断制备反应结束的实验现象是 。图示装置
存在的两处缺陷,请提出相应改进建议 。
(2)已知电负性Cl>H>Si, 在浓NaOH溶液中发生反应的化学方程式为 。
(3)采用如下方法测定溶有少量HCl的 纯度。
g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,② (填操作名
称),③称量等操作,测得所得固体氧化物质量为 g,从下列仪器中选出①、②中需使用的仪器,依次为(填标号)。测得样品纯度为 (用含 、 的代数式表示)。
16.(14分)氨气是常用的储氢介质,肼( )被视为一种极具应用潜力的液相化学储氢材料。回答下列
问题:
(1)工业合成氨的反应历程和能量变化如图所示:
①反应 的 。
②对总反应速率影响较大的步骤的能垒(活化能)为 。
(2)为了研究反应的热效应,科研人员计算了在一定范围内下列反应的平衡常数 。
ⅰ、
ⅱ、
ⅲ、
① 时,在恒容容器中,加入足量 (1)发生反应ⅰ和ⅱ。平衡时,测得容器内压强为 ,
,则 ,反应ⅰ的平衡常数 。
② 和 的线性关系如图所示,据此分析, 0(填“大于”或“小于”);对于反
应ⅲ,图中A、B两点的正反应速率大小关系是: (B点) (A点)(填“大于”“小于”或
“等于”); 的范围是 (填标号)。A. B.0~1 C. D.
(3)一种以液态肼( )为燃料的电池装置如图3所示,该电池以空气中的氧气为氧化剂, 溶液为
电解质溶液,则负极的电极反应式为 。
17.(14分) 是一种用途广泛的磁性材料,以 为原料制备 并获得副产物 水合物的
工艺如下。
时各物质溶度积见下表:
物质
溶度积
回答下列问题:
(1) 中 元素的化合价是 和 。 的核外电子排布式为 。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是 。
(3)反应釜2中,加入 和分散剂的同时通入空气。
①反应的离子方程式为 。
②为加快反应速率,可采取的措施有 。(写出两项即可)。
(4)①反应釜3中, 时, 浓度为 ,理论上 不超过 。
②称取 水合物 ,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸
中,用 标准溶液滴定,消耗 。滴定达到终点的现象为 ,该副产物中
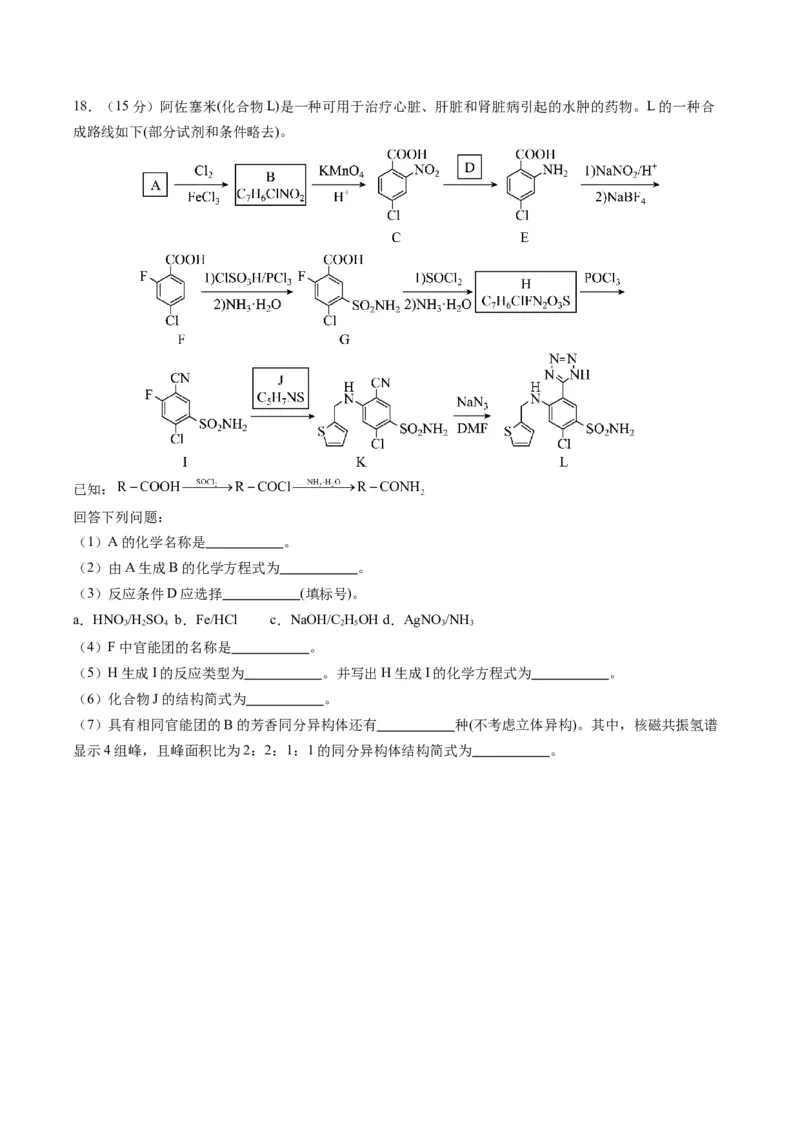
的质量分数为 。18.(15分)阿佐塞米(化合物L)是一种可用于治疗心脏、肝脏和肾脏病引起的水肿的药物。L的一种合
成路线如下(部分试剂和条件略去)。
已知:
回答下列问题:
(1)A的化学名称是 。
(2)由A生成B的化学方程式为 。
(3)反应条件D应选择 (填标号)。
a.HNO/H SO b.Fe/HCl c.NaOH/C HOH d.AgNO/NH
3 2 4 2 5 3 3
(4)F中官能团的名称是 。
(5)H生成I的反应类型为 。并写出H生成I的化学方程式为 。
(6)化合物J的结构简式为 。
(7)具有相同官能团的B的芳香同分异构体还有 种(不考虑立体异构)。其中,核磁共振氢谱
显示4组峰,且峰面积比为2:2:1:1的同分异构体结构简式为 。