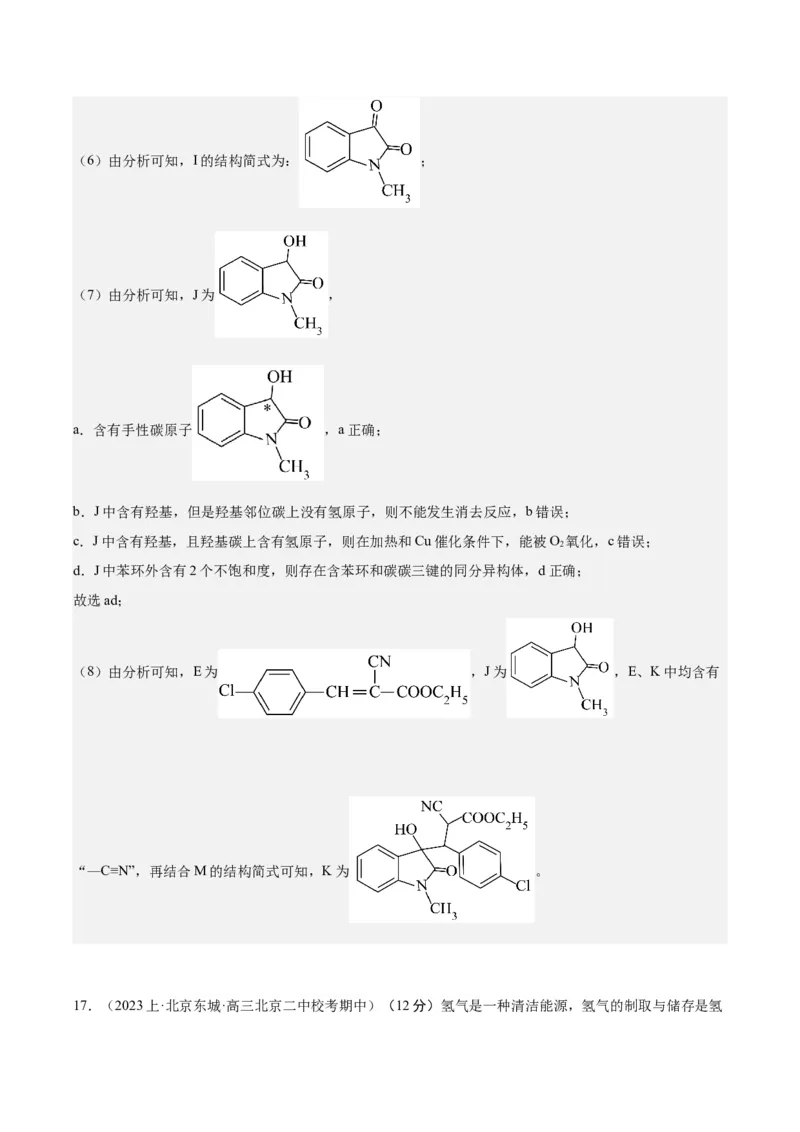
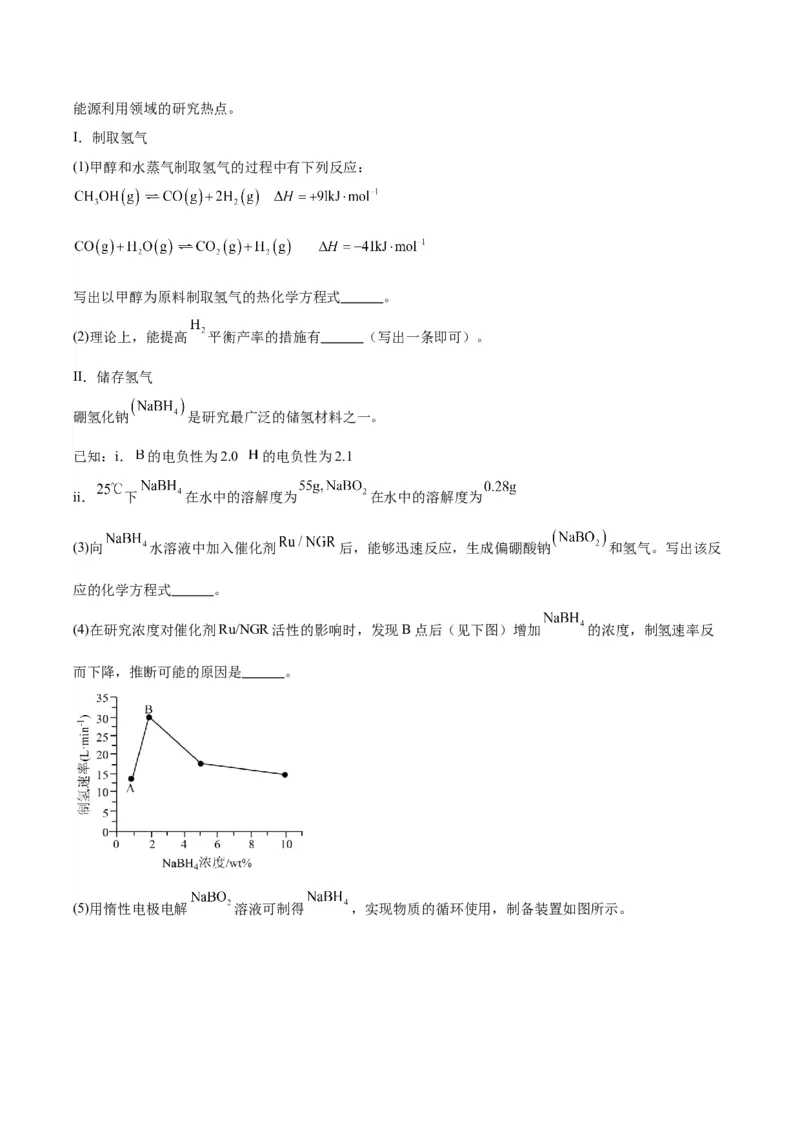
文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟(北京专用)
黄金卷06
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 S 32 Fe 56 Ce 140
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.(2023上·北京顺义·高三牛栏山一中校考)有关下列晶体的说法正确的是
A.该晶体溶于水后可以导电,该晶体一定是离子晶体
B.HO含共价键,因此冰是共价晶体
2
C.如图所示晶胞对应的化学式为ABX
3
D.一种化合物只能形成一种晶体结构
【答案】C
【解析】A.水溶液可以导电的晶体,可能为共价化合物,也可能为离子晶体,A错误;
B.HO含共价键,但是冰是分子晶体,B错误;
2
C.如图所示晶胞中,A为顶点,个数为 ,B为体心,个数为1,X为面心,额数为 ,对应
的化学式为ABX ,C正确;
3
D.一种化合物可能由于原子排列方式不同,能形成多种晶体结构,D错误;
故选C。
2.(2023·北京门头沟·统考一模)下列化学用语或图示表达不正确的是
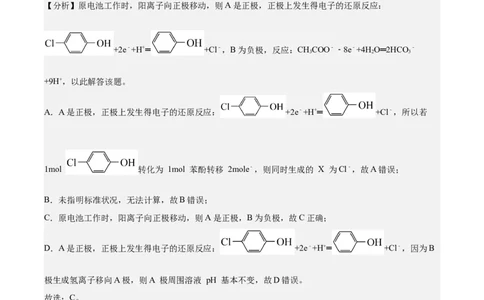
A.氯化钙的电子式:B.基态C原子的轨道表示式:
C.顺-2-丁烯的分子结构模型:
D.Cl-Cl的p-pσ键电子云图形:
【答案】B
【解析】A.氯化钙的电子式为 ,A正确;
B.基态C原子的轨道表示式为 ,B错误;
C.顺-2-丁烯的分子结构模型为 ,C正确;
D.p-pσ键的原子轨道头碰头方式重叠,则Cl-Cl的p-pσ键电子云图形为 ,D正确;
故选B。
3.(2023上·北京海淀·高三清华附中校考)依据下列实验现象推测,其反应原理不涉及氧化还原反应的是
A.向饱和NaCl溶液中依次通入过量NH 、CO,析出沉淀
3 2
B.把钠放入CuSO 溶液中,有蓝色沉淀生成
4
C.向酸性KMnO 溶液中加入HO,溶液紫色褪去
4 2 2
D.氯水在光照条件下放置一段时间后,溶液的pH降低
【答案】A
【解析】A.根据侯氏制碱法可知,该反应为: ,该反应中没有
元素化合价发生变化,不是氧化还原反应,A项符合题意;
B.把钠放入 溶液中,发生反应: ,有氢氧化铜沉淀
生成,有元素化合价发生变化,涉及氧化还原反应,B项不符合题意;
C.向酸性 溶液中加入 ,发生反应: ,溶液紫色
褪去,有元素化合价发生变化,涉及氧化还原反应,C项不符合题意;D.氯气在光照条件下放置一段时间后,溶液的pH降低,是因为发生反应: ,有元
素化合价发生变化,涉及氧化还原反应,D项不符合题意;
答案选A。
4.(2023下·北京海淀·高三首都师范大学附属中学校考)有研究认为,强碱性溶液中反应
分三步进行,其中两步如下:
第一步:
第二步:……
第三步:
下列说法不正确的是
A.反应第二步为 B.升高温度可以使 增大
C.由K可判断,第三步不是整个过程的决速步 D. 分子的空间结构为V型
【答案】C
【解析】A.总反应为I-+ClO-═IO-+Cl-,其中第一步为ClO-+H O→HClO+OH-,第三步为HIO+OH-→IO-
2
+H O,则总反应式减去第一步和第三步反应即可得第二步为HClO+I-→HIO+Cl-,故A正确;
2
B.ClO-的水解是吸热反应,升高温度,可以使 增大,故B正确;
C.平衡常数只能体现反应进行的程度,无法判断反应的速率快慢,即由K不能确定反应第三步是否是整
个过程最慢的反应,故C错误;
D.HClO中心原子的价电子对数为 ,孤电子对数为2,则分子的空间结构为V型,故D正确;
故选C。
5.(2017·北京海淀·人大附中校考三模)科学家尝试用微生物电池除去废水中的有害的有机物,其原理如
图所示。下列有关说法正确的是A.若1mol 转化为1mol苯酚转移2mole-,则同时生成的X为氯气
B.用该电池电解饱和食盐水(使用情性电极的电解槽)每产生22.4L的氢气,B极上生成0.5mol
C.A极为正极,B极为负极
D.电池工作过程中A极周围溶液pH不断增大
【答案】C
【解析】
【分析】原电池工作时,阳离子向正极移动,则A是正极,正极上发生得电子的还原反应:
+2e﹣+H+═ +Cl﹣,B为负极,反应:CHCOO﹣﹣8e﹣+4H O═2HCO﹣
3 2 3
+9H+,以此解答该题。
A.A是正极,正极上发生得电子的还原反应: +2e﹣+H+═ +Cl﹣,所以若
1mol 转化为 1mol 苯酚转移 2mole﹣,则同时生成的 X 为Cl﹣,故A错误;
B.未指明标准状况,无法计算,故B错误;
C.原电池工作时,阳离子向正极移动,则A是正极,B为负极,故C正确;
D.A是正极,正极上发生得电子的还原反应: +2e﹣+H+═ +Cl﹣,因为B
极生成氢离子移向A极,则A 极周围溶液 pH 基本不变,故D错误。
故选:C。
【点评】本题考查新型电池,为高频考点,题目难度不大,注意把握原电池的工作原理以及电极反应式的
书写,解答本题的关键是根据物质的性质判断原电池的正负极。
6.(2023上·北京通州·高三统考期中)下列方程式与所给事实不相符的是
A. 通过灼热铁粉:
B.用 作抗胃酸药:C. 与 反应:
D. 通入酸性 溶液中:
【答案】A
【解析】A. 通过灼热铁粉: ,A错误;
B.用 作抗胃酸药,实际上是与胃酸中的HCl反应,其离子方程式为:
,B正确;
C. 与 反应产生碳酸钠和氧气,其化学方程式为: ,C正确;
D. 通入酸性 溶液中会发生氧化还原反应,其离子方程式为:
,D正确;
故选A。
7.(2023·北京海淀·人大附中校考三模)下列由实验现象所得结论不正确的是
A.向 溶液中滴加氢硫酸,立即产生淡黄色沉淀,证明 具有氧化性
B.向酸性 溶液中加入 粉末,紫色褪去,证明 中含Fe(Ⅱ)
C.向某溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成,证明溶液存在
D.向 溶液中加入几滴氯水振荡,再加 萃取,下层呈紫色,上层无色,证明还原性
【答案】C
【解析】A. 中硫显+4价,与 发生归中反应, 被氧化为硫单质,体现了 的氧化性,A
正确;
B. 与酸反应得到铁盐与亚铁盐,还原性的亚铁离子将高锰酸钾还原,紫色褪去,证明 中含
Fe(Ⅱ),B正确;
C.若溶液中存在Ag+,也会产生白色沉淀,C错误;D.少量氯水加入到 溶液中,再加 萃取,下层呈紫色说明产生了I 单质,亚铁离子未优先反应,
2
由此说明还原性 ,D正确;
答案选C。
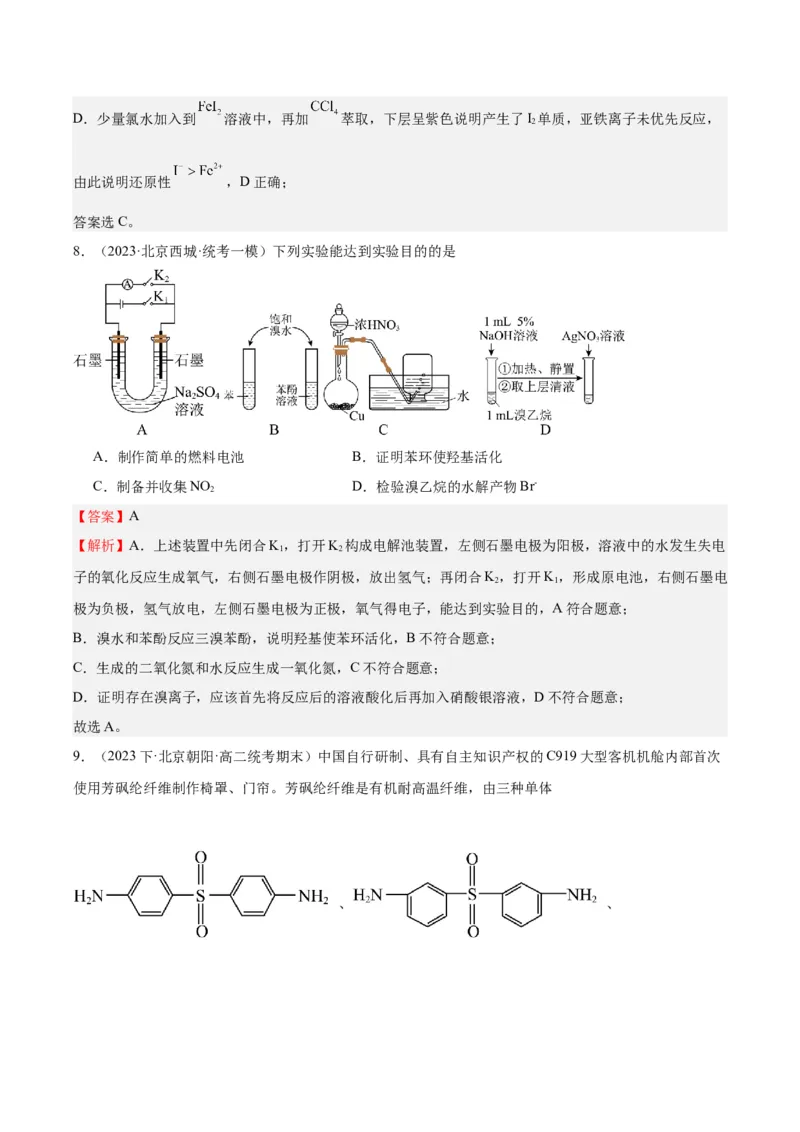
8.(2023·北京西城·统考一模)下列实验能达到实验目的的是
A.制作简单的燃料电池 B.证明苯环使羟基活化
C.制备并收集NO D.检验溴乙烷的水解产物Br-
2
【答案】A
【解析】A.上述装置中先闭合K,打开K 构成电解池装置,左侧石墨电极为阳极,溶液中的水发生失电
1 2
子的氧化反应生成氧气,右侧石墨电极作阴极,放出氢气;再闭合K,打开K,形成原电池,右侧石墨电
2 1
极为负极,氢气放电,左侧石墨电极为正极,氧气得电子,能达到实验目的,A符合题意;
B.溴水和苯酚反应三溴苯酚,说明羟基使苯环活化,B不符合题意;
C.生成的二氧化氮和水反应生成一氧化氮,C不符合题意;
D.证明存在溴离子,应该首先将反应后的溶液酸化后再加入硝酸银溶液,D不符合题意;
故选A。
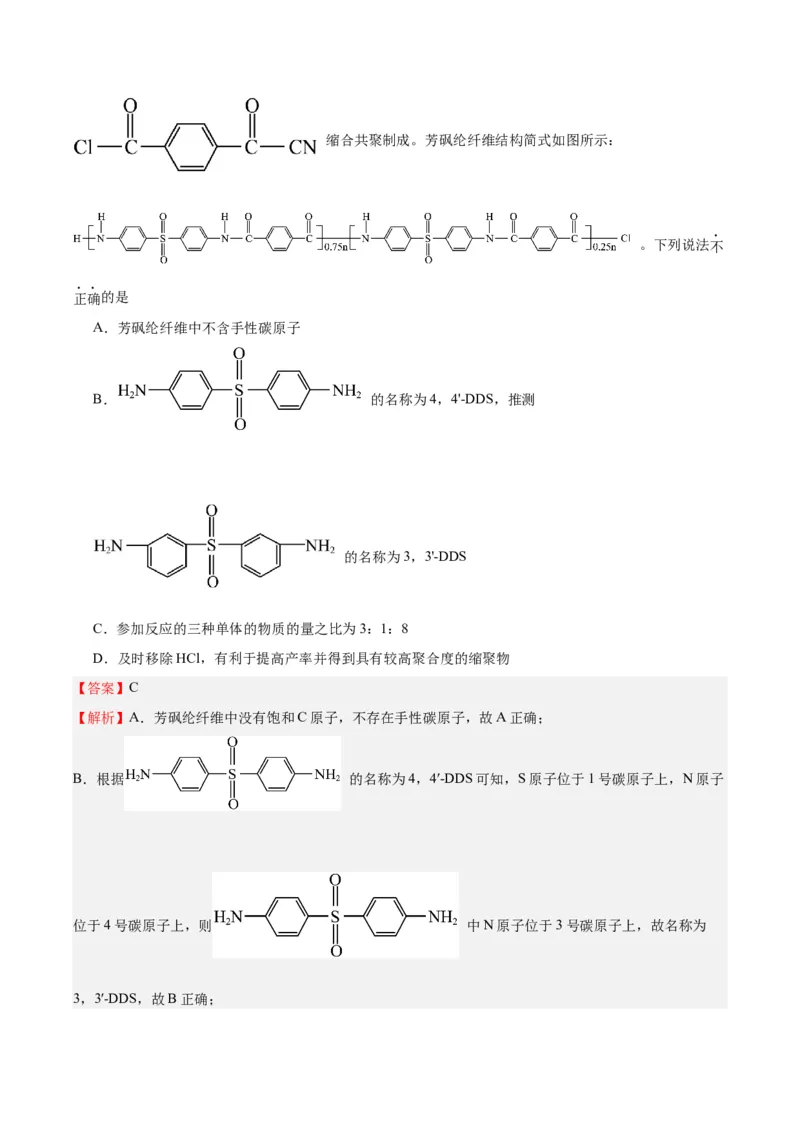
9.(2023下·北京朝阳·高二统考期末)中国自行研制、具有自主知识产权的C919大型客机机舱内部首次
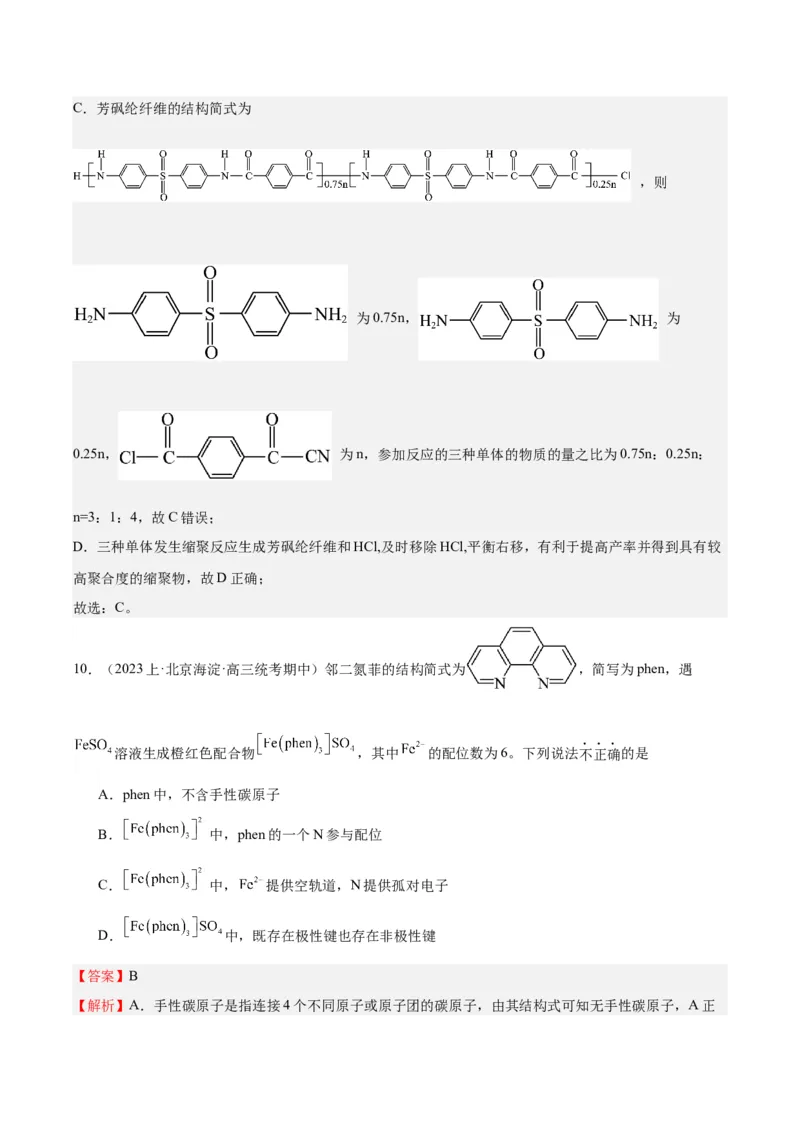
使用芳砜纶纤维制作椅罩、门帘。芳砜纶纤维是有机耐高温纤维,由三种单体
、 、缩合共聚制成。芳砜纶纤维结构简式如图所示:
。下列说法不
正确的是
A.芳砜纶纤维中不含手性碳原子
B. 的名称为4,4'-DDS,推测
的名称为3,3'-DDS
C.参加反应的三种单体的物质的量之比为3:1:8
D.及时移除HCl,有利于提高产率并得到具有较高聚合度的缩聚物
【答案】C
【解析】A.芳砜纶纤维中没有饱和C原子,不存在手性碳原子,故A正确;
B.根据 的名称为4,4′-DDS可知,S原子位于1号碳原子上,N原子
位于4号碳原子上,则 中N原子位于3号碳原子上,故名称为
3,3′-DDS,故B正确;C.芳砜纶纤维的结构简式为
,则
为0.75n, 为
0.25n, 为n,参加反应的三种单体的物质的量之比为0.75n:0.25n:
n=3:1:4,故C错误;
D.三种单体发生缩聚反应生成芳砜纶纤维和HCl,及时移除HCl,平衡右移,有利于提高产率并得到具有较
高聚合度的缩聚物,故D正确;
故选:C。
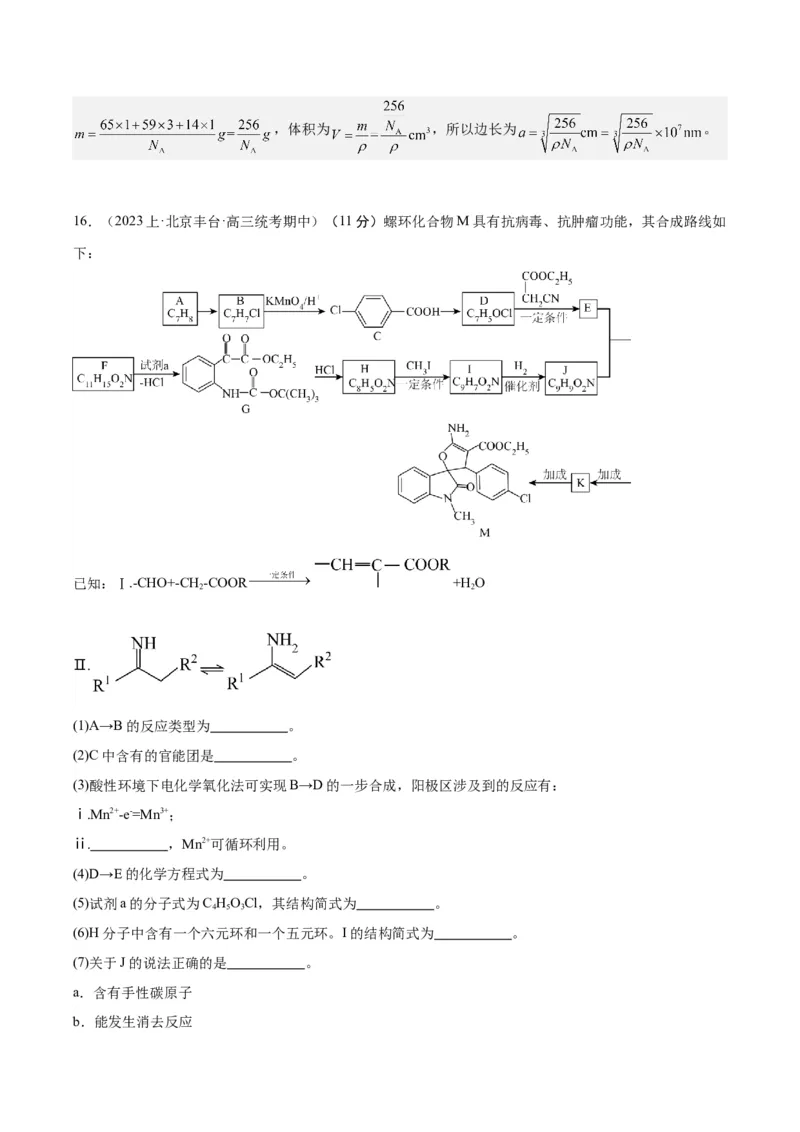
10.(2023上·北京海淀·高三统考期中)邻二氮菲的结构简式为 ,简写为phen,遇
溶液生成橙红色配合物 ,其中 的配位数为6。下列说法不正确的是
A.phen中,不含手性碳原子
B. 中,phen的一个N参与配位
C. 中, 提供空轨道,N提供孤对电子
D. 中,既存在极性键也存在非极性键
【答案】B
【解析】A.手性碳原子是指连接4个不同原子或原子团的碳原子,由其结构式可知无手性碳原子,A正确;
B.由于亚铁离子的配位数为6,故 中phen有2个N原子参与配位,B错误;
C.在物质 中,中心原子 提供空轨道,N提供孤对电子,C正确;
D.硫和氧、碳和氮之间为极性键,但phen中C和C为非极性键,D正确;
故选B。
11.(2023下·北京大兴·高二统考期末)维生素C是重要的营养素,其分子结构如图。下列关于维生素C
的叙述不正确的是
A.维生素C的分子式为C HO
6 8 6
B.维生素C中的官能团有五种
C.维生素C易溶于水,可能与其分子中含有多个羟基有关
D.向碘和淀粉的混合液中加入维生素C,蓝色褪去,证明维生素C具有还原性
【答案】B
【解析】A.根据该物质的结构可知其分子式为C HO,A正确;
6 8
B.维生素C中的官能团有羟基、碳碳双键、酯基3种,B错误;
C.分子中有多个羟基,可以与水分子间形成氢键,易溶于水,C正确;
D.分子中含有羟基和碳碳双键,易被氧化,具有较强还原能力,碘具有氧化性,向碘和淀粉的混合液中
加入维生素C,蓝色褪去,可以说明维生素C具有还原性,D正确;
故选B。
12.(2023上·北京通州·高三统考期中) 的一种制备方法如下图所示,下列说法不正确的是
A.加入 的目的是富集B.生成的沉淀通过转化可循环使用
C.当 后,发生反应
D.加入铁粉发生的离子反应是
【答案】C
【分析】净化除氯后含I的海水,加入AgNO,进行富集,生成含有AgI的悬浊液,继续加入铁粉,发生
3
反应: ,过滤掉析出的Ag,向FeI 中加入过量Cl,可得到I,据此分析解答;
2 2 2
【解析】A.根据分析可知,加入 的目的是富集 ,A正确;
B.转化生成沉淀为Ag,与硝酸反应生成AgNO,产物可在富集操作中循环使用,B正确;
3
C.当 ,刚好发生反应: ,当 后, 可能进一步被氧化,
C错误;
D.根据分析可知,加入铁粉发生的离子反应是 ,D正确;
答案选C。
13.(2023上·北京·高三首都师范大学附属中学校考)下图是乙烯催化氧化生成乙醛的过程(部分相关离子
未画出),下列描述正确的是
A.过程Ⅰ和过程Ⅴ均发生了氧化还原反应
B.若原料是丙烯,则产物可能是丙醛
C.整个转化过程中,只有 在反应中起到催化剂的作用D.根据整个过程的总反应,理论上生成1mol ,电子转移为4mol
【答案】B
【分析】根据反应机理图可知,过程I为 +CH =CH PdCl (CH=CH )-+Cl-;过程II为
2 2 3 2 2
PdCl (CH=CH )-+H O PdCl (H O)(CH =CH )+Cl-;过程III为PdCl (H O)(CH =CH )+H O
3 2 2 2 2 2 2 2 2 2 2 2 2
+H+;过程IV为 +H O,过程V为
2
CHCHO+Pd+H++2Cl-,过程VI为Pd+2Cu2++4Cl- +2Cu+;过程VII为4Cu+
3
+O +4H+=4Cu2++2H O,则(I+II+III+IV+V+VI)+VII得到反应的总方程式为:2CH=CH + O
2 2 2 2 2
2CHCHO,据此结合反应历程分析。
3
【解析】A.过程Ⅰ中没有元素化合价的升降,过程Ⅴ中生成单质Pd,有元素化合价的升降,属于氧化还
原反应,A错误;
B.若原料是丙烯,根据过程IV可知脱水过程可能生成 ,也可能生成
,则最终产物可能是丙醛和丙酮,B正确;
C.整个转化过程中,除了 ,还有Cu2+均在反应中起到催化剂的作用,C错误;
D.根据整个过程的总反应2CH=CH + O 2CHCHO可知,理论上生成1molCH CHO,电子转移
2 2 2 3 3为2mol,D错误;
故选B。
14.(2022·北京丰台·北京市第十中学校考三模)室温时,向100mL0.1mol•L-1NH HSO 溶液中滴加
4 4
0.1mol•L-1NaOH溶液,溶液pH随NaOH溶液体积的变化如图所示。下列说法正确的是
A.a点处存在c(NH )+c(NH•H O)=0.1mol•L-1
3 2
B.b点处存在c(Na+)>c(SO )>c(NH )>c(H+)=c(OH-)
C.由b到c发生反应的离子方程式为H++NH +2OH-=NH•H O+HO
3 2 2
D.图中a、b、c、d四个点,水的电离程度最大的是d点
【答案】B
【解析】A.a点处溶液的体积是原来的两倍,c(NH )+c(NH•H O)=0.05mol•L-1,A错误;
3 2
B.b点处加入的氢氧化钠溶液的体积大于100mL,故c(Na+)>c(SO ),SO 和NH 均来自于
NH HSO ,随着氢氧化钠溶液的加入,铵根的浓度的减小有两个原因,一是体积的增大,二是铵根和氢氧
4 4
根反应,故c(SO )>c(NH ),此时溶液中的c(H+)=c(OH-)=10-7mol/L浓度最小,B正确;
C.由起点到a发生反应的离子方程式为H++OH-=H O,由b到c发生反应的离子方程式为NH +OH-
2
=NH•H O,C错误;
3 2
D.加酸、碱均抑制水的电离,水解促进电离,a点为(NH )SO 、NaSO 的混合溶液,b点为(NH )SO 、
4 2 4 2 4 4 2 4
NaSO 、氨水的混合溶液但此时溶液呈中性,c点为(NH )SO 、NH ·H O和NaSO 的混合溶液,d点为
2 4 4 2 4 3 2 2 4
NaSO 和NH ·H O的混合溶液,则a点水的电离程度最大,D错误。
2 4 3 2故选B。
第二部分
本题共5题,共58分。
15.(2023上·北京·高三北京师大附中校考)(11分)含化合物具有非常广泛的应用。
(1)基态氮原子的电子有 种空间运动状态。
(2)很多有机化合物中含有氮元素。
物质 A(对氨基苯甲酸) B(邻氨基苯甲酸)
结构简式
熔点 188℃ 145℃
作用 防晒剂 制造药物及香料
①组成物质A的4种元素的电负性由大到小的顺序是 。
②A的熔点高于B的原因是 。
③A可以与多种过渡金属元素形成不同结构的配合物。其中A和 可形成链状结构,在下图虚线内画出
A的结构简式 。
(3)氮元素可以与短周期金属元素形成化合物。 是离子化合物,比较两种微粒的半径:
(填“>”、“<”或“=”),从结构角度解释 。
(4)氮元素可以与过渡金属元素形成化合物,其具备高硬度、高化学稳定性和优越的催化活性等性质。某三
元氨化物是良好的超导材料,其晶胞结构如图所示。
①基态Ni原子价层电子的轨道表示式为 。
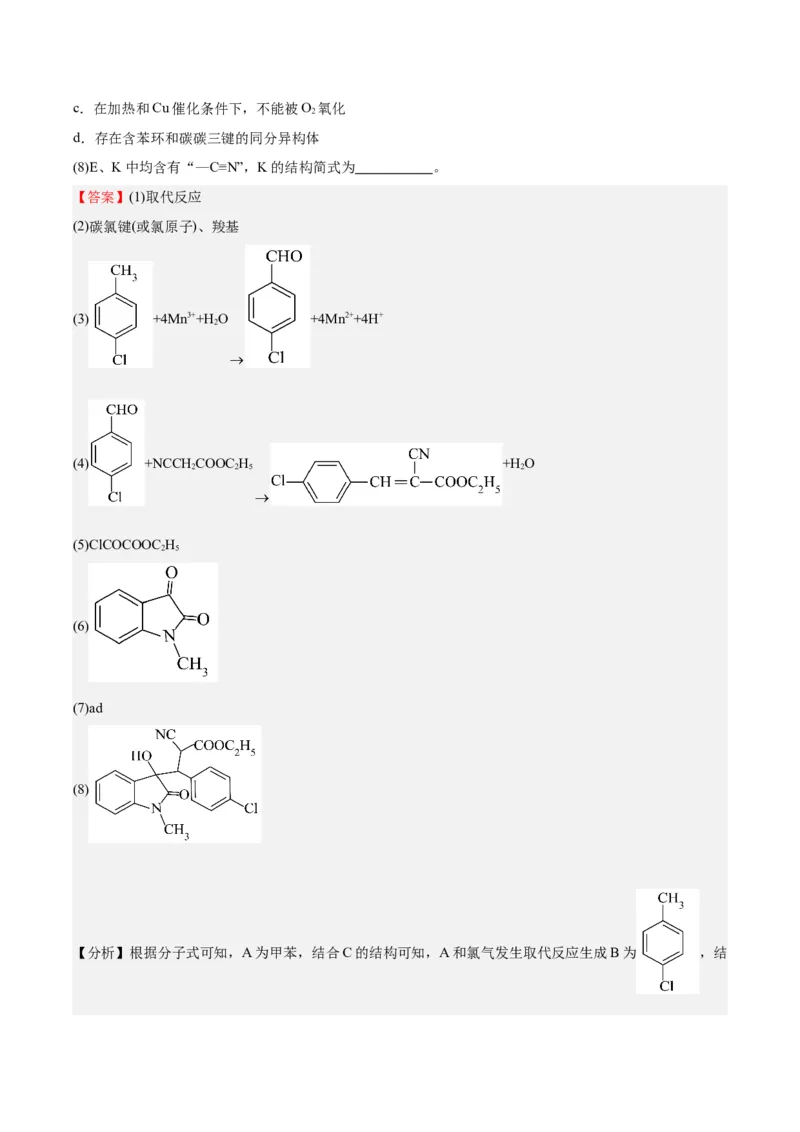
②与Zn原子距离最近且相等的Ni原子有 个。③ 表示阿伏加德罗常数的值。若此晶体的密度为 ,则晶胞的边长为 nm。(
)
【答案】(1)5
(2) O>N>C>H B易形成分子内氢键,A只存在分子间氢键,影响物质熔点的是分子间氢键,所
以A的熔点高于B
(3) < 电子层结构相同的离子,核电荷数越大离子半径越小
(4) 12
【解析】(1)基态N原子的核外电子排布式为1s22s22p3,电子的空间运动状态数=轨道数,有5种;
(2)①组成物质A的4种元素为C、H、N、O,同周期元素从左到右元素的电负性逐渐增大,则有电负
性C<N<O,H的电负性最小,故有:O>N>C>H;
②B(邻氨基苯甲酸)易形成分子内氢键,A(对氨基苯甲酸)只存在分子间氢键,影响物质熔点的是分子间氢
键,所以A的熔点高于B;
③N、O原子提供孤电子对,Ag+提供空轨道,其中A和Ag+可形成链状结构,A的结构简式为:
;
(3)相同电子层结构的离子,核电荷数越大,离子半径越小,故半径:Mg2+