文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷07
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.分类是学习和研究化学的重要方法,下列分类不合理的是
A. 属于钾盐、碳酸盐 B. 属于可溶性强碱
C.液氯属于混合物 D. 属于碱性氧化物
【答案】C
【解析】A. 既属于钾盐又属于碳酸盐,A项不符合题意;
B. 属于可溶性强碱,B项不符合题意;
C.液氯是 处于液态,属于单质,是纯净物,C项符合题意;
D. 属于碱性氧化物,D项不符合题意;
故答案为:C。
2.下列变化或应用与氧化还原反应无关的是
A.呼吸面具中常用NaO 作供氧剂
2 2
B.油酸甘油酯氢化得到硬脂酸甘油酯
C.琥珀酸亚铁补铁剂与维生素C同服
D.鸡蛋清溶液中加入饱和(NH )SO 溶液变浑浊
4 2 4
【答案】D
【分析】氧化还原反应的特征是反应中有化合价升降。
【解析】A.呼吸面具中常用NaO 作供氧剂是过氧化钠和二氧化碳生成氧气和碳酸钠,有化合价变化,
2 2反应中有化合价升降,是氧化还原反应,故A不符合题意;
B.油酸甘油酯氢化得到硬脂酸甘油酯,加氢是还原反应,反应中有化合价升降,是氧化还原反应,故B
不符合题意;
C.琥珀酸亚铁补铁剂与维生素C同服防止亚铁离子被氧化,涉及到氧化还原反应,故C不符合题意;
D.鸡蛋清溶液中加入饱和(NH )SO 溶液变浑浊是盐析是物理变化,不是氧化还原反应,故D符合题意;
4 2 4
故选D。
3.下列有关实验的说法正确的是
A.溴水应保存在带磨口玻璃塞的棕色细口试剂瓶中
B.使用分液漏斗前,应向分液漏斗中加少量水,检查旋塞芯处是否漏水,待确认不漏水后即可使用
C.蒸发操作中,将蒸发皿放在铁架台的铁圈上,并垫上石棉网加热
D.配制一定物质的量浓度的溶液时,容量瓶中有少量的水会导致溶液浓度偏低
【答案】A
【解析】A.溴水中的次溴酸遇光易分解且溴水易腐蚀橡胶塞,所以溴水应保存在带磨口玻璃塞的棕色细
口试剂瓶中,A正确;
B.使用前分液漏斗有两处要检漏,上口塞子和下口旋塞,所以在分液漏斗的检漏操作时,应先向分液漏
斗中加少量水,检查旋塞芯处是否漏水,然后将漏斗倒转过来,再检查玻璃塞是否漏水,待确认不漏水后
方可使用,B错误;
C.蒸发时,蒸发皿可以放在铁圈上直接加热,蒸发皿耐高温,不用垫石棉网,C错误;
D.配制一定物质的量浓度的溶液时,容量瓶中有少量的水不会干扰实验结果,D错误;
答案选A。
4.物质的性质决定用途和保存方式,下列两者对应关系不正确的是
A. 见光易分解,浓硝酸用棕色瓶保存
B. 具有强氧化性,可用于杀菌消毒
C. 具有还原性,可用于漂白纸浆
D. 难溶于稀盐酸,医学上常用作“钡餐”
【答案】C
【解析】A.浓硝酸不稳定见光易分解生成NO 和O,因此用棕色瓶避光保存,A正确;
2 2
B.HO 具有强氧化性,氧元素化合价-1价变化为0价,可用于杀菌消毒,B正确;
2 2C. 能和有色物质反应生成无色物质而具有漂白性,所以能漂白纸张,漂白纸张与 的还原性无关,
C错误;
D.在人体的胃液中有盐酸, 难溶于稀盐酸,医学上常用作“钡餐”,D正确;
故选C。
5.下列说法正确的是
A.碱性:Ca(OH >Mg(OH) B.半径:K+>Cl-
)2 2
C.酸性:HClO> H SO D.最低负化合价:N>O
2 4
【答案】A
【解析】A.金属性Ca>Mg,则最高价氧化物的水化物的碱性为:Ca(OH) >Mg(OH) ,故A正确;
2 2
B.电子层结构相同,核电荷数越大离子半径越小,故离子半径:Cl->K+,故B错误;
C.金属性:Cl>S,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,所以酸性:HClO
4
>HSO ,HClO不是最高价含氧酸,故C错误;
2 4
D.N的最低负价为-3价,O的最低负价为-2价,故D错误;
故选A。
6.元素Be、Mg、Ca位于周期表中ⅡA族。下列说法正确的是
A.电负性:
B.第一电离能:
C. 、 、 形成的晶体均为离子晶体
D.最高价氧化物的水化物的碱性:
【答案】B
【解析】A.同一主族元素,从上到下,电负性逐渐减小, ,A错误;
B.同一主族元素,从上到下,第一电离能逐渐减小, ,B正确;
C. 与 相似, 形成的是共价键, 形成的晶体为分子晶体,C错误;
D.同一主族元素,从上到下,最高价氧化物的水化物的碱性增强, ,D错误;
答案选B。
7.一种由 和 转化为高附加值产品 的催化反应历程如图所示。下列说法正确的是
A.①→②放出能量并形成 键
B.该反应的平衡常数
C. 过程中,有 键发生断裂
D.该反应中每生成 ,转移电子的数目约为
【答案】C
【解析】A.由图中可知,①→②过程中物质的能量降低,说明为放热过程,并且形成了C-C化学键,A
错误;
B.由图中可知,该反应的总方程式为: ,则平衡常数 ,B
错误;
C.由图可知,在催化剂表面生成①的过程中,存在 键发生断裂,C正确;
D.该反应的总方程式为: ,CO 中C元素由+4价下降到0价,甲烷中碳元素化
2
合价由-4升高为0,电子转移为 ,则每生成1mol 转移电子4mol,电子的数目约为
,D错误;
故选C。8.奥培米芬是一种雌激素受体调节剂,下列说法正确的是
A.属于芳香烃
B.存在3种官能团
C.含有-OH等亲水基团,具有较好的水溶性
D.在KOH醇溶液或浓硫酸中加热均能发生消去反应
【答案】D
【解析】A. 组成元素有C、H、O、Cl,不是烃,A错误;
B.结构中含有碳碳双键、碳氯键、醚键、羟基四种官能团,B错误;
C.结构中含有Cl原子、醚键以及苯环,更多的是憎水基,在水中溶解度不大,C错误;
D.结构中存在Cl原子和羟基,且邻位碳上均有氢原子,在KOH醇溶液或浓硫酸中加热均能发生消去反
应,D正确;
答案选D。
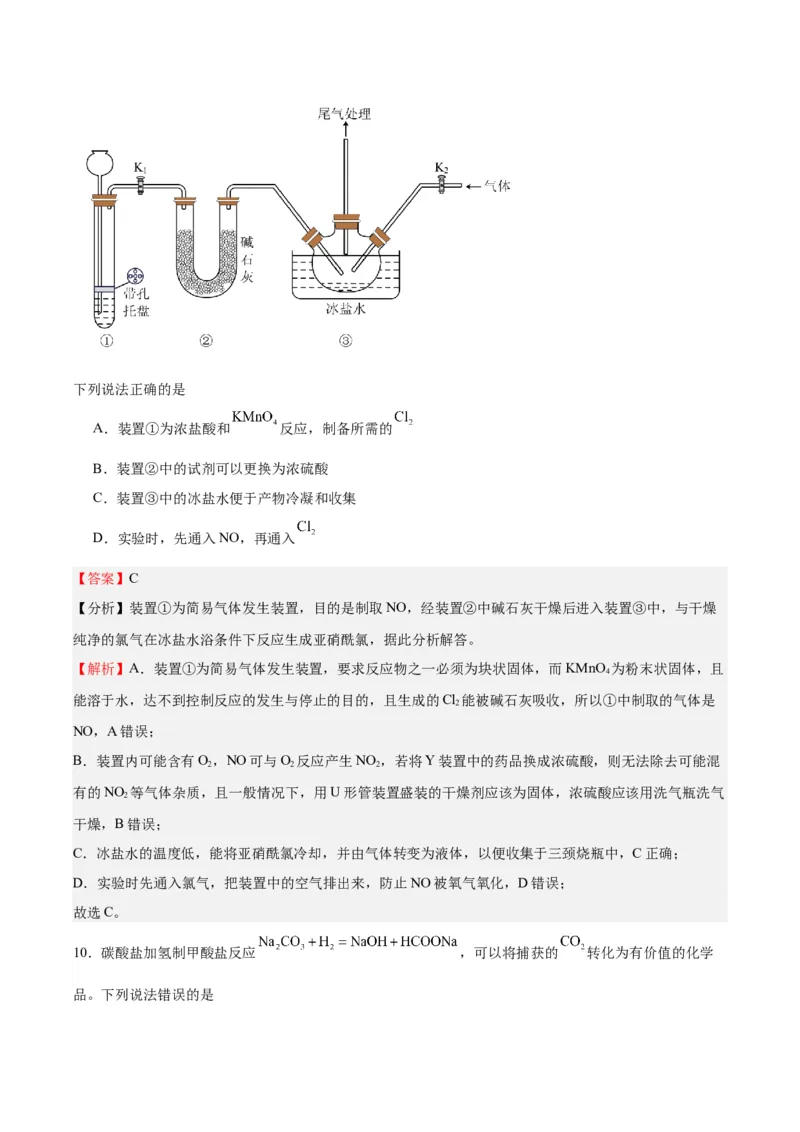
9.实验室可利用NO与 反应制备亚硝酰氯(NOCl),装置如图。已知亚硝酰氯的沸点为-5.5℃,遇水生
成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。下列说法正确的是
A.装置①为浓盐酸和 反应,制备所需的
B.装置②中的试剂可以更换为浓硫酸
C.装置③中的冰盐水便于产物冷凝和收集
D.实验时,先通入NO,再通入
【答案】C
【分析】装置①为简易气体发生装置,目的是制取NO,经装置②中碱石灰干燥后进入装置③中,与干燥
纯净的氯气在冰盐水浴条件下反应生成亚硝酰氯,据此分析解答。
【解析】A.装置①为简易气体发生装置,要求反应物之一必须为块状固体,而KMnO 为粉末状固体,且
4
能溶于水,达不到控制反应的发生与停止的目的,且生成的Cl 能被碱石灰吸收,所以①中制取的气体是
2
NO,A错误;
B.装置内可能含有O,NO可与O 反应产生NO ,若将Y装置中的药品换成浓硫酸,则无法除去可能混
2 2 2
有的NO 等气体杂质,且一般情况下,用U形管装置盛装的干燥剂应该为固体,浓硫酸应该用洗气瓶洗气
2
干燥,B错误;
C.冰盐水的温度低,能将亚硝酰氯冷却,并由气体转变为液体,以便收集于三颈烧瓶中,C正确;
D.实验时先通入氯气,把装置中的空气排出来,防止NO被氧气氧化,D错误;
故选C。
10.碳酸盐加氢制甲酸盐反应 ,可以将捕获的 转化为有价值的化学
品。下列说法错误的是A.标况下22.4L二氧化碳完全转化为甲酸盐转移电子数为
B.室温下,等浓度的 和HCOONa溶液,前者的pH大说明
C.该工艺中NaOH可以循环利用
D.碳酸钠溶液中含碳元素微粒浓度顺序为
【答案】B
【解析】A.标况下22.4L二氧化碳的物质的量为1mol,根据反应方程式可知,二氧化碳完全转化为甲酸
盐中C由+4价变为+2价,1mol二氧化碳完全转化为甲酸盐转移电子数为2N ,选项A正确;
A
B.室温下,等浓度的NaCO 和HCOONa溶液前者的pH大,说明碳酸根离子水解程度大于甲酸根离子,
2 3
越弱越水解,但只能说明 ,选项B错误;
C.该工艺中NaOH吸收 转化为NaCO,再发生反应 ,NaOH可以循
2 3
环利用,选项C正确;
D.碳酸钠为强电解质,完全电离出 离子, 的第一步水解大于第二步水解,且水解是微弱的,故
溶液中含碳元素微粒浓度顺序为 ,选项D正确;
答案选B。
11.以天然气为原料经由合成气(CO、 )制备 的反应转化关系如图所示。设 为阿伏加德罗常
数的值,下列说法正确的是
A.22.4L 中所含的质子总数为10
B.1mol 中含有的 键数为5C.1mol 完全分解为C和 ,转移的电子数为
D.1mol石墨和1mol金刚石中所含共价键数目相同
【答案】B
【解析】A.22.4L ,未给标况,无法计算甲烷的物质的量,A错误;
B.1个 分子中有5个 键,故1mol 中含有的 键数为5 ,B正确;
C.1mol 完全分解为C和 ,转移的电子数为4 ,C错误;
D.1mol石墨中有1.5mol的共价键,1mol金刚石中有2mol的共价键,D错误;
故选B。
12.铁黄 是一类重要的颜料。以烧渣(主要成分为 、 、 等)为原料生产铁黄的流程
如图所示。
下列说法错误的是
A.“磁选”的目的是富集铁
B.“浸渣”的主要成分是二氧化硅
C.“沉铁”时氨水浓度越大,产品的纯度越高
D.“氧化”时发生的反应为
【答案】C
【分析】烧渣经过磁选,富集铁元素,加入硫酸酸浸经过滤得到的滤液中含Fe2+、Fe3+、Cu2+,加入Fe使
Fe3+、Cu2+还原,滤液中加入氨水产生沉淀,然后通入空气加热氧化,经过滤得到FeOOH。
【解析】A.由分析可知,“磁选”的目的是富集铁,故A正确;
B.硫酸酸浸中, 、 与硫酸反应,所以“浸渣”的主要成分是二氧化硅,故B正确;
C.“沉铁”时氨水浓度越大,碱性越强,会生成氢氧化亚铁沉淀,使产品的纯度降低,故C错误;
D.“氧化”时,通入空气加热氧化,使二价铁氧化为三价铁,发生的反应为,故D正确;
故选C。
二、非选择题:本题共4小题,共64分。
13.(16分)第四周期的元素,如:钛( Ti)、铁( Fe)、砷、硒、锌等及其相关化合物在化工、医药、材
22 26
料等领域有着广泛的应用。回答下列问题:
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为 ,与Ti同周期的所有过渡元素的基态原
子中,最外层电子数与钛不同的元素有 种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,
避免生成Fe3+,从结构角度来看Fe2+易被氧化成Fe3+的原因是 。
(3)SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H—S—C≡N)和异硫氰酸( )。
①写出与SCN-互为等电子体的一种微粒 (分子或离子);
②硫氰酸分子中π键和σ键的个数之比为 ;
③异硫氰酸的沸点比硫氰酸沸点高的原因是 。
(4)硒化锌的晶胞结构如图所示,图中x和y点所堆积的原子均为 (填元素符号);若该晶胞密度
为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1,用N 代表阿伏加德罗常数的值,则晶胞参数a为
A
nm。
【答案】(1) 球形 2
(2)Fe3+价电子排布为3d5,半满状态,构型更稳定
(3) N O(或CO、CS、OCN-) 2:3 异硫氰酸可以形成分子间氢键
2 2 2
(4) Zn【解析】(1)基态Ti原子的价层电子排布式为3d24s2,最高能层为第四能层,s电子云轮廓形状为球形;
与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有Cr:3d54s1,Cu:3d104s1,共
两种。
(2)从结构角度来看,Fe2+的价电子排布式是3d6,再失一个电子形成3d5半充满稳定结构,故易被氧化成
Fe3+。
(3)①与SCN-互为等电子体的微粒有NO、CO、CS、OCN-等;
2 2 2
②硫氰酸(H—S—C≡N)中π键和σ键的个数之比为2∶3;
③异硫氰酸分子间可以形成氢键,故其沸点比硫氰酸沸点高。
(4)硒化锌的晶胞结构中x和y点所堆积的原子均为Zn,若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为
为Mg·mol-1,用N 代表阿伏加德罗常数的值,则晶胞参数a为 nm。
A
14.(16分)抗帕金森病药物恩他卡朋的一种合成路线如下(部分反应条件已省略):
已知:
(Ⅰ)R -OH R -X;
1 1
(Ⅱ)R COOH R -COX;
2 2
(Ⅲ)R-COX R -CONH
3 2
请回答:
(1)恩他卡朋含氧官能团的名称是 。
(2)化合物J的结构简式是 。
(3)下列有关说法不正确的是_______。A.恩他卡朋的分子式是C H NO
14 14 2 5
B.反应①②③④⑤涉及取代、氧化、加成等反应类型
C.化合物D与足量H 充分还原后的产物中共含3个手性碳原子
2
D.工业上在低温、CHCl 溶剂条件下实现D→E转化主要为了调控反应的速率
2 2
(4)写出反应⑥的化学方程式 。
(5)设计上图中以甲醛(HCHO)为原料制备化合物G的路线 (用流程图表示,无机试剂任选)。
(6)化合物E同时符合以下条件的同分异构体(不包括立体异构体)中,其结构简式除
外还有 。
①只含有一个环的芳香族化合物
②核磁共振氢谱显示共有3组峰,强度比为2:2:3
③分子中不含有亚硝基(-N=O)和酯基
【答案】(1)羟基、硝基、酰胺基
(2)NH(C H)
2 5 2
(3)ABD
(4) ;
(5)
(6)【分析】经推断可得转化流程如下:
【解析】(1)由结构简式可知,恩他卡朋含氧官能团的名称是:羟基、硝基、酰胺基;
(2)由题意知化合物J的结构简式是:NH(C H);
2 5 2
(3)A. 恩他卡朋的分子式是C H NO,A错误;
14 15 3 5
B. 反应①②③④⑤涉及反应类型无加成反应,B错误;
C. 化合物D与足量H 充分还原后的产物是 ,共含3个手性碳原子,C正确;
2
D. 工业上在低温、CHCl 溶剂条件下实现D→E转化主要为了防止硝酸高温分解以及HNO 和CHCl 挥发,
2 2 3 2 2
D错误;
答案是ABD;
(4)反应⑥的方程式为: ;
(5)以甲醛(HCHO)为原料制备化合物G的路线为:
;
(6)化合物E同时符合只含有一个环的芳香族化合物、核磁共振氢谱显示共有3组峰,强度比为2:2:
3、分子中不含有亚硝基(-N=O)和酯基的同分异构体中,还有:。
15.(16分)高纯碳酸锰广泛应用于电子工业,是制备高性能磁性材料的原料。某化学小组在实验室模拟
用软锰矿粉(主要成分为 )制备 。回答下列问题:
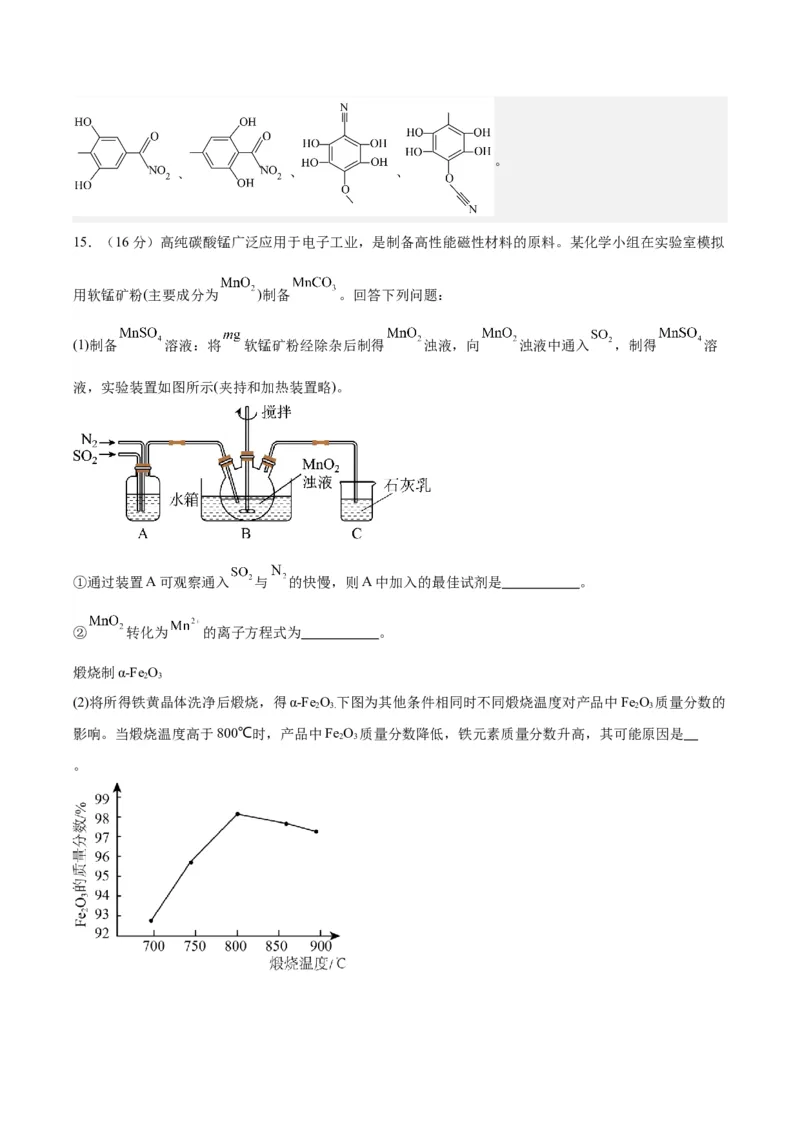
(1)制备 溶液:将 软锰矿粉经除杂后制得 浊液,向 浊液中通入 ,制得 溶
液,实验装置如图所示(夹持和加热装置略)。
①通过装置A可观察通入 与 的快慢,则A中加入的最佳试剂是 。
② 转化为 的离子方程式为 。
煅烧制α-Fe O
2 3
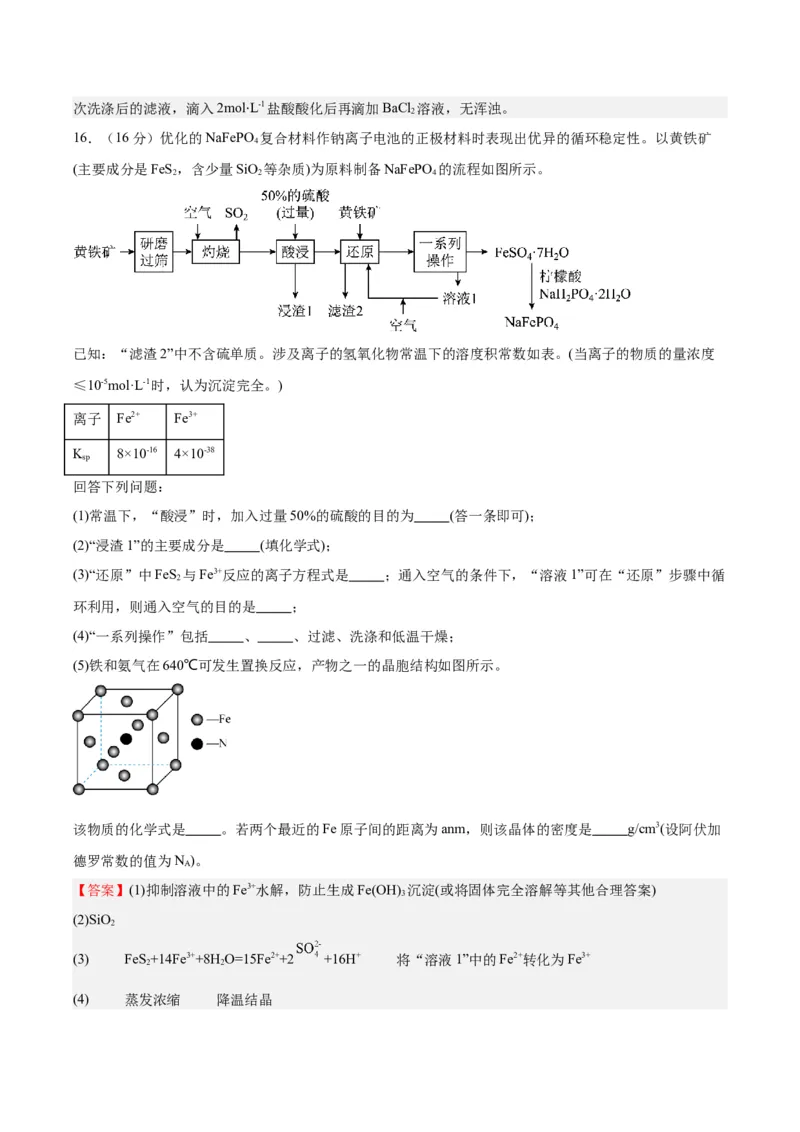
(2)将所得铁黄晶体洗净后煅烧,得α-Fe O 下图为其他条件相同时不同煅烧温度对产品中Fe O 质量分数的
2 3. 2 3
影响。当煅烧温度高于800℃时,产品中Fe O 质量分数降低,铁元素质量分数升高,其可能原因是
2 3
。(3)煅烧 也能生成α-Fe O 实验室以 溶液为原料制备高产率、较纯净的α-Fe O
2 3. 2 3.
已知: 开始沉淀的 ,请补充完整实验方案:在搅拌下 ,将固体干燥,得到纯
净的 放入管式炉内煅烧2h,获得产品α-Fe O (必须使用的试剂: 溶液、
2 3.
盐酸、 溶液、蒸馏水)。
【答案】(1) 饱和NaHSO 溶液 MnO +SO=Mn2++
3 2 2
(2)部分Fe O 分解生成Fe O 或FeO
2 3 3 4
(3)向100mL0.1molL-1FeSO 溶液中缓慢滴加约200mL0.1molL-1NH HCO 溶液,静置后过滤,所得沉淀用
4 4 3
蒸馏水洗涤2~3次⋅:取最后一次洗涤后的滤液,滴入2molL⋅-1盐酸酸化后再滴加BaCl 溶液,无浑浊
2
⋅
【分析】A中通过气体的气泡的快慢来调节气体的通入速率,故该试剂不能和二氧化硫反应,为使SO 尽
2
可能转化完全,就是要使装置中的二氧化硫全部进入烧瓶中,MnO 和二氧化硫反应生成硫酸锰,实验中
2
若将N 换成空气,则空气中的氧气可以将二氧化硫氧化生成硫酸根离子;
2
【解析】(1)①A中通过气体的气泡的快慢来调节气体的通入速率,故该试剂不能和二氧化硫反应,故
A中加入的最佳试剂是饱和NaHSO 溶液;
3
②MnO 和二氧化硫反应生成硫酸锰,反应的离子方程式为MnO +SO=Mn2++ ;
2 2 2
(2)当煅烧温度高于800℃时,产品中Fe O 质量分数降低,铁元素质量分数升高,则表明Fe O 转化为其
2 3 2 3
它的铁的氧化物,同时生成O,其可能原因是:部分Fe O 分解生成Fe O 或FeO,故答案为:部分Fe O
2 2 3 3 4 2 3
分解生成Fe O 或FeO;
3 4
(3)FeSO 生成FeCO,显然需要加入NH HCO ,要得到纯净的FeCO,需要对沉淀进行洗涤、检验最后
4 3 4 3 3
一次洗涤液中是否含有 ,需要加入盐酸酸化的BaCl 溶液,所以完整实验方案:在搅拌下向
2
100mL0.1molL-1FeSO 溶液中缓慢滴加约2000mL0.1molL-1NH HCO 溶液,静置后过滤,所得沉淀用蒸馏
4 4 3
水洗涤2~3次⋅ :取最后一次洗涤后的滤液,滴入2molL⋅-1盐酸酸化后再滴加BaCl 溶液,无浑浊,将固体
2
干燥,得到纯净的FeCO 放入管式炉内煅烧2h,获得产品⋅ α-Fe O,故答案为:向100mL0.1molL-1FeSO 溶
3 2 3 4
液中缓慢滴加约200mL0.1molL-1NH HCO 溶液,静置后过滤,所得沉淀用蒸馏水洗涤2~3次⋅:取最后一
4 3
⋅次洗涤后的滤液,滴入2molL-1盐酸酸化后再滴加BaCl 溶液,无浑浊。
2
16.(16分)优化的NaFePO⋅
4
复合材料作钠离子电池的正极材料时表现出优异的循环稳定性。以黄铁矿
(主要成分是FeS,含少量SiO 等杂质)为原料制备NaFePO 的流程如图所示。
2 2 4
已知:“滤渣2”中不含硫单质。涉及离子的氢氧化物常温下的溶度积常数如表。(当离子的物质的量浓度
≤10-5mol·L-1时,认为沉淀完全。)
离子 Fe2+ Fe3+
K 8×10-16 4×10-38
sp
回答下列问题:
(1)常温下,“酸浸”时,加入过量50%的硫酸的目的为 (答一条即可);
(2)“浸渣1”的主要成分是 (填化学式);
(3)“还原”中FeS 与Fe3+反应的离子方程式是 ;通入空气的条件下,“溶液1”可在“还原”步骤中循
2
环利用,则通入空气的目的是 ;
(4)“一系列操作”包括 、 、过滤、洗涤和低温干燥;
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示。
该物质的化学式是 。若两个最近的Fe原子间的距离为anm,则该晶体的密度是 g/cm3(设阿伏加
德罗常数的值为N )。
A
【答案】(1)抑制溶液中的Fe3+水解,防止生成Fe(OH) 沉淀(或将固体完全溶解等其他合理答案)
3
(2)SiO
2
(3) FeS +14Fe3++8H O=15Fe2++2 +16H+ 将“溶液1”中的Fe2+转化为Fe3+
2 2
(4) 蒸发浓缩 降温结晶(5) Fe N
4
【分析】以黄铁矿(主要成分是FeS,含少量SiO 等杂质)为原料制备NaFePO ,黄铁矿研磨过筛,然后通
2 2 4
入空气焙烧,FeS 转化为氧化铁、SO 气体,然后加入50%的硫酸,得到硫酸铁溶液,SiO 不溶,过滤得
2 2 2
到滤渣1为SiO,滤液加入黄铁矿,发生氧化还原反应,生成硫酸亚铁,过滤除去不溶的SiO,经系列操
2 2
作得到硫酸亚铁晶体,加入柠檬酸、磷酸二氢钠晶体得到产品,据此解答。
【解析】(1)铁离子水解显酸性,常温下,“酸浸”时,加入过量50%的硫酸的目的为抑制溶液中的
Fe3+水解,防止生成Fe(OH)3沉淀(或将固体完全溶解等其他合理答案)。
(2)根据分析, “浸渣1”的主要成分是SiO。
2
(3)“还原”中FeS 与Fe3+反应生成硫酸根离子和亚铁离子,离子方程式为FeS+14Fe3+ +8H O=15Fe2+
2 2 2
+2SO +16H+; “溶液1”中存在亚铁离子,可在“还原”步骤中循环利用,结合反应流程,则通入空气
的目的是将“溶液1”中的Fe2+转化为Fe3+。
(4)“一系列操作”目的是通过硫酸亚铁溶液得到晶体,包括蒸发浓缩、降温结晶、过滤、 洗涤和低温
干燥。
(5)由晶胞结构可知,N原子的个数为1,Fe原子的个数为8 =4,该物质的化学式是Fe N,若两
4
个最近的Fe原子间的距离为anm,则晶胞的边长为 nm,则该晶体的密度是 g/cm3=
g/cm3。