文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷07
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 S 32
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.古代科学典籍富载化学知识,下述之物见其还原性者为
A.胆矾( ):“熬胆矾铁釜,久之亦化为铜”
B.脂水(石油):“高奴县出脂水,……颇似淳漆,燃之如麻,但烟甚浓”
C.胡粉 :“胡粉得雌黄( )而色黑(PbS),盖相恶也”
D.炉甘石( ):“其(炉甘石)底铺薪,发火煅红,……即倭铅(Zn)也”
2.下列有关化学实验的叙述正确的是
A.实验时手指不小心沾上苯酚,立即用70℃以上的热水清洗
B.滴定接近终点时,用锥形瓶内壁触碰滴定管的尖嘴
C.凡是给玻璃仪器加热,都要加垫石棉网,以防止仪器炸裂
D. 晶体中含有少量 杂质,可以用冷却结晶法来提纯
3.下列说法正确的是
A.Mg(OH) 难溶于水,故其饱和溶液不能使酚酞变红
2
B.气态的非金属单质分子均为非极性分子
C.新制氯水放置一段时间后酸性增强
D.白磷和金属钠均可用适量煤油贮存
4.苯炔不对称芳基化反应如下:
下列说法错误的是
A.箭头b所示C-H键比箭头a所示C-H键活泼
B.苯炔不能使酸性高锰酸钾溶液褪色,也不与溴水反应
C.有机物X分子、有机物Y分子均含有1个手性碳原子
D.有机物Y分子中苯环上的一氯代物有三种
5. “点击化学”研究获得2022年诺贝尔化学奖表彰,利用该原理可制得如图所示含 大π键的产物。
已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误的是A.铜离子降低了反应的活化能
B.反应物中黑球元素的电负性强于N
C.产物中α、β两位置的N原子中,α位置的N原子更容易形成配位键
D.反应物中氮氮键比产物中氮氮键的键长短
6.在高温高压的水溶液中, 与 发生反应 ,下
列说法正确的是
A.氧化剂与还原剂的物质的量之比为2:3
B.每生成4.48L ,转移电子数为
C.反应中若有19.7g Au元素被还原,则生成0.05mol
D.若将此反应设计成原电池,则 在正极发生反应
7.下列反应的离子方程式正确的是
A.向NaSO 溶液中滴加稀HNO 溶液: +2H+=SO↑+ H O
2 3 3 2 2
B.用过量氨水吸收废气中的SO :NH ·H O+SO = +
2 3 2 2
C.电解MgCl 水溶液的离子方程式:2Cl- +2H O H↑+Cl↑+ 2OH-
2 2 2 2
D.酸性KCr O 溶液遇NaNO 变成绿色: + 3 + 8H+= 3 + 2Cr3+ +4H O
2 2 7 2 2
8.为探究类卤离子 与 的还原性强弱,某同学进行了如下实验:
①分别配制0.1mol·L-1的KSCN溶液、FeSO 溶液;
4
②向0.1mol·L-1的KSCN溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4
③向0.1mol·L-1的FeSO 溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4 4
④向等体积浓度均为0.1mol·L-1的KSCN和FeSO 混合溶液中滴加酸性KMnO 溶液,溶液先变红后褪色。
4 4
下列说法正确的是
A.实验①中必须用到分液漏斗、锥形瓶等玻璃仪器
B.实验②中 将 还原为
C.实验③中反应的离子方程式为
D.实验④说明还原性:
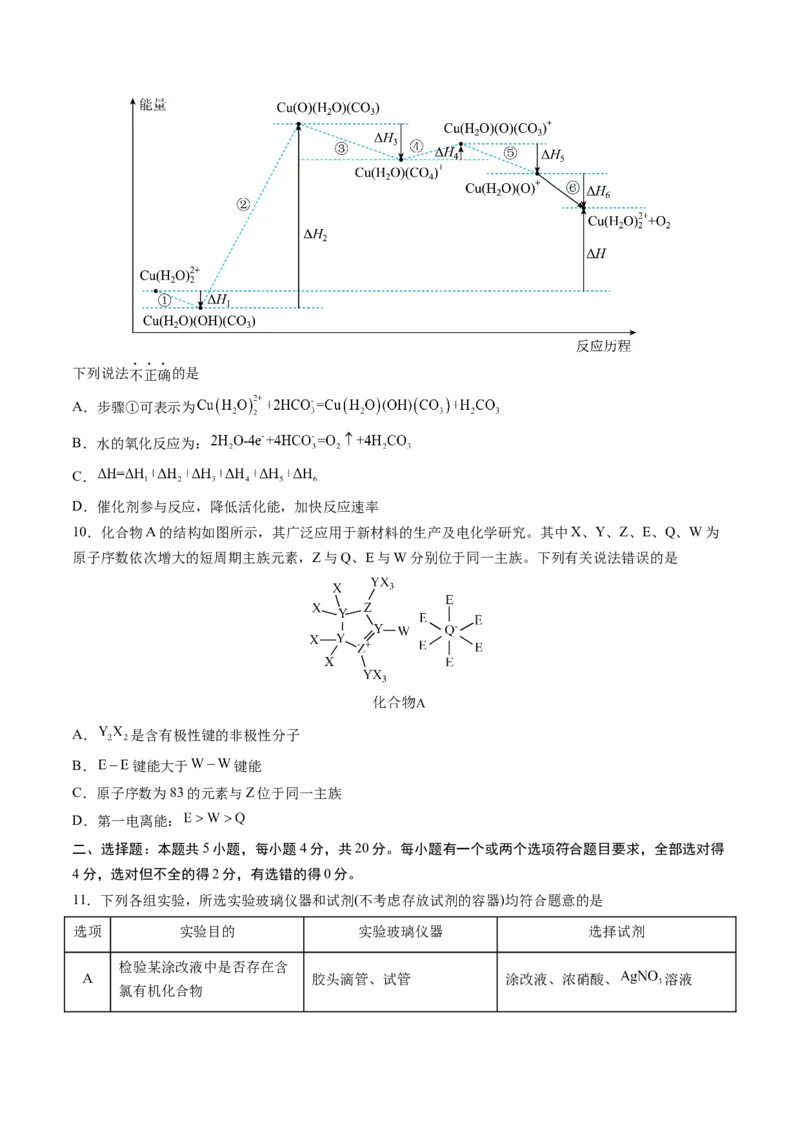
9.光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用 表示]实现在NaHCO 溶液
3
中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:下列说法不正确的是
A.步骤①可表示为
B.水的氧化反应为:
C.
D.催化剂参与反应,降低活化能,加快反应速率
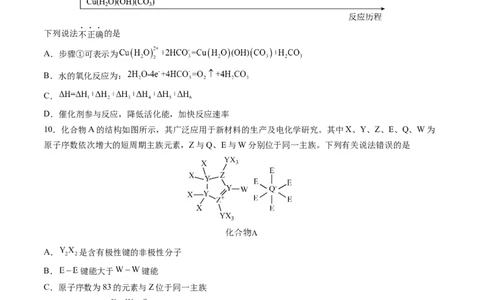
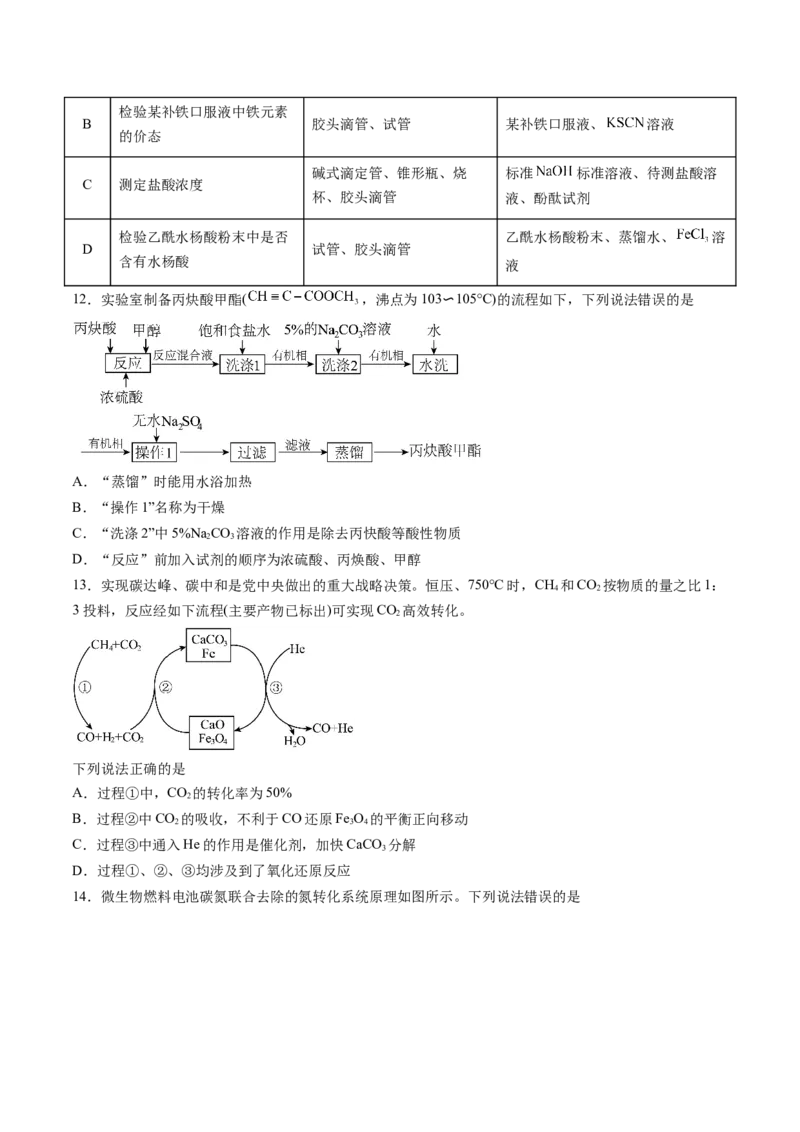
10.化合物A的结构如图所示,其广泛应用于新材料的生产及电化学研究。其中X、Y、Z、E、Q、W为
原子序数依次增大的短周期主族元素,Z与Q、E与W分别位于同一主族。下列有关说法错误的是
A. 是含有极性键的非极性分子
B. 键能大于 键能
C.原子序数为83的元素与Z位于同一主族
D.第一电离能:
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.下列各组实验,所选实验玻璃仪器和试剂(不考虑存放试剂的容器)均符合题意的是
选项 实验目的 实验玻璃仪器 选择试剂
检验某涂改液中是否存在含
A 胶头滴管、试管 涂改液、浓硝酸、 溶液
氯有机化合物检验某补铁口服液中铁元素
B 胶头滴管、试管 某补铁口服液、 溶液
的价态
碱式滴定管、锥形瓶、烧 标准 标准溶液、待测盐酸溶
C 测定盐酸浓度
杯、胶头滴管 液、酚酞试剂
检验乙酰水杨酸粉末中是否 乙酰水杨酸粉末、蒸馏水、 溶
D 试管、胶头滴管
含有水杨酸 液
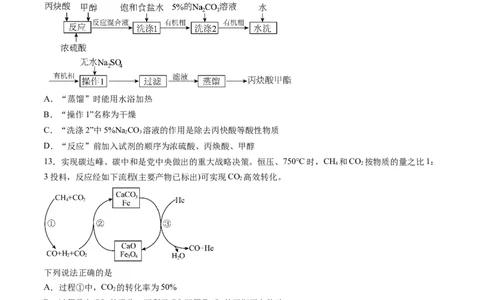
12.实验室制备丙炔酸甲酯( ,沸点为103〜105°C)的流程如下,下列说法错误的是
A.“蒸馏”时能用水浴加热
B.“操作1”名称为干燥
C.“洗涤2”中5%Na CO 溶液的作用是除去丙快酸等酸性物质
2 3
D.“反应”前加入试剂的顺序为浓硫酸、丙焕酸、甲醇
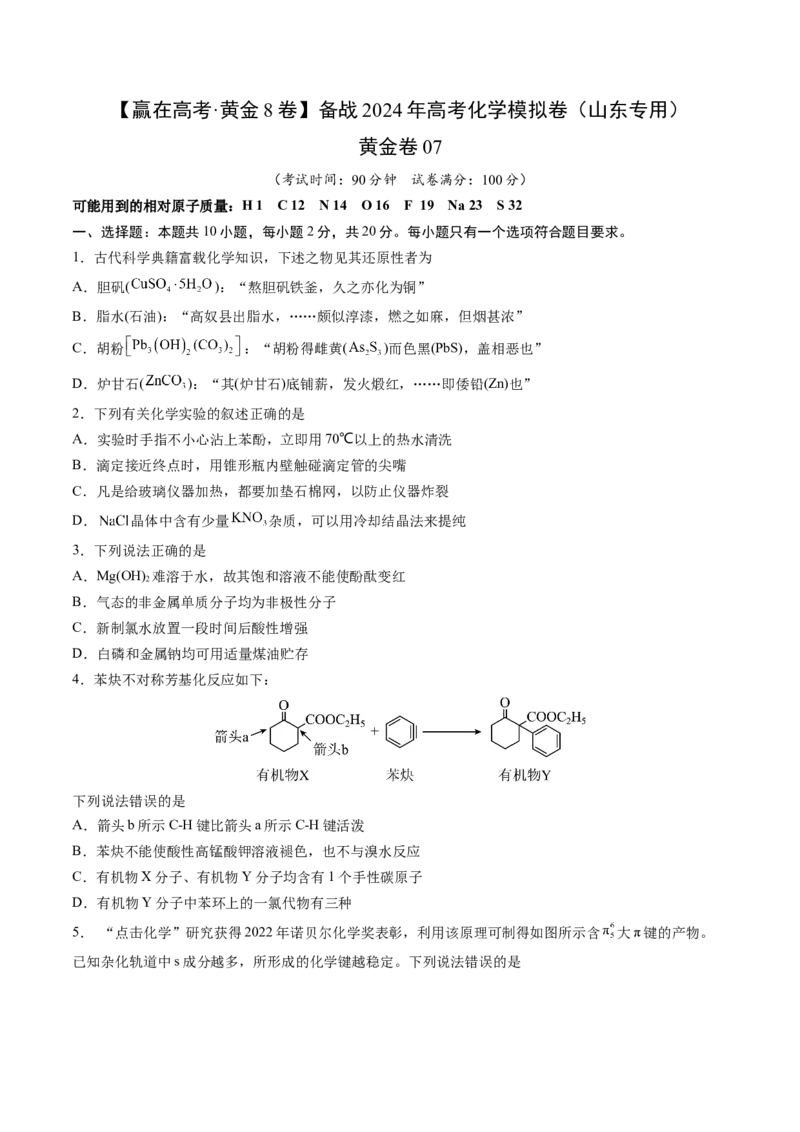
13.实现碳达峰、碳中和是党中央做出的重大战略决策。恒压、750°C时,CH 和CO 按物质的量之比1:
4 2
3投料,反应经如下流程(主要产物已标出)可实现CO 高效转化。
2
下列说法正确的是
A.过程①中,CO 的转化率为50%
2
B.过程②中CO 的吸收,不利于CO还原Fe O 的平衡正向移动
2 3 4
C.过程③中通入He的作用是催化剂,加快CaCO 分解
3
D.过程①、②、③均涉及到了氧化还原反应
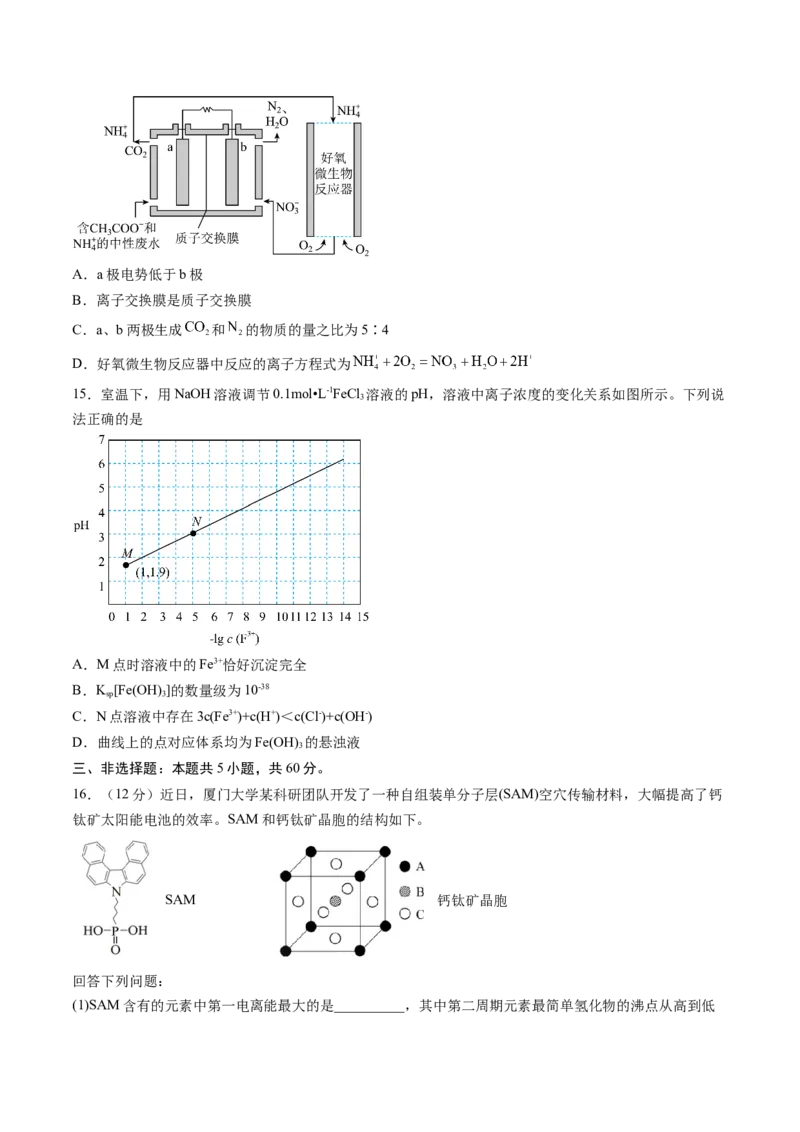
14.微生物燃料电池碳氮联合去除的氮转化系统原理如图所示。下列说法错误的是A.a极电势低于b极
B.离子交换膜是质子交换膜
C.a、b两极生成 和 的物质的量之比为5∶4
D.好氧微生物反应器中反应的离子方程式为
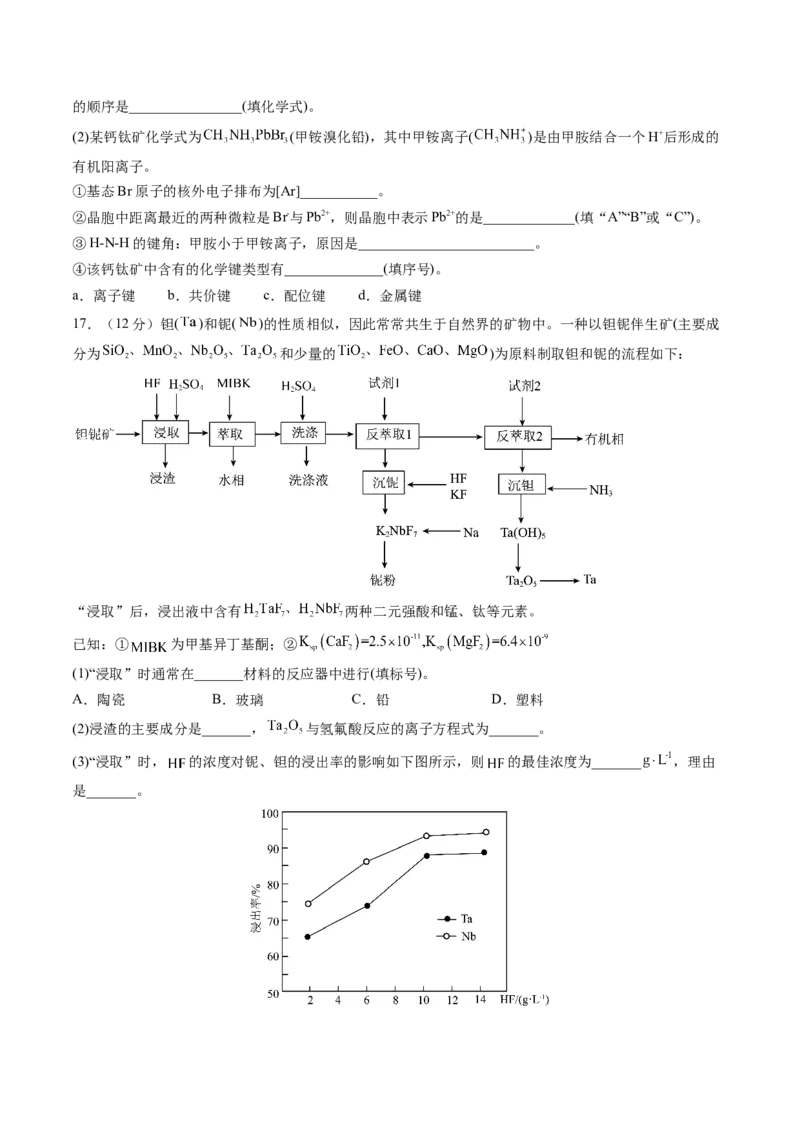
15.室温下,用NaOH溶液调节0.1mol•L-1FeCl 溶液的pH,溶液中离子浓度的变化关系如图所示。下列说
3
法正确的是
A.M点时溶液中的Fe3+恰好沉淀完全
B.K [Fe(OH) ]的数量级为10-38
sp 3
C.N点溶液中存在3c(Fe3+)+c(H+)<c(Cl-)+c(OH-)
D.曲线上的点对应体系均为Fe(OH) 的悬浊液
3
三、非选择题:本题共5小题,共60分。
16.(12分)近日,厦门大学某科研团队开发了一种自组装单分子层(SAM)空穴传输材料,大幅提高了钙
钛矿太阳能电池的效率。SAM和钙钛矿晶胞的结构如下。
SAM 钙钛矿晶胞
回答下列问题:
(1)SAM含有的元素中第一电离能最大的是__________,其中第二周期元素最简单氢化物的沸点从高到低的顺序是________________(填化学式)。
(2)某钙钛矿化学式为 (甲铵溴化铅),其中甲铵离子( )是由甲胺结合一个H+后形成的
有机阳离子。
①基态Br原子的核外电子排布为[Ar]___________。
②晶胞中距离最近的两种微粒是Br-与Pb2+,则晶胞中表示Pb2+的是_____________(填“A”“B”或“C”)。
③H-N-H的键角:甲胺小于甲铵离子,原因是_________________________。
④该钙钛矿中含有的化学键类型有______________(填序号)。
a.离子键 b.共价键 c.配位键 d.金属键
17.(12分)钽( )和铌( )的性质相似,因此常常共生于自然界的矿物中。一种以钽铌伴生矿(主要成
分为 和少量的 )为原料制取钽和铌的流程如下:
“浸取”后,浸出液中含有 两种二元强酸和锰、钛等元素。
已知:① 为甲基异丁基酮;②
(1)“浸取”时通常在_______材料的反应器中进行(填标号)。
A.陶瓷 B.玻璃 C.铅 D.塑料
(2)浸渣的主要成分是_______, 与氢氟酸反应的离子方程式为_______。
(3)“浸取”时, 的浓度对铌、钽的浸出率的影响如下图所示,则 的最佳浓度为_______ ,理由
是_______。(4)金属铌可用金属钠还原 制取,也可用电解熔融的 制取。
①流程中钠热还原法制备铌粉的化学方程式为_______。
②传统的熔盐电解法采用的电解质体系通常为 ,电解总化学反应方程式为_______。
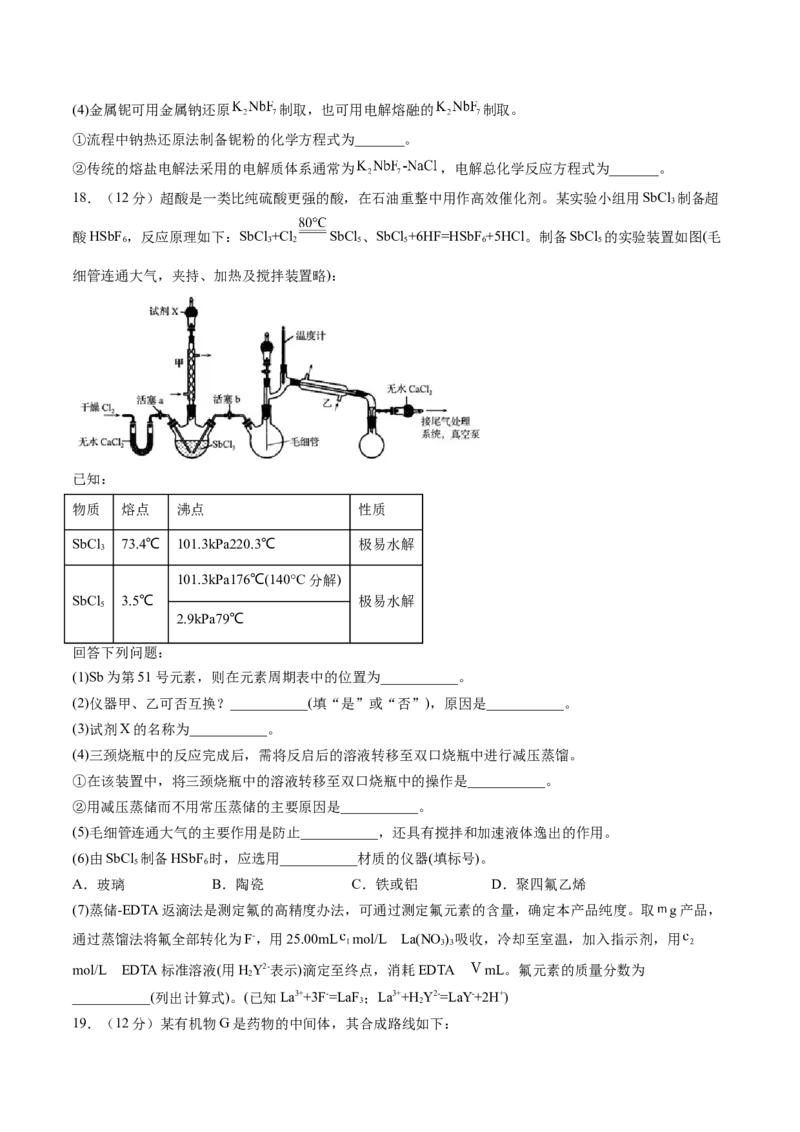
18.(12分)超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组用SbCl 制备超
3
酸HSbF ,反应原理如下:SbCl +Cl SbCl 、SbCl +6HF=HSbF +5HCl。制备SbCl 的实验装置如图(毛
6 3 2 5 5 6 5
细管连通大气,夹持、加热及搅拌装置略):
已知:
物质 熔点 沸点 性质
SbCl 73.4℃ 101.3kPa220.3℃ 极易水解
3
101.3kPa176℃(140°C分解)
SbCl 3.5℃ 极易水解
5
2.9kPa79℃
回答下列问题:
(1)Sb为第51号元素,则在元素周期表中的位置为___________。
(2)仪器甲、乙可否互换?___________(填“是”或“否”),原因是___________。
(3)试剂X的名称为___________。
(4)三颈烧瓶中的反应完成后,需将反启后的溶液转移至双口烧瓶中进行减压蒸馏。
①在该装置中,将三颈烧瓶中的溶液转移至双口烧瓶中的操作是___________。
②用减压蒸储而不用常压蒸储的主要原因是___________。
(5)毛细管连通大气的主要作用是防止___________,还具有搅拌和加速液体逸出的作用。
(6)由SbCl 制备HSbF 时,应选用___________材质的仪器(填标号)。
5 6
A.玻璃 B.陶瓷 C.铁或铝 D.聚四氟乙烯
(7)蒸储-EDTA返滴法是测定氟的高精度办法,可通过测定氟元素的含量,确定本产品纯度。取 g产品,
通过蒸馏法将氟全部转化为F-,用25.00mL mol/L La(NO ) 吸收,冷却至室温,加入指示剂,用
3 3
mol/L EDTA标准溶液(用HY2-表示)滴定至终点,消耗EDTA mL。氟元素的质量分数为
2
___________(列出计算式)。(已知La3++3F-=LaF ;La3++H Y2-=LaY-+2H+)
3 2
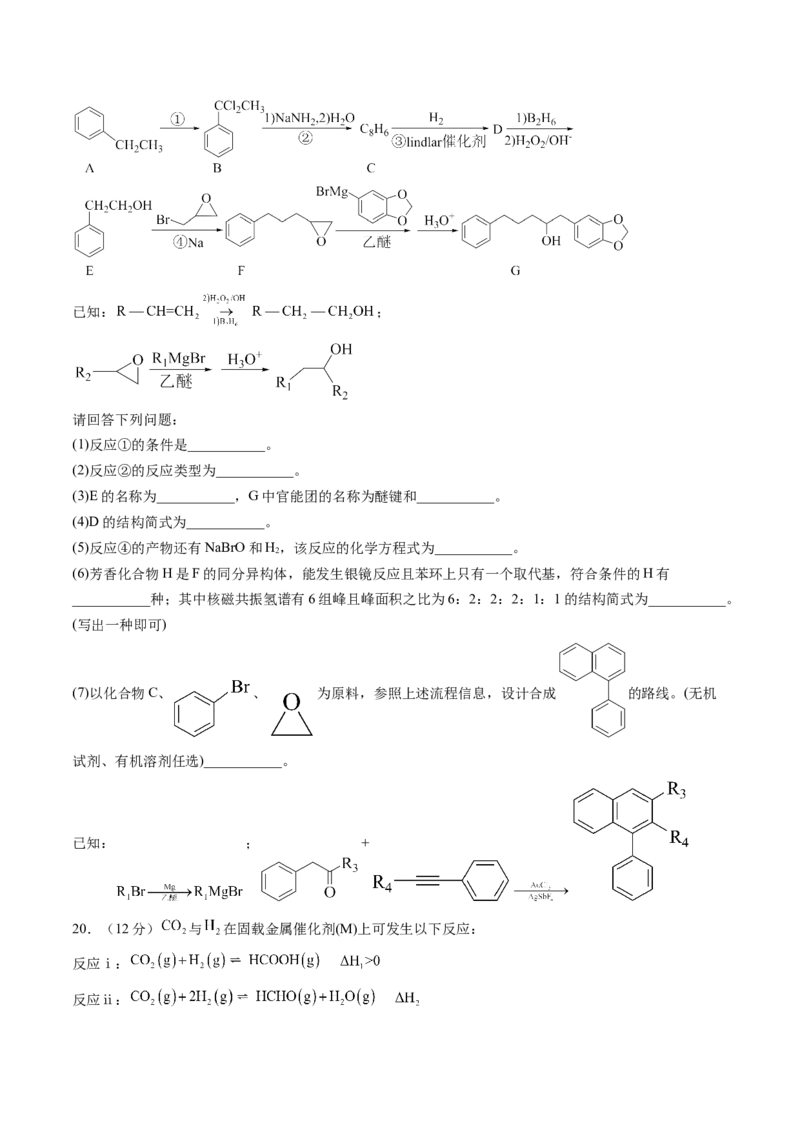
19.(12分)某有机物G是药物的中间体,其合成路线如下:已知: ;
请回答下列问题:
(1)反应①的条件是___________。
(2)反应②的反应类型为___________。
(3)E的名称为___________,G中官能团的名称为醚键和___________。
(4)D的结构简式为___________。
(5)反应④的产物还有NaBrO和H,该反应的化学方程式为___________。
2
(6)芳香化合物H是F的同分异构体,能发生银镜反应且苯环上只有一个取代基,符合条件的H有
___________种;其中核磁共振氢谱有6组峰且峰面积之比为6:2:2:2:1:1的结构简式为___________。
(写出一种即可)
(7)以化合物C、 、 为原料,参照上述流程信息,设计合成 的路线。(无机
试剂、有机溶剂任选)___________。
已知: ; +
20.(12分) 与 在固载金属催化剂(M)上可发生以下反应:
反应ⅰ:
反应ⅱ:反应ⅲ:……
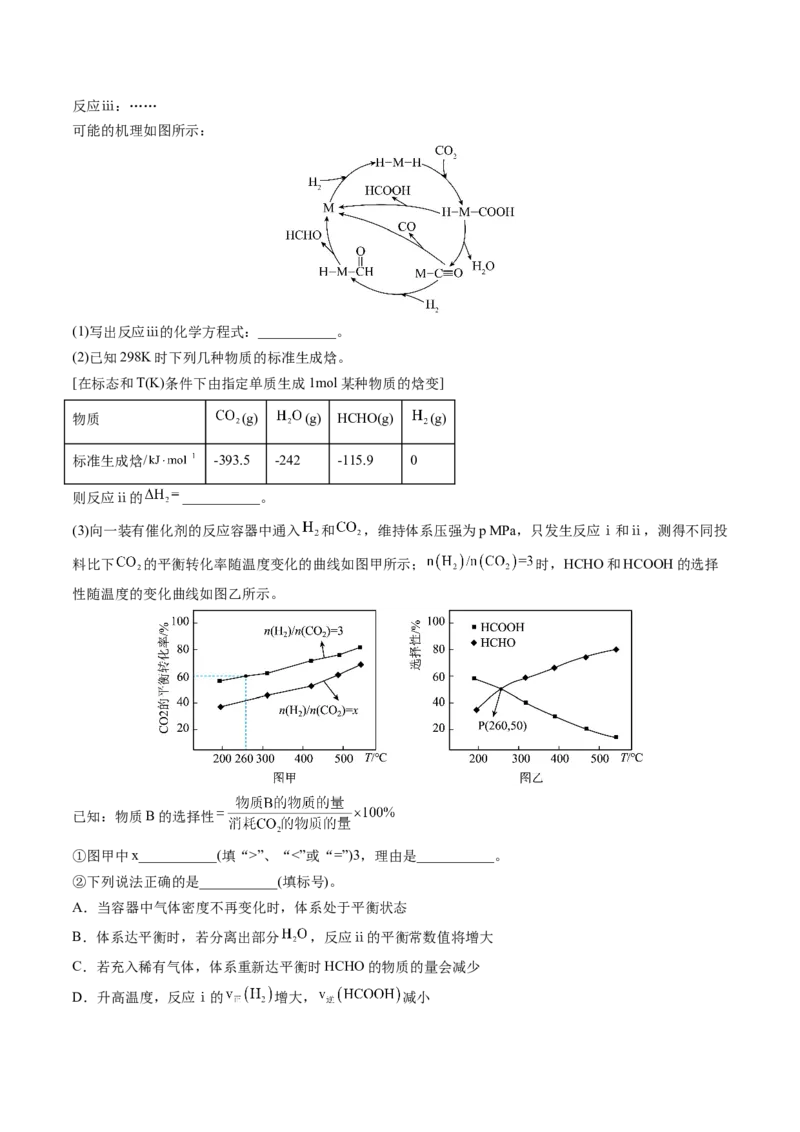
可能的机理如图所示:
(1)写出反应ⅲ的化学方程式:___________。
(2)已知298K时下列几种物质的标准生成焓。
[在标态和T(K)条件下由指定单质生成1mol某种物质的焓变]
物质 (g) (g) HCHO(g) (g)
标准生成焓/ -393.5 -242 -115.9 0
则反应ⅱ的 ___________。
(3)向一装有催化剂的反应容器中通入 和 ,维持体系压强为p MPa,只发生反应ⅰ和ⅱ,测得不同投
料比下 的平衡转化率随温度变化的曲线如图甲所示; 时,HCHO和HCOOH的选择
性随温度的变化曲线如图乙所示。
已知:物质B的选择性
①图甲中x___________(填“>”、“<”或“=”)3,理由是___________。
②下列说法正确的是___________(填标号)。
A.当容器中气体密度不再变化时,体系处于平衡状态
B.体系达平衡时,若分离出部分 ,反应ⅱ的平衡常数值将增大
C.若充入稀有气体,体系重新达平衡时HCHO的物质的量会减少
D.升高温度,反应ⅰ的 增大, 减小③P点对应的体系中消耗了2.7mol ,则体系中充入的 ___________mol,此时反应ⅰ的平衡常
数 ___________。(列出计算式即可) 为以分+压表示的平衡常数,分压=总压×物质的量分数)。