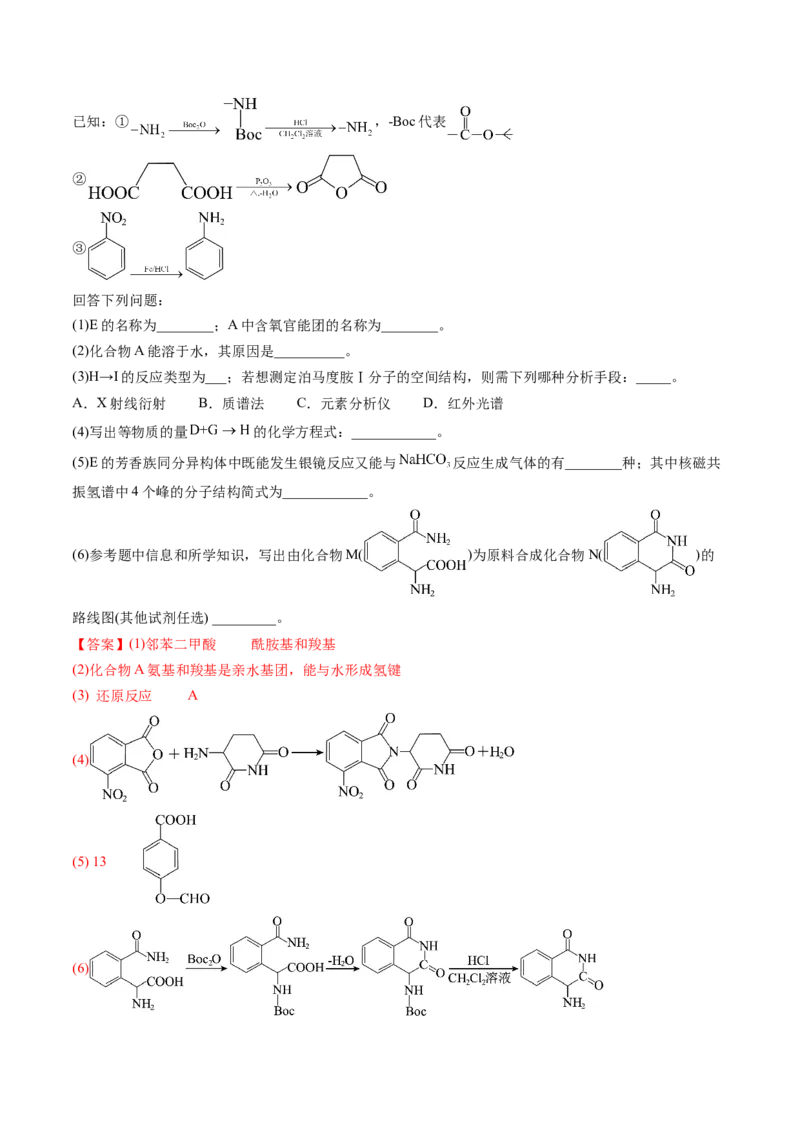
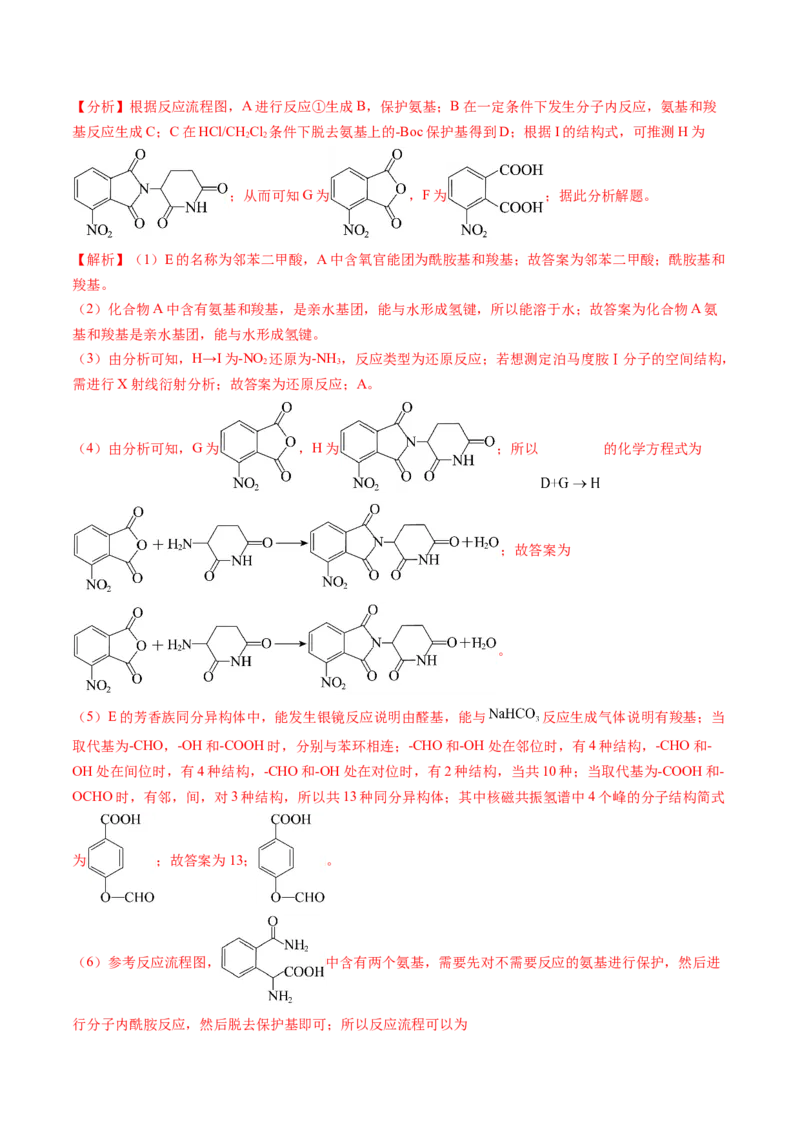
文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷08
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 S 32
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.我国在航天、航海等领域取得重大进展。下列说法不正确的是
A.“天问一号”火星车的热控保温材料——纳米气凝胶,可产生丁达尔效应
B.北斗导航卫星的芯片与光导纤维的主要成分相同
C.海洋开发走向“深蓝时代”,大型舰船的底部常镶嵌锌块,防止船底腐蚀
D.航空母舰“福建舰”,相控阵雷达使用的碳化硅属于新型无机材料
【答案】B
【解析】A.纳米气凝胶为胶体,可发生丁达尔效应,A项正确;
B.芯片为Si,而光导纤维为SiO,B项错误;
2
C.加入锌块与Fe形成原电池,Zn作负极发生反应,而Fe作正极被保护,C项正确;
D.碳化硅高硬度和高熔点,耐腐蚀的新型无机非金属材料,D项正确;
故选B。
2.某实验小组用如下实验用品检验黑木耳中铁元素。下列说法错误的是
A.将黑木耳灼烧灰化,选用的仪器有①、②、⑥、⑦和⑨
B.用浓硝酸溶解木耳灰并获得滤液,选用的仪器有④、⑤、⑦和⑩
C.检验滤液中的 ,选用③、⑧和⑩
D.利用上述仪器也可进行硫酸铜结晶水含量的测定
【答案】D
【解析】A.将黑木耳灰化,应该在坩埚中灼烧,装置图为 ,用的仪器有①、②、⑥、⑦
和⑨,故A正确;B.用用胶头滴管把浓硝酸滴入木耳灰,使木耳灰溶解,用过滤的方法获得滤液,过滤装置图为
,选用的仪器有④、⑤、⑦和⑩,故B正确;
C.检验滤液中的 ,取少量滤液于试管中,用胶头滴管滴加几滴KSCN溶液,若溶液变红说明含有
Fe3+,选用③、⑧和⑩,故C正确;
D.利用上述仪器进行硫酸铜结晶水含量的测定,需要称重,缺少天平,故D错误;
选D。
3.下列关于元素及其化合物的性质说法不正确的是
A.浓硫酸与蔗糖反应,观察到蔗糖变黑,体现了浓硫酸的脱水性
B.硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处
C.燃油发动机产生的 、 与 反应能生成 和 ,因此可以直接排放
D.铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物
【答案】C
【解析】A.浓硫酸与蔗糖反应,观察到蔗糖变黑变为碳,体现了浓硫酸的脱水性,A正确;
B.硝酸见光受热易分解为二氧化氮和氧气,一般保存在棕色试剂瓶中,放置在阴凉处,B正确;
C. 、 与 反应需要在催化剂作用下转化为无毒的气体,因此需要催化转化后排放,C错误;
D.铝与酸、碱均会反应,故铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物,D正确;
故选C。
4.设 为阿伏伽德罗常数的值,下列说法不正确的是
A.标准状况下, 乙烯中含有的 键数目为
B. 的醋酸溶液中含有的 数目为
C. 与足量单质硫充分反应,转移的电子数为
D. 与足量 溶液充分反应,生成 分子的数目为
【答案】B
【解析】A.标准状况下, 乙烯为 ,含有的 键数目 ,A项正确;
B.醋酸为弱酸,故 的醋酸溶液中含有的 数目小于 ,B项错误;
C. 为 ,由于生成的产物为 ,故转移的电子数为 ,C项正确;
D. 与足量 溶液充分反应,生成 的数目为 ,D项正确;
故选B。5.铝的卤化物AlX(X=Cl、Br、I)气态时以Al X 双聚形态存在,下列说法错误的是
3 2 6
性质 AlF AlCl AlBr AlI
3 3 3 3
熔点/℃ 1290 192.4 97.8 189.4
沸点/℃ 1272 180 256 382
A.AlF 晶体类型与其他三种不同
3
B.1molAl Cl 中所含配位键数目为4N
2 6 A
C.Al X 中Al、X原子价电子层均满足8e-结构
2 6
D.AlCl 熔点高于AlBr 原因是Cl的电负性大于Br,具有一定离子晶体特征
3 3
【答案】B
【解析】A.AlF 为离子晶体,其他三个为分子晶体,A正确;
3
B.每个Al与周围的三个Cl共用一对电子,与另一个Cl形成配位键,故1molAl Cl 中所含配位键数目为
2 6
2N ,B错误;
A
C.每个Al与周围的三个Cl共用一对电子,与另一个Cl形成配位键,均满足8电子结构,C正确;
D.AlCl 熔点高于AlBr 原因是Cl的电负性大于Br,具有一定离子晶体特征,D正确;
3 3
故选B。
6.下列图示装置能达到实验目的的是
A B C D
验证1-溴丁烷发生消去反应的产物中有1-丁 从 溶液中获得
碱式滴定管排气泡 分离碘单质
烯 晶体
【答案】B
【解析】A.碱式滴定管排气泡时,尖嘴应该朝上,选项A错误;
B.过滤可从含碘的悬浊液中分离碘单质,选项B正确;
C.挥发的乙醇也可以使酸性高锰酸钾溶液褪色,干扰1-丁烯的检验,选项C错误;
D.在加热过程中, 发生水解,不能得到 晶体,选项D错误;
答案选B。
7.最新研究发现化合物N可以提高生物检测的速度和灵敏度。一种合成化合物N的方法如下图所示。下列说法正确的是
A.化合物M可发生加成和取代反应
B.化合物M的二氯代物有2种
C.化合物N中所有原子均可共面
D.化合物N与乙酸互为同分异构体
【答案】D
【解析】A.化合物M中没有不饱和的碳碳双键或者碳氧双键,所以不能发生加成反应,A错误;
B.根据M分子的结构,二氯代物有3种,B错误;
C.化合物N含有2个饱和碳原子,不可能所有的原子共平面,C错误;
D.化合物N的分子式为: ,与乙酸 互为同分异构体,D正确;
故选D。
8.BHET是一种重要的化工原料,我国科学家利用聚对苯二甲酸类塑料 制备对苯二甲酸双羟乙酯
的化学反应如图所示。下列叙述不正确的是
A. 中元素的电负性:
B. 中所有原子可能处于同一平面
C. 中碳原子和氧原子的杂化方式均为
D. 和 均能发生水解反应和加成反应
【答案】B
【解析】A. 中含C、H、O三种元素,其电负性为: ,A项正确;
B. 中含有成单键的碳原子,所有原子不可能处于同一平面,B项错误;
C. 中碳原子和氧原子的杂化方式均为 ,C项正确;
中均含有酯基和苯环,均能发生水解反应和加成反应,D项正确;
故选B。
9. 与砂糖混用为补血剂。合成 工艺流程如下:已知:“还原”工序中不生成S单质。下列说法错误的是
A.“焙烧”时,空气和 逆流可提高焙烧效率
B.“焙烧”过程中氧化剂和还原剂的物质的量之比为11∶4
C.“还原”工序中,反应的离子方程式为
D.“沉铁”时, 与 结合生成 ,促进了 的电离
【答案】C
【分析】 在空气中焙烧生成氧化铁,氧化铁加入稀硫酸酸浸,得到硫酸铁溶液,加入 还原,再加
入碳酸氢铵沉铁,得到碳酸亚铁。
【解析】A.“焙烧”时,空气和 逆流可增大接触面积,提高焙烧效率,选项A正确;
B.“焙烧”过程中发生反应4FeS+11O 2Fe O+8SO,其中氧气为氧化剂,二硫化亚铁为还原剂,则
2 2 2 3 2
氧化剂和还原剂的物质的量之比为11:4,选项B正确;
C.“还原”工序中,无S单质生成,反应的离子方程式为 ,选项
C错误;
D.“沉铁”时, 与 结合生成 ,使得碳酸根离子浓度减小,平衡 正向
移动,促进了 的电离,选项D正确;
故选C。
10. X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对应
水化物反应生成盐; Y元素原子的核外电子只有8种运动状态;Z为短周期金属元素,其简单离子的半径
在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
A.第一电离能: X>Y> Z B.键角 >
C.W为第四周期d区元素 D.X和Y的最简单气态氢化物中,前者更易液化
【答案】D
【分析】X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对
应水化物反应生成盐;X是N元素;Y元素原子的核外电子只有8种运动状态,Y是O元素;Z为短周期
金属元素,其简单离子的半径在同周期中最小,Z是Al元素;基态W原子的未成对电子数为6,W是Cr
元素。
【解析】A.Al是金属元素,第一电离能最小,N原子2p能级半充满,结构稳定,第一电离能大于同周期
相邻元素,所以第一电离能: N>O>Al,故A正确;
B. 中N原子价电子对数为 ,无孤电子对; 中N原子价电子对数为 ,有1个孤电
子对,所以键角 > ,故B正确;
C.W是Cr元素,价电子排布为3d54s1,为第四周期d区元素,故C正确;
D.NH 常温下为气体,HO常温下为液体,HO的沸点大于NH ,HO更易液化,故D错误;
3 2 2 3 2选D。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.实验I浑浊不消失,实验Ⅱ和Ⅲ中浊液变澄清。
下列分析不正确的是
A. 浊液中:
B.实验Ⅱ中 溶液抑制了 的水解
C.实验Ⅲ中发生了反应:
D.以上实验说明 溶液中 既存在电离平衡又存在水解平衡
【答案】B
【解析】A.实验l浑浊不消失,NaHCO 浊液为饱和溶液,pH= 8显碱性,说明溶液中碳酸氢根离子水解
3
程度大于其电离程度,溶液中离子浓度关系: ,选项A正确;
B.氯化铵溶液中铵根离子水解显酸性,促进碳酸氢根离子的水解,碳酸氢钠溶解,溶液变澄清,选项B
错误;
C.实验Ⅲ中浊液变澄清,说明加入氨水和碳酸氢根离子电离出的氢离子反应,促进碳酸氢根离子电离平
衡正向进行,反应的化学方程式为: 2NaHCO + 2NH ·H O=(NH )CO + Na CO + 2H O,选项C正确;
3 3 2 4 2 3 2 3 2
D.实验Ⅱ说明碳酸氢根离子存在水解平衡,实验I中说明存在碳酸氢根离子的电离平衡,以上实验说明
NaHCO 溶液中 既存在电离平衡又存在水解平衡,选项D正确;
3
答案选B。
12.钛酸钡 是电子陶瓷基础母体原料,超细微 粉体的制备方法如下。
已知:
下列说法不正确的是
A.向 中先加入 ,可防止其水解生成
B.得到溶液1的反应:C.加入过量氨水,有利于提高 的产率
D.“煅烧”得到的气体A是 和 的混合物
【答案】C
【分析】 与草酸先生成TiO(C O) ,再向体系中加入钡离子,发生反应的离子方程式为:TiO(C O)
2 4 2 4
+Ba2++4H O=BaTiO(C O)·4H O↓,生成的BaTiO(C O)·4H O再经过隔绝空气煅烧,得到BaTiO ,同
2 2 4 2 2 2 4 2 2 3
时得到CO、CO 及水蒸气,涉及的方程式为BaTiO(C O)·4H O BaTiO +2CO↑+2CO ↑+4H O,据此分
2 2 4 2 2 3 2 2
析解答。
【解析】A.根据已知信息可知,四氯化钛水解显酸性,所以向 中先加入 ,可抑制其水解,从
而防止生成 ,A正确;
B.根据分析可知,得到溶液1的反应: ,
B正确;
C.加入过量氨水,则溶液碱性过强,可能会生成TiO(OH)+,从而降低TiO(C O) 的浓度,不利于提高
2 4
的产率,C错误;
D.根据分析,结合原子守恒可知“煅烧”得到的气体A是 和 的混合物,D正确;
故选C。
13.以[PIMPS]H PW O 为催化剂,可实现苯甲硫醚高效催化氧化,其反应机理如图所示。下列说法错误
2 12 40
的是
A.当有1mol苯甲硫醚被氧化为最终产物时共转移4mole-
B.HO 分子参加的反应一定有电子转移
2 2C.苯甲硫醚的催化氧化最终生成 , 催化氧化过程中温度不宜过高
D.催化剂中的-W=O部位与HO 作用生成活性过氧物
2 2
【答案】AB
【解析】A.根据图示,当有1mol苯甲硫醚被氧化为最终产物,消耗2molH O,HO 中O元素化合价
2 2 2 2
由-1降低为-2,共转移2mole-,故A错误;
B. 与HO 反应生成 ,元素化合价不变,没有有电子转移,故B错误;
2 2
C.双氧水加热易分解,所以催化氧化过程中温度不宜过高,故C正确;
D.催化剂中的-W=O部位与HO 作用生成活性过氧物 ,故D正确;
2 2
选AB。
14.目前可采用“双极膜组”电渗析法淡化海水,同时获得副产品A和B,模拟工作原理如图所示。M和
N为离子交换膜,在直流电作用下,双极阴阳膜(BP)复合层间的 解离成 和 ,作为 和 的离
子源。下列说法正确的是
A.X电极为阴极,电极反应式为2Cl-+2e-=Cl
2
B.M为阳离子交换膜,N为阴离子交换膜,BP膜的作用是选择性通过Cl-和Na+
C.每生成5.6L气体a,理论上获得副产品A和B各0.5mol
D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)
【答案】AD
【分析】由BP双极膜中H+、OH-移动方向可知:X电极为电解池的阳极,电极反应式为:2 +2e-=Cl,
2
Y电极为阴极,电极反应式为:2H++2e-=H ,电解总反应为: ,精制食盐水
2
中钠离子经过M离子交换膜移向产品A室,与BP双极膜中转移过来的氢氧根结合生成氢氧化钠,所以M膜为阳离子交换膜,盐室中氯离子经过N离子交换膜移向产品B室,与BP双极膜中转移过来的氢离子结
合生成氯化氢,所以N为阴离子交换膜。
【解析】A.由图中氢氧根移动方向可知X电极为阳极,电极反应式为:2 +2e-=Cl,A正确;
2
B.由题意可知,精制食盐水中钠离子经过M离子交换膜移向产品A室,与BP双极膜中转移过来的氢氧
根结合生成氢氧化钠,所以M膜为阳离子交换膜,盐室中氯离子经过N离子交换膜移向产品B室,与BP
双极膜中转移过来的氢离子结合生成氯化氢,所以N为阴离子交换膜,BP双极膜的作用是选择性通过氢
离子和氢氧根离子,B错误;
C.阳极反应式为:2 +2e-=Cl,电路中每生成标况下5.6L气体氯气,其物质的量为0.25mol,转移电子
2
0.5mol,理论上获得副产品A(氢氧化钠溶液)和B(氯化氢溶液)各0.5mol,需标明标准状况,C错误;
D.“双极膜组”电渗析法从氯化钠溶液中获得酸(HCl)和碱(NaOH),由此可知:也可从M溶液制备
相应的酸(HX)和碱(MOH),D正确;
故选AD。
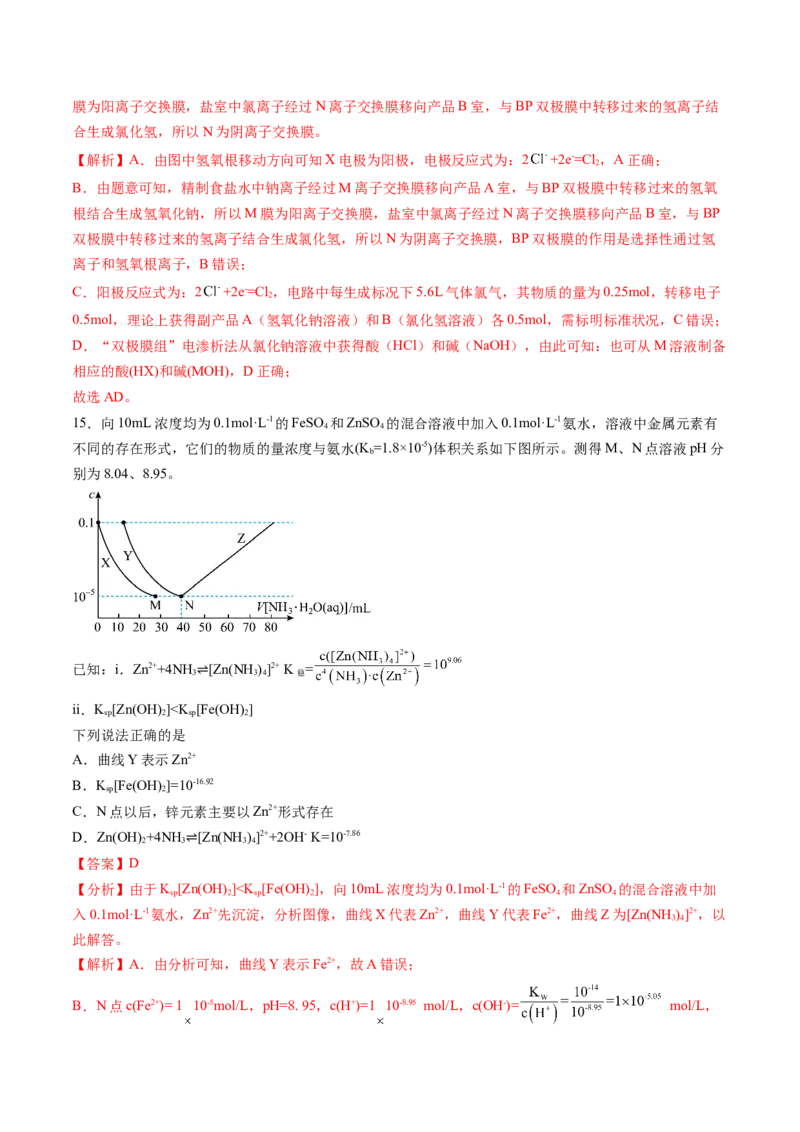
15.向10mL浓度均为0.1mol·L-1的FeSO 和ZnSO 的混合溶液中加入0.1mol·L-1氨水,溶液中金属元素有
4 4
不同的存在形式,它们的物质的量浓度与氨水(K =1.8×10-5)体积关系如下图所示。测得M、N点溶液pH分
b
别为8.04、8.95。
已知:i.Zn2++4NH [Zn(NH )]2+ K =
3 3 4 稳
⇌
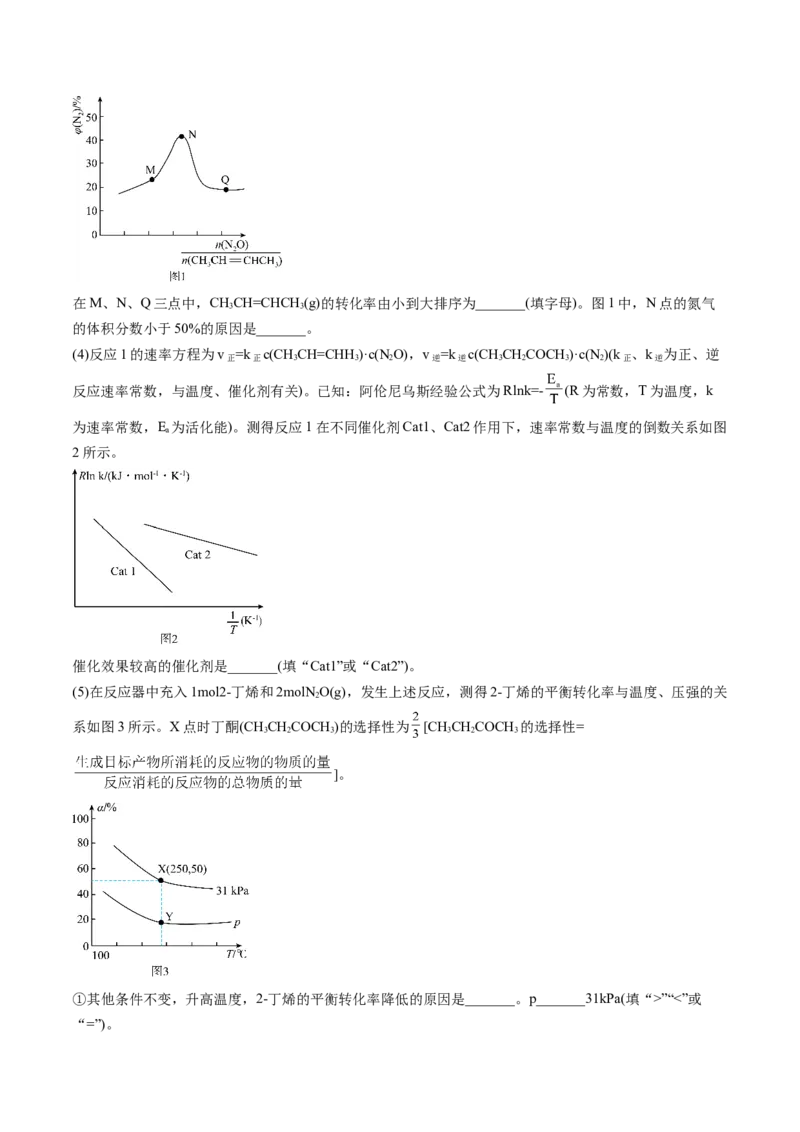
ii.K [Zn(OH) ]”“<”或
“=”)。②Y点反应1的压强平衡常数K 为______________(结果保留两位有效数字)。
p
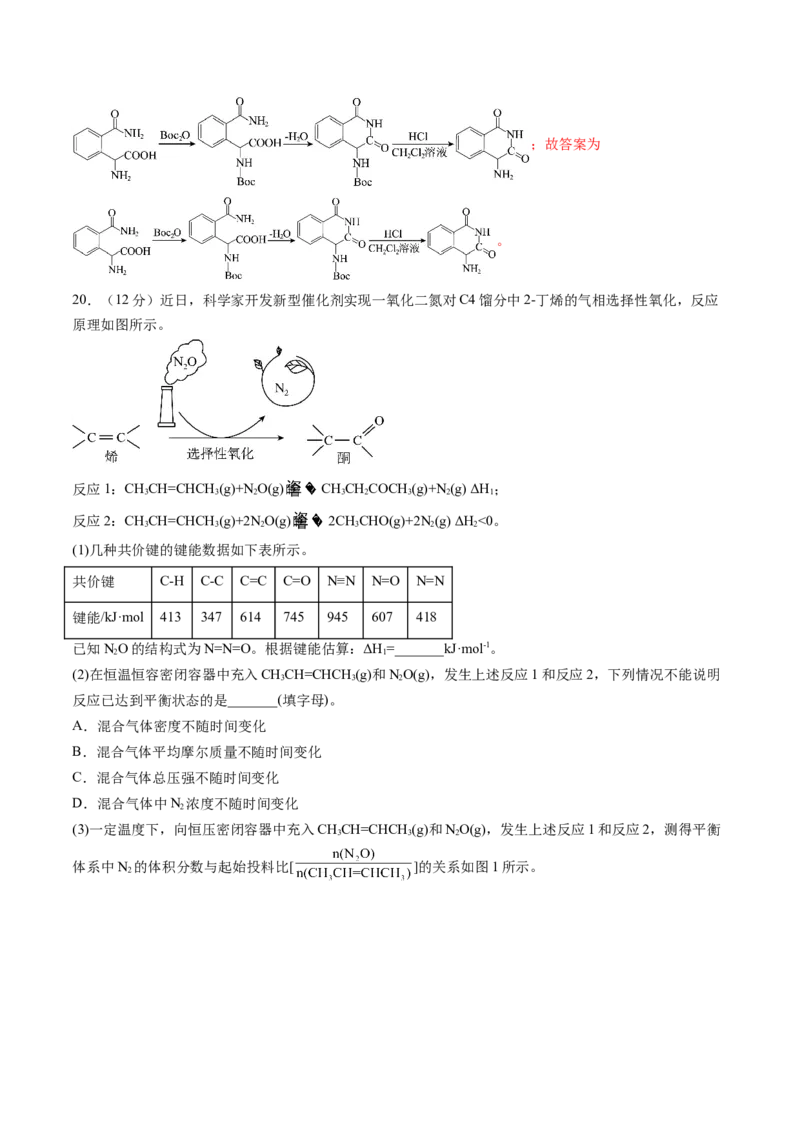
(6)以熔融碳酸盐(如KCO)为电解质,丁烯(C H)/空气燃料电池的能量转化率较高。电池反应为
2 3 4 8
C H+6O =4CO +4H O负极反应式为_______。
4 8 2 2 2
【答案】(1)-398
(2)A
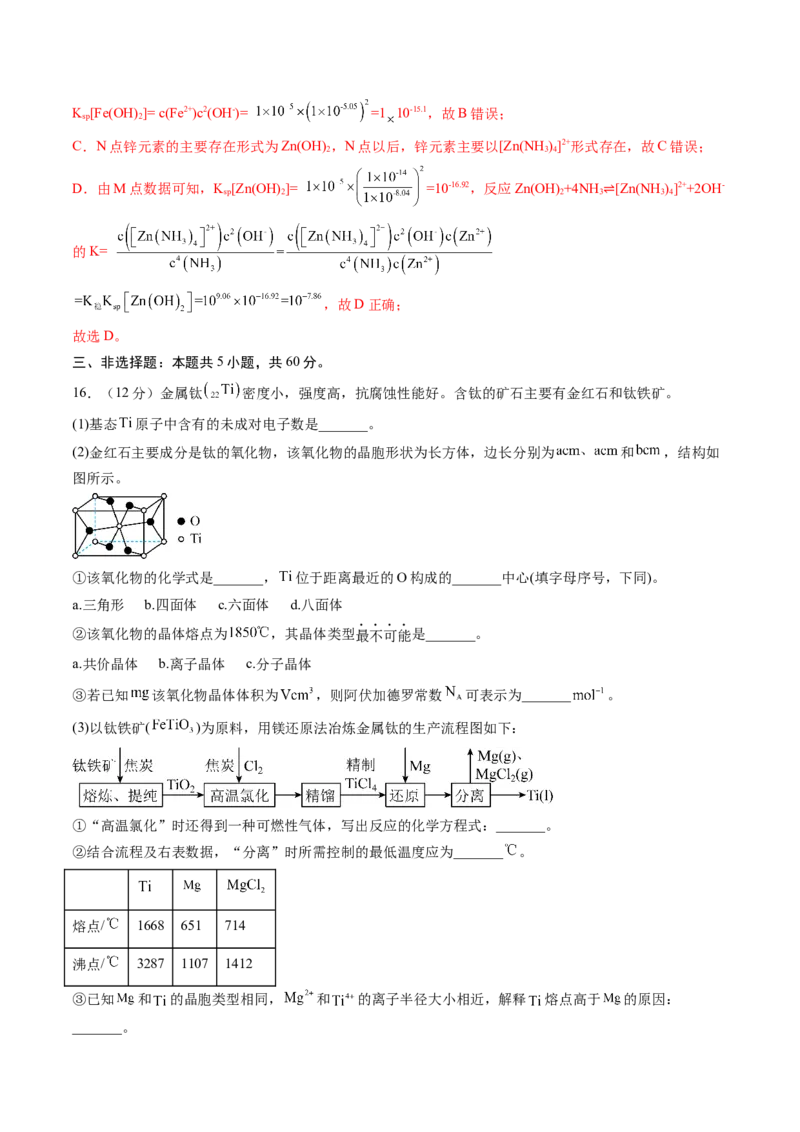
(3) M 0.33
(6)C H-24e-+12 =16CO +4H O
4 8 2 2
【解析】(1)NO的结构式为N=N=O,反应热等于断键吸收的热量减去成键放出的热量,则
2
CHCH=CHCH (g)+NO(g) CHCHCOCH (g)+N(g) ΔH =8 413 kJ·mol+2 347 kJ·mol+614 kJ·mol+418
3 3 2 3 2 3 2 1
kJ·mol+607 kJ·mol-8 413 kJ·mol-3 347 kJ·mol-745 kJ·mol-945 kJ·mol=-398 kJ·mol。
(2)A.反应过程中混合气体的总质量和总体积都不变,密度是定值,当混合气体密度不随时间变化时,
不能说明反应达到平衡,故A选;
B.反应过程中混合气体的总质量不变,总物质的量增大,则混合气体平均摩尔质量减小,当混合气体平
均摩尔质量不随时间变化时,说明反应达到平衡,故B不选;
C.反应过程中混合气体的总物质的量增大,混合气体压强增大,当混合气体总压强不随时间变化时,说
明反应达到平衡,故C不选;
D.混合气体中N 浓度不随时间变化时,说明正逆反应速率相等,反应达到平衡,故D不选;
2
故选A。
(3)CHCH=CHCH (g)的物质的量越多,反应1和反应2平衡正向移动,但CHCH=CHCH (g)的转化率减
3 3 3 3
小,则在M、N、Q三点中,CHCH=CHCH (g)的转化率由小到大排序为M31kPa;
②X点和Y点温度相同,二者平衡常数的压强平衡常数K 相等,计算X点的压强平衡常数K 即可,根据
p p
已知条件列出“三段式”:X点时丁酮(CHCHCOCH )的选择性为 ,则 = ,2-丁烯的转化率 =0.5,得x= ,y= ,反
3 2 3
应1的平衡常数K= =0.33。
p
(6)电池反应为C H+6O =4CO +4H O中,C H 在负极失去电子生成CO,电极方程式为:C H-24e-+12
4 8 2 2 2 4 8 2 4 8
=16CO +4H O。
2 2