文档内容
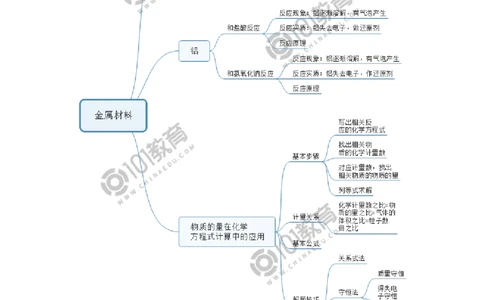
金属材料(1)
重难点 题型 分值
1. 考查合金的概念,性质及用途
2. 通过对化学方程式多角度地理解,提高对各种化学量
相互转化的运用能力;
重点 3. 通过对例题的分析、讲解,培养综合运用知识和综合
计算能力; 填空 8-10分
4. 通过对计算题格式、方法、思维过程的规范化要求、
示范和训练,培养严谨、认真的科学态度。
物质的量、物质的量浓度、气体摩尔体积应用于化学方
难点
程式的计算。
第1页核心知识点一:
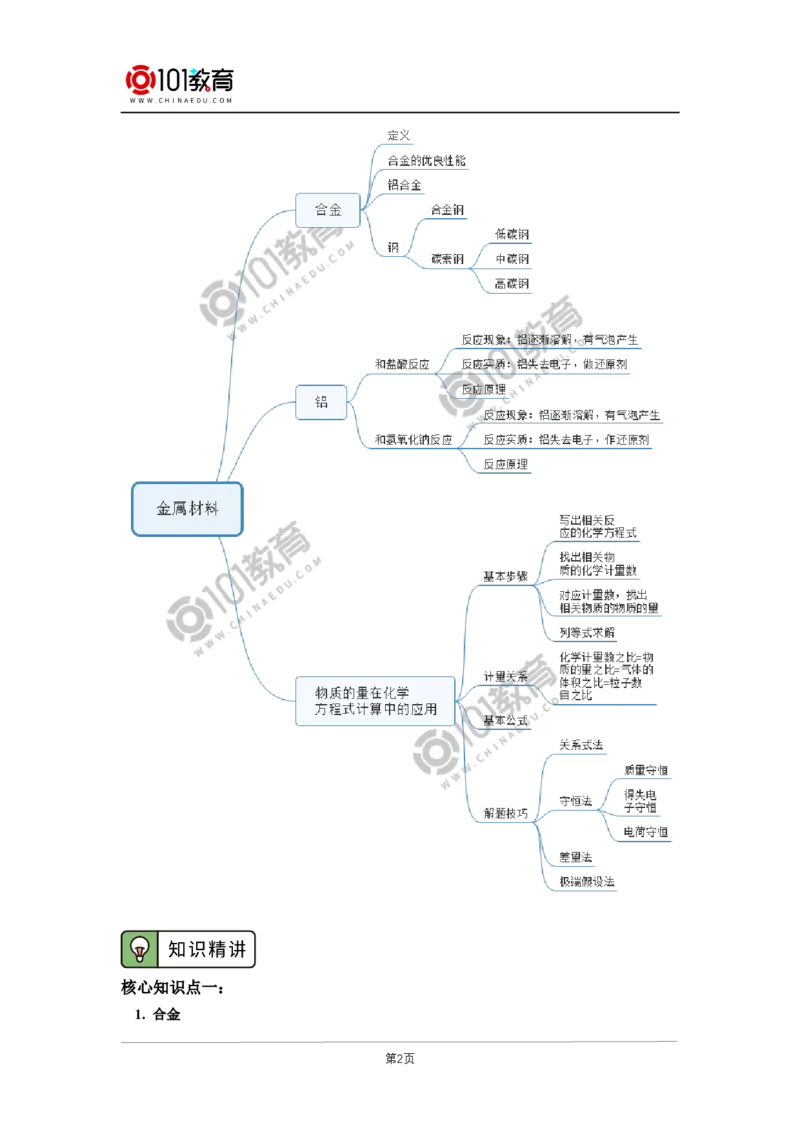
1. 合金
第2页(1)概念:合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属
特性的物质。
(2)性能:合金具有不同于各成分金属的物理、化学或机械性能。
①熔点:一般比它的各成分金属的低;
②硬度和强度:一般比它的各成分金属的大。
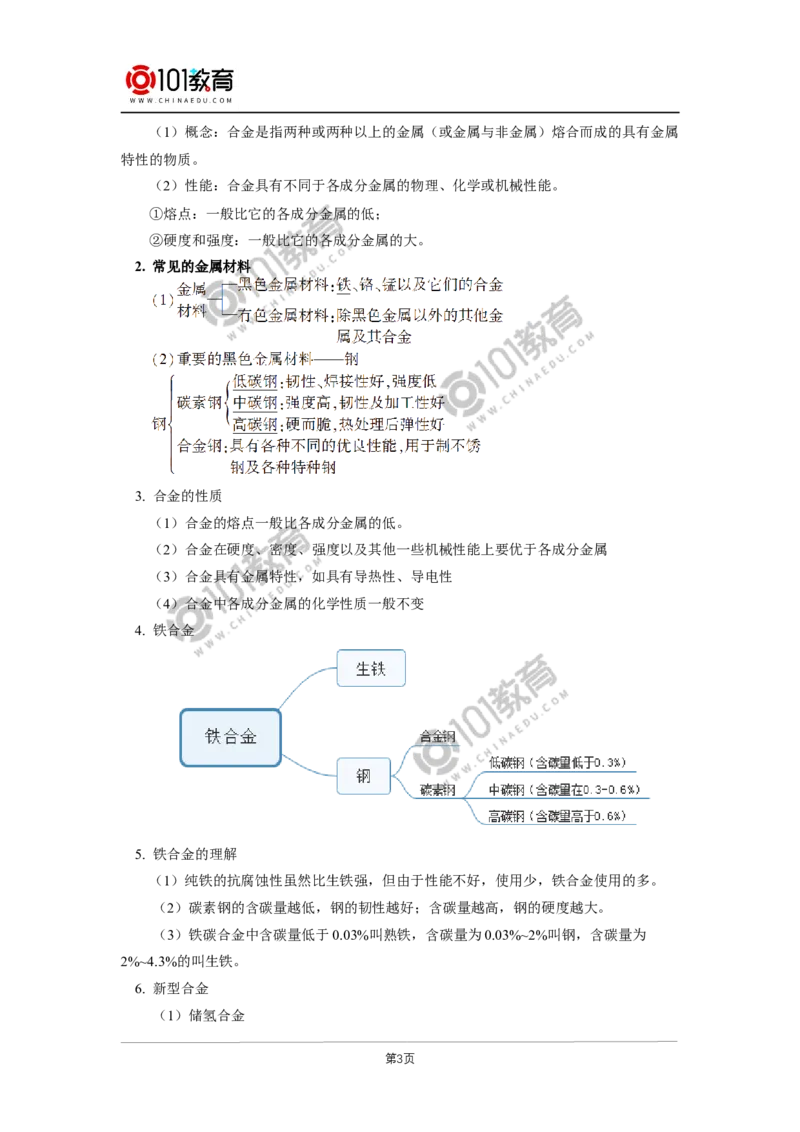
2. 常见的金属材料
3. 合金的性质
(1)合金的熔点一般比各成分金属的低。
(2)合金在硬度、密度、强度以及其他一些机械性能上要优于各成分金属
(3)合金具有金属特性,如具有导热性、导电性
(4)合金中各成分金属的化学性质一般不变
4. 铁合金
5. 铁合金的理解
(1)纯铁的抗腐蚀性虽然比生铁强,但由于性能不好,使用少,铁合金使用的多。
(2)碳素钢的含碳量越低,钢的韧性越好;含碳量越高,钢的硬度越大。
(3)铁碳合金中含碳量低于0.03%叫熟铁,含碳量为0.03%~2%叫钢,含碳量为
2%~4.3%的叫生铁。
6. 新型合金
(1)储氢合金
第3页(2)钛合金
(3)耐热合金
(4)形状记忆合金
(5)泡沫合金
核心知识点二:
一、物质的量在化学方程式计算中的应用
以钠和水反应的化学方程式为例:
2Na + 2HO===2NaOH+H↑
2 2
化学计量数 2 2 2 1
扩大N 倍 2×N 2×N 2×N 1×N
A A A A A
物质的量 2 mol 2 mol 2 mol 1 mol
结论:化学方程式中各物质的化学计量数之比=参加反应的物质的微粒个数之比=参加
反应的物质的物质的量之比=参加反应的物质的气体体积(相同状况)之比。
二、根据化学方程式进行计算的基本步骤
1. 有关物质的量的计算中的“三个规范”
(1)书写规范:各种符号的书写要规范,大写字母与小写字母的意义各不相同。如
“M”表示摩尔质量,而“m”表示质量,“N”表示微粒数,而“n”表示物质的量。
(2)符号规范:
①设未知数直接用各物理量的符号表示,且要注明物质(或粒子)的符号。如设参加
反应HCl溶液的体积为V[HCl(aq)]。
②各物理量及单位、物质的名称、公式等尽量用符号表示。如已知NaOH溶液的体积
和物质的量浓度,求NaOH溶液的质量时就写成:m(NaOH)=c(NaOH)×V[NaOH
第4页(aq)]×M(NaOH)。
(3)单位规范:把已知量代入计算式中计算时都要带单位且单位要统一。
2. 物质的量在化学方程式计算中应用的注意事项
(1)化学方程式中各物质的化学计量数之比等于各物质的物质的量之比,而非质量之
比
(2)计算时,各种物质不一定都用物质的量表示,也可以用质量表示,气态物质还可
以用体积表示,但要注意物质的量与其他各物理量之间的换算关系;只要做到“上下一致,
左右相当”即可。
三、化学计算常用的方法
(1)关系式法
当已知物和未知物之间是靠多个反应来联系时,只需直接确定已知量和未知量之间的
比例关系,即“关系式”
①根据化学方程式确定关系式:写出发生反应的化学方程式,根据量的关系写出关系
式。
如:把CO还原Fe O 生成的CO 通入澄清石灰水中,求生成沉淀的量。
2 3 2
发生反应的化学方程式:3CO+Fe O高温=2Fe+3CO ,CO+Ca(OH)===CaCO ↓+H O。
2 3=== 2 2 2 3 2
则关系式为3CO~3CO ~3CaCO ,即CO~CaCO 。
2 3 3
②根据原子守恒确定关系式:上述例子中也可直接根据碳原子守恒得出CO~CaCO 。
3
(2)守恒法
(3)差量法
根据反应前后物质的有关物理量发生的变化,找出所谓“理论差量”,该差量的大小
与反应物的有关量成正比关系。差量法就是借助这种比例关系,解决一定量变的计算方法。
如Fe+CuSO===Cu+FeSO 固体质量增加
4 4
56 g 64 g 64 g-56 g=8 g
x m g
则 56g/8g=x/mg x=7m g。
第5页核心知识点一:
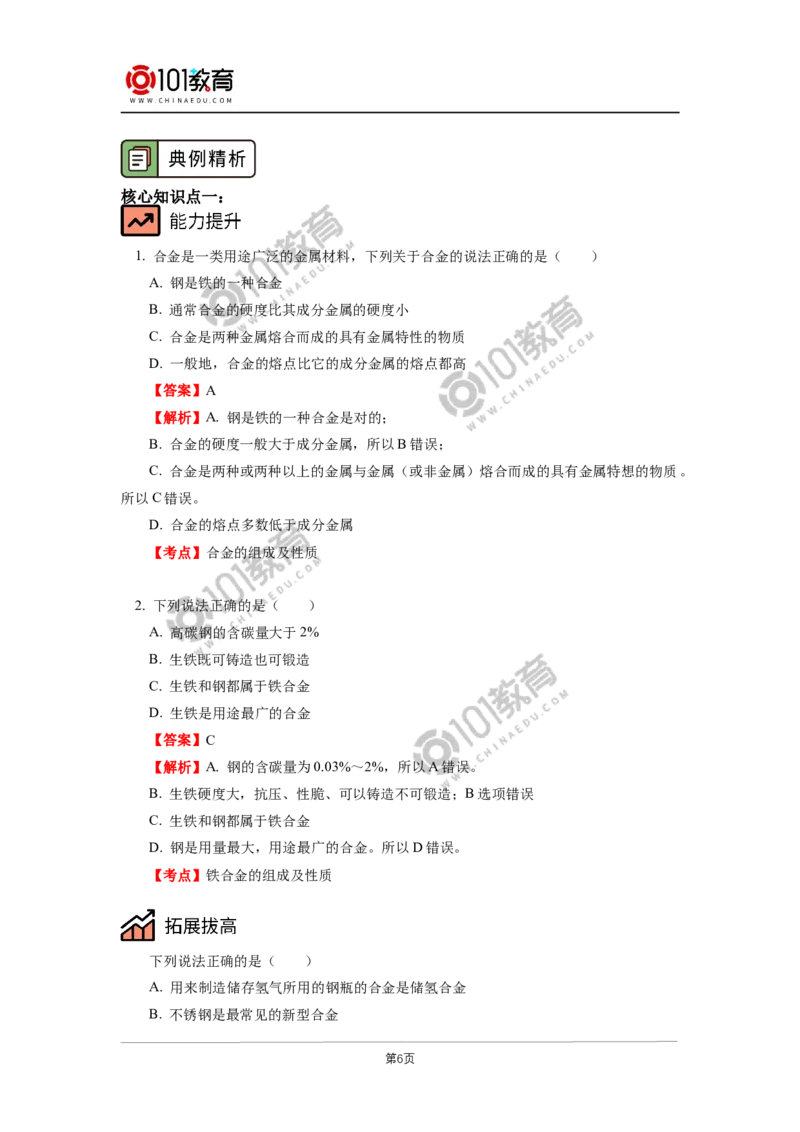
1. 合金是一类用途广泛的金属材料,下列关于合金的说法正确的是( )
A. 钢是铁的一种合金
B. 通常合金的硬度比其成分金属的硬度小
C. 合金是两种金属熔合而成的具有金属特性的物质
D. 一般地,合金的熔点比它的成分金属的熔点都高
【答案】A
【解析】A. 钢是铁的一种合金是对的;
B. 合金的硬度一般大于成分金属,所以B错误;
C. 合金是两种或两种以上的金属与金属(或非金属)熔合而成的具有金属特想的物质。
所以C错误。
D. 合金的熔点多数低于成分金属
【考点】合金的组成及性质
2. 下列说法正确的是( )
A. 高碳钢的含碳量大于2%
B. 生铁既可铸造也可锻造
C. 生铁和钢都属于铁合金
D. 生铁是用途最广的合金
【答案】C
【解析】A. 钢的含碳量为0.03%~2%,所以A错误。
B. 生铁硬度大,抗压、性脆、可以铸造不可锻造;B选项错误
C. 生铁和钢都属于铁合金
D. 钢是用量最大,用途最广的合金。所以D错误。
【考点】铁合金的组成及性质
下列说法正确的是( )
A. 用来制造储存氢气所用的钢瓶的合金是储氢合金
B. 不锈钢是最常见的新型合金
第6页C. 新型合金主要应用于航天航空、生物工程等领域
D. 碳纤维复合材料属于新型合金材料
【答案】C
【解析】A. 用来制造储存氢气所用的钢瓶是铁
B. 不锈钢是最常见的铁合金
C. 新型合金主要应用于航天航空、生物工程等领域
D. 碳纤维复合材料不属于新型合金材料
【考点】常见的新型合金
核心知识点二:
等物质的量的Fe、Mg、Al与同体积、同浓度的HCl反应,产生H 的体积相同(相同
2
状况),下列判断正确的是( )
A. 反应掉的三种金属的质量相等
B. 反应后的三种金属质量相等
C. 所用盐酸均过量
D. 三种金属可以都有剩余
【答案】D
【解析】在题目条件下产生相同的氢气,反应掉的三种金属的质量和剩余金属的质量
均不相等,如果盐酸过量,则产生的氢气的体积不相等。
【考点】物质的量的相关计算
铁粉可与高温水蒸气反应,若反应后得到的干燥固体质量比反应前铁粉的质量增加了
32g,则参加反应的铁粉的物质的量是( )
A. 0.5 mol B. 1 mol C. 1.5 mol D. 2 mol
【答案】C
【解析】3Fe+4HO(g) Fe O+4H Δm
2 3 4 2
3 mol 64 g
n(Fe) 32 g
3mol 64g
=
n(Fe) 32g
,解得n(Fe)=1.5 mol。
【考点】物质的量在化学方程式中的计算
第7页(答题时间:35分钟)
一、选择题:
1. 所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,
根据下列四种金属的熔沸点:
Na Cu Al Fe
熔点 97.5 ℃ 1 083 ℃ 660 ℃ 1 535 ℃
沸点 883 ℃ 2 595 ℃ 2 200 ℃ 3 000℃
其中不能形成合金的是( )
A. Cu和Na B. Fe与Cu C. Fe与Al D. Al与Na
2. 下列物质中,不属于合金的是( )
A. 硬铝 B. 黄铜 C. 水银 D. 钢铁
3. 有关合金的叙述不正确的是( )
A. 合金的熔点比它的各成分金属的熔点低
B. 合金一定是金属熔合而成的物质
C. 合金的硬度和强度一般比纯金属高
D. 硬铝、黄铜和钢均为合金
4. Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.48 L,下列推断中不
正确的是( )
A. 参加反应的Mg、Al共0.2 mol
B. 参加反应的HCl为0.4 mol
C. Mg、Al在反应中共失去0.4 mol电子
D. 若与足量的稀硫酸反应能产生0.2 mol H
2
5. a g铁粉与含有HSO 的CuSO 溶液完全反应后,得到a g铜,则参与反应的CuSO 与
2 4 4 4
HSO 的物质的量之比为( )
2 4
A. 1∶7 B. 7∶1 C. 7∶8 D. 8∶7
6. 分别将23 g金属钠放入足量的m g水中和24 g金属镁放入足量的m g稀盐酸中,反应
后所得溶液的质量分别为a g和b g。那么a和b的关系应是( )
A. a>b B. a