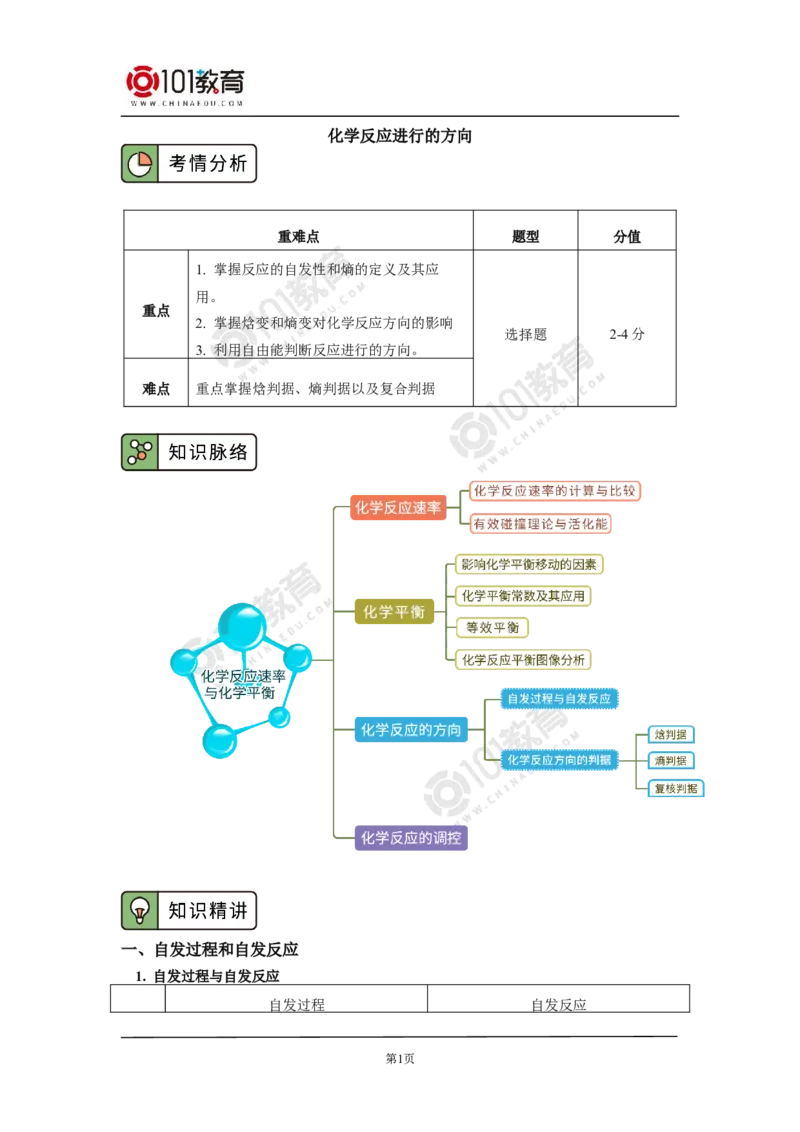
文档内容
化学反应进行的方向
重难点 题型 分值
1. 掌握反应的自发性和熵的定义及其应
用。
重点
2. 掌握焓变和熵变对化学反应方向的影响
选择题 2-4分
3. 利用自由能判断反应进行的方向。
难点 重点掌握焓判据、熵判据以及复合判据
一、自发过程和自发反应
1. 自发过程与自发反应
自发过程 自发反应
第1页在一定条件下,不需要借助外力就能自 在给定的条件下,可以自发进行到显著
含义
发进行的过程 程度的化学反应
具有方向性,即某个方向在一定条件下是自发的,而其逆方向在该条件下是肯定不
特征
能自发进行的
举例 高山流水,自由落体运动 钢铁生锈
(1)可被用来完成有用功。如H 燃烧可设计成原电池
2
应用
(2)非自发过程要想发生,必须对它做功。如通电将水分解为H 和O
2 2
2. 自发过程的特点
(1)体系趋向于从高能状态转变为低能状态。
(2)体系趋向于从有序体系转变为无序体系。
【求甚解】并不是自发反应一定能发生,非自发反应一定不能发生。自发反应和非自
发反应是指该反应过程是否有自发进行的倾向,而这个过程是否一定会发生则不能确定。
例如:碳的燃烧是一个自发反应,但需要借助外界条件“点燃”,反应才能发生。
二、化学反应进行方向的判断
1. 焓判据
焓判据 放热反应过程中体系能量降低,具有自发进行的倾向
焓变与反应自发性的 若该反应为放热反应,即ΔH<0,一般能自发进行;若该反应为吸
关系 热反应,即ΔH>0,一般不能自发进行
有些吸热反应也能自发进行,所以焓变是与反应进行的方向有关的
局限性
因素之一,但不是决定反应能否自发进行的唯一因素
(1)多数自发反应是放热反应
①常温、常压下的自发反应,如酸碱中和反应、铁生锈、氢氧化亚铁被氧化为氢氧化
铁。例如:4Fe(OH) (s) + 2H O(l)+O (g)=4 Fe(OH) (s) ΔH(298K)
2 2 2 3
=-444.3kJ·mol-1
②高温下的自发反应,如甲烷的燃烧反应:CH(g)+2O(g)=CO (g)+2H O(l)
4 2 2 2
ΔH=-890.3kJ·mol-1
(2)有些吸热反应也能自发进行
①常温、常压下的自发反应,如:
NH HCO (s)+CH COOH(aq)=CO (g)+CH COONH (aq)+H O(l)
4 3 3 2 3 4 2
ΔH=+37.30kJ·mol-1
②高温下的自发反应,如碳酸钙的分解:
第2页CaCO (s)=CaO(s)+ CO(g) ΔH=+178.2 kJ·mol-1
3 2
【小结】多数自发进行的化学反应是放热反应,但也有很多吸热反应能自发进行,因
此,只根据焓变来判断反应进行的方向是不全面的。反应焓变是与反应进行方向有关的因
素之一,但不是决定反应能否自发进行的唯一因素。
2. 熵判据
(1)熵:自发过程的体系趋向于由有序转态转变为无序,体系的混乱度增大。体系的
混乱度常用熵来描述,即熵是表示体系混乱或无序程度的物理量。熵的符号为 S,单位为
J·mol-1·K-1。熵值越大,体系的混乱度越大。
(2)影响熵值大小的因素
①物质的种类
同一条件下,不同的物质熵值不同。
②物质的状态
对于同一物质,物质的量相等时,其熵值大小的关系为:S(g)>S(l)>S(s)。
③物质的量
同一状态的同一物质,熵值还与物质的量成正比。物质的量越大,分子越多,熵值越
大。
(2)熵变:ΔS=S(生成物)-S(反应物)。只与反应体系的始态和终态有关,与
反应进行的途径无关,ΔS越大,越有利于反应自发进行。所以熵变是判断反应进行方向的
另一个因素。
(3)熵增原理:在与外界隔离的体系中,自发过程将导致体系的熵增大,即熵变大于
零。
(4)熵判据:体系有自发地向熵增的方向转变的倾向,熵变是影响反应自发进行的一
个因素,但不是唯一因素。
(5)熵变对化学反应方向的影响。
①熵增加的反应在一定条件下都可自发进行。
如2HO(aq)=2HO(l)+O(g)在常温下能自发进行。
2 2 2 2
②有些熵减小的反应也能自发进行。
如NH (g)+HCl(g)=NH Cl(s)。
3 4
3. 熵增的过程与反应
(1)三态变化:s
⃗ΔS>0l ⃗ΔS>0
g。
(2)A(s)+B(g)=2C(g)的ΔS>0。
(3)A(g)+B(g)=2C(g)+D(g)的ΔS>0。
【即时练】判断下列各变化过程是熵增加还是熵减小,在横线上填选项字母。
(1)NH NO 爆炸:2NH NO (s) 2N(g)+4HO(g)+O(g)。______
4 3 4 3 2 2 2
第3页(2)水煤气转化:CO(g)+HO(g)=CO(g)+H(g)。______
2 2 2
(3)臭氧的生成:3O(g)=2O(g)。______
2 3
A. 熵增大 B. 熵减小
C. 不变 D. 熵变很小
【答案】(1)A (2)D (3)B
【解析】(1)NH NO 的爆炸反应是气态物质的物质的量增大的化学反应:(2+4+
4 3
1)-0>0,因此该过程是熵增加的过程。
(2)水煤气转化反应,气态物质的物质的量在反应前后未发生变化:(1+1)-(1
+1)=0,该过程的熵变很小。
(3)生成臭氧后,气态物质的物质的量减小:2-3<0,因此该过程是熵减小的过程。
4. 复合判据
反应进行的方向与自由能变化的关系
ΔG=ΔH-TΔS<0反应能自发进行;ΔG=ΔH-TΔS=0反应达到平衡状态;ΔG=ΔH
-TΔS>0反应不能自发进行。
(1)当ΔH<0,ΔS>0,则ΔG<0,反应一定能自发进行。
(2)当ΔH>0,ΔS<0,则ΔG>0,反应一定能自发进行。
(3)当ΔH>0,ΔS>0或ΔH<0,ΔS<0时,反应能否自发进行与温度有关,一般来
说,低温时焓变影响为主,高温时熵变为主。
象限法判断反应的方向:
【求甚解】一般来说,如果一个过程是自发的,则其逆过程往往是非自发的。
1. 自发反应和非自发反应是可能相互转化的,某一条件下的自发反应可能在另一条件下
就是非自发反应,如2NO(g)+O (g)=2NO g(g)是常温下的自发反应,而在高温条
2 2
件下其逆反应是自发反应。
2. 过程的自发性只能用于判断过程的方向,不能确定过程是否一定会发生以及过程发生
的速率,如涂有防锈漆和未涂有防锈漆的铜制品器件,它们发生腐蚀过程的自发性是相同
的,但只有后者可以实现。
第4页例题1 下列说法正确的是( )
A. 能自发进行的反应一定能迅速发生
B. 反应NH HCO (s)=NH (g)+HO(g)+CO (g)ΔH=+185.57 kJ·mol-1能
4 3 3 2 2
自发进行,是因为体系有自发地向混乱度增大的方向转变的倾向
C. 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为判断反应
能否自发进行的判据
D. 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
【答案】B
【解析】能自发进行的反应并不一定能迅速发生,A项错误;应将焓变和熵变二者综
合起来即利用复合判据进行反应自发性的判断,C项错误;使用催化剂能改变反应的活化
能,但不能改变反应进行的方向,D项错误。
例题2 下列反应均为吸热反应,其中一定不能自发进行的是( )
A. 2CO(g)=2C(s)+O(g)
2
B. 2NO(g)=4NO (g)+O(g)
2 5 2 2
C. MgCO (s)=MgO(s)+CO(g)
3 2
D. (NH )CO(s)=NH HCO (s)+NH (g)
4 2 3 4 3 3
【答案】A
【解析】B、C、D反应的ΔS>0,在加热条件下,可满足ΔH-TΔS<0,反应可自发
进行,而A中ΔS<0,ΔH-TΔS>0,反应不能自发进行。
例题3 在化学反应A(g)+B(g) 2C(g)+D(g) ΔH=Q kJ·mol-1过程
中的能量变化如图所示,回答下列问题。
(1)Q________0 (填“>”“<”或“=”)。
(2)熵变ΔS________0(填“>”“<”或“=”)。
第5页(3)该反应________自发进行(填“能”或“不能”)。
(4)升高温度平衡常数 K________(填“增大”“减小”或“不变”),平衡向
________方向移动。
【答案】(1)< (2)> (3)能 (4)减小 逆反应
【解析】据图像可知,该反应是放热反应,故Q<0。据反应特点可知,该反应是熵增
大的反应;据此可知该反应能自发进行;升高温度,平衡向逆反应方向移动,平衡常数减
小。
(答题时间:40分钟)
一、选择题
1. 下列说法不正确的是( )
A. 焓变是一个与反应能否自发进行有关的因素,放热反应具有自发进行的倾向
B. 在同一条件下物质有不同的熵值,其体系的混乱程度越大,熵值越大
C. 自发反应是指不需要条件就能发生的反应
D. 一个反应能否自发进行与焓变和熵变的共同影响有关
2. 某化学反应的ΔH=-122 kJ·mol-1,ΔS=-431 J·mol-1·K-1,则以下关于此反应的自
发性描述中正确的是( )
A. 在任何温度下都能自发进行
B. 仅在低温下能自发进行
C. 仅在高温下能自发进行
D. 在任何温度下都不能自发进行
3. 下列关于自发过程的叙述中,正确的是( )
A. 只有不需要任何条件就能够自动进行的过程才是自发过程
B. 需要加热才能进行的过程肯定不是自发过程
C. 同一可逆反应的正、逆反应在不同条件下都有自发的可能
D. 非自发过程在任何条件下都不可能变为自发过程
4. 下列自发反应可用焓判据来解释的是( )
A. 2N O(g)=4NO (g)+O(g)ΔH=+56.7 kJ·mol-1
2 5 2 2
B. (NH )CO(s)=NH HCO (s)+NH (g)ΔH=+74.9 kJ·mol-1
4 2 3 4 3 3
C. 2H(g)+O(g)=2HO(l)ΔH=-286 kJ·mol-1
2 2 2
D. CaCO (s)=CaO(s)+CO(g)ΔH=+178.2 kJ·mol-1
3 2
*5. 下列说法正确的是( )
第6页A. 反应2Mg(s)+CO(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH<0
2
B. ΔH<0、ΔS<0的反应在高温条件下能自发进行
C. 反应CaCO (s)=CaO(s)+CO(g)的ΔS<0
3 2
D. 同一物质的固、液、气三种状态的熵值相同
6. 下列反应在任何温度下均能自发进行的是( )
A. 2N (g)+O(g)=2NO(g)ΔH=+163 kJ·mol-1
2 2 2
1
2
B. Ag(s)+ Cl(g)=AgCl(s)ΔH=-127 kJ·mol-1
2
1
2
C. HgO(s)=Hg(l)+ O(g)ΔH=+91 kJ·mol-1
2
1
2
D. H2 (l)= O(g)+HO(l)ΔH=-98 kJ·mol-1
O2 2 2
*7. 有一化学平衡mA(g)+nB(g) pC(g)+qD(g),如图表示的是A的转化
率与压强、温度的关系。下列叙述正确的是( )
A. ΔH>0,ΔS>0
B. ΔH<0,ΔS>0
C. ΔH>0,ΔS<0
D. ΔH<0,ΔS<0
*8. 下列反应过程中,ΔH>0且ΔS>0的是( )
A. NH(g)+HCl(g)=NH Cl(s)
3 4
B. CaCO (s)=CaO(s)+CO(g)
3 2
C. 4Al(s)+3O(g)=2Al O(s)
2 2 3
D. HCl(aq)+NaOH(aq)=NaCl(aq)+HO(l)
2
9. 以下过程可以用熵判据来解释的是( )
A. 硝酸铵自发地溶于水
B. CaO(s)+CO(g)=CaCO (s)
2 3
C. HCl(g)+NH (g)=NH Cl(s)
3 4
D. 2H (g)+O(g)=2HO(l)
2 2 2
第7页第8页1.【答案】C
【解析】ΔH-TΔS<0反应能自发进行,一个反应能否自发进行与焓变和熵变的共同影
响有关,焓变是一个与反应能否自发进行有关的一个因素,放热反应具有自发进行的倾向
但不一定自发,A、D正确;根据熵增原理,体系的混乱程度越大,熵值越大,B正确;自
发性只能用于判断过程的方向,不能确定过程是否一定会发生,C错误。
2.【答案】B
【解析】ΔH<0,ΔS<0时低温有利于自发进行。
3.【答案】C
【解析】在一定条件下,不用借助外力即可自发进行的过程为自发过程,所以自发过
程也是需要特定的条件,A、B项错误;可逆反应在不同的条件下,可以向不同方向自发
进行,故C项正确;改变条件,可以使非自发过程转变为自发过程,D项错误。
4.【答案】C
【解析】从焓变的角度分析,化学反应有由高能状态向低能状态转化,使体系能量降
低的趋势,表现为放热反应较易进行。
5.【答案】A
【解析】反应物中有气体,生成物中没有气体,则ΔS<0,若要使反应自发进行,ΔH
-TΔS<0,则 ΔH必须小于 0,A项正确;根据 ΔH-TΔS<0 时,反应能自发进行,则
ΔH<0、ΔS<0的反应在高温条件下不能自发进行,B项错误;反应物中无气体,生成物中
有气体,则ΔS>0,C项错误;同一物质不同状态的熵值:气体>液体>固体,D项错误。
6.【答案】D
【解析】反应自发进行的前提条件是反应的ΔH-TΔS<0,温度的变化可能使ΔH-
TΔS的符号发生变化。A项,ΔH>0,ΔS<0,在任何温度下,ΔH-TΔS>0,即任何温度下,
反应都不能自发进行;B项,ΔH<0,ΔS<0,在较低温度下,ΔH-TΔS<0,即反应温度不
能过高;C项,ΔH>0,ΔS>0,若使反应自发进行,即ΔH-TΔS<0,必须提高温度,即反
应只有在较高温度下才能自发进行;D项,ΔH<0,ΔS>0,在任何温度下,ΔH-TΔS<0,
即在任何温度下反应均能自发进行。
7.【答案】C
【解析】由图像知压强越大,A的转化率越高,故m+n>p+q,故为ΔS<0;温度越高,
A的转化率越大,则正反应为吸热反应,故ΔH>0。
8.【答案】B
【解析】A是熵减的放热反应;C是熵减的放热反应;D是放热反应。
9.【答案】A
第9页【解析】可以用熵判据来解释,一般情况下是吸热且熵增加的过程。A项,硝酸铵自
发地溶于水,是熵增的过程,可以用熵判据来解释,正确;B项,该反应的ΔH<0,ΔS<
0,反应能自发进行,主要取决于ΔH的大小,不能用熵判据进行解释,错误;C项,该反
应的ΔH<0,ΔS<0,反应能自发进行,主要取决于ΔH的大小,不能用熵判据进行解释,
错误;D项,该反应的ΔH<0,ΔS<0,反应能自发进行,主要取决于ΔH的大小,不能用
熵判据进行解释,错误。
第10页