文档内容
第四章 总结与检测(学案)
知识点一、原电池原理
1.能量的转化
原电池:将化学能转变为电能的装置。
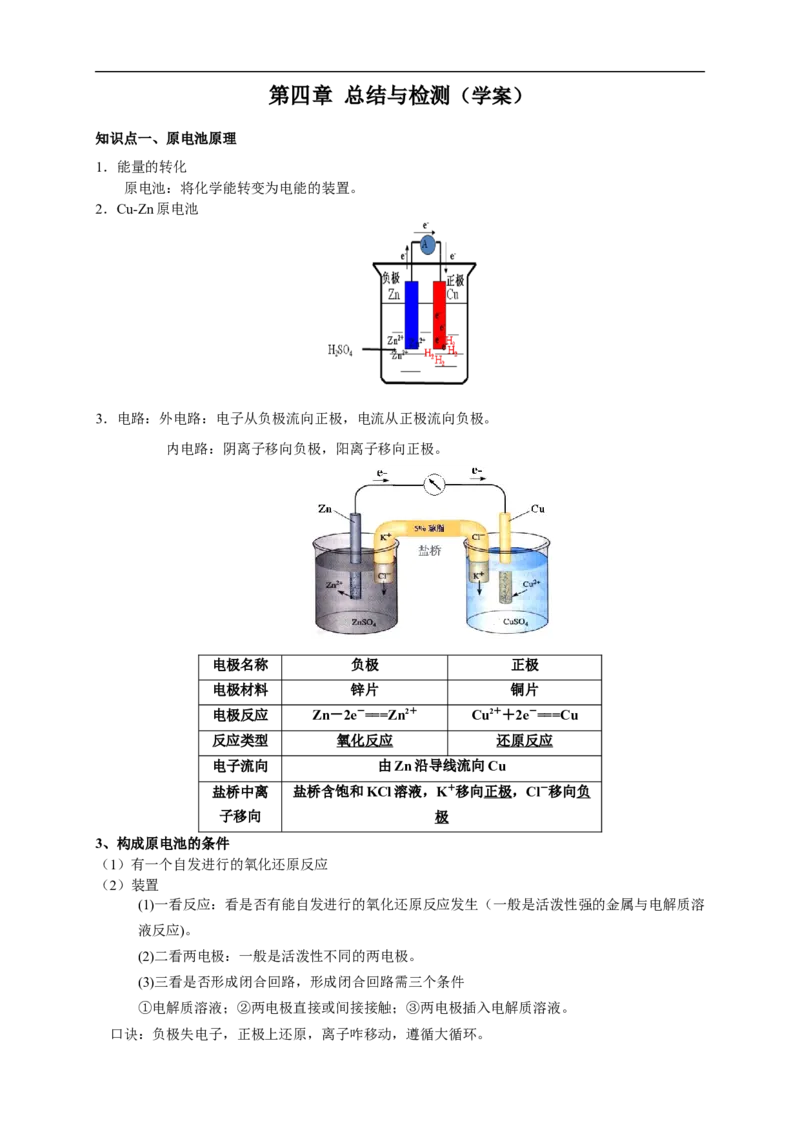
2.Cu-Zn原电池
3.电路:外电路:电子从负极流向正极,电流从正极流向负极。
内电路:阴离子移向负极,阳离子移向正极。
电极名称 负极 正极
电极材料 锌片 铜片
电极反应 Zn-2e-===Zn2+ Cu2++2e-===Cu
反应类型 氧化反应 还原反应
电子流向 由Zn沿导线流向Cu
盐桥中离 盐桥含饱和KCl溶液,K+移向正极,Cl-移向负
子移向 极
3、构成原电池的条件
(1)有一个自发进行的氧化还原反应
(2)装置
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶
液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件
①电解质溶液;②两电极直接或间接接触;③两电极插入电解质溶液。
口诀:负极失电子,正极上还原,离子咋移动,遵循大循环。4.正、负极的判断:
判断依据 负极 正极
活动性较弱的金属或能导电
1、电极材料 活动性较强的金属
的非金属
2、反应类型 氧化反应 还原反应
3、电子流动方向 电子流出极 电子流入极
4、电解质溶液中离子流向 阴离子移向的电极 阳离子移向的电极
5、电流方向 电流流入极 电流流出极
6、与电解质溶液能否发生反应 能 不能
7、反应现象 电极溶解 电极增重或有气泡产生
8、pH变化 降低 升高
5、常见的电池的评价
比能量:电池单位质量或单位体积所能输出电能的多少。
比功率:电池单位质量或单位体积所能输出功率的大小。
质量轻、体积小而输出电能多、功率大、可储存时间长,更适合使用者的需要。
知识点二、化学电源
1.电极方程式的书写
一般来讲,书写原电池的电极反应式应注意如下四点:
1.准确判断原电池的正负极
如果电池的正负极判断失误,则电极反应式必然写错,这是正确书写电极反应式的前提。一般
而言,较活泼的金属成为原电池的负极,但不是绝对的。如将铜片和铝片同时插入浓硝酸中组成原
电池时,铜却是原电池的负极被氧化,因为铝在浓硝酸中表面发生了钝化。此时,其电极反应式为:
负极:Cu-2e- ==Cu2+ 正极:2NO -+4H++2e-==2NO +2H O
3 2 2
又如将镁铝合金放入6mol/L的NaOH溶液中构成原电池时,尽管镁比铝活泼,但镁不和NaOH
溶液反应,所以铝成为负极,其电极反应式为:负极:2Al+8OH—-6e-==2AlO -+4H O 正极:
2 2
6HO+6e-==3H +6OH-
2 2
2.高度注意电解质的酸碱性
在正、负极上发生的电极反应不是孤立的,它往往与电解质溶液紧密联系。如氢—氧燃料电池
有酸式和碱式两种,在酸溶液中负极反应式为:2H-4e-==4H+ 正极反应式为:O+4H++4e-=2H O;如
2 2 2
是在碱溶液中,则不可能有H+出现,在酸溶液中,也不可能出现OH-。又于CH、CHOH等燃料
4 3
电池,在碱溶液中C元素以CO2-离子形式存在,而不是放出CO。
3 2
3.牢牢抓住总的反应方程式
从理论上讲,任何一个自发的氧化还原反应均可设计成原电池。而两个电极反应相加即得总的
反应方程式。所以,对于一个陌生的原电池,只要知道总反应方程式和其中的一个电极反应式,即
可迅速写出另一个电极反应式。
4.不能忽视电子转移数相等
在同一个原电池中,负极失去的电子数必等于正极得到的电子数,所以在书写电极反应式时,要注意电荷守恒。这样可以避免由电极反应式写总反应方程式,或由总反应方程式改写成电极反应
式所带来的失误,同时,也可避免在有关计算中产生误差。
(1)一次电池:放电之后不能充电,内部的氧化还原反应是不可逆的。
干电池:一次电池中电解质溶液制成胶状,不流动。
碱性锌锰电池
构成:负极是__Zn__,正极是__MnO ___,电解质是KOH
2
负极:__Zn-2e-+2OH-=Zn(OH) ____正极:___MnO +e-+H O=MnOOH+OH-____
2 2 2
总反应式:__Zn+2MnO +2H O=2MnOOH+Zn(OH) _____
2 2 2
特点:比能量较高,储存时间较长,可适用于大电流和连续放电。
(2)二次电池
①铅蓄电池
放电电极反应
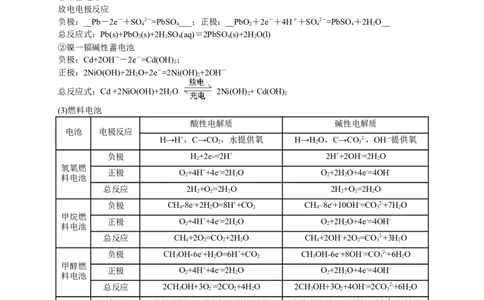
负极:__Pb-2e-+SO 2-=PbSO___;正极:__PbO +2e-+4H++SO 2-=PbSO+2HO__
4 4 2 4 4 2
总反应式:Pb(s)+PbO (s)+2HSO (aq)=2PbSO (s)+2HO(l)
2 2 4 4 2
②镍一镉碱性蓄电池
负极:Cd+2OH--2e-=Cd(OH) ;
2
正极:2NiO(OH)+2H O+2e-=2Ni(OH) +2OH-
2 2
总反应式:Cd +2NiO(OH)+2H O 2Ni(OH) + Cd(OH)
2 2 2
(3)燃料电池
酸性电解质 碱性电解质
电池 电极反应
H→H+,C→CO,水提供氧 H→H O,C→CO2-,OH—提供氧
2 2 3
负极 H+2e-=2H+ 2H++2OH-=2H O
2 2
氢氧燃
正极 O+4H++4e-=2H O O+2H O+4e-=4OH-
料电池 2 2 2 2
总反应 2H+O =2H O 2H+O =2H O
2 2 2 2 2 2
负极 CH-8e-+2H O=8H++CO CH–8e-+10OH-=CO 2-+7H O
4 2 2 4 3 2
甲烷燃
正极 O+4H++4e-=2H O O+2H O+4e-=4OH-
料电池 2 2 2 2
总反应 CH+2O =CO +2H O CH+2OH-+2O =CO 2-+3H O
4 2 2 2 4 2 3 2
负极 CHOH-6e-+H O=6H++CO CHOH-6e-+8OH-=CO 2-+6H O
3 2 2 3 3 2
甲醇燃
正极 O+4H++4e-=2H O O+2H O+4e-=4OH-
料电池 2 2 2 2
总反应 2CHOH+3O -=2CO +4H O 2CHOH+3O +4OH-=2CO 2-+6H O
3 2 2 2 3 2 3 2
负极 C HOH-12e-+3H O=12H++2CO C HOH-12e-+16OH-=2CO 2-+11H O
2 5 2 2 2 5 3 2
乙醇燃料
正极 O+4H++4e-=2H O O+2H O+4e-=4OH-
电池 2 2 2 2
总反应 C HOH-+3O -=2CO +3H O C HOH-+3O +4OH-=2CO 2-+5H O
2 5 2 2 2 2 5 2 3 2
熔融碳酸盐电解质 固体氧化物电解质
电池 电极反应
H→H O,C→CO,CO2—提供氧 H→H O,C→CO,O2—提供氧
2 2 3 2 2
负极 H+CO 2—2e-=H O+CO H+O2—2e-=H O
2 3 2 2 2 2
氢氧燃
正极 O+4e-+2CO =2CO 2- O+4e-=2O2-
料电池 2 2 3 2
总反应 2H+O =2H O 2H+O =2H O
2 2 2 2 2 2负极 CH+4CO 2—8e-=2H O+5CO CH+4CO 2—8e-=2H O+5CO
4 3 2 2 4 3 2 2
甲烷燃
正极 O+4e-+2CO =2CO 2- O+4e-=2O2-
料电池 2 2 3 2
总反应 CH+2O =CO +2H O CH+2O =CO +2H O
4 2 2 2 4 2 2 2
负极 CHOH+3CO 2—6e-=2H O+4CO CHOH+3CO 2—6e-=2H O+4CO
3 3 2 2 3 3 2 2
甲醇燃
正极 O+4e-+2CO =2CO 2- O+4e-=2O2-
料电池 2 2 3 2
总反应 2CHOH+3O -=2CO +4H O 2CHOH+3O -=2CO +4H O
3 2 2 2 3 2 2 2
负极 C HOH+6CO 2—12e-=3H O+7CO C HOH+6O2—12e-=3H O+2CO
2 5 3 2 2 2 5 2 2
乙醇燃料
正极 O+4e-+2CO =2CO 2- O+4e-=2O2-
电池 2 2 3 2
总反应 C HOH-+3O -=2CO +3H O C HOH-+3O -=2CO +3H O
2 5 2 2 2 2 5 2 2 2
除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料;除纯氧气外,空气中
的氧气也可作氧化剂。
燃料电池的能量转化率高于80%,远高于燃烧过程(仅30%左右),有利于节约能源。燃料电池
有广阔的发展前途。
知识点三、原电池原理的应用
1.运用原电池原理,加快化学反应速率
如:实验室中用Zn与稀HSO 反应制取H 时,通常滴入几滴CuSO 溶液。这样做的原因是Zn
2 4 2 4
与置换出的Cu、稀HSO 构成Zn与置换出的Cu、稀HSO 构成了原电池,加快了反应的进行。
2 4 2 4
2.运用原电池原理,设计制造各种化学电源
3.运用原电池原理,对金属实行有效保护
例:为保护轮船船体或大坝闸门的过快腐蚀,通常在船体或闸门外壳上连接一块比船体或闸门
更活泼的金属,以保护船体或闸门。
4.运用原电池原理,判断金属的活动性大小
作为原电池负极的金属,金属活动性一般比作为正极的金属活动性强。
5.运用原电池原理,判断氧化还原进行的方向
6.析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强 (pH≤4.3 ) 水膜酸性很弱或呈中性
电极 负极 Fe-2e-===Fe2+
反应 正极 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
知识点四、电解池原理
能量转化:将电能转变为化学能的装置。
1.电解:电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程。
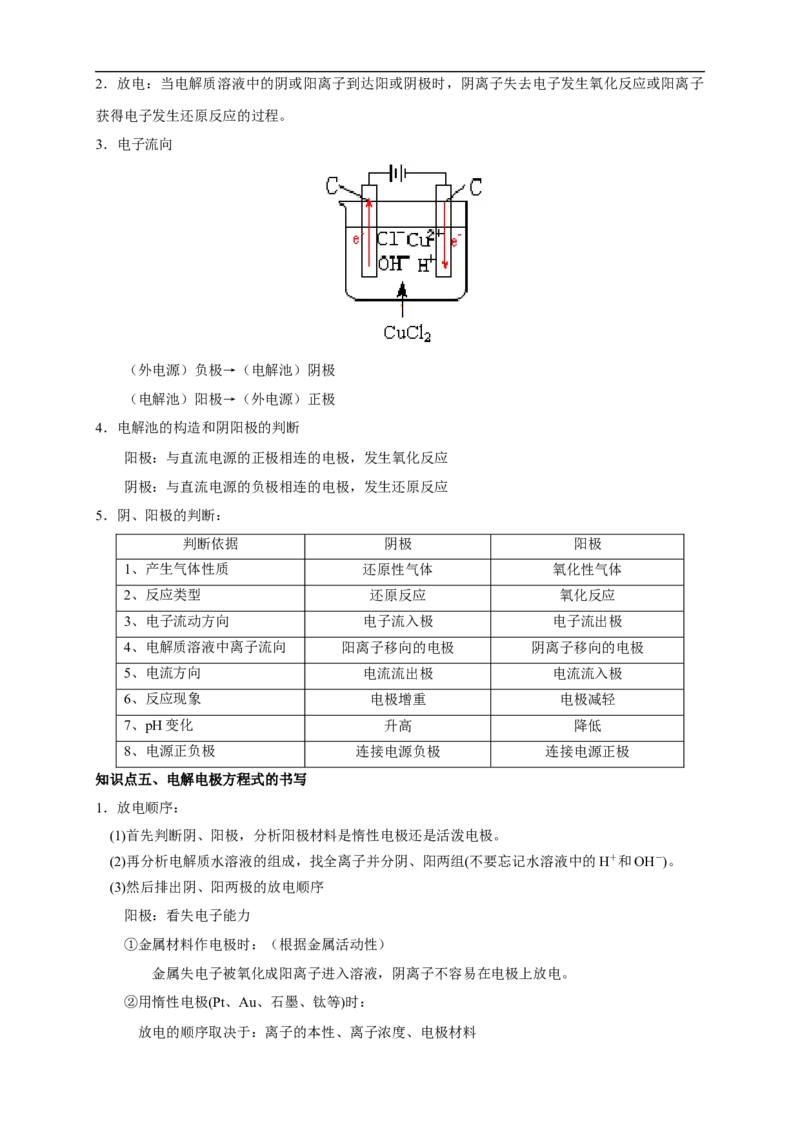
电解是最强有力的氧化还原手段。2.放电:当电解质溶液中的阴或阳离子到达阳或阴极时,阴离子失去电子发生氧化反应或阳离子
获得电子发生还原反应的过程。
3.电子流向
(外电源)负极→(电解池)阴极
(电解池)阳极→(外电源)正极
4.电解池的构造和阴阳极的判断
阳极:与直流电源的正极相连的电极,发生氧化反应
阴极:与直流电源的负极相连的电极,发生还原反应
5.阴、阳极的判断:
判断依据 阴极 阳极
1、产生气体性质 还原性气体 氧化性气体
2、反应类型 还原反应 氧化反应
3、电子流动方向 电子流入极 电子流出极
4、电解质溶液中离子流向 阳离子移向的电极 阴离子移向的电极
5、电流方向 电流流出极 电流流入极
6、反应现象 电极增重 电极减轻
7、pH变化 升高 降低
8、电源正负极 连接电源负极 连接电源正极
知识点五、电解电极方程式的书写
1.放电顺序:
(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组(不要忘记水溶液中的H+和OH-)。
(3)然后排出阴、阳两极的放电顺序
阳极:看失电子能力
①金属材料作电极时:(根据金属活动性)
金属失电子被氧化成阳离子进入溶液,阴离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时:
放电的顺序取决于:离子的本性、离子浓度、电极材料阴极:阳离子放电顺序:Ag+ > Fe3+ >Cu2+ > H+(酸) > Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+
>K+。
阳极:阴离子放电顺序:活泼电极>S2- >SO2- >I- >Br- >Cl->OH->含氧酸根离子>F-。
3
说明:①阴阳离子在两极上放电顺序复杂,与离子性质、溶液浓度、电流强度、电极材料等都
有关,不应将放电顺序绝对化,以上仅是一般规律。
②电解过程中析出的物质的量(或析出物质的质量):在电解若干串联电解池中的溶液时,各
阴极或阳极所通过的电量相等,析出物质的量取决于电路中通过的电量。
③阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电。
④最常用、最重要的放电顺序是:阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。
⑤电解水溶液时,K+~Al3+不可能在阴极放电,即不可能用电解水溶液的方法得到K、Ca、
Na、Mg、Al等金属。
2.四种类型电解质水溶液电解产物分类:
(1)电解水型:含氧酸,强碱,活泼金属含氧酸盐
(2)电解电解质型:无氧酸,不活泼金属的无氧酸盐(氟化物除外)
(3)放氢生碱型:活泼金属的无氧酸盐
(4)放氧生酸型:不活泼金属的含氧酸盐
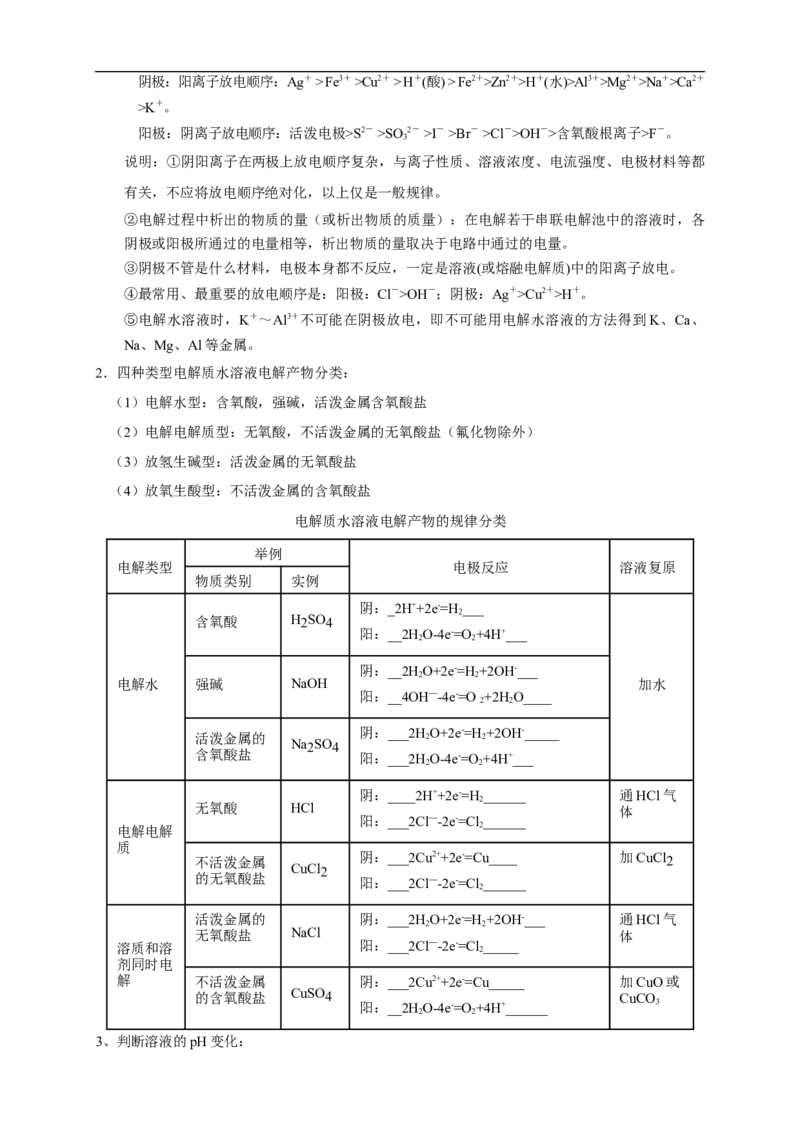
电解质水溶液电解产物的规律分类
举例
电解类型 电极反应 溶液复原
物质类别 实例
阴:_2H++2e-=H ___
2
含氧酸 H2SO4
阳:__2HO-4e-=O +4H+___
2 2
阴:__2HO+2e-=H +2OH-___
2 2
电解水 强碱 NaOH 加水
阳:__4OH—-4e-=O +2H O____
2 2
阴:___2HO+2e-=H +2OH-_____
活泼金属的 2 2
Na2SO4
含氧酸盐
阳:___2HO-4e-=O +4H+___
2 2
阴:____2H++2e-=H ______ 通HCl气
2
无氧酸 HCl 体
阳:___2Cl—-2e-=Cl______
电解电解 2
质
不活泼金属
阴:___2Cu2++2e-=Cu____ 加CuCl2
CuCl2
的无氧酸盐
阳:___2Cl—-2e-=Cl______
2
活泼金属的 阴:___2HO+2e-=H +2OH-___ 通HCl气
2 2
无氧酸盐 NaCl 体
溶质和溶 阳:___2Cl—-2e-=Cl_____
2
剂同时电
解 不活泼金属 阴:___2Cu2++2e-=Cu_____ 加CuO或
的含氧酸盐
CuSO4
CuCO
阳:__2HO-4e-=O +4H+______ 3
2 2
3、判断溶液的pH变化:先分析原溶液的酸碱性,再看电极产物。
(1)如果只产生氢气而没有氧气,则pH变大;
(2)如果只产生氧气而没有氢气,则pH变小;
(3)如果既产生氢气又产生氧气
①若原溶液呈酸性则pH减小;
②若原溶液呈碱性pH增大;
③若原溶液呈中性pH不变。
4.电极区域PH变化:
(1)阴极H+放电产生H,阴极区域pH变大;
2
(2)阳极OH-放电产生O,阳极区域pH变小。
2
知识点六、电解原理的应用
1.电解饱和食盐水
(1)电极反应
阳极反应式:2Cl--2e-===Cl↑(氧化反应)
2
阴极反应式:2HO+ 2e-→H↑+2OH-(还原反应)
2 2
(2)总反应方程式:__2Cl-+2HO=Cl +2OH-_______
2 2
(3)应用:氯碱工业制烧碱、氯气和氢气。
2.电镀
右图为金属表面镀银的工作示意图,据此回答下列问题:
(1)镀件作阴极,镀层金属银作阳极。
(2)电解质溶液是AgNO 溶液等含镀层金属阳离子的盐溶液。
3
(3)电极反应: 阳极:__Ag-e-=Ag+_____;阴极:___Ag++e-=Ag____。
(4)特点:阳极溶解,阴极沉积,电镀液的浓度不变。
3.电解精炼铜
(1)电极材料:阳极为粗铜;阴极为纯铜。
(2)电解质溶液:含Cu2+的盐溶液。
(3)电极反应:
阳极:Zn-2e-===Zn2+、Fe-2e-===Fe2+、Ni-2e-===Ni2+、Cu-2e-===Cu2+;
阴极:Cu2++2e-===Cu。
(4)电解质溶液的浓度变小。
4.电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
(1)冶炼钠
2NaCl(熔融) 2Na+Cl↑
2
电极反应:阳极:__2Cl—-2e-=Cl______;阴极:__Na++e-=Na_____。
2(2)冶炼铝
2Al O(熔融) 4Al+3O↑
2 3 2
电极反应:阳极:____Al3++3e-=Al_______;阴极:_2O2—-4e-=O ____。
2
5.金属的腐蚀和防护
1.金属防腐
(1)判断金属腐蚀快慢的规律
①对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐
蚀>化学腐蚀>有防腐措施的腐蚀。
②对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非
电解质溶液中。
③活动性不同的两种金属,活动性差别越大,腐蚀越快。
④对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。
(2)两种保护方法的比较
外加电流的阴极保护法保护效果大于牺牲阳极的阴极保护法。
3.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法—原电池原理
a.负极:比被保护金属活泼的金属;b.正极:被保护的金属设备。
②外加电流的阴极保护法—电解原理
a.阴极:被保护的金属设备;b.阳极:惰性金属。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
6.电化学定量计算
(1)计算类型
原电池和电解池的计算包括两极产物的定量计算、溶液pH的计算、相对原子质量和阿伏加德罗
常数的计算、产物的量与电量关系的计算等。
(2)方法技巧
①根据电子守恒计算
用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的
电子数相等。
②根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
③根据关系式计算
根据电子守恒,突破电化学的基本计算
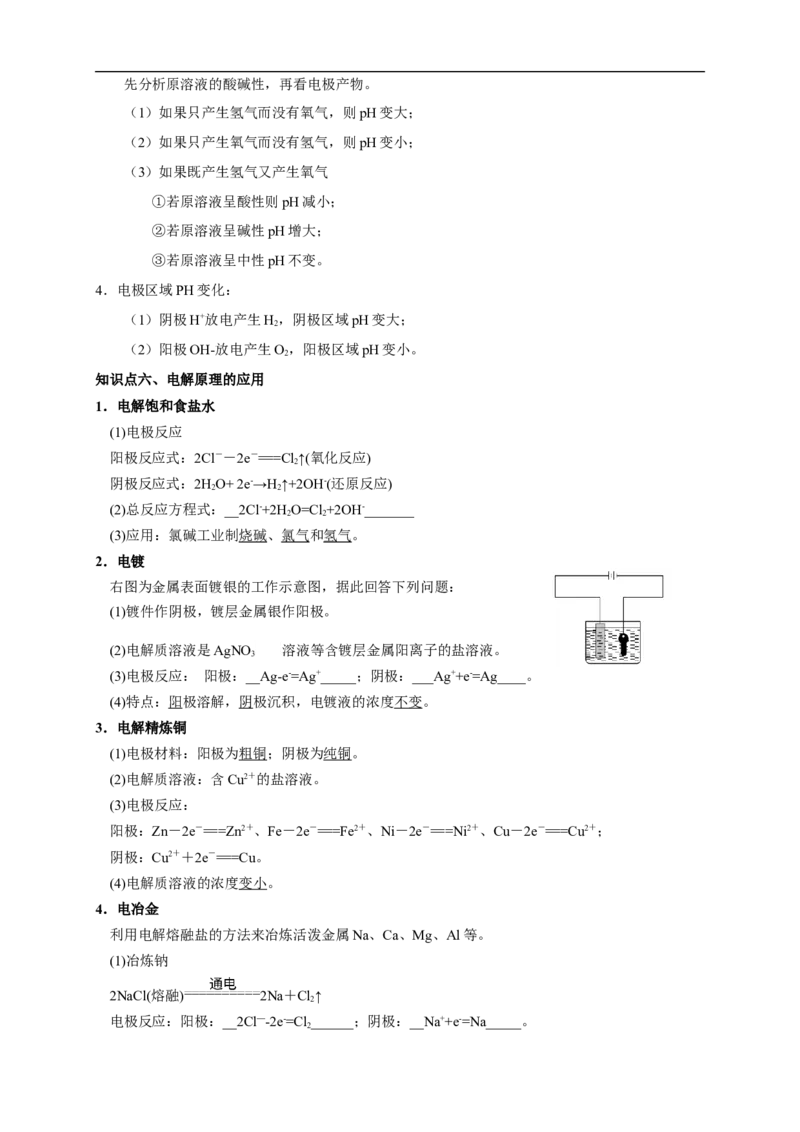
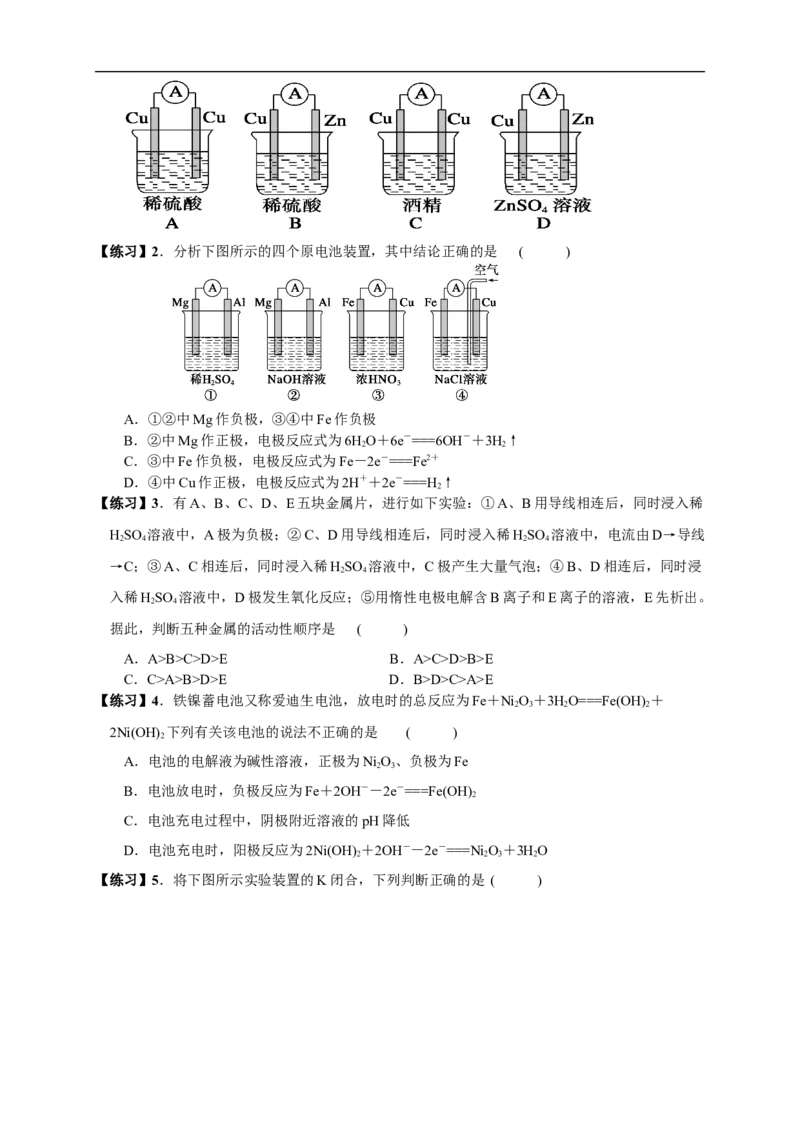
【练习】1.下列装置中能构成原电池产生电流的是 ( )【练习】2.分析下图所示的四个原电池装置,其中结论正确的是 ( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6HO+6e-===6OH-+3H↑
2 2
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H↑
2
【练习】3.有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀
HSO 溶液中,A极为负极;②C、D用导线相连后,同时浸入稀HSO 溶液中,电流由D→导线
2 4 2 4
→C;③A、C相连后,同时浸入稀HSO 溶液中,C极产生大量气泡;④B、D相连后,同时浸
2 4
入稀HSO 溶液中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。
2 4
据此,判断五种金属的活动性顺序是 ( )
A.A>B>C>D>E B.A>C>D>B>E
C.C>A>B>D>E D.B>D>C>A>E
【练习】4.铁镍蓄电池又称爱迪生电池,放电时的总反应为Fe+Ni O+3HO===Fe(OH) +
2 3 2 2
2Ni(OH) 下列有关该电池的说法不正确的是 ( )
2
A.电池的电解液为碱性溶液,正极为Ni O、负极为Fe
2 3
B.电池放电时,负极反应为Fe+2OH--2e-===Fe(OH)
2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH) +2OH--2e-===Ni O+3HO
2 2 3 2
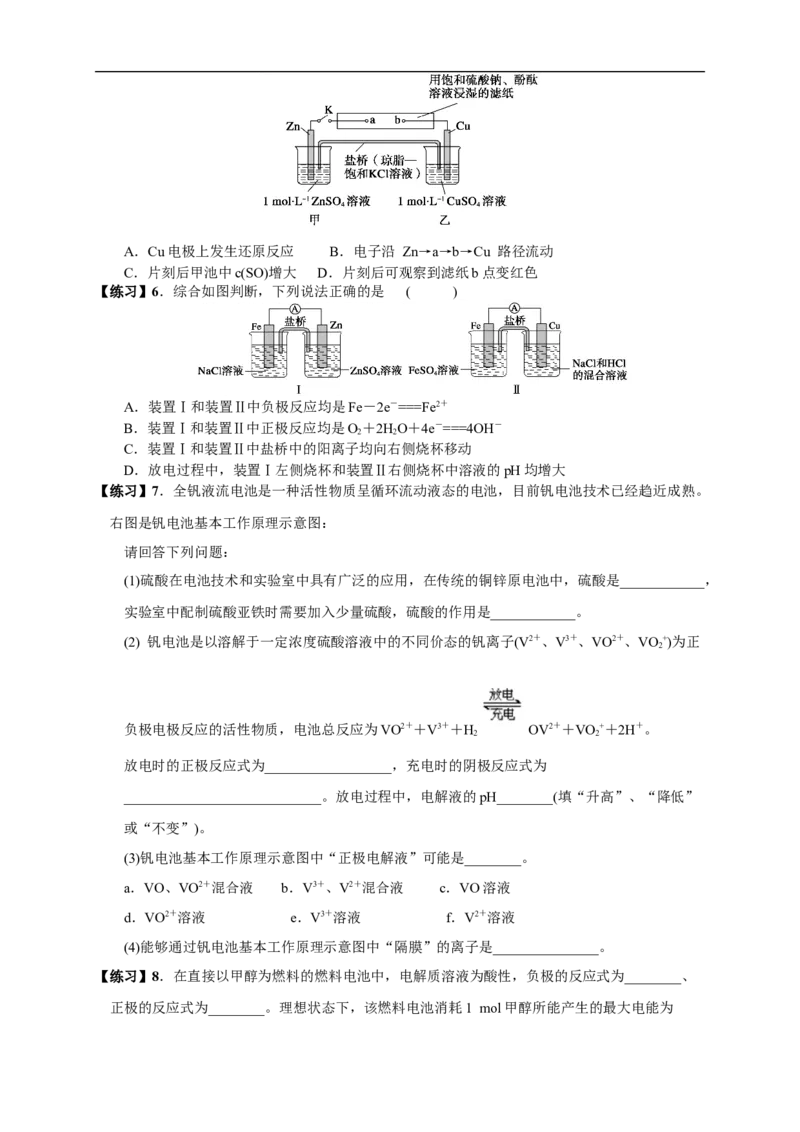
【练习】5.将下图所示实验装置的K闭合,下列判断正确的是 ( )A.Cu电极上发生还原反应 B.电子沿 Zn→a→b→Cu 路径流动
C.片刻后甲池中c(SO)增大 D.片刻后可观察到滤纸b点变红色
【练习】6.综合如图判断,下列说法正确的是 ( )
A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-===Fe2+
B.装置Ⅰ和装置Ⅱ中正极反应均是O+2HO+4e-===4OH-
2 2
C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
【练习】7.全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。
右图是钒电池基本工作原理示意图:
请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是____________,
实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是____________。
(2) 钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO +)为正
2
负极电极反应的活性物质,电池总反应为VO2++V3++H OV2++VO ++2H+。
2 2
放电时的正极反应式为__________________,充电时的阴极反应式为
____________________________。放电过程中,电解液的pH________(填“升高”、“降低”
或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是________。
a.VO、VO2+混合液 b.V3+、V2+混合液 c.VO溶液
d.VO2+溶液 e.V3+溶液 f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是_______________。
【练习】8.在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,负极的反应式为________、
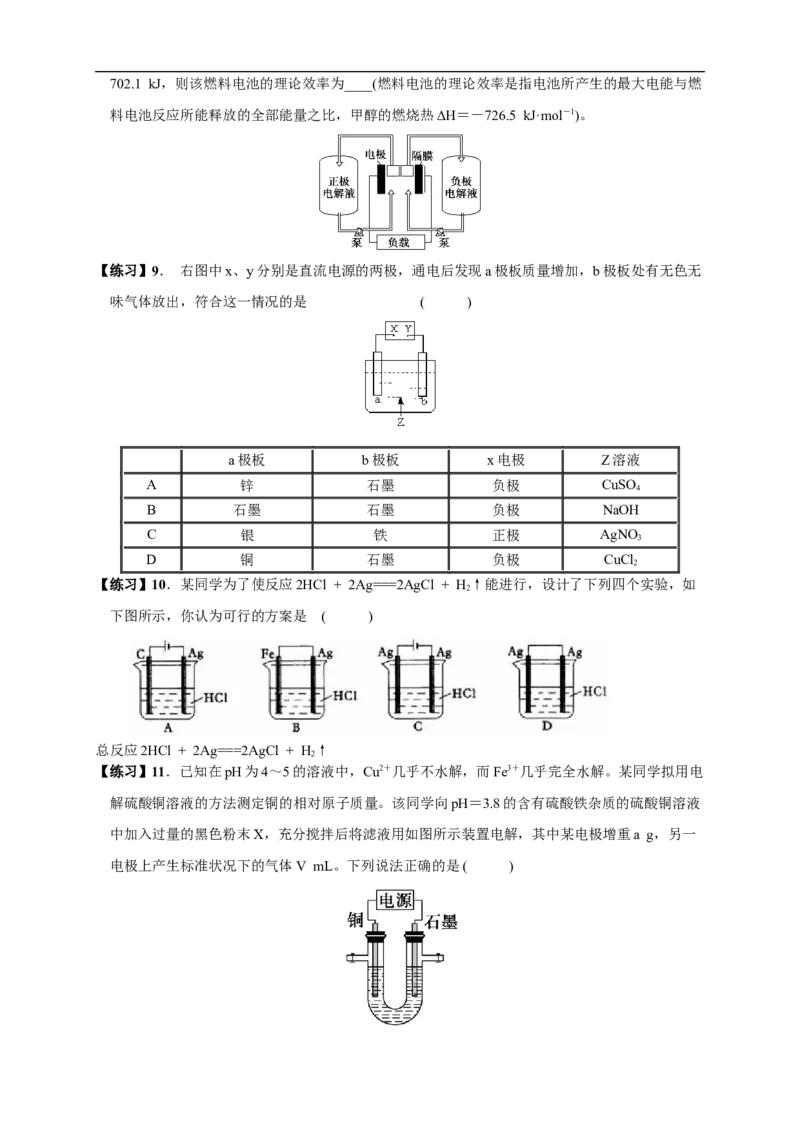
正极的反应式为________。理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为____(燃料电池的理论效率是指电池所产生的最大电能与燃
料电池反应所能释放的全部能量之比,甲醇的燃烧热ΔH=-726.5 kJ·mol-1)。
【练习】9. 右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无
味气体放出,符合这一情况的是 ( )
a极板 b极板 x电极 Z溶液
A 锌 石墨 负极 CuSO
4
B 石墨 石墨 负极 NaOH
C 银 铁 正极 AgNO
3
D 铜 石墨 负极 CuCl
2
【练习】10.某同学为了使反应2HCl + 2Ag===2AgCl + H↑能进行,设计了下列四个实验,如
2
下图所示,你认为可行的方案是 ( )
总反应2HCl + 2Ag===2AgCl + H↑
2
【练习】11.已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某同学拟用电
解硫酸铜溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液
中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一
电极上产生标准状况下的气体V mL。下列说法正确的是( )A.黑色粉末X是铁粉
B.石墨电极的反应式为4OH--4e-===2HO+O↑
2 2
C.铜电极连接电源的正极
D.铜的相对原子质量为
【练习】12.通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1价)溶
液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)︰n(硝酸亚汞)=2︰1,则下列
表述正确的是 ( )
A.在两个阴极上得到的银和汞的物质的量之比n(Ag)︰n(Hg)=2︰1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的分子式为HgNO
3
D.硝酸亚汞的分子式为Hg (NO )
2 3 2
【练习】13.某小组同学设想用如下图图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
(1)X极与电源的________(填“正”或“负”)极相连,氢气从________(填“A”、“B”、“C”或
“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”,下同)交换膜,
N为________交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的反应式
为_________________________________。
(4)若在标准状况下,制得11.2 L氢气,则生成硫酸的质量是_____,转移的电子数为__________。
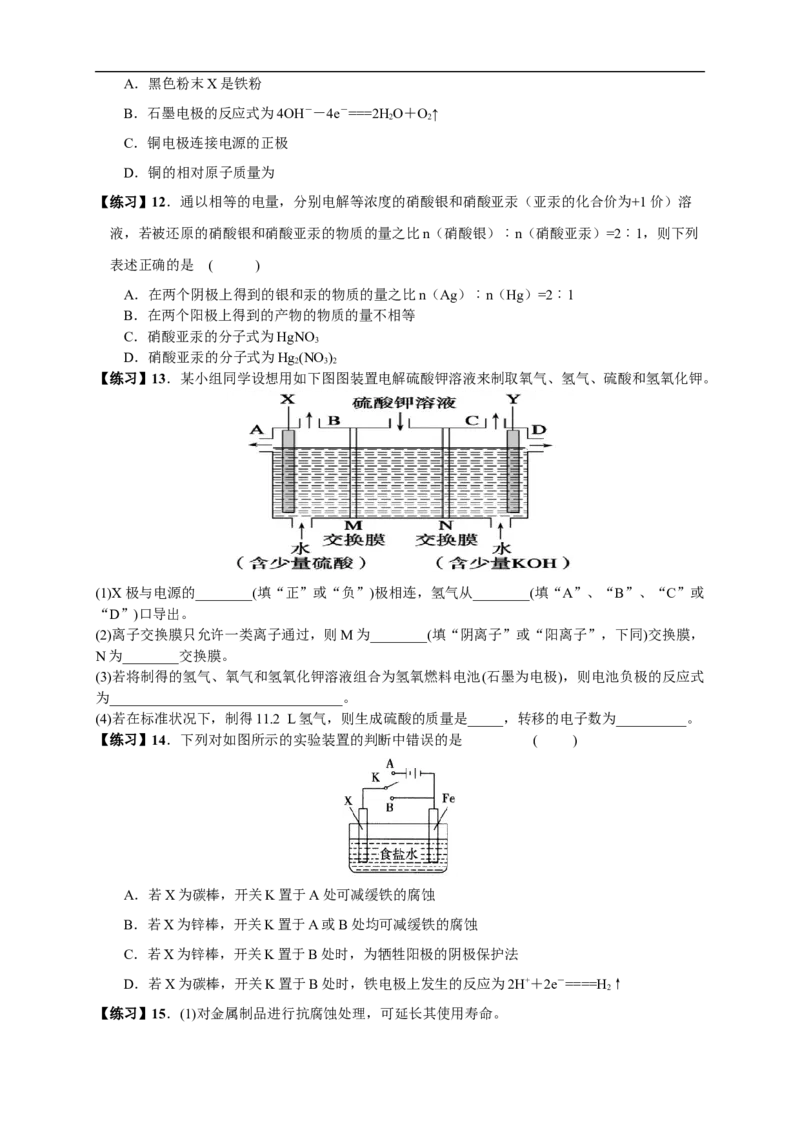
【练习】14.下列对如图所示的实验装置的判断中错误的是 ( )
A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法
D.若X为碳棒,开关K置于B处时,铁电极上发生的反应为2H++2e-====H ↑
2
【练习】15.(1)对金属制品进行抗腐蚀处理,可延长其使用寿命。①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是________(用离子方程
式表示)。为将碱洗槽液中的铝以沉淀的形式回收,最好向槽液中加入下列试剂中的________。
a. NH b.CO
3 2
c. NaOH d.HNO
3
②以铝材为阳极,在HSO 溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
2 4
________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极材料的原因是
__________________________________________。
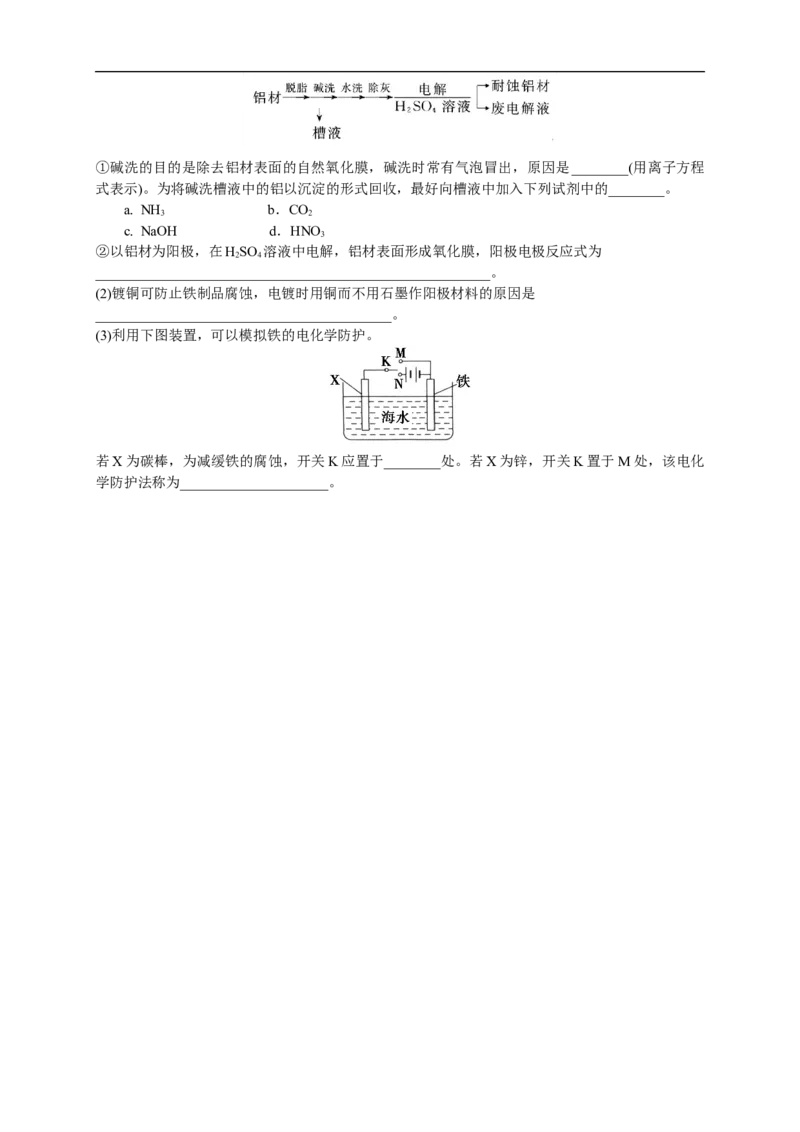
(3)利用下图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化
学防护法称为_____________________。