文档内容
第一章 原子结构与性质
第一节 原子结构
1.1.3 泡利原理、洪特规则、能量最低原理
认识基态原子中核外电子的排布遵循能量最低原理、泡利不相容原理和洪特规则等。
教学重点:
1、掌握泡利原理、洪特规则和能量最低原理
2、掌握1~36号元素的原子核外电子排布图
教学难点:
1~36号元素的原子核外电子排布图
[复习回顾]
1、量子力学告诉我们:ns能级各有 个轨道,np能级各有 个轨道,nd能级各有 个轨
道,nf能级各有 个轨道。
2、每个能级最多可容纳的电子数: ns、np、nd、nf……分别最多可容纳的电子数
。
[学生学习]
1、 泡利原理
(1)自旋:电子自旋有顺时针和逆时针两种状态,常用 表示自旋状态相反的电子。
(2)泡利原理:在一个原子轨道里,最多只能容纳 个电子,而且它们的自旋状态 。
2、电子排布的轨道表示式
(1)电子排布的轨道表示式的定义
(2)H、O的基态原子的轨道表示式
(3)电子排布的轨道表示式的书写方法
(4)概念辨析:简并轨道、单电子、电子对、自旋平行、自旋相反3、洪特规则
(1) 洪特规则内容
当电子排布在同一能级(能量相同)的不同轨道时,总是优先 占据一个轨道,而且自
旋方向 。
如:2p3的电子排布为 ,不能表示为 或 。
(2) 洪特规则特例
当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、f0)状态时,体系的
能量最低,如: Cr的电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1。
24
[思考与讨论]
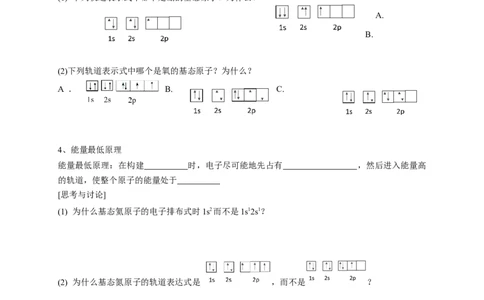
(1) 下列轨道表示式中哪个是硼的基态原子?为什么?
A.
B.
(2)下列轨道表示式中哪个是氧的基态原子?为什么?
A . B. C.
4、能量最低原理
能量最低原理:在构建 时,电子尽可能地先占有 ,然后进入能量高
的轨道,使整个原子的能量处于
[思考与讨论]
(1) 为什么基态氦原子的电子排布式时1s2而不是1s12s1?
(2) 为什么基态氮原子的轨道表达式是 ,而不是 ?
(3) 为什么基态K和Ca的价电子是4s1和4s2,而不是3d1和3d2?
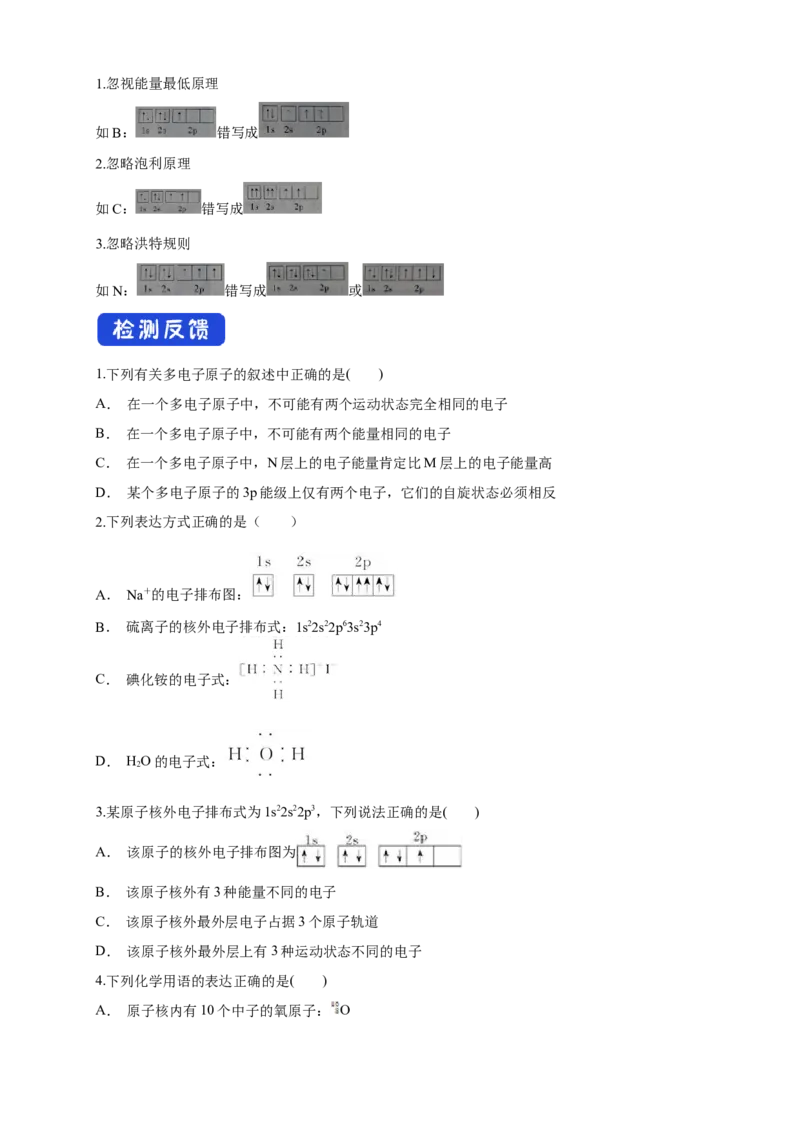
[易错误区]1.忽视能量最低原理
如B: 错写成
2.忽略泡利原理
如C: 错写成
3.忽略洪特规则
如N: 错写成 或
1.下列有关多电子原子的叙述中正确的是( )
A. 在一个多电子原子中,不可能有两个运动状态完全相同的电子
B. 在一个多电子原子中,不可能有两个能量相同的电子
C. 在一个多电子原子中,N层上的电子能量肯定比M层上的电子能量高
D. 某个多电子原子的3p能级上仅有两个电子,它们的自旋状态必须相反
2.下列表达方式正确的是( )
A. Na+的电子排布图:
B. 硫离子的核外电子排布式:1s22s22p63s23p4
C. 碘化铵的电子式:
D. HO的电子式:
2
3.某原子核外电子排布式为1s22s22p3,下列说法正确的是( )
A. 该原子的核外电子排布图为
B. 该原子核外有3种能量不同的电子
C. 该原子核外最外层电子占据3个原子轨道
D. 该原子核外最外层上有3种运动状态不同的电子
4.下列化学用语的表达正确的是( )
A. 原子核内有10个中子的氧原子: OB. 氯原子的结构示意图:
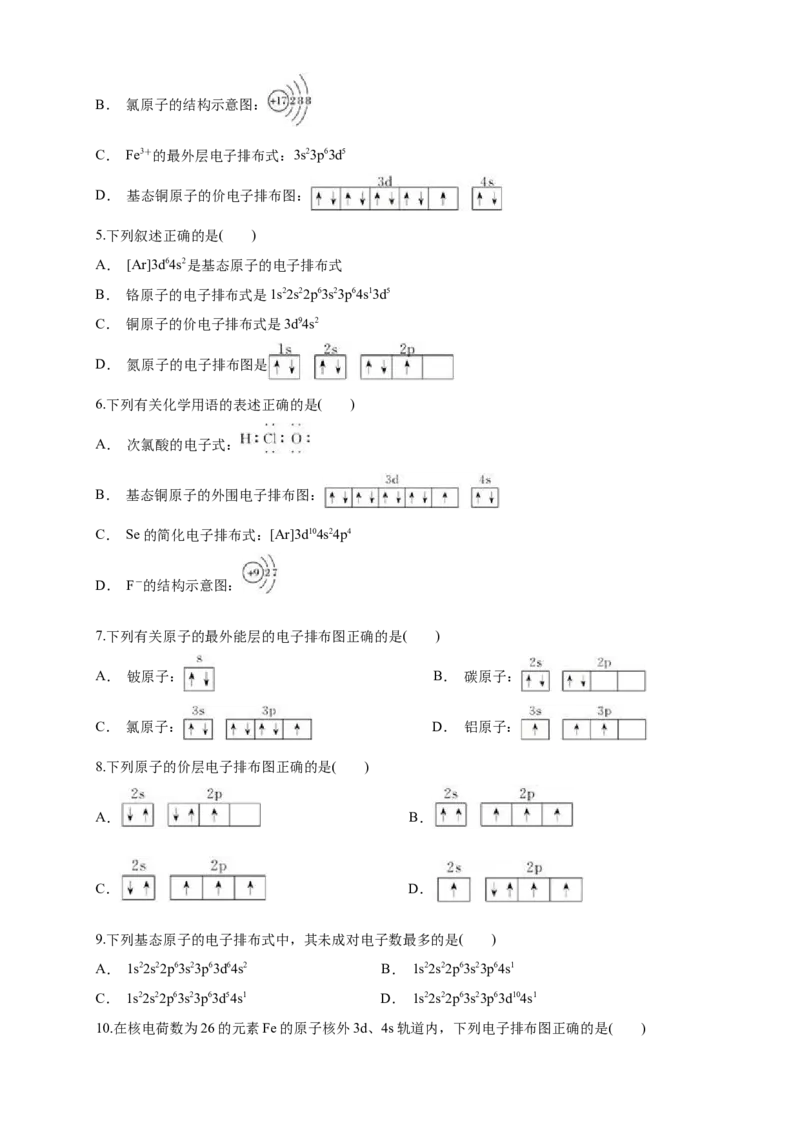
C. Fe3+的最外层电子排布式:3s23p63d5
D. 基态铜原子的价电子排布图:
5.下列叙述正确的是( )
A. [Ar]3d64s2是基态原子的电子排布式
B. 铬原子的电子排布式是1s22s22p63s23p64s13d5
C. 铜原子的价电子排布式是3d94s2
D. 氮原子的电子排布图是
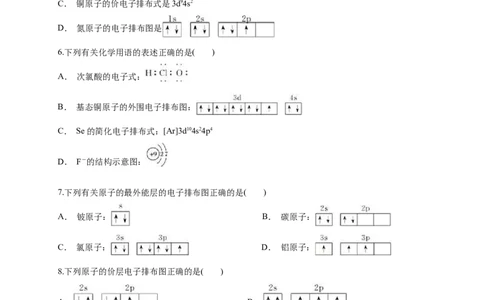
6.下列有关化学用语的表述正确的是( )
A. 次氯酸的电子式:
B. 基态铜原子的外围电子排布图:
C. Se的简化电子排布式:[Ar]3d104s24p4
D. F-的结构示意图:
7.下列有关原子的最外能层的电子排布图正确的是( )
A. 铍原子: B. 碳原子:
C. 氯原子: D. 铝原子:
8.下列原子的价层电子排布图正确的是( )
A. B.
C. D.
9.下列基态原子的电子排布式中,其未成对电子数最多的是( )
A. 1s22s22p63s23p63d64s2 B. 1s22s22p63s23p64s1
C. 1s22s22p63s23p63d54s1 D. 1s22s22p63s23p63d104s1
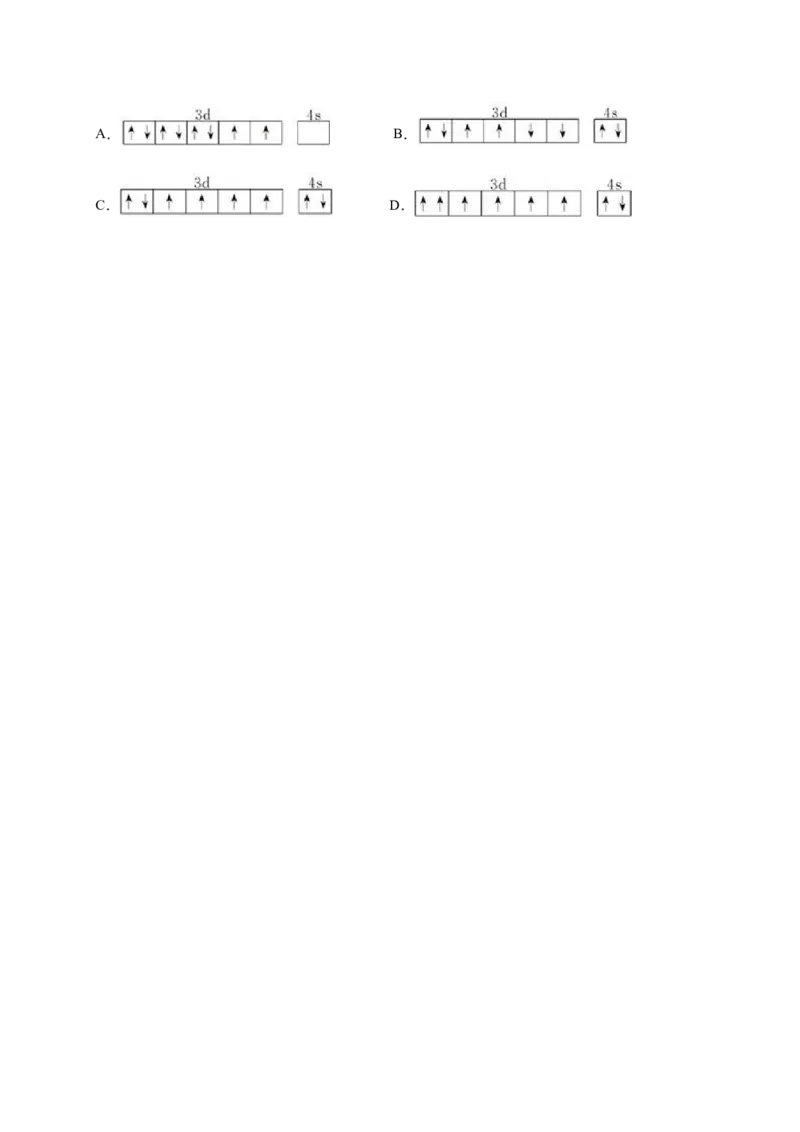
10.在核电荷数为26的元素Fe的原子核外3d、4s轨道内,下列电子排布图正确的是( )A. B.
C. D.