文档内容
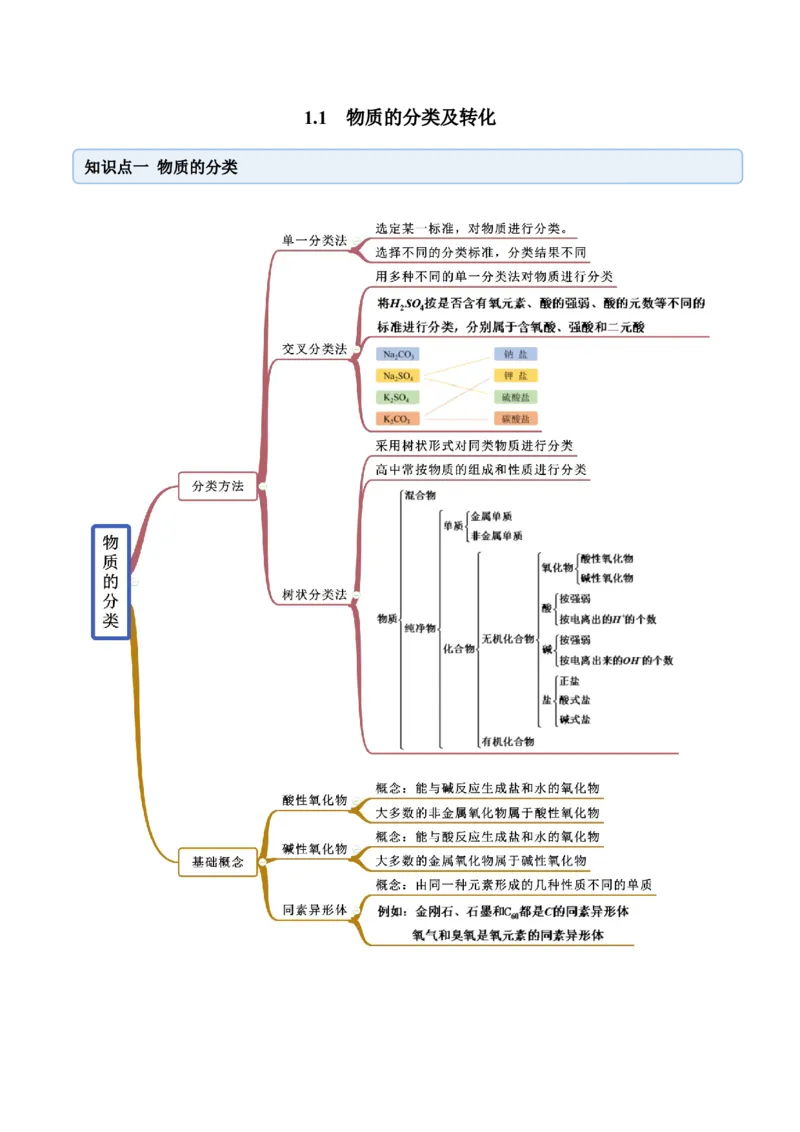
1.1 物质的分类及转化
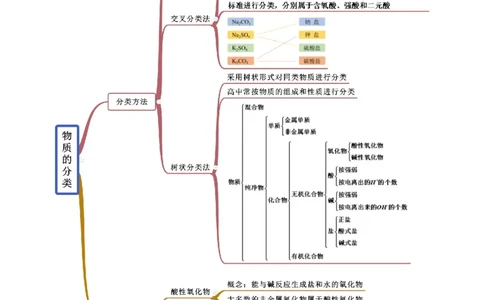
知识点一 物质的分类【例1-1】(2020·全国专题练习)分类可以使我们更好地认识物质的性质。下列物质的分类正确的是
( )
A.混合物:生铁 液氯 盐酸 B.酸性氧化物: CO NO
C.电解质:HCl D.胶体:雾 豆浆 AgCl悬浊液
【答案】C
【解析】A. 液氯属于纯净物,A项错误;
B. CO、NO不能与碱反应,不属于酸性氧化物,B项错误;
C. HCl、 均为强电解质, 属于弱电解质,C项正确;
D. 雾属于气溶胶,豆浆属于液溶胶,AgCl悬浊液不属于胶体,属于浊液,D项错误;答案选C。
碱:电离出来的阴离子全部是氢氧根离子的化合物为碱
酸:电离出来的阳离子全部是氢离子的化合物为酸
盐:由金属阳离子或铵根离子和酸根离子构成的化合物为盐
碱性氧化物:能与酸反应生成盐和水的氧化物为碱性氧化物
酸性氧化物:能与碱反应生成盐和水的氧化物为酸性氧化物
【一隅三反】
1.(2020·全国课时练习)下列物质所属类别正确的一组是
A.混合物:空气、水煤气、碱石灰
B.碱性氧化物:氧化钙、过氧化钙、氧化铁
C.酸性氧化物:二氧化硫、七氧化二锰、一氧化碳
D.正盐:氯化钠、碳酸钠、碳酸氢钠
【答案】A
【解析】A. 空气为 、 等气体的混合物,水煤气为CO、 等气体的混合物,碱石灰为CaO、
NaOH的混合物,A项正确;
B. 过氧化钙不是碱性氧化物,B项错误;
C. 一氧化碳不是酸性氧化物,C项错误;
D. 碳酸氢钠不是正盐,属于酸式盐,D项错误;故选A。
2.(2020·全国课时练习)下列物质中符合图中阴影部分表示的分类标准的是( )A. B. C. D.
【答案】B
【解析】A. 不属于钠盐,故不选A;
B. 属于正盐、碳酸盐和钠盐,故选B;
C. 不属于碳酸盐,故不选C;
D. 属于酸式盐,不是正盐,故不选D;答案选B。
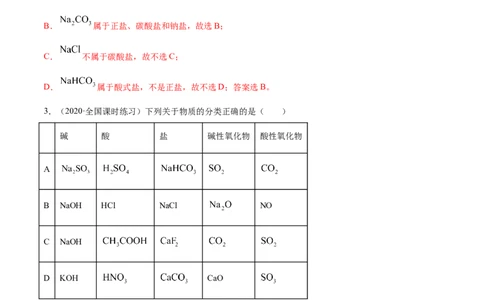
3.(2020·全国课时练习)下列关于物质的分类正确的是( )
碱 酸 盐 碱性氧化物 酸性氧化物
A
B NaOH HCl NaCl NO
C NaOH
D KOH CaO
【答案】D
【解析】A. 不属于碱, 不属于碱性氧化物,选项A错误;
B.NO不属于酸性氧化物,选项B错误;
C. 不属于碱性氧化物,选项C错误;
D.KOH属于碱, 属于酸, 属于盐,CaO属于碱性氧化物, 属于酸性氧化物,选项D正确;
答案选D。
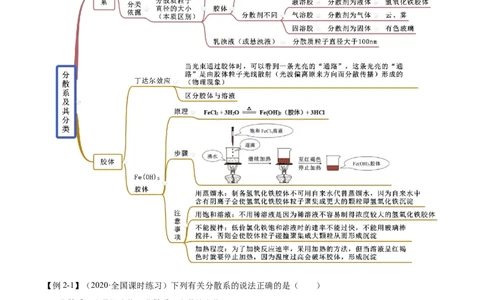
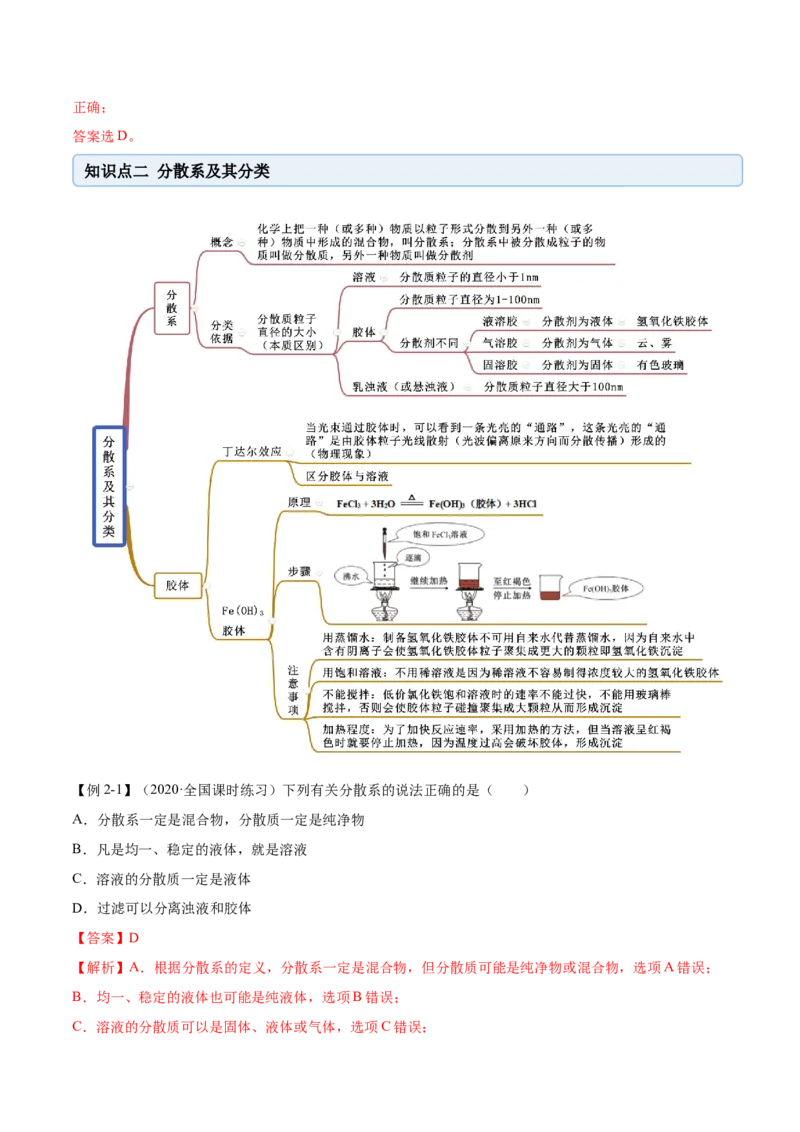
知识点二 分散系及其分类
【例2-1】(2020·全国课时练习)下列有关分散系的说法正确的是( )
A.分散系一定是混合物,分散质一定是纯净物
B.凡是均一、稳定的液体,就是溶液
C.溶液的分散质一定是液体
D.过滤可以分离浊液和胶体
【答案】D
【解析】A.根据分散系的定义,分散系一定是混合物,但分散质可能是纯净物或混合物,选项A错误;
B.均一、稳定的液体也可能是纯液体,选项B错误;
C.溶液的分散质可以是固体、液体或气体,选项C错误;D.根据分散质微粒直径的大小可知,胶体的分散质微粒可透过滤纸,而浊液的分散质微粒不能透过滤纸,
选项D正确。答案选D。
【例1-2】(2020·全国课时练习)某化学课外活动小组制备氢氧化铁胶体并检验其性质:
(1)把饱和 溶液逐滴滴入沸水中,能形成胶体,其反应的化学方程式为_______(填字母,下同)。
a
b
(2)为验证制得的分散系是胶体,下列方法中最简单的是__________。
a 用一束可见光照射该分散系,观察是否产生丁达尔现象
b 向分散系中加入氯化钠,观察是否聚沉
c 在分散系中插入石墨电极,接通直流电源,观察与直流电源负极相连的一极颜色是否变深
(3)取少量的氢氧化铁胶体于试管中,逐滴加入稀硫酸,其现象是__________。
a 出现红褐色沉淀b 红褐色溶液变为棕黄色c 先出现红褐色沉淀,然后沉淀逐渐溶解
(4)氢氧化铁胶体能稳定存在的原因是__________。
A .胶体的分散质微粒直径小于1nmB.胶体的分散质微粒均带正电荷C.胶体的分散质微粒能透过滤纸
【答案】(1)b (2)a (3)c (4)B
【解析】(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时
立即停止加热,所得的分散系称为Fe(OH) 胶体,反应的化学方程式为
3
,答案选b;(2)检验胶体最简单的方法是利用丁达尔现象,
答案选a;(3)稀硫酸产生的硫酸根离子使氢氧化铁胶体聚沉形成红褐色沉淀,然后稀硫酸与氢氧化铁反
应,沉淀溶解,答案选c;
(4)氢氧化铁胶体的分散质微粒均带正电荷,胶体的分散质微粒之间相互排斥,所以氢氧化铁胶体能稳
定存在,答案选B。
【一隅三反】
1.(2019·天山·新疆实验高一期中)胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能透过滤纸
B.胶体是纯净物,其他分散系是混合物C.胶体能产生丁达尔现象
D.胶体的分散质粒子直径在1~100nm之间
【答案】D
【解析】A.胶体的分散质能透过滤纸,溶液中的溶质也能透过滤纸,不能证明胶体的存在,A不正确;
B.胶体属于分散系,是混合物,B不正确;
C.胶体能产生丁达尔现象,这是胶体的性质,不是本质特征,C不正确;
D.胶体区分于其它分散系的本质特征是分散质粒子直径在1~100nm之间,D正确;故选D。
2.(2020·全国课时练习)下列说法不正确的是( )
A.利用丁达尔效应可以区分溶液和胶体,但这不是它们的本质区别
B.胶体的分散质粒子大小在1nm到l00nm之间,能通过滤纸不能透过半透膜
C.氢氧化铁胶体在电场作用下“红褐色”向阴极移动,是因为氢氧化铁胶粒带正电
D .将氢氧化钠浓溶液滴入饱和氯化铁溶液,制得氢氧化铁胶体
【答案】D
【解析】A.溶液与胶体的本质区别在于分散质微粒直径大小,前者小于1nm,后者介于1nm~100nm之
间,丁达尔效应是胶体的特性,利用丁达尔效应可以区分溶液和胶体,故A正确;
B.胶体与其他分散系的本质区别是分散质粒子的大小,胶体分散质粒子的直径大小在1nm~100nm之间,
能发生丁达尔效应、能透过滤纸、不能透过半透膜都是胶体的性质,故B正确;
C.胶体能发生电泳现象是由于胶体粒子带电荷,氢氧化铁胶体在电场作用下“红褐色”向阴极移动,是
因为氢氧化铁胶粒带正电,故C正确;
D.氢氧化钠是电解质,电解质可使胶体发生聚沉,向饱和FeCl 溶液中滴加氢氧化钠生成的是氢氧化铁沉
3
淀,向沸水中滴加饱和氯化铁溶液加热至红褐色液体为氢氧化铁胶体,故D错误;答案选D。
3.(2020·重庆高一期末)阅读下面短文,并回答问题。
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,
将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是
丁达尔效应。产生丁达尔效应的实质是光的散射。
表1分散系对可见光的不同作用:
溶液 胶体 浊液
光路示意图对光的主要作用 透射 散射 反射或折射
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760nm的范围,略大于
一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质
的粒子直径大于入射光的波长,主要发生反射或折射现象。
(1)产生丁达尔效应的实质是_____。
(2)制备Fe(OH) 胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的_____溶
3
液,继续煮沸至液体呈_____色即可。
(3)胶体区别于其他分散系的本质特征是_____(填序号)。
A.胶体有丁达尔效应
B.胶体粒子可以透过滤纸
C.胶体的胶粒带有电荷
D.胶体粒子的直径在1~100nm之间
(4)CuSO 溶液无明显丁达尔效应的原因是_____。
4
【答案】光的散射 FeCl 红褐 D CuSO 溶液不是胶体
3 4
【解析】(1)由题干中信息可得产生丁达尔效应的实质是光的散射。故答案为:光的散射;
(2)制备Fe(OH) 胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的FeCl 溶
3 3
液,继续煮沸至液体呈红褐色即可。故答案为:FeCl ;红褐;
3
(3)胶体区别于其他分散系的本质特征是胶体粒子的直径在1~100nm之间,故答案为:D;
(4)CuSO 溶液无明显丁达尔效应的原因是CuSO 溶液不是胶体。故答案为:CuSO 溶液不是胶体。
4 4 4
4.(2020·全国高一课时练习)取一定量 粉末(红棕色)加入适量某浓度的盐酸中,得到呈棕黄色的饱
和 溶液,所发生反应的化学方程式为_________________________________。利用此溶液进行以下实
验:
(1)取少量该 溶液置于试管甲中,滴入NaOH溶液,可以观察到有红褐色沉淀生成,反应的化学方程
式为______________________________________,此反应属于________________________(填基本反应类
型)。
(2)在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL该 溶液,继续煮沸至溶液呈__________色,即可制得 胶体。
(3)另取一小烧杯乙加入25mL蒸馏水,然后再加入2mL该 溶液,振荡均匀,将乙烧杯与另一盛有
胶体的丙烧杯一起放置在暗处,分别用红色激光笔照射烧杯中的液体,可以看到___________(填
“乙”或“丙”)烧杯中产生丁达尔效应。用这个实验可以区别________________________
(4)取丙烧杯中的少量 胶体置于试管乙中,向试管乙中滴加一定量的稀盐酸,边滴加边振荡,在
此过程中可看到试管乙中生成的红褐色沉淀逐渐溶解,最终又得到棕黄色的溶液,发生此变化的化学方程
式为___________________________________,此反应属于_____________________(填基本反应类型)。
【答案】
(1) 复分解反应 (2)红褐
(3)丙 胶体和溶液
(4) 复分解反应
【解析】取一定量 粉末(红棕色)加入适量某浓度的盐酸中,得到呈棕黄色的饱和 溶液,所发生
反应的化学方程式为 。
(1) 与NaOH反应有红褐色氢氧化铁沉淀生成,反应的化学方程式为
,此反应属于复分解反应。
(2)氢氧化铁胶体的制备:在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL该 溶
液,继续煮沸至溶液呈红褐色,即可制得 胶体。
(3)胶体具有丁达尔效应,而溶液不具有,故可以看到丙烧杯中产生丁达尔效应,丁达尔效应可以区溶液和
胶体。
(4)向少量 胶体中中滴加一定量的稀盐酸,边滴加边振荡,在此过程中氢氧化铁胶体先发生聚沉产生红褐色沉淀氢氧化铁,氢氧化铁再与盐酸反应生成氯化铁和水,化学方程式为
,此反应属复分解反应。
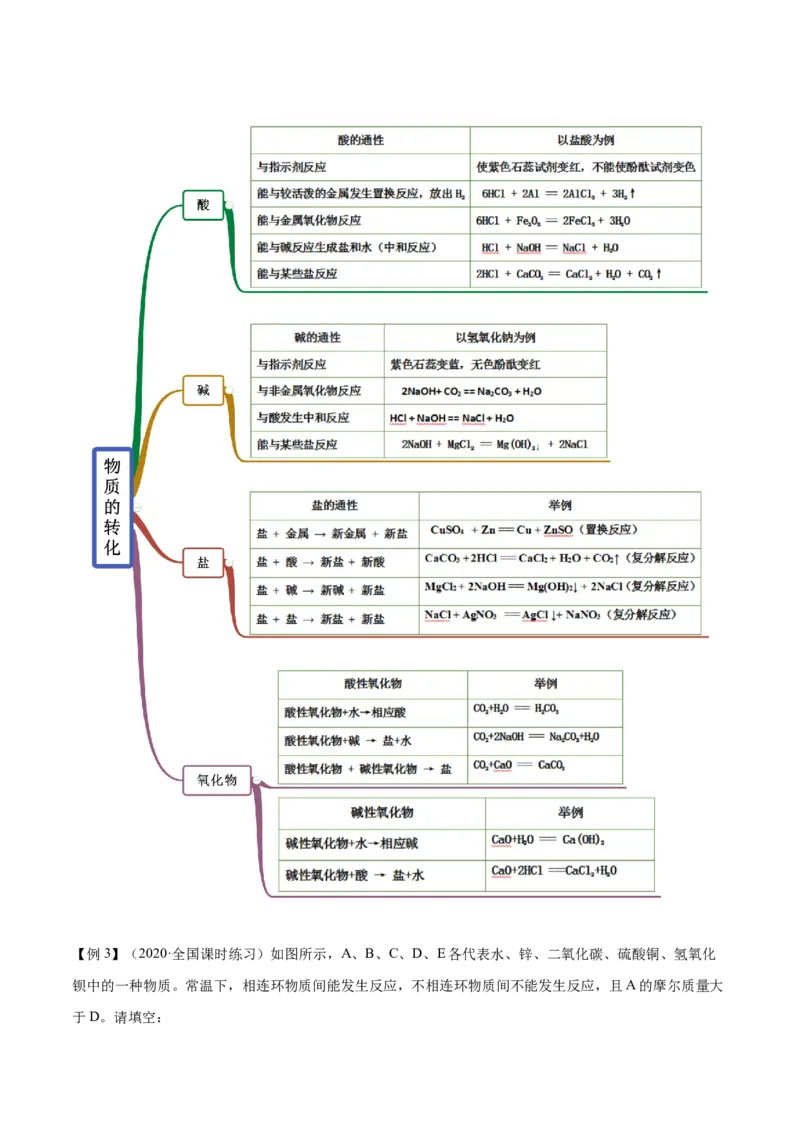
知识点三 物质的转化【例3】(2020·全国课时练习)如图所示,A、B、C、D、E各代表水、锌、二氧化碳、硫酸铜、氢氧化
钡中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且A的摩尔质量大
于D。请填空:(1)写出下列物质的化学式:A_______________,D_______________,E_______________。
(2)写出B与C反应的化学方程式:_______________。
(3)相连环物质间发生的反应中,置换反应共有_______________个。
【答案】(1)Zn
(2)
(3)1
【解析】(1) Zn能与CuSO 溶液反应,CuSO 能与Ba(OH) 反应,Ba(OH) 能与CO 反应,CO 能与HO反
4 4 2 2 2 2 2
应,故A和E是Zn和HO中的一种,B和D为CuSO 或CO 中的一种,由于相对分子质量:B>D,故B
2 4 2
是CuSO ,D是CO,A是Zn,C是Ba(OH) ,E是HO,所以A的化学式是Zn;D的化学式是CuSO ;E
4 2 2 2 4
的化学式是CO;
2
(2)B是CuSO ,D是Ba(OH) ,CuSO 和Ba(OH) 反应生成BaSO 沉淀和Cu(OH) 沉淀,反应的化学方程式
4 2 4 2 4 2
为:CuSO +Ba(OH) =BaSO ↓+ Cu(OH) ↓;
4 2 4 2
(3)置换反应是单质和化合物反应产生另一种单质和另一种化合物的反应。在上述反应中单质只有Zn,因
此Zn与CuSO 反应产生ZnSO 和Cu的反应为置换反应,其它反应均不是置换反应,故属于置换反应的只
4 4
有1个。
【一隅三反】
1.(2020·全国课时练习)下列物质在给定条件下的转化均能一步实现的是
A.Fe O Fe FeCl
3 4 3
B.HO H HO
2 2 2 2
C.CaCl 溶液 CaCO CO
2 3 2
D.CuSO 溶液 Cu CuO
4
【答案】D
【解析】A. 铁与稀盐酸反应生成的是氯化亚铁,不是氯化铁,不能一步实现,A错误;B. 过氧化氢分解生成的是氧气和水,不能生成氢气,B错误;
C. 由于盐酸的酸性大于碳酸,所以氯化钙溶液中通入二氧化碳,不能生成碳酸钙沉淀,C错误;
D. 铁比铜活泼,故铁可以与硫酸铜反应生成硫酸亚铁和铜,铜可以与氧气反应生成氧化铜,D正确;
答案选D。
2.(2018·江苏省上冈高级中学高一期中)某同学要在奥运五连环中填入物质,使相连物质间能发生反应,
不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是 ( )
A.硫酸镁B.氧气C.二氧化碳D.氧化钙
【答案】C
【解析】由信息可知,相连环物质间能发生反应,不相连环物质间不能发生反应,
, ,
二氧化碳为酸性氧化物和氢氧化钠溶液反应生成盐和水,二氧化碳高温下和碳反应生成一氧化碳,
, ,
稀硫酸和碳不反应,氧气和氢氧化钠溶液不反应,氧气与Fe反应,氧化钙和碳不反应,
“五连环”中有空缺的一环应填入的物质为CO。故选C。
2
3.(2020·全国课时练习)初中化学常见物质A-I分别是下列物质中的一种:锌、氢氧化钠、硫酸铜溶液、
稀盐酸、碳酸钠溶液、石灰水、生石灰、石灰石和水。他们之间相互的反应(每种物质只能用一次)恰好
包含了化合反应(A+B)、分解反应(C)、置换反应(D+E)、中和反应(F+G)、复分解反应(H+I)
等反应类型。试回答下列问题:
(1)A+B的反应化学方程式是______________________。
(2)C的化学式为___________;硫酸铜溶液参加___________反应(填反应类型)。
(3)H+I的反应方程式是_________________________________。
【答案】(1)CaO+H O =Ca(OH) (2)CaCO 置换
2 2 3
(3)NaCO+Ca(OH) =CaCO +2NaOH
2 3 2 3
【解析】(1)所有物质中能发生化合反应的是氧化钙与水的反应,反应方程式为CaO+H O =Ca(OH) 。
2 2
(2)所有物质中能发生分解反应的是碳酸钙,则C为CaCO ;硫酸铜与锌发生置换反应。
3