文档内容
化学反应速率的影响因素
【学习目标】
知识与技能:
1.探究温度、浓度和催化剂对化学反应速率的影响结果
2.进一步理解化学反应速率的概念及表示方法。
3.进一步掌握影响化学反应速率的因素。
【学习重难点】
重点:影响化学反应速率的外界因素。
难点:实验方法的选择及反应条件的控制在实验探究中的重要性。
【学习过程】
[引入]
1.由现象到本质(带着问题走出课本):
利用蓝瓶子实验引入课题:实验比较法研究影响化学反应速率的外界因素。同样的试剂,
用不同的力度振荡,显示蓝色的程度不一样。说明外因对反应的快慢有影响。
[对旧知识的回顾]
2.由定性到定量
(1)化学反应速率的表示方法:__________。
(2)化学反应速率的测定方法:测定的数据:时间变化 ∆ t,浓度变化∆C
还可以测定其它哪些物理量也可以获得反应速率?(学生讨论)
①单位时间内产生_____体积: 如H O 分解制O 或CO 的制取
2 2 2 2
②单位时间内体系_____变化: 如有关NO 、I (淀粉)的反应
2 2
③单位时间内产物质量变化
④单位时间内体系压强变化
视频演示H O 分解制O 反应速率的测定方法,了解描点法作图的方法。
2 2 2
3.由理论到实际(学会探究)
本堂课的主要任务是利用实验探究浓度和温度对 S O 2- + 2H+ = SO + S + H O反应速
2 3 2 2
率的影响;利用实验探究催化剂对H O 分解速率的影响。
2 2
(1)如何测该反应的速率?测单位时间内 SO 的体积产量,还是S单质的固体产量?浑
2浊度
如何测该反应的速率?气泡出现的快慢
(2)讨论下列哪些外界因素对该反应有影响?
①浓度 ②温度 ③ 催化剂
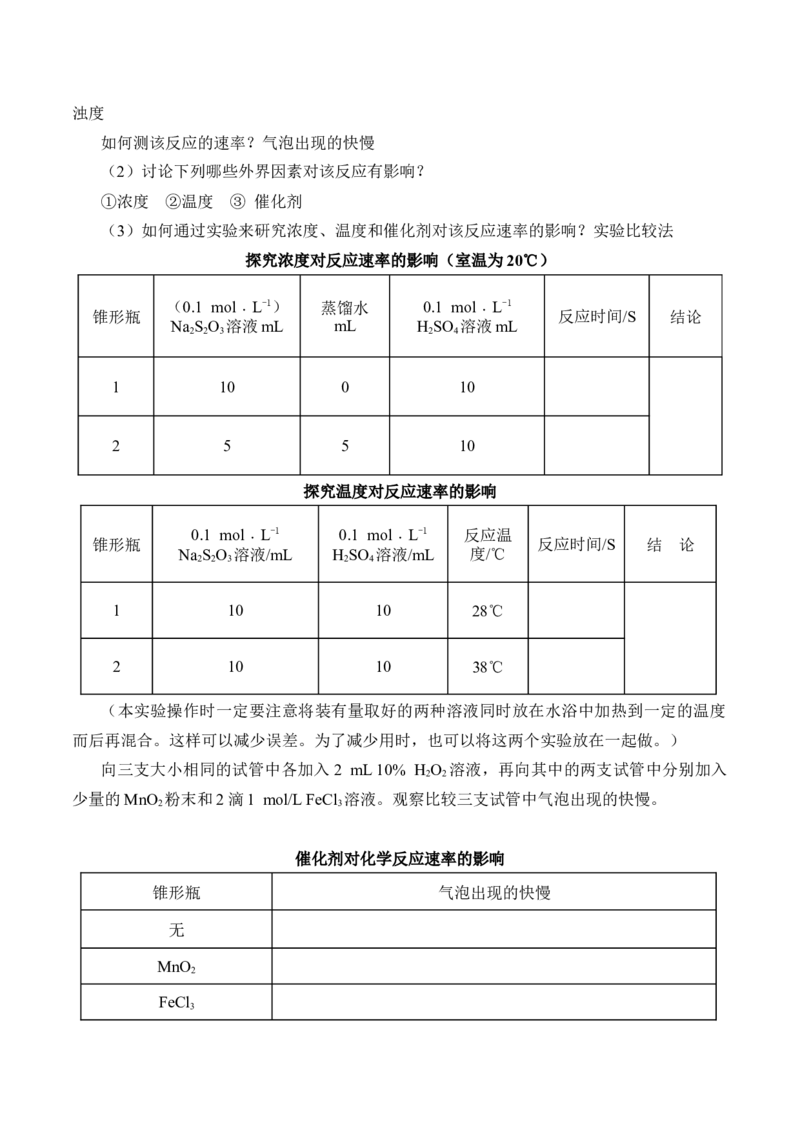
(3)如何通过实验来研究浓度、温度和催化剂对该反应速率的影响?实验比较法
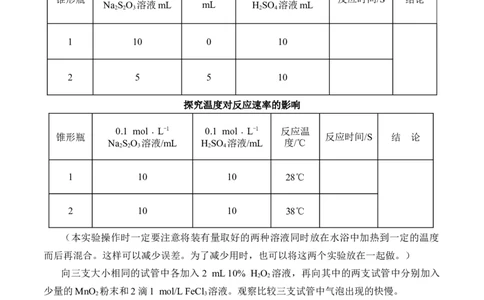
探究浓度对反应速率的影响(室温为20℃)
(0.1 mol﹒L-1) 蒸馏水 0.1 mol﹒L-1
锥形瓶 反应时间/S 结论
Na S O 溶液mL mL H SO 溶液mL
2 2 3 2 4
1 10 0 10
2 5 5 10
探究温度对反应速率的影响
0.1 mol﹒L-1 0.1 mol﹒L-1 反应温
锥形瓶 反应时间/S 结 论
Na S O 溶液/mL H SO 溶液/mL 度/℃
2 2 3 2 4
1 10 10 28℃
2 10 10 38℃
(本实验操作时一定要注意将装有量取好的两种溶液同时放在水浴中加热到一定的温度
而后再混合。这样可以减少误差。为了减少用时,也可以将这两个实验放在一起做。)
向三支大小相同的试管中各加入2 mL 10% H O 溶液,再向其中的两支试管中分别加入
2 2
少量的MnO 粉末和2滴1 mol/L FeCl 溶液。观察比较三支试管中气泡出现的快慢。
2 3
催化剂对化学反应速率的影响
锥形瓶 气泡出现的快慢
无
MnO
2
FeCl
3教师先进行演示操作方法,要求学生认真观察,之后进行分组实验,实验完成后交流讨
论。要求组内合作,组间共享。学会数据处理的一般方法。
如何设计实验探究pH对该反应速率的影响?还缺什么实验用品?请讨论后拟定一个实验
方案。
4.学会运用
(1)介绍利用传感器探究浓度对反应速率的影响的实验方法。
(2)讨论与课本实验相比的优点。
[精练反馈]
1.100mL 6mol/L的硫酸和过量的锌粉反应,在一定温度下,为了减缓反应进行的速率,
但又不影响生成氢气的总量,可向溶液中加入适量的( )
A.碳酸钠固体 B.水 C.硝酸钾溶液 D.硫酸铵固体
2.把下列四种X溶液,分别加进四个盛有10mL、2mol/L的盐酸的烧杯中,并且均加水稀
释至50mL,此时,X和盐酸缓缓地进行反应,其中反应速率最快的是( )
A.10mL 2mol/L B.20mL 2mol/L C.10mL 4mol/L D.20mL 3mol/L
3.下列关于压强对化学反应速率的影响的说法中不正确的是( )
A.对任何化学反应,增大压强都可以加快它们的反应速率
B.对于气体反应,增大压强相当于增大反应物浓度,所以反应速率加快
C.增大压强可以加快合成氨的反应速率
D.对于液态或固态反应物,由于压强对它们体积改变很小,可以认为压强与它们的反应
速率无关
4.下列反应中,当其他条件不变时增大压强,化学反应速率加快的是( )
① ②③ ④
A.只有① B.①②③ C.①③④ D.全部
5.在恒温恒容的密闭容器中进行反应:A(g) B(g) + 2C(g)。若反应物的浓度由 2mol/L
降到0.8mol/L需要20s,那么反应物浓度由2mol/L降到1.4mol/L,所需要的时间( )
A.等于10s B.大于10s C.小于10s D.无法判断
6.对已达平衡的下列反应:2X(g)+Y(g) 2Z(g),减小压强对反应产生的影响是
( )
A.逆反应速率增大,正反应速率减小,平衡逆向移动
B.逆反应速率减小,正反应速率增大,平衡正向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
7.在一密闭容器中充入1mol H 和1mol I ,压强为P(Pa),并在一定温度下发生反应:
2 2
H (g)+I (g) 2HI(g)
2 2
①保持容器容积不变,向其中加入 1mol H ,反应速率加快吗?________,理由是
2
____________________________________________________________。
②保持容器容积不变,向其中加入 1mol N (N 不参与反应),反应速率加快吗?
2 2
________,
理由是____________________________________________________________。
③保持容器中气体压强不变,向其中加入1mol N (N 不参与反应),反应速率________,
2 2
理由是____________________________________________________________。
④保持容器中气体压强不变,向其中加入1mol H 和1mol I (g),反应速率________,
2 2
理由是____________________________________________________________。
8.氯酸钾和亚硫酸氢钠发生氧化还原反应生成-1价的氯和+6价的硫的速率如图所示,已
知这个反应的速率除了与反应物浓度有关外,还随着溶液中增大而加快。
①写出该反应的离子方程式__________________________________________
② 为什么反应开始时反应速率加快__________________________________________③ 为什么反应后期反应速率下降__________________________________________