文档内容
第二章 分子结构与性质
第一节 共价键
第一课时 共价键
基础达标
1.下列说法中不正确的是( )
A.σ键是原子轨道以“头碰头”的方式相互重叠
B.π键的电子云形状与σ键的电子云形状相同
C.两个原子形成多个共价键时,σ键只有一个
D.形成共价键时原子轨道之间重叠程度越大,体系能量越低,键越稳定
【答案】B
【解析】σ键是原子轨道以“头碰头”的方式相互重叠,A项正确;π键的电子云形状
与σ键的电子云形状不同,B项错误;双键、三键中,只有一个σ键,其他为π键,C项正
确;形成共价键时原子轨道之间重叠程度越大,键越稳定,体系能量越低,D项正确。
2.根据氢原子和氟原子的核外电子排布,下列对 F 和HF分子中共价键的描述正确的是
2
( )
A.两者都是s-sσ键
B.两者都是p-pσ键
C.前者为p-pσ键,后者为s-pσ键
D.前者为s-sσ键,后者为s-pσ键
【答案】C
【解析】H、F原子的核外电子排布式分别为1s1、1s22s22p5,形成F 时,两个F原子的
2
2p轨道发生重叠,未成对电子形成共用电子对,故F 中共价键是p-pσ键。形成HF时,H
2
原子的1s轨道和F原子的2p轨道发生重叠,未成对电子形成共用电子对,故HF分子中共
价键是s-pσ键。
3.下列说法不正确的是( )
A.H 分子中含σ键而N 分子中还含π键
2 2
B.π键是由两个p轨道“肩并肩”重叠形成的
C.乙烷分子中的键全为σ键而乙烯分子中含σ键和π键D. σ键一定是有s轨道参与形成的
【答案】D
【解析】H 分子中只含有H—H单键,只有σ键,N 分子中含有N≡N键,含有σ键和
2 2
π键,故A正确;π键是由两个轨道“肩并肩”重叠形成,σ键是“头碰头”重叠形成,故
B正确;乙烷分子中均为单键,乙烯中含 C=C键,有1个π键,则乙烷分子中的键全为σ
键而乙烯分子中含σ键和π键,故C正确;p-pσ键中没有s轨道参加,故D错误。
4.已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,N一N、N=N、
N≡N键的键能之比为1.00:2.17:4.90,而C—C、C=C、C≡C键的键能之比为1.00:1.77:2.34下
列有关叙述不正确的是( )
A.乙烯分子中σ键、π键的电子云形状对称性不同
B.乙炔分子中π键重叠程度比σ键小,易发生加成反应
C.氮分子中的N≡N键非常牢固,不易发生加成反应
D.氮气和乙炔都易在空气中点燃
【答案】D
【解析】由题意知,N≡N键键能大于N—N键键能的三倍,N=N键键能大于N一N键
键能的两倍;而C≡C键键能小于C—C键键能的三倍,C=C键键能小于C-C键键能的两
倍。说明乙炔分子和乙烯分子中的π键不牢固,易发生加成反应,也易发生氧化反应;而
氮分子中的N≡N键非常牢固,化学性质稳定,不易发生加成反应及氧化反应。σ键的电子
云形状呈轴对称,π键的电子云形状呈镜面对称。
5.下列说法正确的是( )
①共价键的本质是相互吸引的电性作用
②共价化合物一定含共价键,一定不含离子键
③水的非直线形结构是由共价键的饱和性决定的
④由非金属元素组成的化合物一定是共价化合物
⑤分子中不一定存在共价键
⑥烯烃比烷烃的化学性质活泼是由于烷烃中的σ键比烯烃中的σ键稳定
A.②⑤ B.④⑥ C.②③④ D.①③⑥
【答案】A
【解析】共价键的本质是电性作用而不是相互吸引,①错误;有离子键的化合物为离
子化合物,所以共价化合物中没有离子键,②正确;水的非直线形结构是由共价键的方向
性决定的,③错误;氯化铵中只有非金属元素,但是它是离子化合物,④错误;稀有气体分子中没有共价键,⑤正确;烯烃比烷烃活泼是因为烯烃中的π键比较活泼,⑥错误。
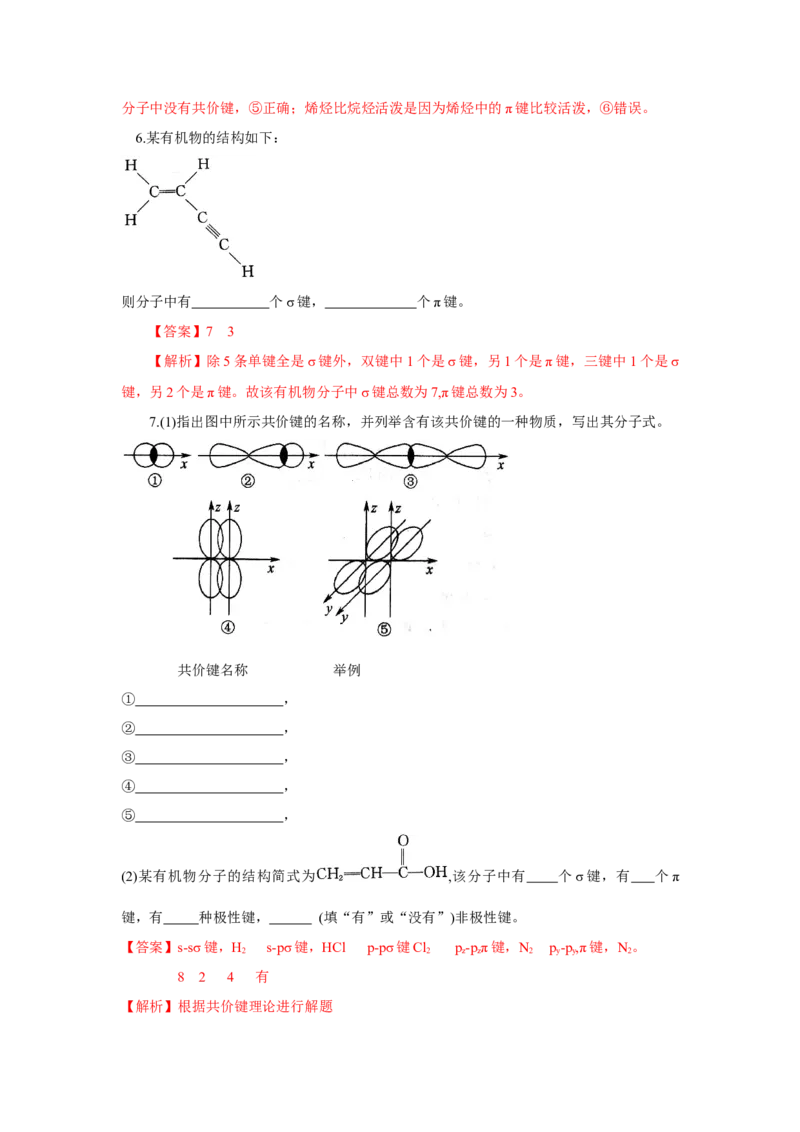
6.某有机物的结构如下:
则分子中有 个σ键, 个π键。
【答案】7 3
【解析】除5条单键全是σ键外,双键中1个是σ键,另1个是π键,三键中1个是σ
键,另2个是π键。故该有机物分子中σ键总数为7,π键总数为3。
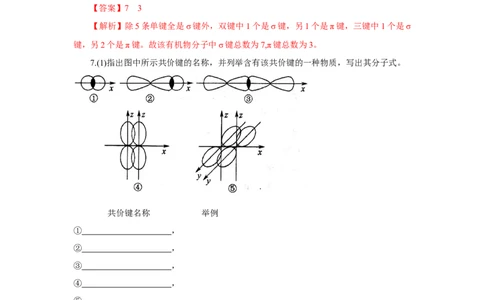
7.(1)指出图中所示共价键的名称,并列举含有该共价键的一种物质,写出其分子式。
共价键名称 举例
① ,
② ,
③ ,
④ ,
⑤ ,
(2)某有机物分子的结构简式为 ,该分子中有 个σ键,有 个π
键,有 种极性键, (填“有”或“没有”)非极性键。
【答案】s-sσ键,H s-pσ键,HCl p-pσ键Cl p-pπ键,N p-p,π键,N。
2 2 z z 2 y y 2
8 2 4 有
【解析】根据共价键理论进行解题能力提升
8.下列分子中,既有σ键又有π键的是( )
①CH; ②CO ; ③N; ④H O; ⑤C H; ⑥HClO
4 2 2 2 2 2 4
A.①②③④⑤⑥ B.②③④⑤⑥ C.②③④⑤ D.②③⑤
【答案】D
【解析】① CH 中只含有 C-H 键,所以分子中不含有 π 键;② CO 的结构式为
4 2
O=C=O,所以分子中既有σ键又有π键;③N 的结构式为N≡N,所以分子中既有σ键又有π
2
键;④ HO 的结构式为 H—O—O—H,所以分子中不含有 π 键;⑤ C H 的结构简式为
2 2 2 4
CH=CH ,所以分子中既有σ键又有π键;⑥HClO的结构式为H—O—Cl,所以分子中不含
2 2
有π键。答案:D
9.下列有关化学键类型的判断不正确的是( )
A.s-s σ键与s-p σ键的对称性相同
B.分子中含有共价键,则至少含有一个σ键
C.已知乙炔的结构式为 H—C≡C—H,则乙炔分子中存在 2个σ键(C—H)和3个π键
(C≡C)
D.乙烷分子中只存在σ键,即6个C一H键和1个C-C键都为σ键,不存在π键
【答案】C
【解析】s-sσ键无方向性,s-pσ键轴对称,A正确;在含有共价键的分子中一定有 σ
键,B正确;单键都为σ键,乙烷分子结构式为 ,其中6个C一H键和1个C
—C键都为σ键,D正确;共价三键中一个为σ键,另外两个为π键,故乙炔(H-C≡C-H)分
子中有2个C-Hσ键,C≡C键中有1个σ键、2个π键,C错误。
10. NF 分子中四个原子都在同一平面内,由于几何形状的不同,存在顺式和反式两种
2 2
同分异构体。据此判断NF 分子中两个N原子之间化学键的组成为( )
2 2
A.一个σ键和两个π键 B.仅有一个σ键 C.仅有一个π键 D.一个σ键和一
个π键【答案】D
【解析】氮原子最外有5个电子,形成3对共用电子对达到稳定结构,由题干知NF
2 2
为平面结构,且有顺式和反式两种同分异构体,可推测知分子中存在 N=N,其结构式为F-
N=N-F,所以两个氮原子之间含有一个σ键和个π键。
11.a、b、c、d为四种由短周期元素构成的中性粒子,它们都有 14个电子,且粒子内部
以共价键结合。请回答下列问题。
(1)a 单质由原子组成,a 单质可用作半导体材料,a 原子核外电子排布式为
。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为 。人一旦吸入
b 气 体 后 , 就 易 引 起 中 毒 , 是 因 为
。
(3)c是双核单质,写出其电子式: 。分子中所含共价键的类型
为
(填“极性键”或“非极性键”)。
(4)d是四核化合物,其结构式为 ;d分子内所含共价键有 个σ
键, 个π键;σ键与π键的强度大小关系为σ π(填“>”“<”或“=”),原因是
【答案】(1)1s22s22p63s23p2
(2)CO CO会与血液中的血红蛋白结合,使血红蛋白丧失输送氧气的能力
而中毒
(3) 非极性键
(4)H-C≡C-H 3 2 > 形成σ键的原子轨道的重叠程度比π键的重叠程
度大,形成的共价键强。
【解析】(1)由题意知,a是Si,Si可作半导体材料;(2)b是含两个原子的化合物,根据
其性质:无色无味气体,易引起中毒,推断b为CO,CO一旦进入肺里,会与血液中的血红
蛋白结合而使血红蛋白丧失输送氧气的能力,使中毒;(3)c是双原子单质,每个原子有7
个电子,故c为N,含非极性键;(4)d是四核化合物,即4个原子共有14个电子,只能是
2
经,故d为C H,C H 的结构式为H-C≡C-H,有两个H-Cσ键,一个C-Cσ键,两个π键。
2 2 2 2直 击 高 考