文档内容
第二章 海水中的重要元素—钠和氯
第一节 钠及其化合物
第二课时 钠的几种化合物 焰色试验
【学习目标】1.通过NaO、NaO 与水反应的对比实验探究、原理分析,掌握钠的两种氧化物的重要
2 2 2
性质,建立基于类别、核心元素价态等认识物质性质、设计物质转化的基本思维模型。
2.通过NaCO 、NaHCO 的水溶性和稳定性的实验探究,掌握两种钠盐性质上的异同点及二者之间的
2 3 3
相互转化关系,培养证据推理与模型认知、科学探究与创新意识的化学核心素养。
3.通过学习碳酸钠和碳酸钾焰色试验,知道焰色试验的操作方法,掌握钠、钾及其化合物的检验方
法,了解焰色试验在生产和生活中的应用,感受化学的魅力,
【学习重点】NaO、NaO 的性质、NaCO、NaHCO 的性质及相互转化
2 2 2 2 3 3
【学习难点】NaO 的化学性质、NaCO、NaHCO 的相互转化
2 2 2 3 3
【课前预习】
旧知回顾:1.氧化物的定义: 。氧化物
可分为 等。
2.NaO 属于 氧化物(填“酸性”或“碱性”)能和 、 、 等物质
2
反应,化学方程式分别为: 。NaOH是一
种强碱,俗称 、 、 ,在空气中易吸收 而发生 。能和 、
、 _______等物质反应。
新知预习: 1.而过氧化钠是 氧化物。氧化钠和过氧化钠均能与水的反应,其化学方程式分
别为: 、 ;它们与CO 反应的化学方程式
2
分别为: 、 。
.
2.按照组成元素分类,碳酸钠和碳酸氢钠属于 盐,碳酸钠具有 性,而碳酸氢
钠
受热易 。化学方程式为 。
【课中探究】
情景导入:趣味实验“滴水生火”。把少量淡黄色粉末平铺在脱脂棉上,用玻璃棒轻轻压拨,使粉末
进入脱脂棉中,用胶头滴管滴加蒸馏水,观察棉花会燃烧。这是为什么呢?
一、氧化钠和过氧化钠
活动一、探究氧化钠和过氧化钠与水的反应
任务一、结合教材P37“思考与讨论”,联系碱性氧化物的通性,思考氧化钠具有哪些重要的化学性
质?你认为基于物质类别研究物质性质的认知模型时什么?任务二、类比NaO,预测NaO 的化学性质,完成教材P37【实验2-3】,观察过氧化钠与水的反应
2 2 2
现象,思考其原理,填写下表内容。
【答案要点】①预测:
②实验探究:NaO 与水的反应。
2 2
实验操作
将1⁓2 mL水滴入盛有1~2 g过氧化钠固体的试管中立即把带火星的木条伸入
试管中,检验生成的气体;用手轻轻触摸试管外壁,感受有什么变化;用PH试
纸检验溶液的酸碱性,观察有何现象。
实验现象
实验结论
【对应练习】1.NaO和NaO 具有相似的性质是( )
2 2 2
A.颜色 B.水溶液的酸碱性 C.氧化性 D.碱性氧化物
2.在一定温度下,向饱和的烧碱溶液中加入一定量的过氧化钠,充分反应后恢复到原来温度,下列
说法正确的是( )
A.溶液中Na+浓度增大,有O 放出 B.溶液碱性不变,有H 放出
2 2
C.溶液中Na+数目减少,有O 放出 D.溶液碱性增强,有O 放出
2 2
活动二、探究氧化钠和过氧化钠与CO 的反应
2
任务一、实验探究“吹气生火”:把少量淡黄色粉末平铺在脱脂棉上,用玻璃棒轻轻压拨,使粉末进
入脱脂棉中。用细长玻璃管向淡黄色粉末中缓缓吹气,观察现象,思考其原理?(见PPT视频)
任务二、归纳小结:比较氧化钠与过氧化钠的异同点,完成下表内容。名称 氧化钠 过氧化钠
化学式
氧的价态
颜色状态
生成条件
与水反应
与 CO 反
2
化
应
学
性 相同点
质
不同点
任务三、根据NaO 与水反应的原理,请写出NaO 与盐酸反应的化学方程式,由此说明NaO 属于碱
2 2 2 2 2 2
性氧化物吗?为什么?
【对应训练】1.下列关于过氧化钠和氧化钠性质异同点的叙述中错误的是( )
A.长期置于空气中最终所得固体产物相同
B.都能与二氧化碳或水发生化合反应
C.与水反应都有氢氧化钠生成
D.过氧化钠是强氧化剂,而氧化钠只是一种碱性氧化物
2.下列叙述正确的是( )
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②Na O与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成O
2 2 2 3 2 2 2 2
③Na O是淡黄色物质,NaO 是白色物质
2 2 2
④Na O 可作供氧剂,而NaO不可
2 2 2
⑤Na O 和NaO焰色反应均为黄色
2 2 2
A.都正确 B.①③④
C.②③⑤ D.④⑤
二、碳酸钠和碳酸氢钠
活动一、探究碳酸钠和碳酸氢钠的物理性质
任务一、根据教材P38页【实验2-4】:在两支试管中分别加入少量NaCO 和NaHCO (各约 1 g),完成
2 3 3
下列实验,并将实验现象和相应的结论填入下表:
实验操作 NaCO NaHCO
2 3 3①观察NaCO 和NaHCO 的外观并
2 3 3
进行描述
②向以上两支试管中分别滴入几滴
水,振荡,观察现象;将温度计分
别插入其中,温度计的示数有何变
化
③继续向②的试管中分别加入 5
mL 水,用力振荡,有何现象
④分别向③所得的溶液中滴入1~2
滴酚酞溶液,有何现象
初步结论
任务二、观察样品,结合上述实验,比较碳酸钠和碳酸氢钠的物理性质,联系生活实际,说出你所知
道的它们的用途,填写下表内容。
名称 碳酸钠 碳酸氢钠
化学式
俗名
颜色、状态
水溶性
用途
任务三、问题探究:金属钠长期暴露于空气中,最终生成的什么物质?写出核心化学方程式。
【对应训练】1.下列关于小苏打的叙述准确的是( )
A.化学式为NaCO B.受热不分解 C.属于盐 D.与盐酸不反应
2 3
2.现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶
解于水得到溶液,并采取下列措施,其中可以实现实验目的的是( )
A.测所得溶液的pH
B.取溶液少量,向其中滴入酚酞观察溶液是否变红
C.取溶液少量,向其中加入盐酸观察是否有气泡产生
D.取溶液少量,向其中加入CuSO 溶液,观察是否有沉淀产生
4
活动二、探究碳酸钠和碳酸氢钠的稳定性
任务一、实验探究:根据教材P39页【实验2-5】,按图示装置分别给碳酸钠、碳酸氢钠加热,比较它们的稳定性,完成下表内容。
实验装置
实验原理
实验用品 NaCO 固体、NaHCO 固体、澄清石灰水;硬质试管、试管、酒精灯、铁架台。
2 3 3
实验步骤 如图所示,分别加热 NaCO 固体和NaHCO 固体,观察实验现象,比较碳酸钠、碳酸氢钠
2 3 3
的热稳定性。
实验现象
实验结论
实验说明
任务二、问题探究:实验过程中,若通入二氧化碳时间较长,发现澄清的石灰水先变浑浊然后又变
清,你知道为什么吗? 若将澄清石灰水换成饱和碳酸钠,又会有什么现象呢?
【对应训练】1.有关NaHCO 和NaCO 的性质,以下叙述错误的是( )
3 2 3
A.等质量的NaHCO 和NaCO 与足量盐酸反应,在相同条件下NaCO 产生的CO 体积大
3 2 3 2 3 2
B.等物质的量的NaCO 和NaHCO 与同浓度盐酸完全反应,所消耗盐酸的体积NaCO 是NaHCO 的
2 3 3 2 3 3
两倍
C.向NaCO 饱和溶液中通入CO,有NaHCO 结晶析出
2 3 2 3
D.NaCO 溶液和NaHCO 溶液都呈碱性
2 3 3
2.下列有关NaCO 和NaHCO 的叙述中正确的是( )
2 3 3
A.向NaCO 溶液中逐滴加入等物质的量的稀盐酸,生成的CO 与原NaCO 的物质的量之比为1:2
2 3 2 2 3
B.等质量的NaHCO 和NaCO 分别与足量盐酸反应,在同温同压下,生成的CO 体积相同
3 2 3 2
C.相同温度下物质的量浓度相同时,NaCO 溶液的pH小于NaHCO 溶液
2 3 3
D.用套管实验比较NaCO 和NaHCO 分解温度高低,将NaHCO 放在内部小试管中
2 3 3 3
活动三、焰色试验任务一、实验:分小组完成教材P40页【实验2-6】或观看视频实验,注意操作方法,并观察常见几
种金属的焰色试验颜色填写在下表中。
常见一些金属元素的焰色
金属元素 锂 钠 钾 铷
焰色
金属元素 钙 锶 钡 铜
焰色
任务二、讨论交流:什么是焰色试验?在做焰色试验时,要注意哪些问题?填写下表内容。
定义
实验 碳酸钠溶液、碳酸钾溶液、盐酸;铂丝(或铁丝)、酒精灯(或煤油灯)、蓝色钴玻璃。
用品
①把熔嵌在玻璃棒上的铂丝(或用光洁无锈的铁丝)放在酒精灯(最好用煤气灯)外焰里灼
烧,至与原来火焰颜色相同时为止。用铂丝(或铁丝)蘸取碳酸钠溶液,在外焰上灼烧,观
实验 察火焰颜色。
步骤
②将铂丝(或铁丝)用盐酸洗净后,在外焰上灼烧至没有颜色时,再蘸取碳酸钾做同样的实
验,此时要透过蓝色钴玻璃观察火焰的颜色。
实验
注意
事项
【对应练习】1.利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩。下
列说法中正确的是 ( )
A.非金属单质燃烧时火焰均为无色 B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.焰色反应均应透过蓝色钴玻璃观察 D.只有金属单质灼烧时火焰才有颜色
2.2022年北京冬奥会开幕式璀璨夺目的焰火与化学的焰色试验有关。关于焰色试验说法正确的是(
)
A.做焰色试验时可用铜丝代替铂丝
B.NaO和NaOH的焰色均为黄色
2
C.需用稀硫酸清洗铂丝并在火焰上灼烧至与原来火焰颜色相同
D.检验NaCO 中混有的少量KCO 可在火焰上灼烧直接观察焰色
2 3 2 3
【课后巩固】1.(易)教材作业:P43页练习1、2、5
2.(易)一团棉花包裹少量过氧化钠放在石棉网上,将CO 气体缓缓通入棉花中的过氧化钠上,棉
2
花很快燃烧起来,根据实验分析可知,下列表达不正确的是( )
A.CO 对棉花燃烧起助燃作用 B.过氧化钠与CO 反应放热
2 2
C.反应生成的O 有利于棉花燃烧 D.过氧化钠与CO 反应属于氧化还原反应
2 23.(中)下列关于钠及其化合物的说法不正确的是( )
A.NaO 粉末加入 Ca(HCO ) 溶液中,会产生气体和浑浊
2 2 3 2
B.Na、NaO、NaO 长期放置在空气中,最终都将变成碳酸钠
2 2 2
C.氧化钠属于碱性氧化物,与水反应可以生成氢氧化钠和氧气
D.向包有NaO 粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明NaO 与 反应放热且
2 2 2 2
有氧气生成
4.(中)下列有关NaHCO 和NaCO 的叙述正确的是( )
3 2 3
A.NaHCO 比NaCO 热稳定性强
3 2 3
B.可以利用加热的方法来鉴别NaHCO 和NaCO
3 2 3
C.NaHCO 和NaCO 固体溶于水均放出热量
3 2 3
D.分别向NaHCO 和NaCO 溶液中滴加酚酞溶液,只有NaCO 溶液颜色变红
3 2 3 2 3
5.(易)下列有关焰色反应实验操作注意事项的说法中正确的是 ( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确 C.仅有⑤不正确 D.全对
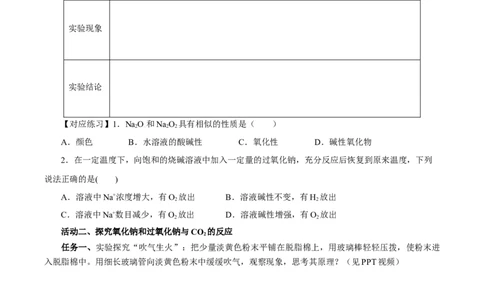
6.(中)有关NaO 性质实验如下:
2 2
已知:①NaO 与水反应经历了NaO+2HO =2NaOH+HO;
2 2 2 2 2 2 2
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是( )
A.双氧水能使酚酞褪色 B.浓氢氧化钠能使酚酞褪色
C.双氧水和浓氢氧化钠都能使酚酞褪色 D.可利用二氧化锰和水来完善实验方案
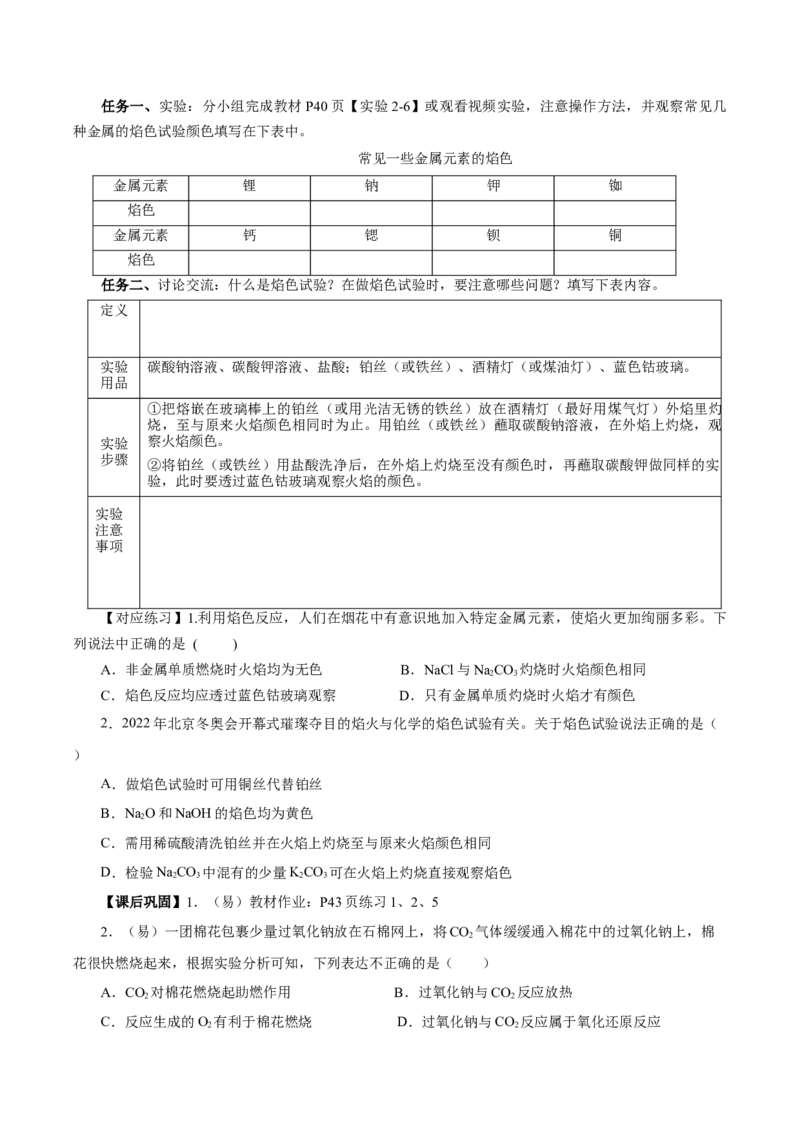
7.(易)焰色试验过程中铂丝的清洗和灼烧与钾焰色试验的观察两项操作如图所示:
下列叙述中不正确的是( )A.每次实验中都要先将铂丝灼烧至火焰无色,再蘸取被检验物质
B.钾的焰色试验要透过蓝色钴玻璃观察
C.实验时最好选择本身颜色较深的火焰
D.没有铂丝可用无锈铁丝代替进行实验
8.(中)对比分析钠及其化合物的特点,请回答下列问题。
(1)图1转化关系①→⑧中,属于氧化还原反应的有___________(填序号),其中用于呼吸面具或潜水艇
中氧气来源的反应的化学方程式为__________________________________(写出一个即可)。
(2)日常生活中常用到苏打和小苏打,鉴别它们的方法有多种。例如图2所示装置,这是根据它们具有
不同的___________加以鉴别的。实验过程中,当试管B中盛放的澄清溶液出现白色浑浊时,试管A中发
生反应的化学方程式为________________________________________________。