文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.2.2 杂化轨道理论简介
一.选择题
1. 通常把原子总数和价电子总数相同的分子或离子称为等电子体,人们发现等电子体的空间结构
相同,则下列有关说法中正确的是
A. 和 是等电子体,键角均为
B. 和 是等电子体,均为平面三角形结构
C. 和 是等电子体,均为三角锥形结构
D. 和CO是等电子体,化学性质完全相同
2. 下列说法中正确的是
A. 型的分子空间构型必为平面三角形
B. 分子是三角锥形,这是因为磷原子是 杂化的结果
C. 杂化轨道是由任意的1个s轨道和3个p轨道混合形成的4个 杂化轨道
D. 中心原子采取 杂化的分子,其几何构型可能是四面体形或三角锥形或V形
3. 下列对应关系不正确的是
选项 A. B. C. D.
中心原子所在族 ⅣA ⅤA ⅣA ⅥA
分子通式
立体构型 正四面体形 平面三角形 直线形 V形
A. A B. B C. C D. D
4. 下列描述中正确的是A. 的空间构型为平面三角形
B. 的中心原子有6对成键电子对,无孤电子对
C. 和 的中心原子均为 杂化
D. 和 的空间构型均为直线形
5. 根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是
中心原子杂化方
选项 分子式 价层电子对互斥模型 分子或离子的立体构型
式
A sp 直线形 直线形
B HCHO 平面三角形 三角锥形
C 四面体形 平面三角形
D 正四面体形 正四面体形
6. 徐光宪在 分子共和国 一书中介绍了许多明星分子,如 、 、 、
等。下列说法正确的是
A. 分子中的O为 杂化
B. 分子中C原子为sp杂化
C. 分子中的B原子 杂化
D. 分子中C原子均为 杂化
7. 无机苯 的结构与苯类似,也有大 键。下列关于 的说法错误的是
A. 其熔点主要取决于所含化学键的键能
B. 形成大 键的电子全部由N提供
C. 分子中B和N的杂化方式相同
D. 分子中所有原子共平面
8. 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法
错误的是
A. 该分子中N、O、F的第一电离能由大到小的顺序为B. 该分子中 键的键能大于 键的键能
C. 该分子中所有N原子都为 杂化
D. 该分子中 键与 键数目之比为15:4
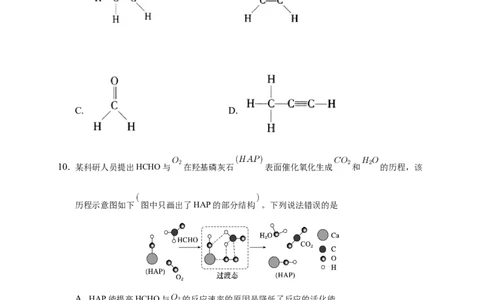
9. 下列分子所含原子中,既有 杂化又有 杂化的是
A. B.
C. D.
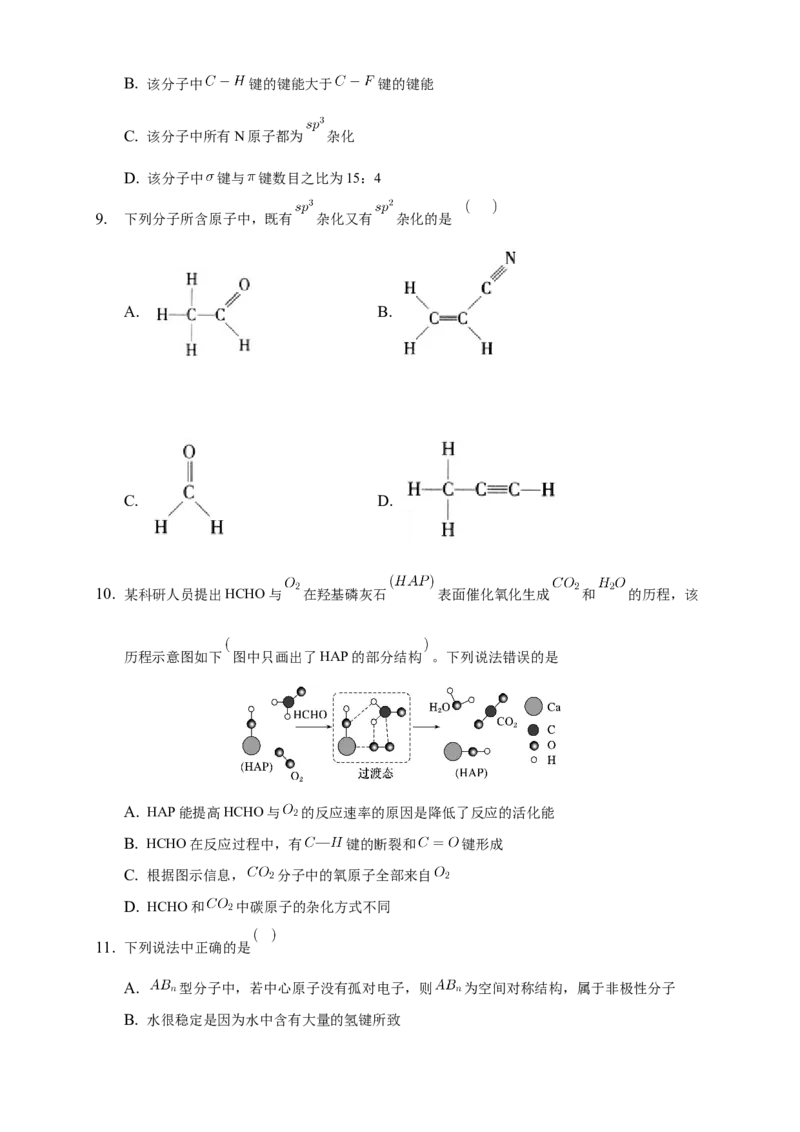
10. 某科研人员提出HCHO与 在羟基磷灰石 表面催化氧化生成 和 的历程,该
历程示意图如下 图中只画出了HAP的部分结构 。下列说法错误的是
A. HAP能提高HCHO与 的反应速率的原因是降低了反应的活化能
B. HCHO在反应过程中,有 键的断裂和 键形成
C. 根据图示信息, 分子中的氧原子全部来自
D. HCHO和 中碳原子的杂化方式不同
11. 下列说法中正确的是
A. 型分子中,若中心原子没有孤对电子,则 为空间对称结构,属于非极性分子
B. 水很稳定是因为水中含有大量的氢键所致C. 、 、 分子中的O、N、C分别形成2个、3个、4个 键,故O、N、C原子
分别采取 、 、 杂化
D. 配合物 中,中心离子是 ,配位体是 ,配位数是1
12. 价层电子对互斥理论 是关于分子几何构型的经验规律,该理论认为,分子的稳定结
构应使中心原子价层电子对之间的斥力最小,且不同价层电子对之间排斥力相对大小满足:孤
对电子 孤对电子 孤对电子 键对电子 键对电子 键对电子。如 分子中
下列推断不合理的是
A. 分子中
B. 键角 小于 键角
C. 已知 分子为正四面体, 中的 小于 中的
D. 离子中 小于 分子中
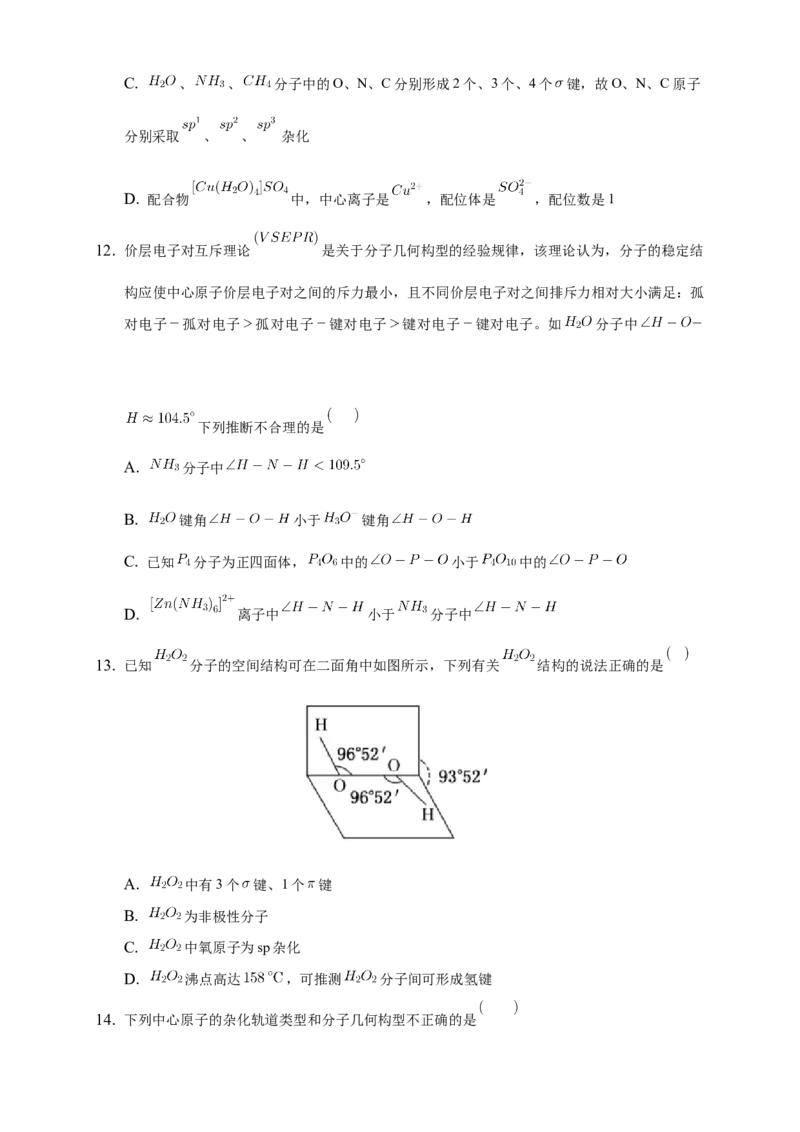
13. 已知 分子的空间结构可在二面角中如图所示,下列有关 结构的说法正确的是
A. 中有3个 键、1个 键
B. 为非极性分子
C. 中氧原子为sp杂化
D. 沸点高达 ,可推测 分子间可形成氢键
14. 下列中心原子的杂化轨道类型和分子几何构型不正确的是A. 中P原子 杂化,为三角锥形
B. 中N原子 杂化,为正四面体形
C. 中S原子sp杂化,为直线形
D. 中S原子 杂化,为V形
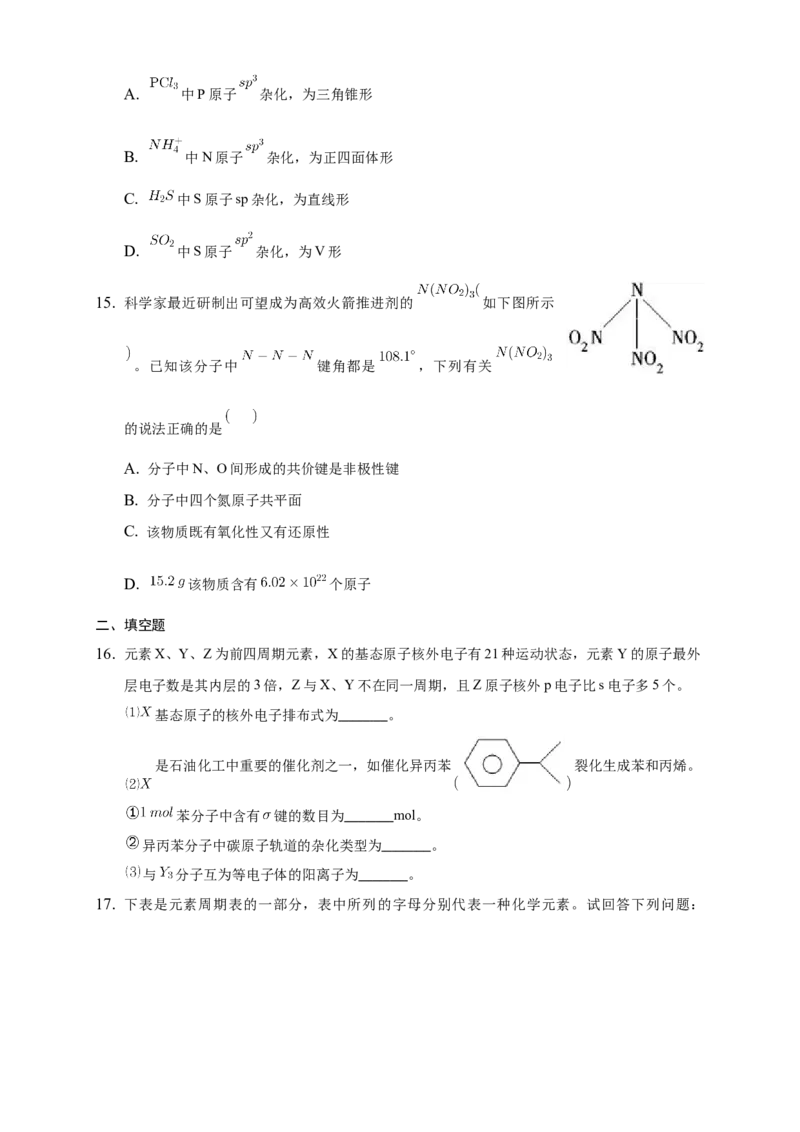
15. 科学家最近研制出可望成为高效火箭推进剂的 如下图所示
。已知该分子中 键角都是 ,下列有关
的说法正确的是
A. 分子中N、O间形成的共价键是非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 该物质含有 个原子
二、填空题
16. 元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外
层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
基态原子的核外电子排布式为 。
是石油化工中重要的催化剂之一,如催化异丙苯 裂化生成苯和丙烯。
苯分子中含有 键的数目为 mol。
异丙苯分子中碳原子轨道的杂化类型为 。
与 分子互为等电子体的阳离子为 。
17. 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:元素p为26号元素,请写出其基态原子的电子排布式________________。
与a反应的产物的分子中,中心原子的杂化形式为________________。
的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
________________________________________。
、p两元素的部分电离能数据列于下表:
元素 o p
717 759
电离能
1509 1561
3248 2957
比较两元素的 、 可知,气态 再失去一个电子比气态 再失去一个电子难。对此,你
的解释是______________________________________________。
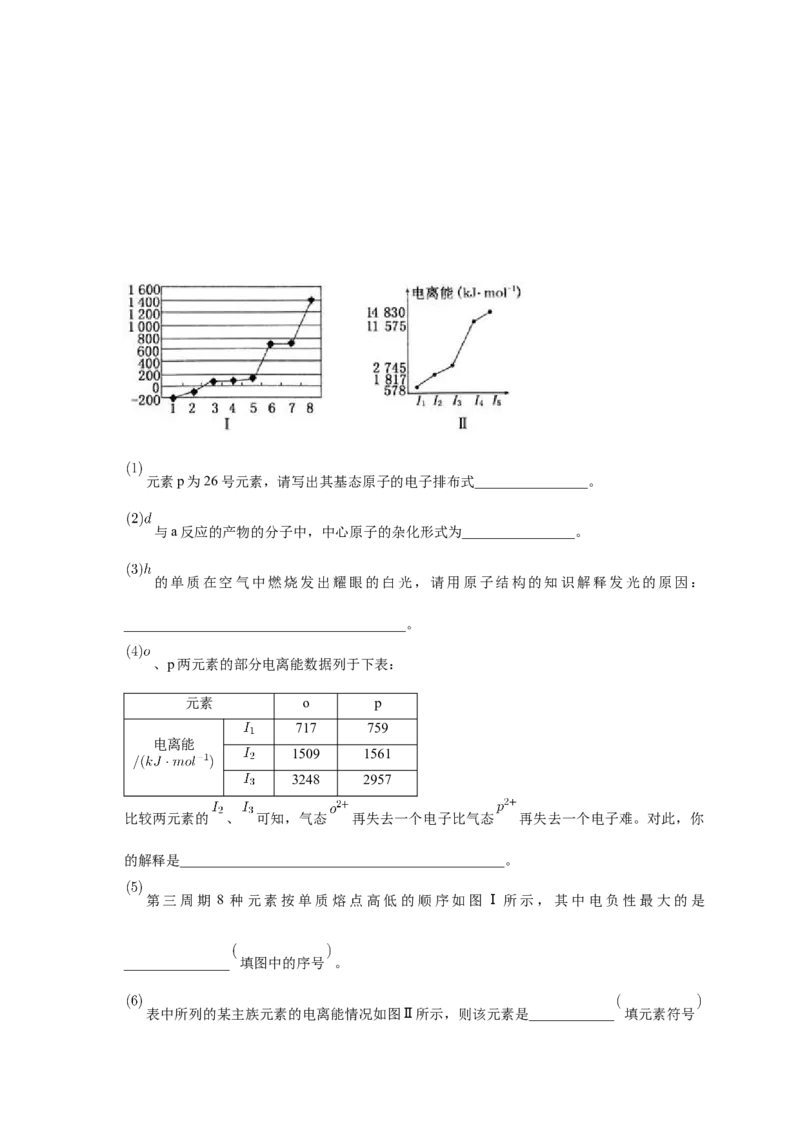
第三周期 8 种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是
_______________ 填图中的序号 。
表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是____________ 填元素符号。
18. 请完成下列各题的填空:
氢化钠 电子式为 ______ ,氢负离子的离子结构示意图为 ______ ;
元素X的最外层电子数是次外层电子数的2倍,该元素名称是 ______ ,该元素核外电子
排布式为 ______ ,画出该元素的外围电子排布图 ______ ;
前四周期元素中,未成对电子数为5的元素符号是 ______ ,该元素在周期表中的位置为
第______ 周期, ______ 族, ______ 区;
、N、O的第一电离能由大到小的顺序为 ______ ,由这三种元素和氢原子共同组成的离
子化合物的化学式为 ______ ;
亚硒酸根离子 的VSEPR模型为 ______ ,其中心原子的轨道杂化方式为 ______
;