文档内容
第三章 水溶液中的离子反应与平衡
课题 第二节 水的电离和溶液的 pH
第一课时
1、知道水是一种弱电解质,外界条件会影响其电离平衡的移动,
知识与技 2、知道水的离子积常数不仅适用与纯水,也适用于稀的电解质溶液。
能
3、了解测定溶液pH的方法有pH试纸测量(广泛pH试纸和精密pH试纸)、pH
教
计测量和酸碱滴定测量,了解各种方法的优缺点及适用条件。
学
目
过程与方 经历对水的离子积常数的分析,加深对弱电解质电离平衡的认识,了解一般与特
标
法
殊的辩证关系。
情感态度 了解化学定量分析的方法,体验化学在科学研究中作用和地位,提高学生的科学
与价值观
素质。
教学
重点 溶液的酸碱性及其定量表示方法, 水的离子积常数的运用
教学
难点 溶液的酸碱性的定量表示方法, 水的离子积常数的运用
教
学
设
教 本章是上一章化学平衡理论的延伸和扩展。第一节弱电解质的电离课标要求主要是认识电解质
材
的强弱和能用化学平衡理论描述电解质在水溶液中的电离平衡。本节理论性较强,是理论与实践相 分
析
结合的一节,掌握方法是学好本节知识的关键。
学
情 在初中和必修一教材中,学生已学过有关酸碱盐及电离知识,同时通过对本教材第
分
二章化学平衡理论知识的学习,学生也普遍具有了研究的热情
析
教
法
情景教学法与启发式教学相结合
设
计
课
想
件
使 PPT课件
课
件
教学 教 学 内 容 设计意图
环节
教师活动设计 学生活动设计【引入】
由复习强电解质盐酸的电离和弱电解质醋酸的电离入
手,提出问题——水是如何电离的?如何用实验证明水的电
离过程?
精确的纯水导电实验
[设计意图]从运用已学知识分析、推导新知识入手,减少学
生的陌生感,做好知识的铺垫。
学习
一、水的电离与水的离子积常数
[教师] 精确的纯水导电实验说明什么?
[学生]水是一种极弱的电解质,电离方程式可表示为:
培训学生分析问
HO+HO HO+ +OH- 或HO H+ +OH-
2 2 3 2
题和总结总题 的
[教师]请用公式表述水的电离常数 能力
导
学
[学生分析]1L纯水的物质的量是556mol,经实验测得250C 分析
达 ·
标
时,发生电离的水只有 1×10-7mol,二者相比,水的电离部
分太小,可以忽略不计。因此电离前后水的物质的量几乎不
变,可以视为常数,常数乘以常数必然为一个新的常数,用
Kw 表示,即为水的离子积常数,简称水的离子积。
w
Kw= c(H+)·c(OH—)
由于250C时,c(H+)= c(OH—)= 1×10-7mol/L
所以250C时,Kw= c(H+)·c(OH—)=1×10-14
[探究]影响水的电离平衡的因素
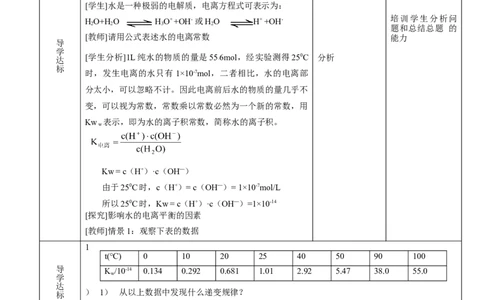
[教师]情景1:观察下表的数据
1
t(℃) 0 10 20 25 40 50 90 100
导 K /10-14 0.134 0.292 0.681 1.01 2.92 5.47 38.0 55.0
w
学
达
标
) 1) 从以上数据中发现什么递变规律?
2)以上数据说明温度与水的电离程度之间存在什么关系?[学生小结]在 HO H+ +OH-中,
2
升高温度,水的电离程度______,水的电离平衡
向____移动,Kw_____。
根据所学知识分析平衡
降低温度,水的电离程度______,水的电离平衡 分析、回答 移动
向____移动,Kw_____
导
[PPT小结]温度越高,K 越大。 K 在一定温度下是个
学 w w
达 常数。
标 升高温度,促进水的电离。
水的电离是一个吸热过程。
[教师]水的离子积Kw= [H+ ][OH-]=1×10-14不仅适用于纯
水,也适用于稀的电解质水溶液。
[教师]情景2:比较下列情况下,C(H+) 和C(OH—)的值或
变化趋势。
纯水 加入少量盐酸 加入少量NaOH
C(H+)
C(OH—)
C(H+) 与C(OH—)大小比较
导
学 [学生小结]:对于电离平衡 HO H+ +OH-中
2
达
标 c(H+) c(OH-) c(H+)与c(OH-)大小比较 Kw 酸碱性 水的电离平衡
蒸 蒸馏水
馏
加酸后
水
加碱后
[设计意图]加深对水的离子积常数Kw的认识与理解,为
Kw在酸碱溶液中的应用做好准备。
[教师]情景3:有哪些方法可以抑制水的电离?
导 [学生] 加酸、加碱、降温。 学习
学
达 [小结]酸、碱由于电离产生的H+或OH-对水的电离平衡
记忆
标
起抑制作用,使水的电离程度减小,而某些盐溶液中由
于Ac-、NH +等“弱离子”因结合水电离出的H+或OH
4
-能促进水的电离平衡(下一节介绍),使水的电离程度
增大,但无论哪种情况,只要温度不变,K 就不变。
W①水中加酸或碱均抑制水的电离,但由水电离出的c
(H+)与c(OH—)总是相等。
②任何电解质溶液中,H+与OH—总是共存,c(H+)与
c(OH—)此增彼长,且Kw = c(H+)·c(OH—)不变。
通过练习掌握所学知识
-5
[教师]情景4:请计算(1)常温下,浓度为1×10 mol/L 练习
+
的盐酸溶液中,由水电离产生的c(H )是多少?
-5
(2)常温下,浓度为1×10 mol/L的NaOH溶液中,由
-
水电离产生的c(OH )是多少?
+ -9
(3)在常温下,由水电离产生的c(H ) =1×10 mol/L的
溶液,则该溶液的酸碱性如何?
[引申]判断溶液酸碱性强弱的依据是什么?
[学生小结]溶液的酸碱性
酸性溶液:c (H+) ___ c (OH—), c (H+) ____ 1.0×10-
7mol/L
碱性溶液:c (H+) __ c (OH—) ,c (H+) _____ 1.0×10-7mol/L
掌握pH的相关知识点
中性溶液:c (H+) ___ c (OH—) ,c (H+) __ _ 1.0×10-7mol/L
学会计算
导 + -
二、c(H ) 和 c(OH ) 与溶液酸碱性、pH的关系
学
达 [教师]溶液的酸碱性如何表示?
标
1、溶液的酸碱性可用c(H+)与c(OH-)相对大小决
定。
判断正误:
1)任何水溶液中都存在水的电离平衡。
2)任何水溶液中(不论酸、碱或中性) 都存在
Kw=10-14 。
3)某温度下,某液体c(H+)= 10-7mol/L,则该溶液一
定是纯水。
+ -
2、c(H ) 和 c(OH )都较小的稀溶液(<1mol/L),化学
+
上常采用pH来表示溶液酸碱性的强弱。pH表示c(H )的
负对数,pH=-lg[H+] lg 2 = 0.3 lg 3 = 0.447
中性溶液c(H+)=1×10-7mol/L pH=7
酸性溶液c(H+)>1×10-7mol/L pH<7
碱性溶液c(H+)<1×10-7mol/L pH>7
[小结]pH的适应范围:稀溶液,0~14之间;
酸性溶液中c(H+)越大,酸性越强,pH越小;碱性
溶液中c(OH-)越大,c(H+)越小,pH越大,碱性例:c(H+ )= 0.1 mol /L pH=-lg 10-1 = 1
c(H+) = 0.01mol /L pH=-lg 10-2 = 2
c(H+) = 0.001mol /L pH=-lg 10-3 = 3
(4)pH改变与c(H+)浓度变化关系
pH改变一个单位,c(H+)改变1 0倍;
pH改变n个单位, c(H+)改变10n倍
记忆 学会测定 pH的几种方
[教师]如何测定pH?
法方法
pH的测定方法:
粗略测定:(1)酸碱指示剂——甲基橙、石蕊、酚酞
常用酸碱指示剂及其变色范围:
(2)pH试纸 ——最简单的方法。
操作:将一小块pH试纸放在洁净的玻璃片
上,用玻璃棒沾取未知液点试纸中部,然后与标准比色
卡比较读数即可。
注意:①事先不能用水湿润pH试纸;
②只能读取整数值或范围
③用广泛pH试纸可识别pH差值约为1;精密pH
试纸可识别0.2或0.3的pH差值
精确测定:pH计
三.pH的应用
设作 卷子两张
计业
板
书
设
一、水的电离与水的离子积常数
1、水的离子积常数
Kw= c(H+)·c(OH—)
由于250C时,c(H+)= c(OH—)= 1×10-7mol/L
所以250C时,Kw= c(H+)·c(OH—)=1×10-14
2、影响水的电离平衡的因素
升高温度,促进水的电离。水的电离是一个吸热过程。
+ -
二、c(H ) 和 c(OH ) 与溶液酸碱性、pH的关系
1、溶液的酸碱性可用c(H+)与c(OH-)表示。
+ - +
2、c(H ) 和 c(OH )都较小的稀溶液(<1mol/L), pH表示c(H )的负对数,pH=-lg[H+]
计
pH的测定方法:
粗略测定:(1)酸碱指示剂——甲基橙、石蕊、酚酞
(2)pH试纸 ——最简单的方法。
注意:①事先不能用水湿润pH试纸;②只能读取整数值或范围
(3)精确测定:pH计
三、pH的应用