文档内容
3.2.1 水的电离 溶液的酸碱性与 pH(学案)
1.了解水的电离、离子积常数。
2.了解溶液pH的定义。
3.了解测定溶液pH的方法,能进行pH的简单计算。
1.pH的计算。
pH试纸收到使用方法是_____________________________________________________。
一、水的电离
1.水的电离
水 是 一 种 极 弱 的 电 解 质 , 电 离 方 程 式 为 HO + HO⇌H O + + OH - , 简 写 为
2 2 3
C(H+ )∙C(OH-
)
___________________________,水的电离常数K =
电离
C(H O)
2
2.水的离子积常数
(1)K 的推导
w
C(H+ )∙C(OH-
)
水的电离平衡常数K = ,则c(H+)·c(OH-)=K ·c(HO)。从实验可知,在
电离 C(H O) 电离 2
2
室温时 55.6mol 纯水中只有 1×10-7molH O电离,电离前后 HO的物质的量几乎不变,因此
2 2
c(HO)可视为常数,K 也为一常数,所以K ·c(HO)必然也为常数,用K 表示,因此有c(H
2 电离 电离 2 w
+)·c(OH-)=K 。
w
25℃时,c(H+)=c(OH-)=______________mol/L;K =c(H+)·c(OH-)=______________
W
(2)K 的影响因素
w
水的离子积K ,只受______________的影响,______________,K 增大。
w w
(3)K 的适用范围
w
K 不仅适用于纯水,还可适用于______________。
w
二、溶液的酸碱性和pH
1.溶液的酸碱性
(1)常温下溶液的酸碱性与pH的关系
①pH<7,溶液呈__________;②pH=7,溶液呈__________;③pH>7,溶液呈__________。
(2)溶液的酸碱性与c(H+)、c(OH-)的关系溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
①c(H+)>c(OH-)溶液呈______________;②c(H+)=c(OH-)溶液呈______________;③c(H+)
<c(OH-)溶液呈______________。
2.pH
(1)表达式:pH=______________。
(2)意义:pH越大,溶液碱性______________;pH越小,溶液酸性______________。
(3)适用范围:1×10-14mol·L-1≤c(H+)≤1mol·L-1的溶液。
二、稀释过程溶液pH值的变化规律:
1.强酸溶液:稀释10n倍时,pH稀=pH原+n(但始终不能大于或等于7)
2.弱酸溶液:稀释10n倍时,pH稀〈pH原+n(但始终不能大于或等于7)
3.强碱溶液:稀释10n倍时,pH稀=pH原-n(但始终不能小于或等于7)
4.弱碱溶液:稀释10n倍时,pH稀〉pH原-n(但始终不能小于或等于7)
5.不论任何溶液,稀释时pH均是向7靠近(即向中性靠近);任何溶液无限稀释后 pH均接近
7
6.稀释时,弱酸、弱碱和水解的盐溶液的pH变化得慢,强酸、强碱变化得快。
四、溶液酸、碱性的测定方法
(1)指示剂法
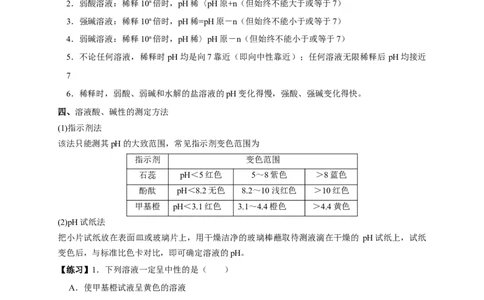
该法只能测其pH的大致范围,常见指示剂变色范围为
指示剂 变色范围
石蕊 pH<5红色 5~8紫色 >8蓝色
酚酞 pH<8.2无色 8.2~10浅红色 >10红色
甲基橙 pH<3.1红色 3.1~4.4橙色 >4.4黄色
(2)pH试纸法
把小片试纸放在表面皿或玻璃片上,用干燥洁净的玻璃棒蘸取待测液滴在干燥的 pH试纸上,试纸
变色后,与标准比色卡对比,即可确定溶液的pH。
【练习】1.下列溶液一定呈中性的是( )
A.使甲基橙试液呈黄色的溶液
B.c(H+)=c(OH﹣)=10﹣6mol/L溶液
C.pH=7的溶液
D.酸与碱恰好完全反应生成正盐的溶液
【练习】2.25℃时,下列溶液中水的电离程度最小的是( )
A.0.01mol/L醋酸溶液 B.0.01mol/L NH Cl溶液
4
C.0.01mol/L NaHSO 溶液 D.0.01mol/L NaHCO 溶液
4 3
【练习】3.常温下,某溶液中由水电离出来的 c(H+)=1.0×10﹣13mol•L﹣1,该溶液可能是
( )稀盐酸 氯化铵水溶液 硝酸钠水溶液 氢氧化钠水溶液
①A. ② B.③ ④C. D.
【练习】①4④.下列操作中,能使①电②离平衡H
2
O H++O②H﹣ ③正向移动且溶液呈酸③性④的是( )
A.向水中加入Na 2 CO 3 溶液 ⇌
B.向水中加入NaHSO 溶液
4
C.向水中加入Al (SO ) 溶液
2 4 3
D.将水加热到100℃,使水的pH=6
【练习】5.40℃时水的离子积K =2.9×10﹣14,则在40℃时,c(H+)=1×10﹣7mo1•L﹣1 的溶
w
液( )
A.呈酸性 B.呈碱性 C.呈中性 D.无法判断
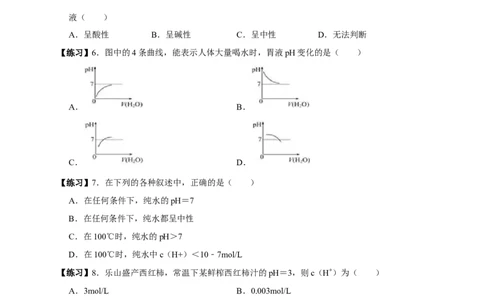
【练习】6.图中的4条曲线,能表示人体大量喝水时,胃液pH变化的是( )
A. B.
C. D.
【练习】7.在下列的各种叙述中,正确的是( )
A.在任何条件下,纯水的pH=7
B.在任何条件下,纯水都呈中性
C.在100℃时,纯水的pH>7
D.在100℃时,纯水中c(H+)<10﹣7mol/L
【练习】8.乐山盛产西红柿,常温下某鲜榨西红柿汁的pH=3,则c(H+)为( )
A.3mol/L B.0.003mol/L
C.1×10﹣11mol/L D.1×10﹣3mol/L
【练习】9.常温下,在pH=12的NaOH溶液中,由水电离出的c(OH﹣)为( )
A.1.0×10﹣7mol/L B.1.0×10﹣6mol/L
C.1.0×10﹣3mol/L D.1.0×10﹣12mol/L
【练习】10.如表是不同温度下水的离子积数据:
温度/℃ 25 t t
1 2
水的离子积K 1×10﹣14 a 1×10﹣12
w试回答以下问题:
(1)若25<t <t ,则a_____1×10﹣14(填“>”“<”或“=”)。
1 2
(2)25℃时,某Na SO 溶液中c(SO 2﹣)=5×10﹣4mol•L﹣1,取该溶液1 mL加水稀释至
2 4 4
10mL,则稀释后溶液中c(Na+):c(OH﹣)=_____。
(3)在t
2
℃下pH=10的NaOH溶液中,水电离产生的OH﹣浓度c(OH﹣)
水
=_____。
(4)t ℃下,将pH=11的苛性钠溶液V L与pH=1的稀硫酸V L混合(设混合后溶液的体积
2 1 2
为原两溶液体积之和),所得混合溶液的pH=2,则V :V =_____。
1 2
1.下列溶液肯定显酸性的是( )
A.含H+的溶液 B.加酚酞显无色的溶液
C.pH<7的溶液 D.c(H+)>c(OH﹣)的溶液
2.下列物质对水的电离平衡没有影响的是( )
A.NaF B.KI C.KAl(SO ) D.NaHSO
4 2 4
3.25℃时,0.005mol/L Ba(OH) 中H+浓度是( )
2
A.1×10﹣12mol/L B.1×10﹣13mol/L
C.5×10﹣12mol/L D.5×10﹣13mol/L
4.100℃时,K =1×10﹣12,对纯水的叙述正确的是( )
w
A.pH=6显弱酸性
B.c(H+)=10﹣6 mol/L,溶液为中性
C.K 是常温时的10﹣2倍
w
D.常温下,pH=6的溶液为中性
5.pH相同的盐酸和醋酸两种溶液,它们的( )
A.H+的物质的量相同 B.物质的量浓度相同
C.H+的物质的量浓度不同 D.H+的物质的量浓度相同
6.对于溶液的酸碱性,下列说法正确的是( )
A.pH=7的溶液一定呈中性
B.同温时,溶液pH相差3,则c(H+)相差3倍
C.pH=6的HCl加水稀释1000倍后,溶液呈碱性
D.同温时,pH=5的CH COOH溶液酸性比pH=6的盐酸的酸性强
3
7.下列说法正确的是( )
A.强电解质溶液的导电能力一定大于弱电解质溶液的导电能力
B.pH=4.5的番茄汁中的c(H+)是pH=6.5的牛奶中的2倍C.0.1mol•L﹣1CH COOH溶液与0.1mol•L﹣1盐酸的pH相等
3
D.CH COONa溶液中只存在两种分子
3
8.某可口可乐饮料的pH=3,某西红柿汁饮料的pH=4,则这两种饮料中的c(OH﹣)之比是(
)
A.3:4 B.1:10 C.10:1 D.无法确定
9.已知常温下柠檬水的pH是3,纯碱溶液的pH是13,两溶液中的c(H+)浓度之比为( )
A.3:11 B.1:1
C.10﹣3:10﹣13 D.10﹣11:10﹣13
【课前复习答案】把小片试纸放在表面皿或玻璃片上,用干燥洁净的玻璃棒蘸取待测液滴在干燥的
pH试纸上,试纸变色后,与标准比色卡对比,即可确定溶液的pH。
【知识点填空答案】
HO H++OH-;10-7;1×10-14;温度;温度升高;电解质水溶液;酸性;中性;碱性;酸性;中
2
性;;碱性;-lgc(H+)
⇌
【练习答案】(1-9):BCACBABDD;(10):>;1000:1;10﹣10mol•L﹣1;9:11
【检测反馈答案】DBABDDDBC