文档内容
3.2.1水的电离(分层作业)
1.下列操作可以使水的离子积常数K 增大的是
w
A.通入少量氨气 B.通入少量氯化氢气体
C.加热 D.加入少量氯化钠固体
2.25℃时,水的电离达到平衡:HO⇌H++OH- ;△H>0,下列叙述正确的是
2
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.将水加热,K 增大,pH不变
W
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
W
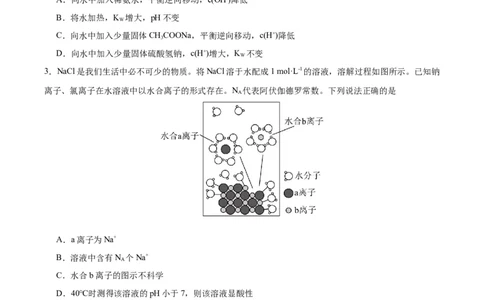
3.NaCl是我们生活中必不可少的物质。将NaCl溶于水配成1 mol·L-1的溶液,溶解过程如图所示。已知钠
离子、氯离子在水溶液中以水合离子的形式存在。N 代表阿伏伽德罗常数。下列说法正确的是
A
A.a离子为Na+
B.溶液中含有N 个Na+
A
C.水合b离子的图示不科学
D.40℃时测得该溶液的pH小于7,则该溶液显酸性
4.已知水的电离方程式:HO⇌H++OH-。下列叙述中,正确的是
2
A.向水中加入少量硫酸氢钠溶液,c(H+)增大,K 增大
W
B.降低温度,K 减小,pH不变
W
C.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低
D.向水中加入少量NaClO固体,平衡向正反应方向移动,c(H+)降低
5.常温下,下列四种溶液中,水的电离程度最大的是
A.pH=5的NH Cl NH Cl溶液 B.pH=5的HSO 溶液
4 4 2 4C.pH=8的CHCOONa溶液 D.pH=8的NaOH溶液
3
6.研究弱电解质的电离,有重要的实际意义。
下表是不同温度下水的离子积常数:
温度/℃ 25 t t
1 2
水的离子积常数 1×10﹣14 K 1×10﹣12
W
试回答以下问题:
(1)若25℃<t<t,则K 1×10﹣14(填“>”、“<”或“=”),判断的理由是 。
1 2 W
(2)若25℃时,pH=3的盐酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性(填“酸”、“中”或
“碱”),溶液中c(Na+) c(Cl﹣)(填“>”、“=”或“<”)。
(3)醋酸是一种常见的有机酸。醋酸的电离方程式为 。
保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是 。
A.c(CHCOO-) B.c(H+)
3
C.c(OH-) D.CHCOOH电离平衡常数
3
(4)向0.1 mol·L-1CHCOOH溶液中加水稀释,c(CHCOO-) / c(CH COOH)的比值将 (填“变大”、
3 3 3
“不变”或“变小”)。
(5)下列事实一定能说明CHCOOH是弱电解质的是 (填字母)。
3
A.相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B.1 mol·L-1 CHCOOH溶液能使紫色石蕊试液变红
3
C.25℃时,1 mol·L-1 CHCOOH溶液的pH约为2
3
D.10 mL 1mol·L-1的CHCOOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
3
E.相同物质的量浓度的CHCOOH和HCl溶液中,水的电离程度的大小关系为a大于b
3
(6)某些弱酸的电离常数如下:
化学式 CHCOOH HSCN HCN HClO HCO
3 2 3
电 离 K=4.4×10-7
1
1.8×10-5 1.3×10-1 4.9×10-10 3.0×10-8
常 数 K=4.7×10-11
2
下列反应可以发生的是_______(填字母)。
A.CHCOOH+NaCO=NaHCO+CHCOONa
3 2 3 3 3
B.CHCOOH+NaCN=CHCOONa+HCN
3 3
C.CO+HO+2NaClO=Na CO+2HClO
2 2 2 3
D.NaHCO +HCN=NaCN+HO+CO↑
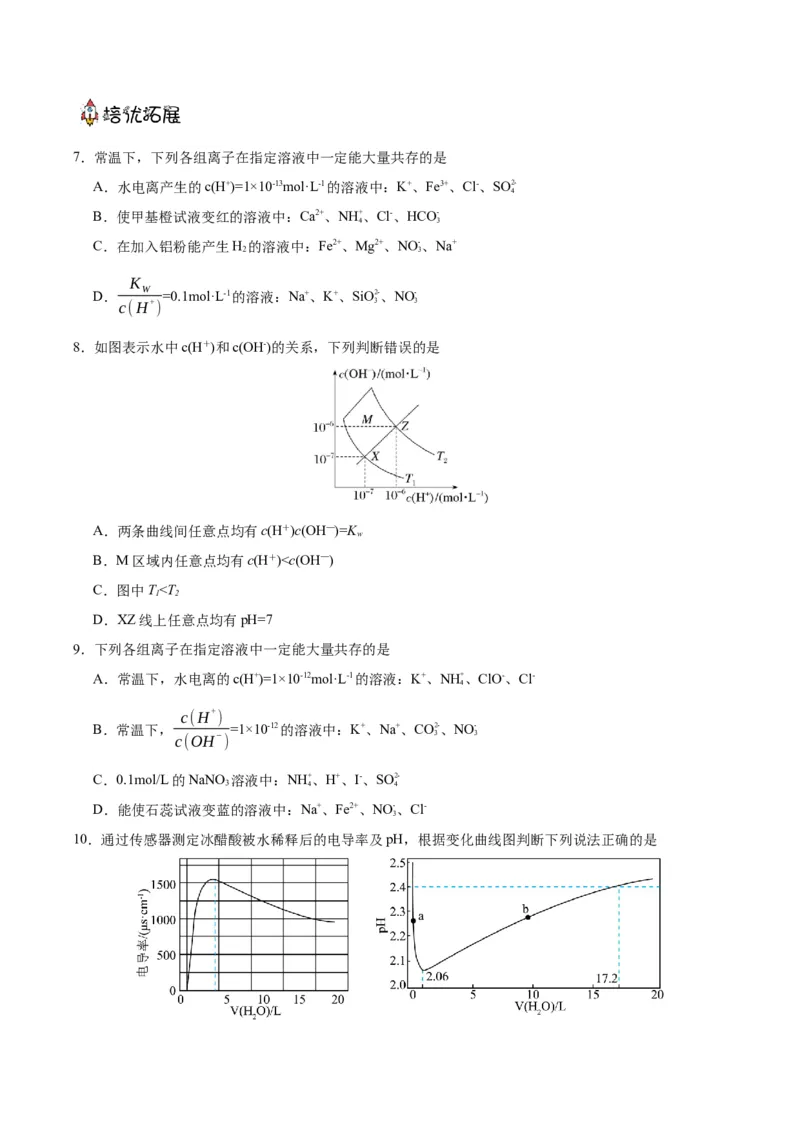
3 2 27.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离产生的c(H+)=1×10-13mol·L-1的溶液中:K+、Fe3+、Cl-、SO2-
4
B.使甲基橙试液变红的溶液中:Ca2+、NH+ 、Cl-、HCO-
4 3
C.在加入铝粉能产生H 的溶液中:Fe2+、Mg2+、NO- 、Na+
2 3
K
W
D. =0.1mol·L-1的溶液:Na+、K+、SiO2- 、NO-
c(H+
)
3 3
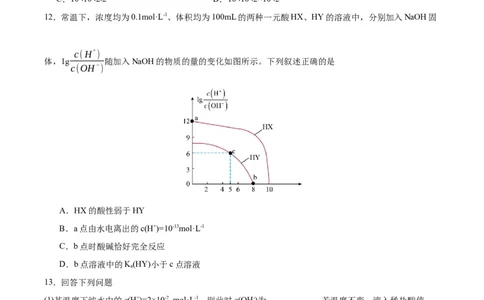
8.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是
A.两条曲线间任意点均有c(H+)c(OH—)=K
w
B.M区域内任意点均有c(H+)