文档内容
第三章 烃的衍生物
第二节 醇、酚
第一课时 醇
【学习目标】
1.通过分析乙醇的分子结构,认识和理解醇类的结构共性、醇的定义和分类。
2.通过分析乙醇的性质,从官能团角度预测醇类的性质,并通过实验和素材证实,再归纳总结醇类的化学
性质及其反应规律。
3.通过素材,结合醇类性质,理解醇类的应月用对社会生活产生的利与弊,能辩证地看待醇类。
【学习重点】醇的消去反应和氧化反应
【学习难点】醇的化学性质
【课前预习】
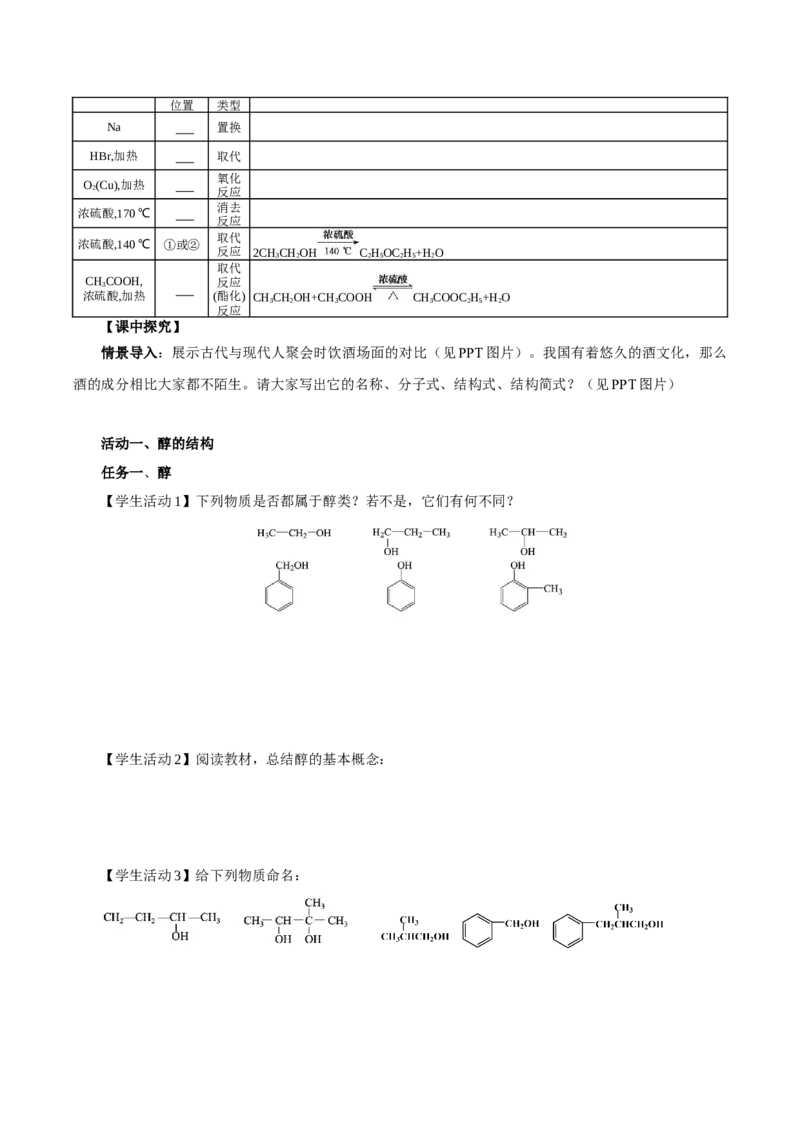
1.醇的概念和分类
(1)概念
羟基与饱和碳原子相连的化合物称为醇。饱和一元醇的分子通式为 或CH O(n≥1)。
n 2n+2
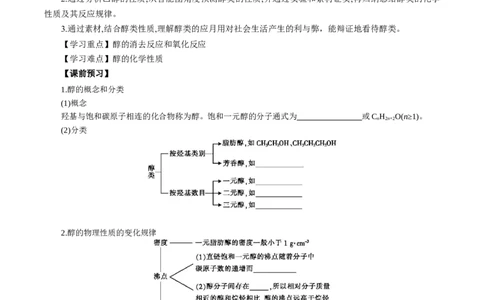
(2)分类
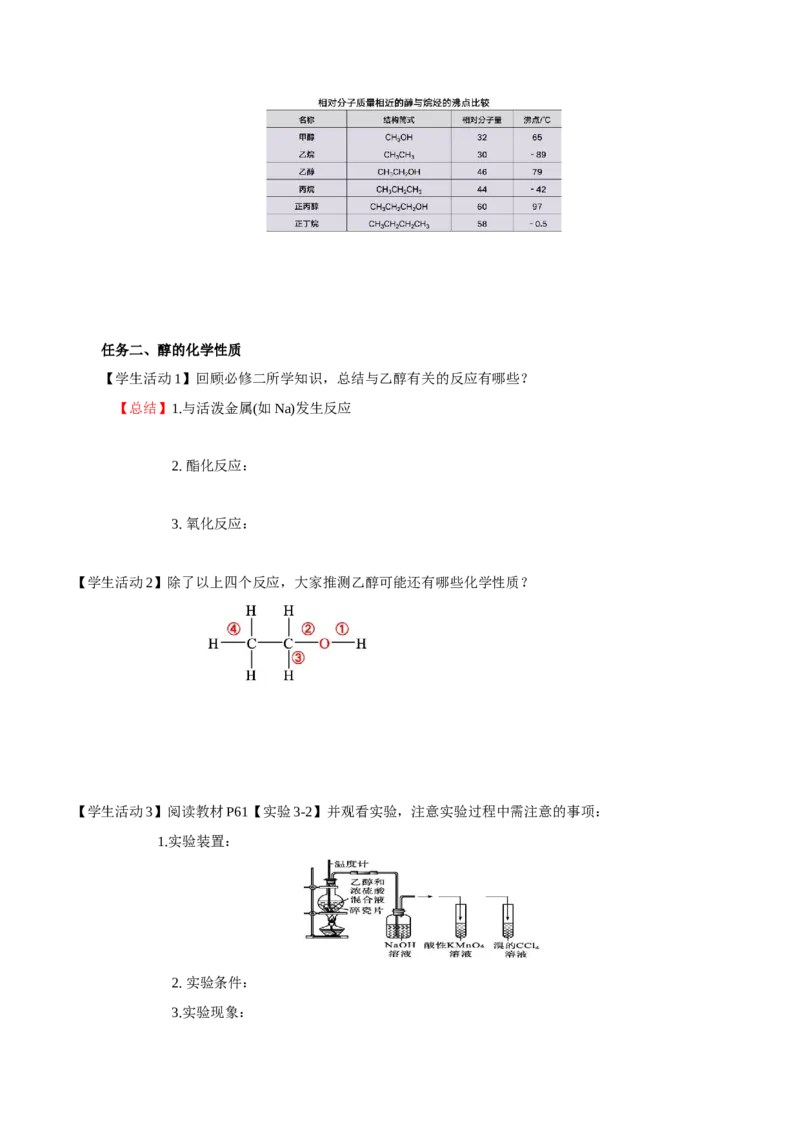
2.醇的物理性质的变化规律
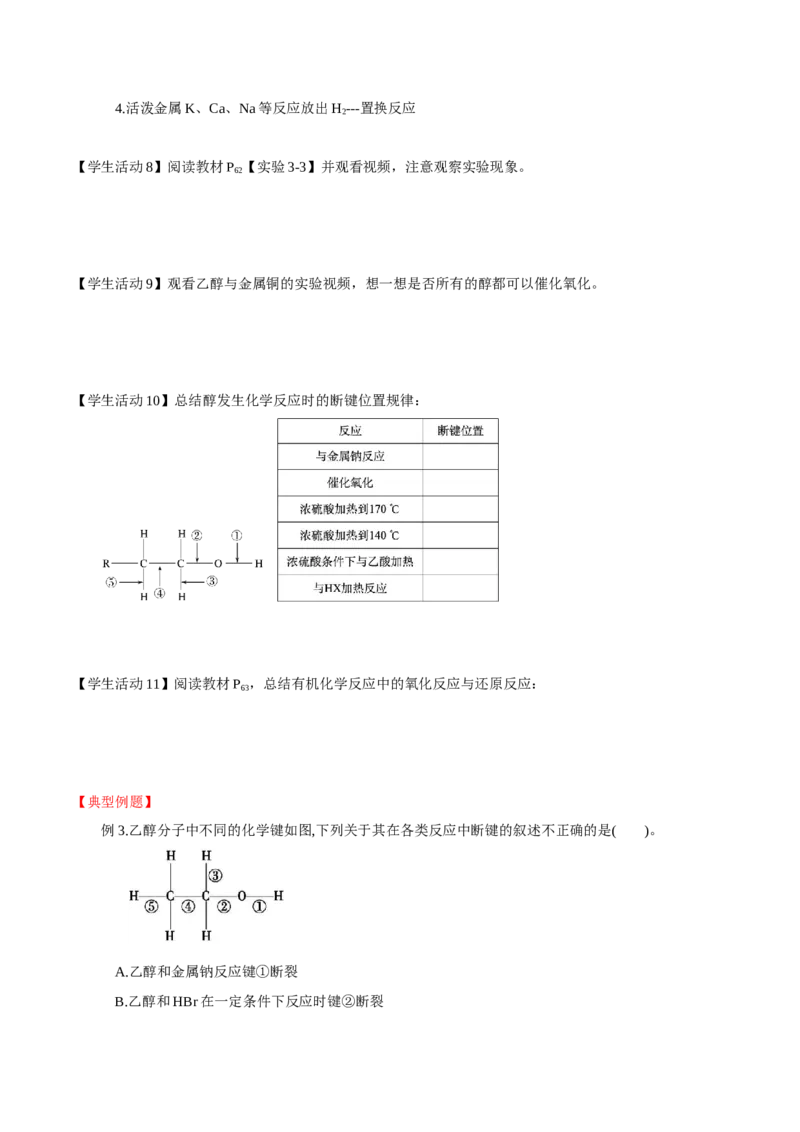
3.醇的化学性质 (以乙醇为例):
反应物及条件 断键 反应 化学方程式位置 类型
Na 置换
HBr,加热 取代
氧化
O(Cu),加热
2 反应
消去
浓硫酸,170 ℃
反应
取代
浓硫酸,140 ℃ ①或②
反应 2CHCHOH CHOCH+HO
3 2 2 5 2 5 2
取代
CHCOOH, 反应
3
浓硫酸,加热 (酯化) CHCHOH+CHCOOH CHCOOCH+HO
3 2 3 3 2 5 2
反应
【课中探究】
情景导入:展示古代与现代人聚会时饮酒场面的对比(见PPT图片)。我国有着悠久的酒文化,那么
酒的成分相比大家都不陌生。请大家写出它的名称、分子式、结构式、结构简式?(见PPT图片)
活动一、醇的结构
任务一、醇
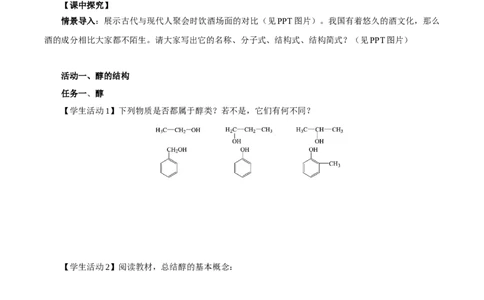
【学生活动1】下列物质是否都属于醇类?若不是,它们有何不同?
【学生活动2】阅读教材,总结醇的基本概念:
【学生活动3】给下列物质命名:任务二、醇的代表物
【学生活动1】阅读教材P ,总结甲醇、乙二醇、丙三醇的结构特点?
60
【典型例题】
例1:只用水就能鉴别的一组物质是( )。
A.苯、乙醇、四氯化碳 B.乙醇、乙酸、乙烷
C.乙二醇、甘油、溴乙烷 D.苯、己烷、甲苯
例2.下列叙述正确的是( )。
A.甲醇既可发生取代反应也可发生加成反应
B.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
C.烷烃的沸点高低仅取决于碳原子数的多少
D.戊二烯与环戊烷互为同分异构体
活动二、醇的性质
任务一、醇的物理性质
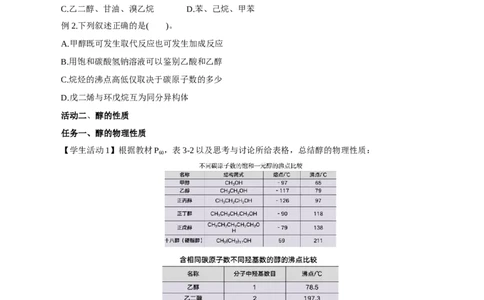
【学生活动1】根据教材P ,表3-2以及思考与讨论所给表格,总结醇的物理性质:
60任务二、醇的化学性质
【学生活动1】回顾必修二所学知识,总结与乙醇有关的反应有哪些?
【总结】1.与活泼金属(如Na)发生反应
2.酯化反应:
3.氧化反应:
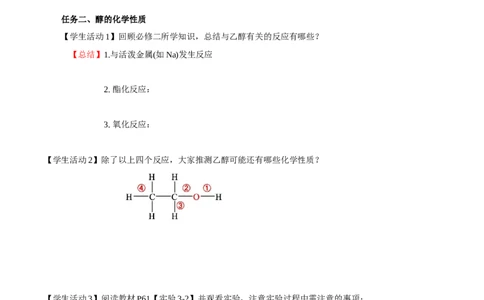
【学生活动2】除了以上四个反应,大家推测乙醇可能还有哪些化学性质?
【学生活动3】阅读教材P61【实验3-2】并观看实验,注意实验过程中需注意的事项:
1.实验装置:
2.实验条件:
3.实验现象:4.实验结论:
【学生活动4】通过阅读教材以及观看实验视频,回答下列问题:
1.混合乙醇和浓硫酸时应如何操作?
2.乙醇与浓硫酸体积比为何要为1∶3?
3.为什么要加入碎瓷片,温度计的放置位置?
4.为什么反应过程中溶液会变黑?
5.为什么要将生成的气体先通入NaOH溶液?
6.酸性KMnO4和溴的CCl4溶液褪色说明了什么?
7.为何使液体温度迅速升到170℃?
8.溴乙烷与乙醇都能发生消去反应,二者的反应有什么异同?
【学生活动5】所有的醇都能发生消去反应吗?
【学生活动6】判断下列物质能否发生消去反应,若能则其生成物有多少种?
【学生活动7】阅读教材,总结乙醇可以发生的取代反应。
【总结】1.酯化反应
2.与氢卤酸反应---生成卤代烃和水
3.分子间脱水4.活泼金属K、Ca、Na等反应放出H---置换反应
2
【学生活动8】阅读教材P 【实验3-3】并观看视频,注意观察实验现象。
62
【学生活动9】观看乙醇与金属铜的实验视频,想一想是否所有的醇都可以催化氧化。
【学生活动10】总结醇发生化学反应时的断键位置规律:
【学生活动11】阅读教材P ,总结有机化学反应中的氧化反应与还原反应:
63
【典型例题】
例3.乙醇分子中不同的化学键如图,下列关于其在各类反应中断键的叙述不正确的是( )。
A.乙醇和金属钠反应键①断裂
B.乙醇和HBr在一定条件下反应时键②断裂C.乙醇和浓硫酸共热至140 ℃时键①或键②断裂,170 ℃时键②③断裂
D.乙醇在Ag催化下和O 反应键①③断裂
2
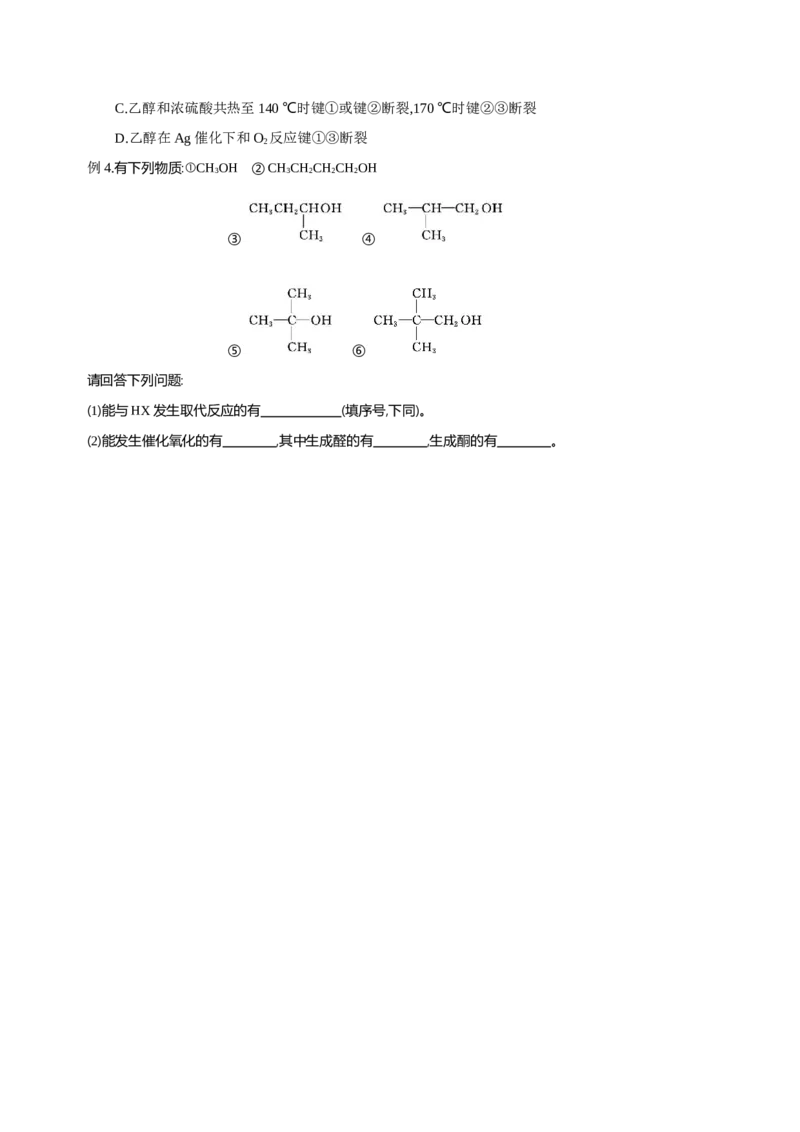
例4.有下列物质:①CHOH ②CHCHCHCHOH
3 3 2 2 2
③ ④
⑤ ⑥
请回答下列问题:
(1)能与HX发生取代反应的有 (填序号,下同)。
(2)能发生催化氧化的有 ,其中生成醛的有 ,生成酮的有 。