文档内容
第三章 晶体结构与性质
第二节 分子晶体与共价晶体
第一课时 分子晶体
1.借助共价晶体模型认识共价晶体的结构特点。
2.能够从化学键的特征,分析理解共价晶体的物理特性。
教学重点:共价晶体的结构特点与性质之间的关系
教学难点:共价晶体的结构特点与性质之间的关系
3.晶胞中粒子数目的计算(以金属铜为例):
一、共价晶体
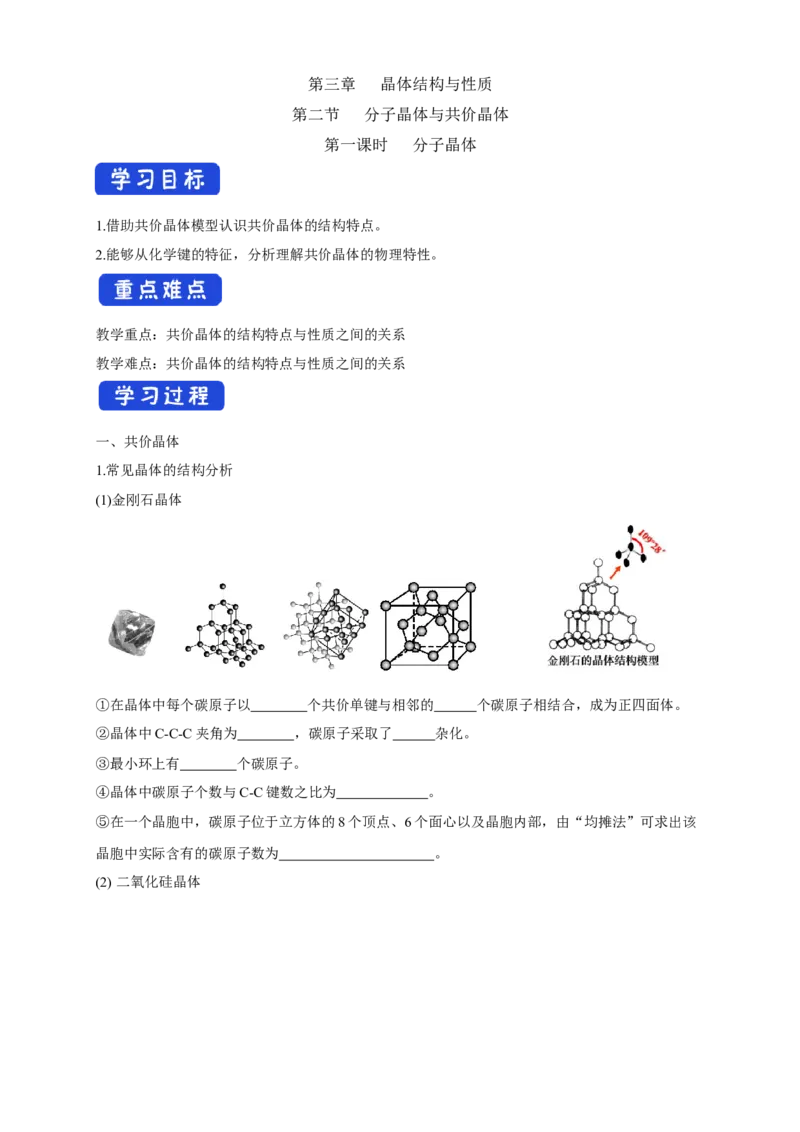
1.常见晶体的结构分析
在铜(1的)金晶刚胞石结晶体构中,铜原子不全属于该晶胞,按均摊原则,金属铜的一个
晶胞的原子数=8× +6× =4。
结合下图,钠、1锌、1碘、金刚石晶胞中含有原子的数目分别为2、2、8、
8。 8 2
钠、锌、碘、金刚石晶胞示意图
①在晶体中每个碳原子以 个共价单键与相邻的 个碳原子相结合,成为正四面体。
②晶体中C-C-C夹角为 ,碳原子采取了 杂化。
③最小环上有 个碳原子。
④晶体中碳原子个数与C-C键数之比为 。
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该
晶胞中实际含有的碳原子数为 。
(2) 二氧化硅晶体①每个硅原子与相邻的 个氧原子以共价键相结合构成 结构,硅原子在正四面体
的中心,4个氧原子在正四面体的4个顶点。晶体中Si原子与O原子个数比为 。
②每个Si原子与4个O原子成键,每个O原子与 个Si原子成键,最小的环是
元环。
③每个最小的环实际拥有的硅原子为 ,氧原子数为 。
④1molSiO 晶体中含Si—O键数目为 ,在SiO 晶体中Si、O原子均采取 杂化。
2 2
⑤SiO 具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维
2
的原料。
【小结】
一、共价晶体
1、共价晶体的概念:
2、组成微粒:
3、微粒间的作用力:
4、分类:
5、共价晶体的通性
①熔点 。共价晶体中,原子间以较强的共价键相结合,要使物质熔化就要克服共价
键,需要很高的能量。
②硬度 。
③一般不导电,但晶体硅是半导体。
④难溶于一般溶剂。
【思考·讨论】
(1)SiO 是二氧化硅的分子式吗?
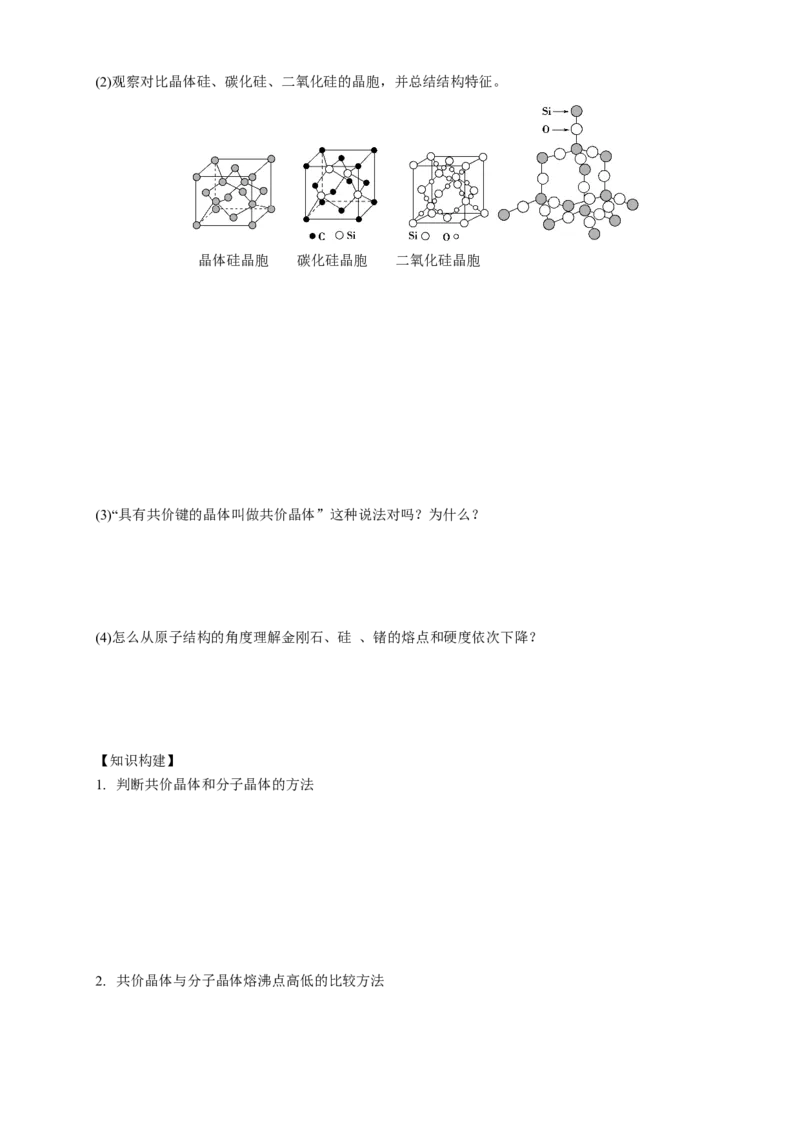
2(2)观察对比晶体硅、碳化硅、二氧化硅的晶胞,并总结结构特征。
晶体硅晶胞 碳化硅晶胞 二氧化硅晶胞
(3)“具有共价键的晶体叫做共价晶体”这种说法对吗?为什么?
(4)怎么从原子结构的角度理解金刚石、硅 、锗的熔点和硬度依次下降?
【知识构建】
1. 判断共价晶体和分子晶体的方法
2. 共价晶体与分子晶体熔沸点高低的比较方法3. 共价晶体与分子晶体的比较
1. 下列说法正确的是
A. 晶体中存在共价键
B. 溶于水能电离出 和 ,所以硫酸是离子化合物
C. 属于原子晶体,熔化破坏共价键和分子间作用力
D. 是分子晶体,加热升华过程中只需克服分子间作用力
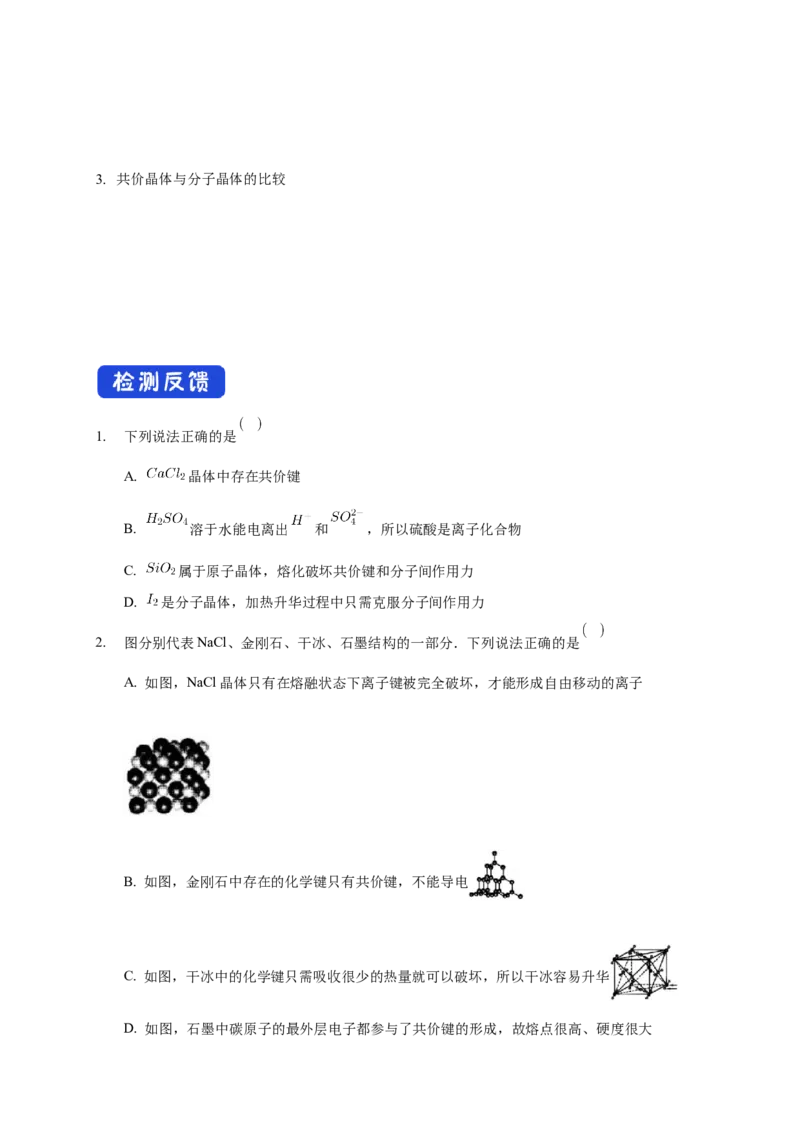
2. 图分别代表NaCl、金刚石、干冰、石墨结构的一部分.下列说法正确的是
A. 如图,NaCl晶体只有在熔融状态下离子键被完全破坏,才能形成自由移动的离子
B. 如图,金刚石中存在的化学键只有共价键,不能导电
C. 如图,干冰中的化学键只需吸收很少的热量就可以破坏,所以干冰容易升华
D. 如图,石墨中碳原子的最外层电子都参与了共价键的形成,故熔点很高、硬度很大3. 以下关于晶体性质说法不正确的是
A. 熔点:金刚石 碳化硅 晶体硅
B. 沸点:
C. 冰和干冰都是分子晶体,每个分子周围都有12个紧邻的分子
D. 区分晶体和非晶体最可靠的方法是 射线衍射实验
4. 氮化硼 晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状
结构,可作高温润滑剂;立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所
示。关于这两种晶体的说法正确的是
A. 六方相氮化硼与石墨一样可以导电
B. 立方相氮化硼含有 键和 键,所以硬度大
C. 两种晶体均为分子晶体
D. 六方相氮化硼晶体层内一个硼原子与相邻氮原子构成平面三角形
5. 下列晶体性质的比较中,错误的是
A. 熔点:金刚石 碳化硅 晶体硅 B. 沸点:
C. 硬度:白磷 冰 二氧化硅 D. 熔点: