文档内容
3.3 醛 酮(精练)
题组一 醛类
1.(2021·全国·高二课时练习)关于甲醛下列叙述不正确的是
A.甲醛是非电解质
B.甲醛的溶液可以用于蔬菜保鲜或保存动物标本
C.甲醛中元素电负性由大到小的顺序为
D.甲醛在通常状况下为易挥发、具有刺激性气味的气体
【答案】B
【解析】A.甲醛是化合物,但其在水溶液中和熔融状态下均不导电,为非电解质,A正确;
B.甲醛的溶液有毒、致癌,不能用于蔬菜保鲜,但可作防腐剂保存动物标本,B错误;
C.同周期元素从左到右电负性逐渐增大,同主族元素从上到下电负性逐渐减小,故电负性由大到小的顺
序为 ,C正确;
D.甲醛在通常状况下为具有刺激性气味的气体,D正确.
故答案为:B
2.(2021·全国·高二课时练习)下列关于醛的说法不正确的是
A.甲醛是甲基跟醛基相连而构成的醛 B.醛的官能团是—CHO
C.甲醛和丙醛互为同系物 D.饱和一元脂肪醛的通式为C H O(n≥1,n为整数)
n 2n
【答案】A
【解析】A.甲醛的结构简式为HCHO,即甲醛分子中不含烃基,甲醛是氢原子跟醛基相连而构成的醛,
故A错误;
B.醛的官能团是醛基,即-CHO,故B正确;
C.甲醛的结构简式为HCHO,丙醛的结构简式为CHCHCHO,甲醛和丙醛结构相似,分子组成相差两个
3 2
CH 原子团,互为同系物,故C正确;
2
D.饱和一元脂肪醛是指含有一个醛基,烃基为饱和的,不存在不饱和键,则饱和一元脂肪醛的通式为
C H O(n≥1,n为整数),故D正确;
n 2n
答案为A。
3.(2021·北京理工大学附属中学分校高二期中)下列有关醛的说法正确的是
A.甲醛是由甲基跟醛基相连而构成的醛
B.醛的官能团是—COH
C.甲醛和丙醛互为同系物D.饱和一元醛的通式为C H O
n 2n+2
【答案】C
【解析】A.甲基跟醛基相连而构成的醛是乙醛,不是甲醛,乙醛结构简式为CHCHO,甲醛结构简式为
3
HCHO,故A错误;
B.醛的官能团是—CHO,故B错误;
C.甲醛和丙醛结构相似,分子组成相差2个—CH—原子团,因此两者互为同系物,故C正确;
2
D.根据甲醛结构简式为HCHO,乙醛结构简式为CHCHO,得到饱和一元醛的通式为C H O,故D错误。
3 n 2n
综上所述,答案为C。
4.(2021·全国·高二课时练习)探究甲醛与新制Cu(OH) 的反应:①向6 mL 6mol/L NaOH溶液中滴加8
2
滴2% CuSO 溶液,振荡,加入0.5 mL 15%甲醛溶液,混合均匀,水浴加热,迅速产生红色沉淀,产生无
4
色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液
与新制Cu(OH) 共热,未观察到明显现象;已知: ,甲醛是具有强还原性的气体,下
2
列说法正确的是
A.红色沉淀的主要成分不是Cu O,可能是Cu
2
B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
C.从甲醛的结构 推测,其氧化产物可能为碳酸( )因此实验中得到的无色气体中大量含有
CO
2
D.含有-CHO的有机物都可以被新制Cu(OH) 氧化
2
【答案】A
【解析】向6 mL 6 mol·L−1 NaOH溶液中滴加8滴2%CuSO 溶液,配制成新制的Cu(OH) ,加入0.5
4 2
mL15%甲醛溶液,混合均匀,水浴加热,甲醛具有强还原性,与新制的Cu(OH) 发生氧化还原反应,迅速
2
产生红色沉淀,产生无色气体。将所得沉淀洗净后加入浓盐酸,不溶解,根据已知信息:Cu O 浓盐酸
2
[CuCl ]−,可知,红色沉淀不是Cu O,可能是Cu。甲醛被氧化,根据甲醛中碳元素的化合价为+2价,
2 2
可知氧化产物不可能为CO,可能是碳酸盐,由于水浴加热,甲醛具有挥发性,生成的无色气体中混有甲
醛气体,据此分析解答。
A.根据已知信息,Cu O [CuCl ]−,实验操作②中,红色沉淀洗净后加入浓盐酸,不溶解,则可以确
2 2
定红色沉淀的主要成分不是Cu O,可能是Cu,故A正确;
2B.甲醛是具有强还原性的气体,甲醛具有挥发性,生成的无色气体中混有甲醛气体,可将灼热的CuO还
原为铜单质,得到红色固体,所以不能证明气体中含有CO,故B错误;
C.配制新制氢氧化铜悬浊液时,NaOH是过量的,在碱性溶液中不可能产生二氧化碳,故C错误;
D.根据实验操作③,甲酸钠中也含有醛基,与新制的Cu(OH) 反应,未观察到明显现象,含有-CHO的甲
2
酸钠没有被新制Cu(OH) 氧化,故D错误;
2
答案选A。
5.(2021·全国·高三专题练习)(1)醛的官能团是-COH____
(2)甲醛是甲基跟醛基相连而构成的醛_____
(3)饱和一元脂肪醛的分子式符合C H O的通式_____
n 2n
(4)甲醛、乙醛、丙醛均无同分异构体____
(5)凡是能发生银镜反应的有机物都是醛_____
(6)醛类物质发生银镜反应或与新制Cu(OH) 的反应均需在碱性条件下_____
2
(7)1mol甲醛与足量的硝酸银溶液反应,可得到4mol单质银_____
(8)检验醛基用的银氨溶液和氢氧化铜悬浊液都可长时间储存_____
(9)1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成2molAg____
(10)已知甲醛是平面形分子,则苯甲醛的所有原子有可能在同一平面上____
(11)可用新制的Cu(OH) 来区分甲醛和苯甲醛_____
2
(12)乙醛能被弱氧化剂(新制氢氧化铜悬浊液或银氨溶液)氧化,所以也能被酸性KMnO 溶液氧化,使酸性
4
KMnO 溶液褪色_____
4
【答案】(1)错误 (2) 错误 (3) 正确 (4)错误 (5) 错误 (6)正确
(7)正确 (8) 错误 (9) 错误 (10)正确 (11) 错误 (12)正确
【解析】(1)醛的官能团是-CHO,错误;
(2)甲醛是氢原子跟醛基相连而构成的醛,错误;
(3)饱和一元脂肪醛的分子式符合C H O的通式,正确;
n 2n
(4)丙醛与丙酮互为同分异构体,错误;
(5)甲酸类也能发生银镜反应,错误;
(6)醛类物质发生银镜反应或与新制Cu(OH) 的反应均需在碱性条件下,正确;
2
(7)1mol甲醛相当于2mol-CHO,与足量的硝酸银溶液反应,可得到4mol单质银,正确;
(8)检验醛基用的银氨溶液和氢氧化铜悬浊液都不可长时间储存,错误;
(9)1molHCHO与足量银氨溶液在水浴加热条件下充分反应,最多生成4molAg,错误;
(10)已知甲醛是平面形分子,则苯甲醛的所有原子有可能在同一平面上,正确;(11)新制的Cu(OH) 遇甲醛和苯甲醛都生成砖红色沉淀,不可以鉴别,错误;
2
(12)乙醛能被弱氧化剂(新制氢氧化铜悬浊液或银氨溶液)氧化,所以也能被酸性KMnO 溶液氧化,使酸性
4
KMnO 溶液褪色,正确;
4
题组二 乙醛
1.(2021·江苏徐州·高二期中)某学生做乙醛还原性的实验,在一支试管内加入2mL 1 硫酸铜溶
液和4mL 0.4 氢氧化钠溶液,混合后加入0.5mL 40%的乙醛溶液,加热至沸腾,无红色沉淀。实验
失败的原因是
A.氢氧化钠不足 B.硫酸铜不足 C.乙醛溶液太少 D.加热时间不够
【答案】A
【解析】做该实验,与乙醛反应的必须是新制的氢氧化铜碱性悬浊液、氢氧化钠必须相对过量,所以实验
失败的主要原因是氢氧化钠不足;答案选A。
2.(2021·天津河北·高二期末)下列物质,能发生银镜反应的是
A.乙醚 B.乙醇 C.乙醛 D.乙酸乙酯
【答案】C
【解析】A.乙醚中含有醚键,没有醛基,不可以发生银镜反应,A项错误;
B.乙醇中含有羟基,没有醛基,不可以发生银镜反应,B项错误;
C.乙醛中含有醛基,能发生银镜反应,C项正确;
D.乙酸乙酯中含有酯基,没有醛基,不可以发生银镜反应,D项错误;
答案选C。
3.(2021·重庆·高二阶段练习)乙醛的银镜反应实验如下:
步骤1:向试管中加入1mL2%AgNO 溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为
3
灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1mL10%乙醛溶液,振荡,在60~70℃水浴中加热,观察到试管内壁形成了光亮银
镜。
下列说法不正确的是
A.步骤1中观察到的白色沉淀为AgOH
B.步骤2中沉淀溶解是因为生成[Ag(NH)]+
3 2
C.步骤3中产生银镜说明乙醛被还原D.试管内壁的银镜可以用稀硝酸洗去
【答案】C
【解析】A.氨水少量时,氨水中一水合氨电离出氢氧根离子和银离子结合成白色的AgOH沉淀,因此步
骤1中观察到的白色沉淀为AgOH,A正确;
B.AgOH与NH ·H O反应生成 Ag(NH)OH而溶解,AgOH转变成[Ag(NH)]+,B正确;
3 2 3 2 3 2
C.[Ag(NH)]OH和乙醛发生银镜反应生成Ag,Ag元素化合价降低,被还原,而乙醛发生氧化反应,被
3 2
氧化,C错误;
D.因硝酸具有强氧化性能溶解Ag,试管内壁的银镜,可用稀硝酸洗去, D正确;
故选:C。
4.(2021·陕西省黄陵县中学高二期末)下列有关银镜反应实验的说法中正确的是
A.生成银镜过程中需用玻璃棒均匀搅拌
B.向2%的稀氨水中滴入2%的硝酸银溶液,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
【答案】C
【解析】A.生成银镜过程中不能用玻璃棒搅拌,故A错误;
B.配得银氨溶液时,向2%的硝酸银溶液滴入2%的稀氨水,边加边振荡,至生成的沉淀恰好溶解,即得
银氨溶液 ,故B错误;
C.水浴加热能保证试管受热均匀,且易于控制反应温度,直接加热受热不均匀,不利于银镜的生成 ,故
C正确;
D.银和浓盐酸不反应,需要用稀硝酸洗去银镜 ,故D错误;
故选:C。
5.(2021·福建莆田·高二阶段练习)已知Ag+可与NH 结合形成Ag[NH] 。葡萄糖的银镜反应实验如下:
3 3
步骤1:向试管中加入lmL2%AgNO 溶液,边振荡边滴加2%氨水,观察到有白色沉淀产生并迅速转化为
3
灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。
步骤3:再向试管中加入1mL10%葡萄糖溶液,振荡,在60-70℃水浴中加热,观察到试管内壁形成了光亮
的银镜(单质银)
下列说法不正确的是
A.步骤1中观察到的白色沉淀为AgOH
B.步骤2中沉淀溶解是因为生成了可溶于水的银氨离子化合物C.步骤3中产生银镜说明葡萄糖具有还原性
D.银氨离子中含有离子键
【答案】D
【解析】A.AgNO 溶液和少量氨水反应,生成AgOH白色沉淀,故A正确;
3
B.AgNO 溶液和少量氨水反应,先生成AgOH白色沉淀,再滴加氨水,AgOH又和NH •H O反应生成配
3 3 2
合物Ag(NH)OH而溶解,故B正确;
3 2
C.Ag(NH)OH和葡萄糖发生银镜反应生成Ag,银元素化合价降低,被还原,说明葡萄糖具有还原性,
3 2
故C正确;
D.Ag[NH] 中存在配位键和极性共价键,不存在离子键,故D错误;
3
故选D。
6.(2021·辽宁·辽河油田第二高级中学高二阶段练习)某学生用 的 溶液
的 溶液混合,然后加入 的乙醛溶液加热沸腾未见红色沉淀实验失败的主要原因
A.甲醛量太少 B.硫酸铜量少 C.加热时间短 D. 量少
【答案】D
【解析】用2mL2mol/L的CuSO 溶液2mL0.5mol/L的NaOH溶液混合,显然NaOH溶液不足以使CuSO 完
4 4
全转化为Cu(OH) ,因此,该实验失败的主要原因是NaOH量少;
2
答案选D。
7.(2021·全国·高二课时练习)下列有关银镜反应实验的说法不正确的是
A.实验前先用热的烧碱溶液洗涤有油脂的试管,再用蒸馏水洗涤
B.向2%的硝酸银溶液中滴入2%的稀氨水,直至产生的沉淀恰好溶解,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
【答案】D
【解析】A.油脂在碱性条件下发生水解反应,所以做银镜反应实验准备洁净试管时,先加氢氧化钠溶液
加热几分钟,油脂水解生成高级脂肪酸钠和甘油,再用蒸馏水冲洗即可得到干净的试管,故A正确;
B.配制银氨溶液时,若向 的稀氨水中滴加 的硝酸银溶液,氨水过量会生成易爆炸的雷酸银(
),因此配制银氨溶液时应将 的稀氨水滴入 的硝酸银溶液中,直至产生的沉淀恰好溶解为止,
故B正确;
C.水浴加热能保证试管受热均匀,且易于控制反应温度,而直接加热时试管受热不均匀,不利于银镜的
生成,故C正确;D.Ag能够和稀硝酸反应而溶解,因此可用稀硝酸洗去试管内的银镜,不能使用浓盐酸,故D错误;
故选:D。
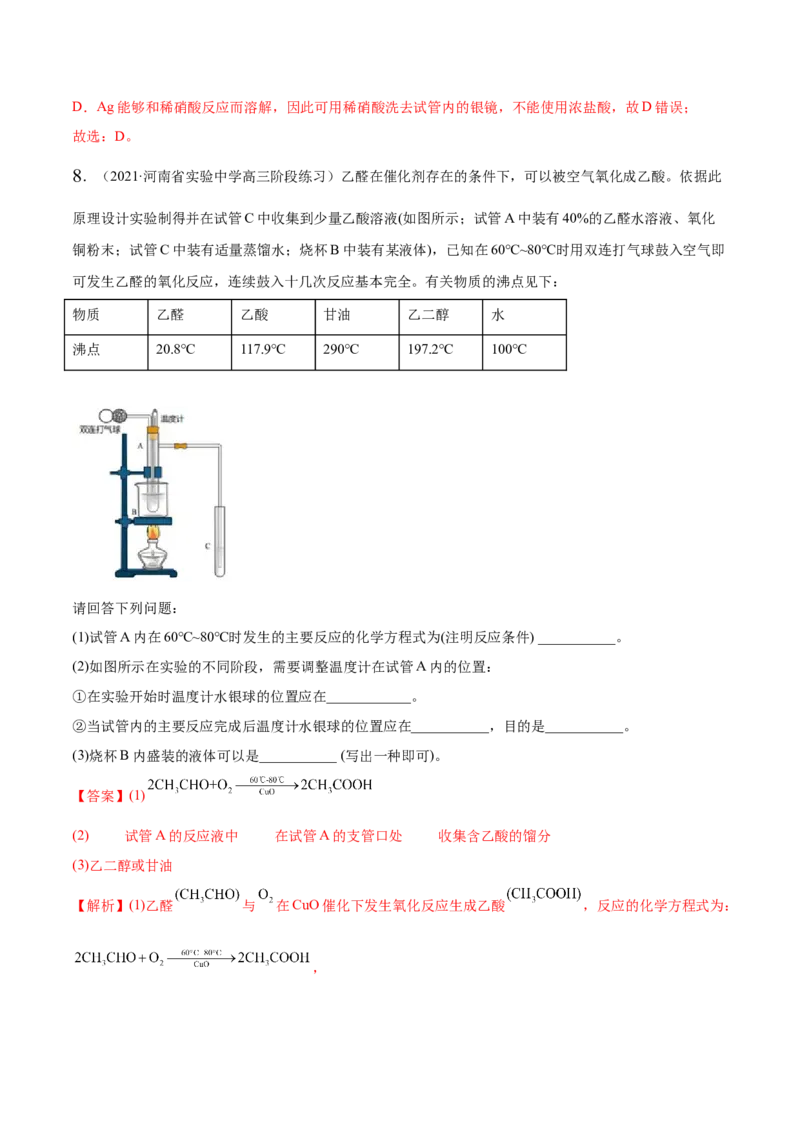
8.(2021·河南省实验中学高三阶段练习)乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此
原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示;试管A中装有40%的乙醛水溶液、氧化
铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体),已知在60℃~80℃时用双连打气球鼓入空气即
可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下:
物质 乙醛 乙酸 甘油 乙二醇 水
沸点 20.8℃ 117.9℃ 290℃ 197.2℃ 100℃
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件) ___________。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置:
①在实验开始时温度计水银球的位置应在____________。
②当试管内的主要反应完成后温度计水银球的位置应在___________,目的是___________。
(3)烧杯B内盛装的液体可以是___________ (写出一种即可)。
【答案】(1)
(2) 试管A的反应液中 在试管A的支管口处 收集含乙酸的馏分
(3)乙二醇或甘油
【解析】(1)乙醛 与 在CuO催化下发生氧化反应生成乙酸 ,反应的化学方程式为:
,故答案为: 。
(2)①实验开始时温度计应测量反应的温度,控制反应温度为60℃~80℃,所以实验开始时温度计水银球的
位置应在试管A的反应液中,目的是测量反应溶液的温度。
故答案为:试管的反应液中。
②当试管A内的主要反应完成后,应进行蒸馏操作进行分离提纯乙酸,由蒸馏原理可知,温度计测量的是
蒸气的温度,所以温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分。
故答案为:在试管A的支管口处;收集含乙酸的馏分。
(3)乙酸的沸点为117.9℃,,要想通过蒸馏的方法得到乙酸,B内盛装的液体的沸点应大于117.9℃,由表
中数据可知烧杯B内盛装的液体可以是乙二醇或甘油。
故答案为:乙二醇或甘油。
9.(2021·广东·广州市第二中学高二期中)某实验小组认为银镜反应用银氨溶液而不直接用AgNO 溶液的
3
原因和溶液酸碱性有关。
I.甲同学进行了如下对比实验:
实验序
装置 试管中的药品 现象
号
2%AgNO 溶液1 mL,加入2%氨水22滴;再加入3滴40%乙 出现光亮的
实验1 3
醛溶液;水浴加热 银镜
2%AgNO 溶液1 mL,加入蒸馏水22滴;再加入3滴40%乙醛
实验2 3 无明显现象
溶液;水浴加热
(1)甲同学认为:AgNO 溶液应该也可以直接氧化乙醛的理由是_______(写出一条即可);而实验II中无明
3
显现象,可能的原因是_______。(写出一条即可)
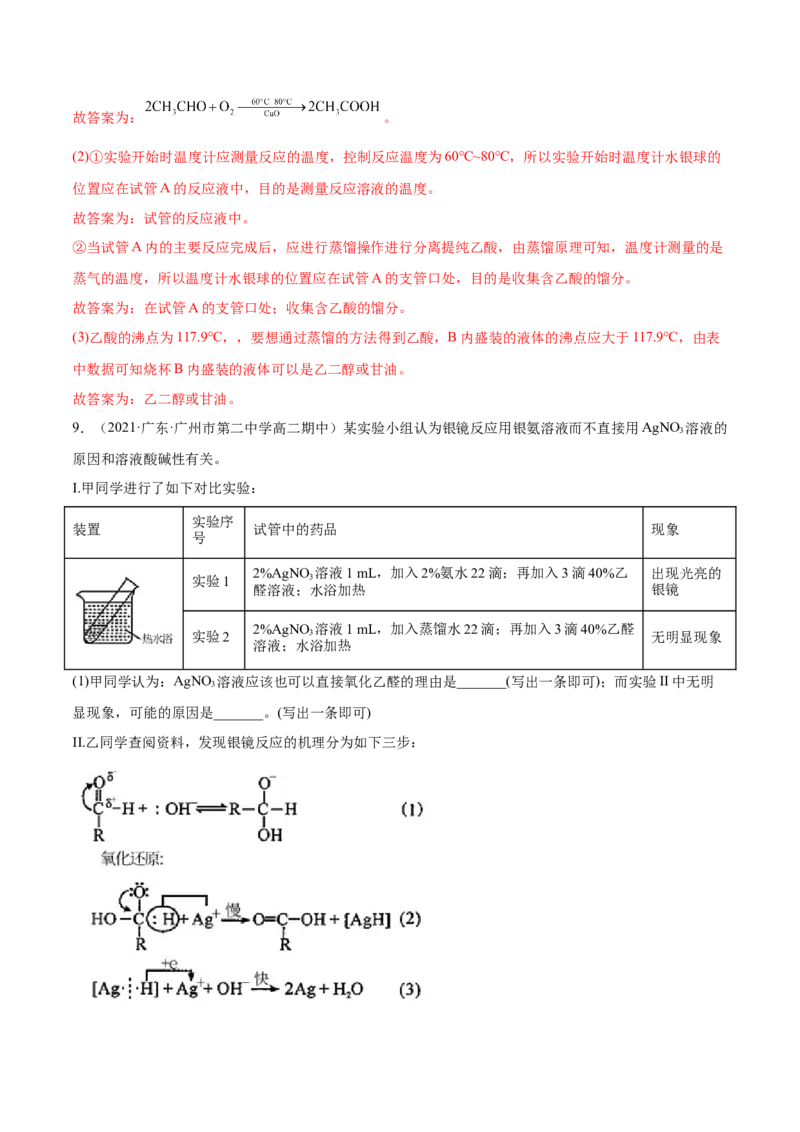
II.乙同学查阅资料,发现银镜反应的机理分为如下三步:(2)据此,乙设计了实验III:1mL 2%AgNO 溶液中,依次加入3滴1mol/L NaOH溶液、2%氨水19滴、3
3
滴40%乙醛溶液:水浴加热,结果比实验I更快出现了银镜,说明_______
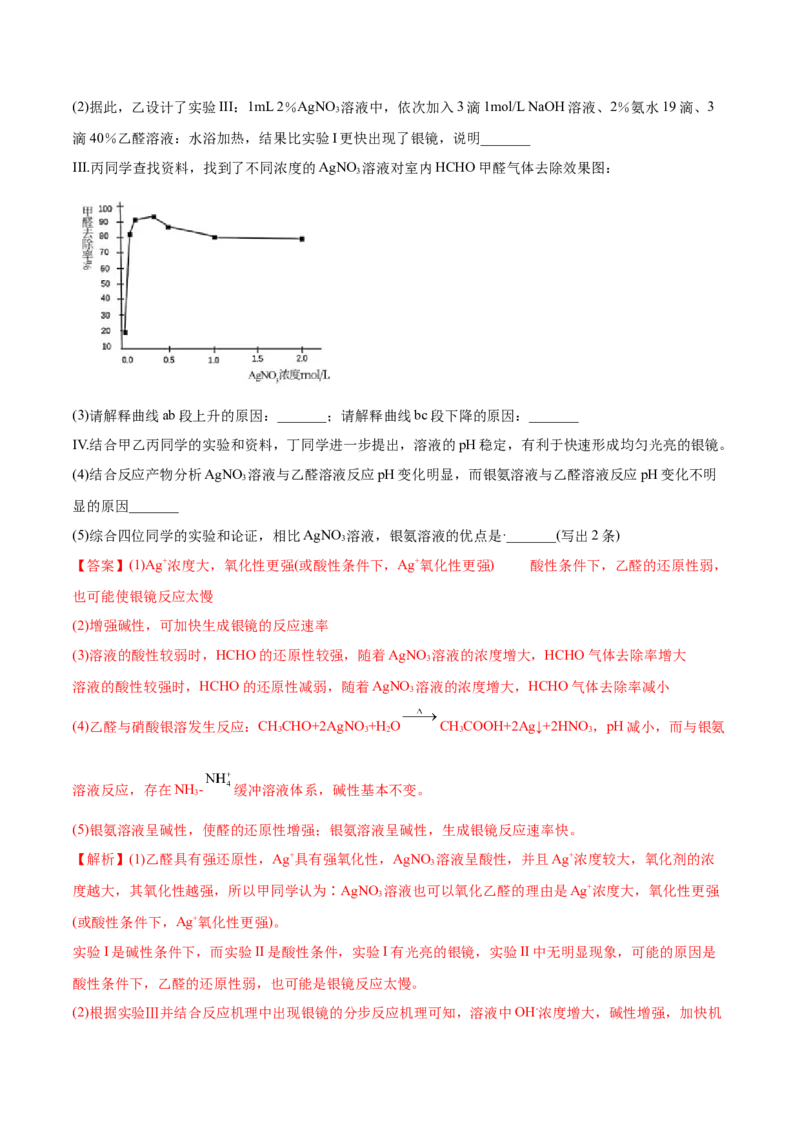
III.丙同学查找资料,找到了不同浓度的AgNO 溶液对室内HCHO甲醛气体去除效果图:
3
(3)请解释曲线ab段上升的原因:_______;请解释曲线bc段下降的原因:_______
IV.结合甲乙丙同学的实验和资料,丁同学进一步提出,溶液的pH稳定,有利于快速形成均匀光亮的银镜。
(4)结合反应产物分析AgNO 溶液与乙醛溶液反应pH变化明显,而银氨溶液与乙醛溶液反应pH变化不明
3
显的原因_______
(5)综合四位同学的实验和论证,相比AgNO 溶液,银氨溶液的优点是·_______(写出2条)
3
【答案】(1)Ag+浓度大,氧化性更强(或酸性条件下,Ag+氧化性更强) 酸性条件下,乙醛的还原性弱,
也可能使银镜反应太慢
(2)增强碱性,可加快生成银镜的反应速率
(3)溶液的酸性较弱时,HCHO的还原性较强,随着AgNO 溶液的浓度增大,HCHO气体去除率增大
3
溶液的酸性较强时,HCHO的还原性减弱,随着AgNO 溶液的浓度增大,HCHO气体去除率减小
3
(4)乙醛与硝酸银溶发生反应:CHCHO+2AgNO +H O CHCOOH+2Ag↓+2HNO ,pH减小,而与银氨
3 3 2 3 3
溶液反应,存在NH - 缓冲溶液体系,碱性基本不变。
3
(5)银氨溶液呈碱性,使醛的还原性增强;银氨溶液呈碱性,生成银镜反应速率快。
【解析】(1)乙醛具有强还原性,Ag+具有强氧化性,AgNO 溶液呈酸性,并且Ag+浓度较大,氧化剂的浓
3
度越大,其氧化性越强,所以甲同学认为∶AgNO 溶液也可以氧化乙醛的理由是Ag+浓度大,氧化性更强
3
(或酸性条件下,Ag+氧化性更强)。
实验I是碱性条件下,而实验II是酸性条件,实验I有光亮的银镜,实验II中无明显现象,可能的原因是
酸性条件下,乙醛的还原性弱,也可能是银镜反应太慢。
(2)根据实验Ⅲ并结合反应机理中出现银镜的分步反应机理可知,溶液中OH-浓度增大,碱性增强,加快机理反应三个步骤的反应速率,加快了生成银镜的反应速率。
(3)AgNO 溶液呈酸性,浓度越低,酸性越弱,曲线ab段对应AgNO 溶液的浓度较小,溶液的酸性较弱,
3 3
但HCHO气体去除率较大;曲线bc段对应AgNO 溶液的浓度较大,溶液酸性较强,但HCHO气体去除率
3
较小,说明HCHO气体去除率大小与溶液的酸性强弱有关,即AgNO 溶液的浓度较小,溶液的酸性较弱,
3
HCHO的还原性较强,HCHO气体去除率较大,AgNO 溶液的浓度较大,溶液的酸性较强,HCHO的还原
3
性较弱,HCHO气体去除率较小。
(4)乙醛被硝酸银溶液氧化,发生的反应为:CHCHO+2AgNO +H O CHCOOH+2Ag↓+2HNO ,溶液
3 3 2 3 3
的pH减小,影响银镜的生成,而与银氨溶液反应﹐存在NH - 缓冲溶液体系,使溶液的碱性基本不变。
3
(5)综合实验可知,AgNO 溶液呈酸性,银氨溶液呈碱性,碱性使醛的还原性增强, 氧化能力减弱,生
3
成银镜反应速率快。
10.(2021·河北·张家口市第一中学高二开学考试)乙醇分子中的羟基在一定条件下可以被氧化为醛基(—
CHO),为验证此性质,有关实验如下:
(1)把一端弯成螺旋状的光亮铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇
的试管里,反复操作几次。变黑后的铜丝插入乙醇里,铜丝表面由黑色变为红色,上述过程中发生反应的
总化学方程式为___________。
Ⅱ.某实验小组用下列装置进行乙醇催化氧化的实验。已知乙醇的沸点为78.5 ℃。
(2)在鼓入空气的条件下进行实验。
①加入药品后,点燃酒精灯给铜网加热,打开止水夹,鼓入空气。
②实验过程中在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是
___________反应。
③甲和乙两个水浴的作用不相同。甲的作用是___________;乙的作用是___________。
(3)在停止鼓入空气的条件下进行实验。
①关闭止水夹,为使乙醇持续进入反应管中,需要进行的操作是___________。
②乙醇蒸气进入反应管后,在铜作催化剂及250~350 ℃ 的条件下发生可逆反应,在试管中收集到与实验Ⅰ相同的产物,并有可燃性气体单质放出。该实验揭示了乙醇催化氧化的本质。写出实验Ⅱ中反应的化学
方程式:___________。
(4)该小组通过以上实验探究提出了下列问题,你认为正确的是___________(填字母)。
a.将铜丝换成铜粉,得到乙醛的时间缩短
b.乙醇催化氧化生成乙醛时,乙醇分子中只有O—H键发生断裂
c.利用金属钠能检验实验Ⅱ右侧试管中有没有乙醇
【答案】(1)2CH CHOH+O 2CHCHO+2H O
3 2 2 3 2
(2)放热 加热 冷凝
(3)加热甲烧杯 CHCHOH CHCHO+H ↑
3 2 3 2
(4)ac
【解析】(1)由题意先后发生2Cu+O 2CuO,CHCHOH+CuO CHCHO+H O+Cu,总反应为
2 3 2 3 2
2CHCHOH+O 2CHCHO+2H O;
3 2 2 3 2
(2)②实验过程中在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是放热
反应;
③甲和乙两个水浴的作用不相同,甲是热水用,作用是加热;乙是冰水浴,作用是冷凝;
(3)①若关闭止水夹,且使乙醇持续进入反应管中,需要进行的操作是加热甲烧杯;
②乙醇蒸气进入反应管后,在铜作催化剂及250~350 ℃ 的条件下发生可逆反应,在试管中收集到与实验
Ⅰ相同的产物(乙醛),并有可燃性气体单质放出,则产物为乙醛和氢气,反应的方程式为CHCHOH
3 2
CHCHO+H ↑;
3 2
(4)a.将铜丝换成铜粉,增大了乙醇、Cu和氧气的接触面积,反应速率加快,得到乙醛的时间缩短,a正
确;
b.乙醇催化氧化生成乙醛时,乙醇分子中只有O—H键、C-H键发生断裂,b错误;
c.乙醇能与钠反应产生氢气,而乙醛不能,因此利用金属钠能检验实验Ⅱ右侧试管中有没有乙醇,c正确;
选ac。
题组三 酮类
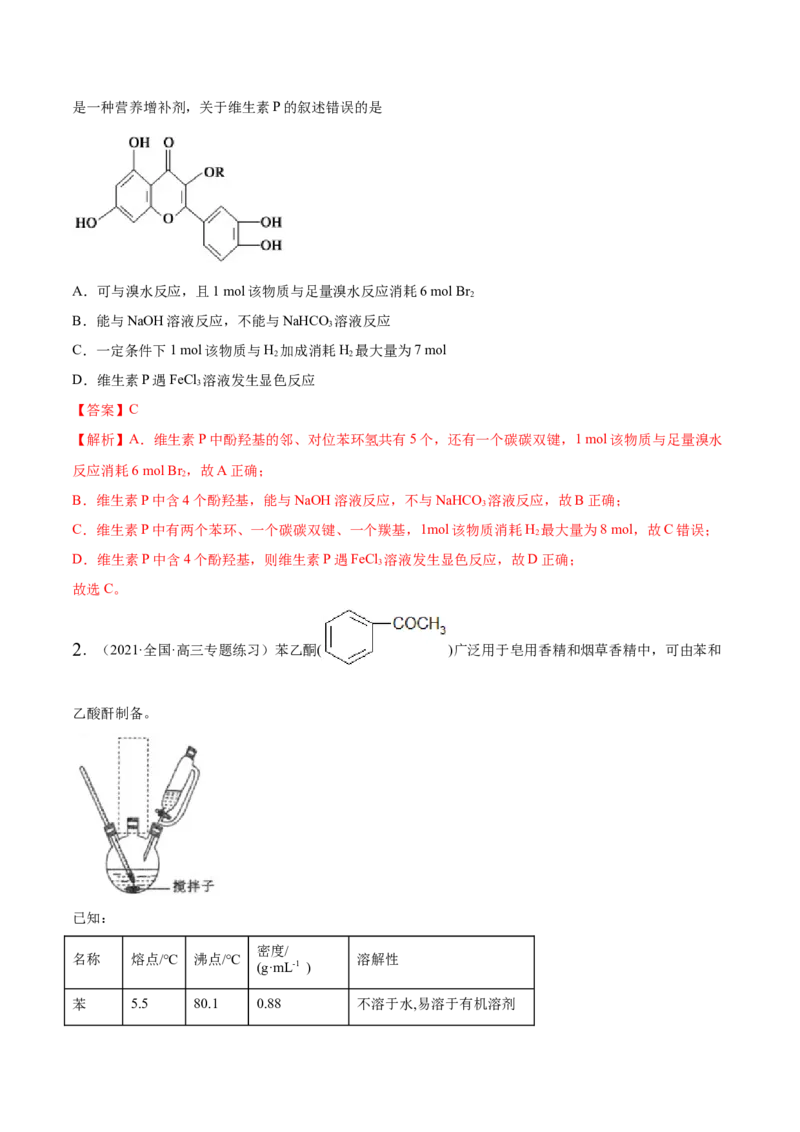
1.(2021·安徽省舒城中学高二阶段练习)天然维生素P(结构如图,图中R为烷基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是
A.可与溴水反应,且1 mol该物质与足量溴水反应消耗6 mol Br
2
B.能与NaOH溶液反应,不能与NaHCO 溶液反应
3
C.一定条件下1 mol该物质与H 加成消耗H 最大量为7 mol
2 2
D.维生素P遇FeCl 溶液发生显色反应
3
【答案】C
【解析】A.维生素P中酚羟基的邻、对位苯环氢共有5个,还有一个碳碳双键,1 mol该物质与足量溴水
反应消耗6 mol Br ,故A正确;
2
B.维生素P中含4个酚羟基,能与NaOH溶液反应,不与NaHCO 溶液反应,故B正确;
3
C.维生素P中有两个苯环、一个碳碳双键、一个羰基,1mol该物质消耗H 最大量为8 mol,故C错误;
2
D.维生素P中含4个酚羟基,则维生素P遇FeCl 溶液发生显色反应,故D正确;
3
故选C。
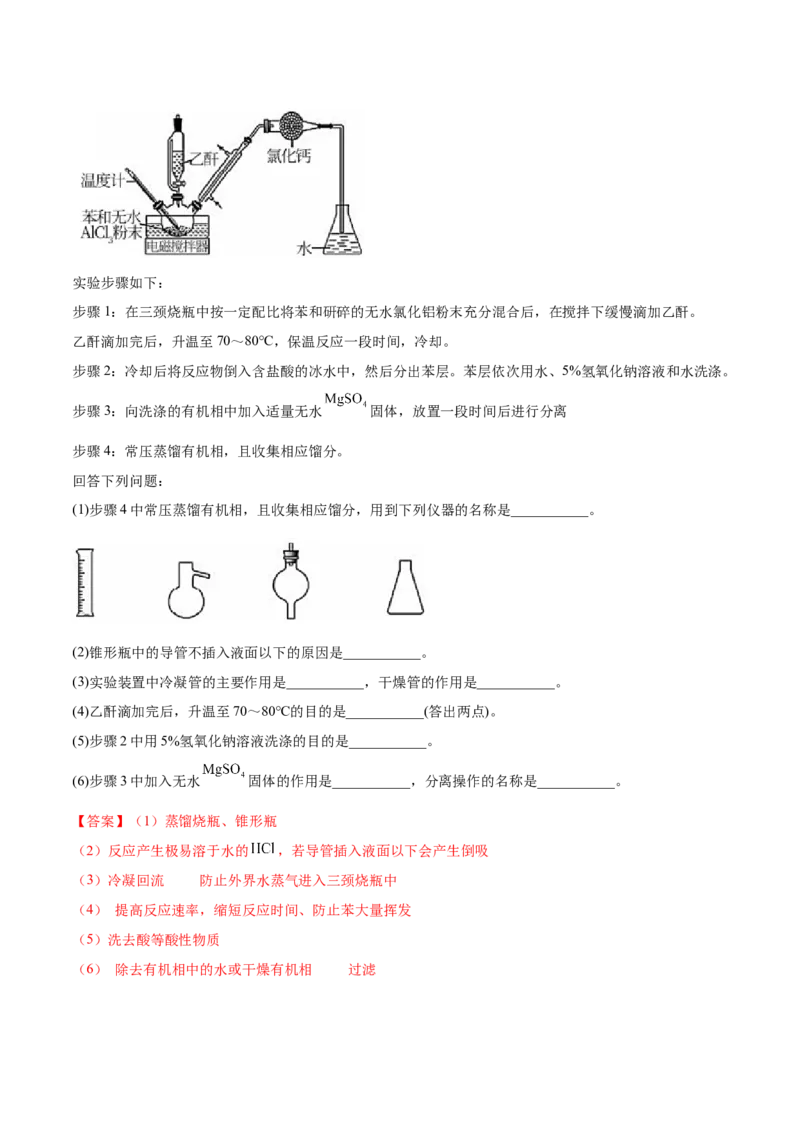
2.(2021·全国·高三专题练习)苯乙酮( )广泛用于皂用香精和烟草香精中,可由苯和
乙酸酐制备。
已知:
密度/
名称 熔点/℃ 沸点/℃ 溶解性
(g·mL-1 )
苯 5.5 80.1 0.88 不溶于水,易溶于有机溶剂苯乙
19.6 203 1.03 微溶于水,易溶于有机溶剂
酮
乙酸
-73 139 1.08 有吸湿性,易溶于有机溶剂
酐
乙酸 16.6 118 1.05 易溶于水,易溶于有机溶剂
步骤I:向三颈烧瓶中加入39 g苯和44.5 g无水氯化铝,在搅拌下滴加25.5 g乙酸酐(C HO),在70~80℃
4 6 3
下加热45min,发生反应: +(CHCO) O +CHCOOH。
3 2 3
步骤II:冷却后将反应物倒入100g冰水中,有白色胶状沉淀生成,采用合适的方法处理,水层用苯萃取,
合并苯层溶液,再依次用30 mL 5% NaOH溶液和30 mL水洗涤,分离出的苯层用无水硫酸镁干燥。
步骤III:常压蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(1)AlCl 在反应中作___________,步骤I中的加热方式为___________。
3
(2)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(3)图示实验装置虚线框内缺少一种仪器,该仪器名称为___________。
(4)步骤II中生成的白色胶状沉淀的化学式为___________,该物质易堵塞滤纸,处理白色胶状沉淀的方法
为___________。
(5)步骤II中用NaOH溶液洗涤的目的是___________。
(6)步骤III中收集苯乙酮的温度应为___________。
【答案】(1)催化剂 70~80℃的水浴加热
(2)B
(3)冷凝管
(4)Al(OH) 加入盐酸,使其溶解,即Al(OH) +3H+=Al3++3H O
3 3 2
(5)除去产品中的乙酸
(6)80.1℃~203℃
【解析】(1)由 +(CHCO) O +CHCOOH可知,AlCl 是反应发生的条件,反应前后
3 2 3 3
AlCl 均存在,故AlCl 在反应中作催化剂;因为需要在70~80℃温度下加热,为便于控制温度且未超过
3 3
100℃,加热方式为70~80℃的水浴加热;(2)由题意知,实验中共用到的药品为39 g苯体积约为V(苯)= =44.3mL,44.5 g无水氯化铝为固体,
其体积可忽略,25.5 g乙酸酐(C HO)体积约为V(乙酸酐)= =23.6mL,液体总体积为
4 6 3
V(总)=44.3mL+23.6mL=67.9mL,根据反应液不超过总容积的 ,即三颈烧瓶的容积V>101.8mL,故选三
颈烧瓶的容积250mL,B符合题意,选B;
(3)由于苯的沸点为80.1℃,而反应的温度需要70~80℃,这样苯易挥发,不利于产物的制取,需要冷凝回
流装置,即加装的仪器为冷凝管;
(4)由题中信息和步骤II的过程可知,产物均易溶于有机溶剂,AlCl 易水解,即冷却后将反应物倒入100g
3
冰水中,产生的白色胶状沉淀为Al(OH) ;处理白色胶状沉淀[Al(OH) ]的方法为加入盐酸,使其溶解,发
3 3
生的反应为Al(OH) +3H+=Al3++3H O;
3 2
(5)由于产物之一乙酸也易溶于有机溶剂,故苯层溶液用30 mL 5% NaOH溶液洗涤,主要是除去产品中的
乙酸;
(6)由题中信息可知,苯的沸点为80.1℃,苯乙酮的沸点为203℃,用常压蒸馏回收苯,再收集苯乙酮,收
集苯乙酮的温度为80.1℃~203℃。
3.(2021·河南·三模)苯乙酮既可用于制香皂和香烟,也可用作纤维素脂和树脂等的溶剂。实验室以苯和
乙酐为原料制备苯乙酮: + +CH COOH,制备过程中还有
3
等副反应发生,实验装置见下图,相关物质的沸点见下表。
物质 苯 苯乙酮 乙酸 乙酐
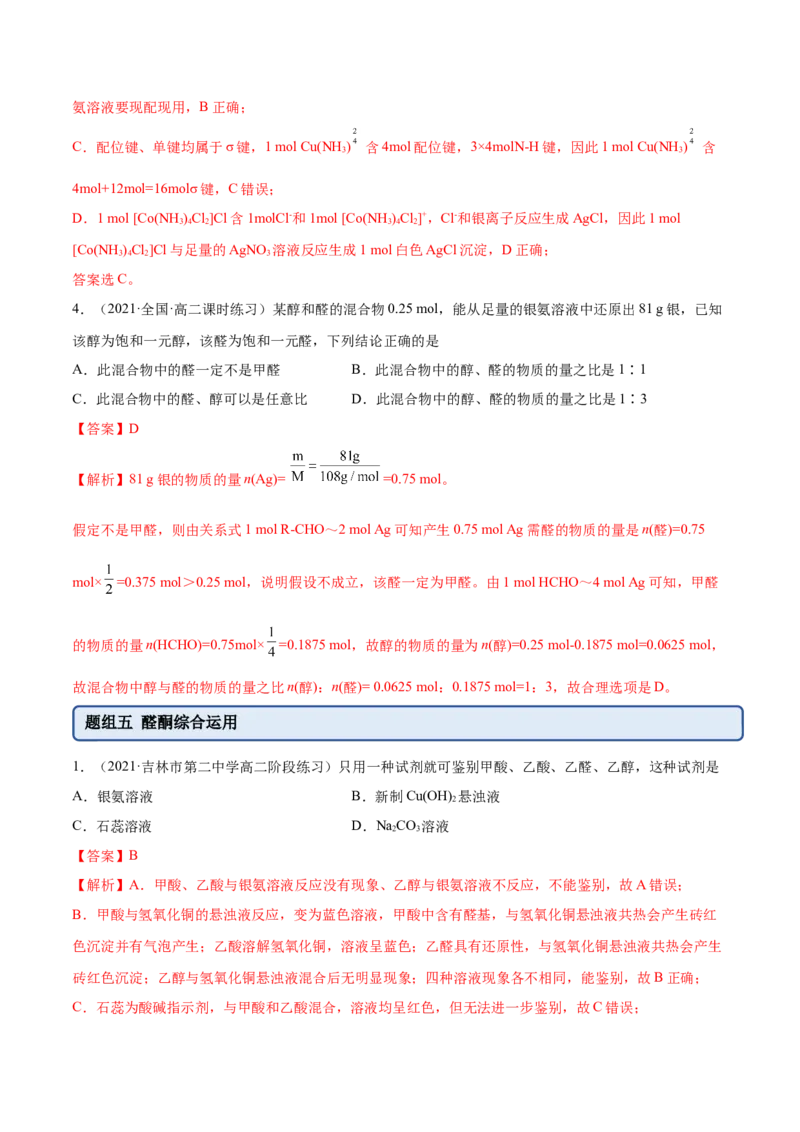
沸点/℃ 80.1 202 117.9 139.8实验步骤如下:
步骤1:在三颈烧瓶中按一定配比将苯和研碎的无水氯化铝粉末充分混合后,在搅拌下缓慢滴加乙酐。
乙酐滴加完后,升温至70~80℃,保温反应一段时间,冷却。
步骤2:冷却后将反应物倒入含盐酸的冰水中,然后分出苯层。苯层依次用水、5%氢氧化钠溶液和水洗涤。
步骤3:向洗涤的有机相中加入适量无水 固体,放置一段时间后进行分离
步骤4:常压蒸馏有机相,且收集相应馏分。
回答下列问题:
(1)步骤4中常压蒸馏有机相,且收集相应馏分,用到下列仪器的名称是___________。
(2)锥形瓶中的导管不插入液面以下的原因是___________。
(3)实验装置中冷凝管的主要作用是___________,干燥管的作用是___________。
(4)乙酐滴加完后,升温至70~80℃的目的是___________(答出两点)。
(5)步骤2中用5%氢氧化钠溶液洗涤的目的是___________。
(6)步骤3中加入无水 固体的作用是___________,分离操作的名称是___________。
【答案】(1)蒸馏烧瓶、锥形瓶
(2)反应产生极易溶于水的 ,若导管插入液面以下会产生倒吸
(3)冷凝回流 防止外界水蒸气进入三颈烧瓶中
(4) 提高反应速率,缩短反应时间、防止苯大量挥发
(5)洗去酸等酸性物质
(6) 除去有机相中的水或干燥有机相 过滤【解析】实验室以苯和乙酐为原料制备苯乙酮: + +CH COOH,常压蒸馏要
3
用到的仪器是蒸馏烧瓶、锥形瓶(收集馏出物),经冷凝回流,充分利用笨和乙酐;用干燥管防止外界水蒸
气进入三颈烧瓶中,制备过程中还有 等副反应发生,反应产
生极易溶于水的 ,所以导管不能插入液面以下,防止倒吸,乙酐滴加完后,升温至70~80℃主要是为
了提高反应速率,缩短反应时间、防止苯大量挥发等,用5%氢氧化钠溶液洗涤的目的是洗去酸等酸性物
质,无水 可以用来除去有机相中的水或干燥有机相,有机相是液体,硫酸镁吸水后还是固体,所以
用过滤的方法分离,以此解答该题。
(1)常压蒸馏要用蒸馏烧瓶、锥形瓶(收集馏出物),故答案为:蒸馏烧瓶、锥形瓶。
(2)因反应生成的CHCOOH与AlCl 在加热条件下反应产生极易溶于水的 ,若导管插入液面以下会产
3 3
生倒吸,故答案为:反应产生极易溶于水的 ,若导管插入液面以下会产生倒吸。
(3)冷凝管的作用是冷凝回流,充分利用笨和乙酐;该反应要保持无水,所以干燥管的作用是防止外界水蒸
气进入三颈烧瓶中,故答案为:冷凝回流、防止外界水蒸气进入三颈烧瓶中。
(4) 乙酐滴加完后,升温至70~80℃的目的是:提高反应速率,缩短反应时间、防止苯大量挥发。
(5) 步骤2中的笨层含有醋酸等酸性物质,即用5%氢氧化钠溶液洗涤的目的是:洗去酸等酸性物质。
(6) 无水 可以用来除去有机相中的水或干燥有机相,有机相是液体,硫酸镁吸水后还是固体,所以
用过滤的方法分离,故答案为:除去有机相中的水或干燥有机相、过滤。
4.(2022·广东揭阳)查尔酮类化合物是黄酮类药物的主要合成中间体。
(1)下列查尔酮类化合物I的说法正确的是________。
A.加入溴的四氯化碳溶液,溶液褪色
B.可发生加成或取代反应
C.不与NaOH溶液发生反应
D.加入新制的氢氧化铜有红色沉淀生成
(2)反应①是制取查尔酮类化合物的一种方法:化合物III的分子式是_________,1mol化合物III最多能与________mol H 发生加成反应。
2
(3)化合物II可由化合物IV(分子式:C H O)在Cu催化氧化下制得,则化合物IV的结构简式为
8 10
______________,化合物IV的一种同分异构体V为芳香族化合物,其核磁共振氢谱上有四组峰,峰面积
之比为为1∶1∶2∶6,则V的结构简式为___________(任写一种)。
(4)聚合物 是一种高分子材料,请利用类似反应①方法,用丙烯和丙醛为有机物原料合
成该聚合物的单体。合成过程中涉及的反应方程式为______、_______、______。
【答案】(1) A B
(2)C H O 8
15 12
(3)
(4)
【解析】试题分析:(1)从结构中可以看出有碳碳双键,故溴的四氯化碳溶液褪色,A对;碳碳双键、苯
环等可以发生加成反应,酚羟基可以发生取代反应,B对;酚羟基显酸性,可以和NaOH溶液发生反应,
C错;结构中没有醛基,不与新制的氢氧化铜反应,D错,选AB。
(2)从结构简式可以看出化合物III的分子式是C H O;结构中的苯环、碳碳双键、羰基都可以发生加成
15 12
反应,故1mol化合物III最多能与8mol H 发生加成反应。
2
(3)化合物II可由化合物IV在Cu催化氧化下制得,可知化合物IV属于醇,要被氧化成羰基,—OH所在的碳原子上只有1个H原子,则化合物IV是 。V为芳香族化合物,其核磁共振氢
谱上有四组峰,峰面积之比为为1∶1∶2∶6,可知苯环上有2个—CH,O原子形成-OH接在苯环上,还
3
有一组峰有2个H原子,由于侧链的碳原子形成了—CH,所以没有—CH—,那么这组峰应该是苯环上两
3 2
个对称碳原子上的H,故结构为: 。
(4)从聚合物的结构可知其单体是:CHCOCH =CHCH CH,根据反应①的特点,需要得到该单体就要
3 2 3
制取 , 再和丙醛反应得到该单体,反应步骤有:
、 、
题组四 有关醛的计算
1.(2021·全国·高二课时练习)丙醛和另一种组成为C H O的物质X的混合物3.2g,与足量的银氨溶液
n 2n
作用后析出10.8g银,则混合物中所含X不可能是
A.甲基丙醛 B.丙酮 C.乙醛 D.丁醛
【答案】C
【解析】反应中生成银的物质的量是10.8g÷108g/mol=0.1mol,根据方程式RCHO+2Ag(NH )OH
3 2
RCOONH +2Ag↓+3NH+H O可知消耗醛的物质的量是0.05mol,则混合物的平均相对分子质量是
4 3 2
3.2÷0.05=64;丙醛的相对分子质量为58<64,所以另一种是相对分子质量大于64的醛,或是不发生银镜反
应的其它物质。则
A. 甲基丙醛的相对分子质量大于64,甲基丙醛可能;
B. 丙酮不能发生银镜反应,丙酮可能;
C. 乙醛的相对分子质量小于64,乙醛不可能;D. 丁醛的相对分子质量大于64,丁醛可能;
答案选C。
2.(2021·全国·高二课时练习)香料茉莉酮是一种人工合成的有机化合物,其结构简式为 ,下
列关于茉莉酮的说法正确的是( )
A.该有机物的化学式是C H O
10 14
B.1 mol该有机物与H 充分反应,消耗4 mol H
2 2
C.该有机物属于不饱和酮类物质,能发生银镜反应
D.该有机物能发生加成反应,但不能发生氧化反应
【答案】A
【解析】A.对茉莉酮结构简式分析可得出其分子式为C H O,故A正确;
11 14
B.该有机物分子中含有一个碳氧双键和两个碳碳双键,则1 mol该有机物与H 充分反应,消耗3 mol
2
H,故B错误;
2
C.该有机物属于不饱和酮类物质,不含醛基,不能发生银镜反应,故C错误;
D.该有机物能发生加成反应,也能发生氧化反应,如碳碳双键能被酸性高锰酸钾溶液氧化、点燃时被氧
气氧化等,故D错误;
答案选A。
3.(2021·河北·秦皇岛一中高二阶段练习)银氨溶液也叫吐伦试剂,常用于制作瓶胆和鉴别还原糖。下列
说法错误的是
A.甲醛是一元醛,1 mol甲醛与足量的银氨溶液反应,转移4 mol电子,生成4 mol Ag
B.配制银氨溶液时,将稀氨水逐滴滴入到硝酸银溶液中至沉淀刚好消失为止,且此溶液不能长期存放,
要现用现配
C.Cu(NH ) 是平面正方形结构,1 mol Cu(NH ) 含12 mol σ键
3 3
D.常温下,1 mol [Co(NH)Cl]Cl与足量的AgNO 溶液反应生成1 mol白色沉淀
3 4 2 3
【答案】C
【解析】A.甲醛结构简式 ,结构特殊,相当于两个-CHO,因此1mol甲醛与足量银氨溶液
反应,转化为1mol(NH)CO,转移1mol×(4-0)=4mol电子,根据得失电子守恒可知得到4molAg,A正确;
4 2 3
B.银氨溶液为Ag(NH)OH溶液,银氨溶液久置会转化为叠氮化银、氮化银、亚氨基化银等物质,因此银
3 2氨溶液要现配现用,B正确;
C.配位键、单键均属于σ键,1 mol Cu(NH ) 含4mol配位键,3×4molN-H键,因此1 mol Cu(NH ) 含
3 3
4mol+12mol=16molσ键,C错误;
D.1 mol [Co(NH)Cl]Cl含1molCl-和1mol [Co(NH )Cl]+,Cl-和银离子反应生成AgCl,因此1 mol
3 4 2 3 4 2
[Co(NH )Cl]Cl与足量的AgNO 溶液反应生成1 mol白色AgCl沉淀,D正确;
3 4 2 3
答案选C。
4.(2021·全国·高二课时练习)某醇和醛的混合物0.25 mol,能从足量的银氨溶液中还原出81 g银,已知
该醇为饱和一元醇,该醛为饱和一元醛,下列结论正确的是
A.此混合物中的醛一定不是甲醛 B.此混合物中的醇、醛的物质的量之比是1∶1
C.此混合物中的醛、醇可以是任意比 D.此混合物中的醇、醛的物质的量之比是1∶3
【答案】D
【解析】81 g银的物质的量n(Ag)= =0.75 mol。
假定不是甲醛,则由关系式1 mol R-CHO~2 mol Ag可知产生0.75 mol Ag需醛的物质的量是n(醛)=0.75
mol× =0.375 mol>0.25 mol,说明假设不成立,该醛一定为甲醛。由1 mol HCHO~4 mol Ag可知,甲醛
的物质的量n(HCHO)=0.75mol× =0.1875 mol,故醇的物质的量为n(醇)=0.25 mol-0.1875 mol=0.0625 mol,
故混合物中醇与醛的物质的量之比n(醇):n(醛)= 0.0625 mol:0.1875 mol=1:3,故合理选项是D。
题组五 醛酮综合运用
1.(2021·吉林市第二中学高二阶段练习)只用一种试剂就可鉴别甲酸、乙酸、乙醛、乙醇,这种试剂是
A.银氨溶液 B.新制Cu(OH) 悬浊液
2
C.石蕊溶液 D.NaCO 溶液
2 3
【答案】B
【解析】A.甲酸、乙酸与银氨溶液反应没有现象、乙醇与银氨溶液不反应,不能鉴别,故A错误;
B.甲酸与氢氧化铜的悬浊液反应,变为蓝色溶液,甲酸中含有醛基,与氢氧化铜悬浊液共热会产生砖红
色沉淀并有气泡产生;乙酸溶解氢氧化铜,溶液呈蓝色;乙醛具有还原性,与氢氧化铜悬浊液共热会产生
砖红色沉淀;乙醇与氢氧化铜悬浊液混合后无明显现象;四种溶液现象各不相同,能鉴别,故B正确;
C.石蕊为酸碱指示剂,与甲酸和乙酸混合,溶液均呈红色,但无法进一步鉴别,故C错误;D.NaCO 溶液与乙酸、甲酸反应生成气体,但与乙醛和乙醇不反应,无法全部鉴别,故D错误;
2 3
故选B。
2.(2021·内蒙古·乌兰浩特一中高二期末)用下列一种试剂可鉴别乙醛、乙酸和乙酸甲酯,该试剂是
A.水 B.氢氧化钠溶液
C.硫酸钠溶液 D.新制Cu(OH) 悬浊液
2
【答案】D
【解析】A.乙醛、乙酸都能溶于水,只有乙酸甲酯不能溶于水,因此不能用水鉴别三种物质,A不符合
题意;
B.氢氧化钠溶液能够溶解乙醛;可以与乙酸反应,液体混溶,也无明显现象;与乙酸甲酯反应,使物质
变为可溶性物质,三种物质不能鉴别,B不符合题意;
C.硫酸钠溶液与三种物质都不能发生反应,其中乙醛、乙酸能够溶解在硫酸钠溶液中,不能鉴别,C不
符合题意;
D.新制Cu(OH) 悬浊液与乙醛混合物现象,加热煮沸,产生砖红色沉淀;与乙酸混合,固体溶解,变为
2
蓝色溶液;与乙酸乙酯混合不能反应,加热也无明显现象,三种物质现象各不相同,可以鉴别,D符合题
意;
故合理选项是D。
3(2021·吉林·希望高中高二阶段练习)下列说法中,正确的是
A.甲醛、乙醛分子中的所有原子都在同一平面上
B.甲醛、乙醛在常温下都是无色有刺激性气味的液体
C.乙醛、丙醛都没有同分异构体
D.醛类既能氧化为羧酸又能还原为醇
【答案】D
【解析】A.乙醛分子中含有-CH,4个原子不可能在同一平面上,A不正确;
3
B.甲醛在常温常压下是无色有刺激性气味的气体,B不正确;
C.丙醛与丙酮等互为同分异构体,C不正确;
D.醛类都含有-CHO,既能被氧化剂(如O、酸性KMnO 等)氧化为羧酸,又能被还原剂(如H 等)还原为醇,
2 4 2
D正确;
故选D。
4.(2021·安徽·高二期末)某有机物W主要用于抗癌、抗氧化、抗溃疡等,其结构简式如图所示。下列
说法正确的是A.W的分子式为
B.1molW最多可以与 发生加成反应
C.W可以使酸性高锰酸钾溶液褪色
D.W分子中所有碳原子一定共面
【答案】C
【解析】A.W的分子式为 ,A项错误;
B.两个苯环与羰基可以与 加成,所以 最多 可以与 加成,B项错误;
C.分子中的醇羟基和酚羟基都可以被酸性高锰酸钾氧化,使高锰酸钾褪色,C项正确;
D.分子中有两个饱和碳原子,形成四面体结构,故所有碳原子不一定共面,D项错误;
答案选C。
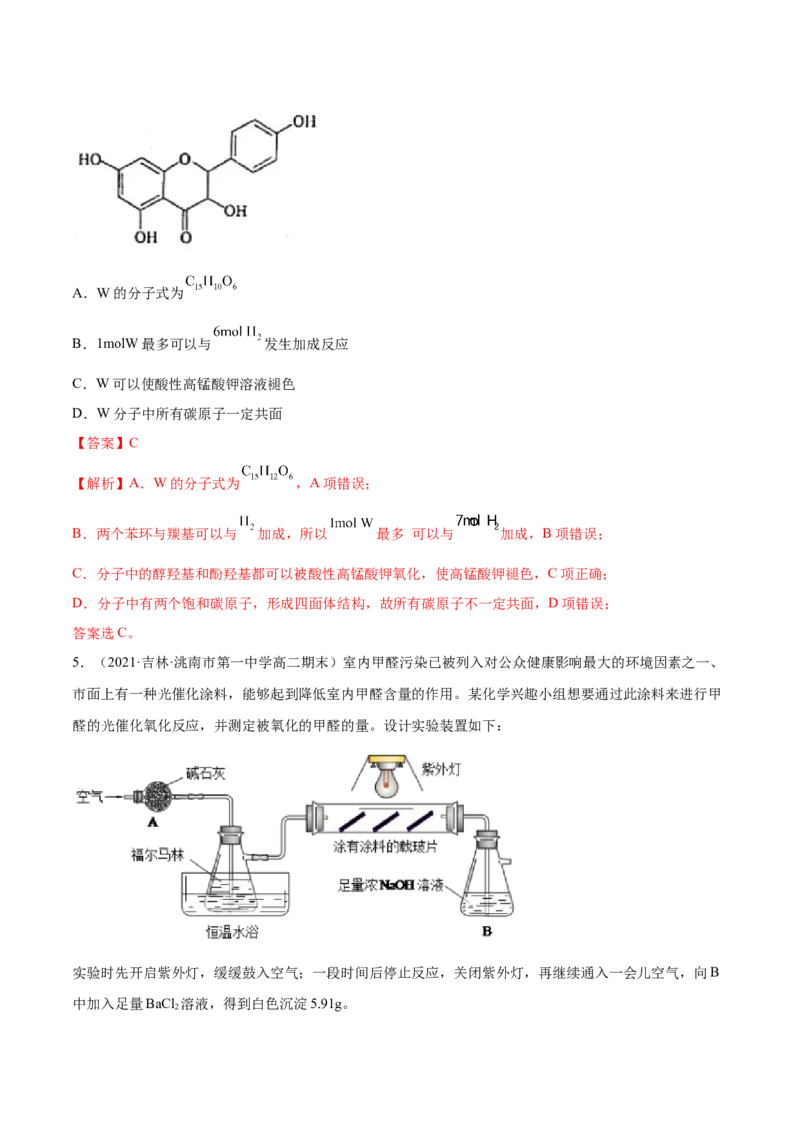
5.(2021·吉林·洮南市第一中学高二期末)室内甲醛污染已被列入对公众健康影响最大的环境因素之一、
市面上有一种光催化涂料,能够起到降低室内甲醛含量的作用。某化学兴趣小组想要通过此涂料来进行甲
醛的光催化氧化反应,并测定被氧化的甲醛的量。设计实验装置如下:
实验时先开启紫外灯,缓缓鼓入空气;一段时间后停止反应,关闭紫外灯,再继续通入一会儿空气,向B
中加入足量BaCl 溶液,得到白色沉淀5.91g。
2(1)甲醛是一种重要的有机原料,用它制取酚醛树脂的化学方程式为_______。
(2)上图装置A中,碱石灰的作用是_______,恒温水浴的目的是_______。
(3)硬质玻璃管中,甲醛在光催化氧化条件下的反应方程式:_______。
(4)计算被氧化的甲醛的物质的量为_______mol。
(5)反应结束后,继续通入一会儿空气的目的是_______。
(6)甲同学认为,反应过程中部分甲醛可能被氧化为甲酸。为验证其存在,甲同学取B中溶液,分别选用下
表试剂进行检验。但乙同学认为试剂选择均不合理,他的理由是:
甲同学选择的试剂 乙同学认为不合理的理由
紫色石蕊试液 _______
新制氢氧化铜 _______
【答案】 (1) +nH O
2
(2) 吸收空气中的CO(防止对产物检验测定造成干扰) 使混合气中甲醛含量稳定(写使甲醛挥发亦
2
可)
(3) HCHO+O CO+H O
2 2 2
(4) 0.03
(5) 将残留在装置中的CO 排出,被NaOH吸收,减小误差
2
(6) B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性) B中可能溶有过量的甲醛,无法证
明是甲酸中醛基
【解析】(1)苯酚与甲醛在一定条件下发生缩聚反应生成酚醛树脂,反应方程式为:
+nH O;
2
(2)碱石灰可吸收空气中的二氧化碳,防止对产物检验测定造成干扰;恒温水浴可使甲醛挥发;故答案为:
吸收空气中的CO(防止对产物检验测定造成干扰);使混合气中甲醛含量稳定(写使甲醛挥发亦可);
2
(3)甲醛在光催化氧化条件下反应生成二氧化碳和水,反应方程式为HCHO+O CO+H O,故
2 2 2答案为:HCHO+O CO+H O;
2 2 2
(4)白色沉淀为碳酸钡,物质的量为 ,根据碳元素守恒,可知被氧化的甲醛的物质的量
为0.03mol,故答案为:0.03;
(5)通入一会儿空气的目的排出装置中的二氧化碳,减小误差,故答案为:将残留在装置中的CO 排出,被
2
NaOH吸收,减小误差;
(6)B中溶液呈碱性(NaOH足量),加紫色石蕊试液无法证明是甲酸;B中可能溶有过量的甲醛,无法证
明是甲酸中醛基,故答案为:B中溶液呈碱性(NaOH足量),无法证明是甲酸(酸性);B中可能溶有过量的
甲醛,无法证明是甲酸中醛基。
6.(2021·福建福州·二模)甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应
在一定条件下所得产物成分进行探究,具体过程如下。
取一定量的NaOH溶液、CuSO 溶液和甲醛于锥形瓶,控制温度40-50℃回流1h,收集到大量气体X,并
4
有红色沉淀生成。
(1)①“控制温度40-50℃”的常用加热方法是_______。
②气体X能燃烧且完全燃烧产物不会使澄清石灰水变浑浊,说明该气体是_______。
(2)在探究甲醛的氧化产物时,发现未生成 。为了进一步确定,甲醛是否被氧化为HCOONa,进行如
图实验(图中省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。
①仪器a的名称是_______。
②b中,NaOH溶液的作用是_______。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为_______。
(3)① 没有颜色,易被氧化,可由Cu O溶于氨水而得。红色沉淀用浓氨水充分浸取后未明显
2
减少,得到蓝色溶液。使溶液呈蓝色的微粒是_______。②另取1.00g红色沉淀,用适量稀盐酸、双氧水溶解完全,加热煮沸溶液4-5min,冷却后加入过量的碘化
钾溶液和淀粉指示剂,再用1.000 mol/L Na SO 溶液滴定,消耗NaSO 溶液15.50mL。因此,红色沉淀中
2 2 3 2 2 3
Cu单质的质量分数 _______(结果保留3位有效数字; ; 。)
(4)若最终测得实验中Cu单质和气体产物物质的量比为1∶1,该条件下甲醛与新制氢氧化铜发生的主要反
应化学方程式为_______。
【答案】(1) 水浴加热 H
2
(2) 分液漏斗 除去CO中混有的HCOOH蒸汽 2∶1
(3)
(4) 92.8%
【解析】取一定量的NaOH溶液、CuSO 溶液和甲醛于锥形瓶,控制温度40-50℃回流1h,收集到大量气
4
体X,气体X能燃烧且完全燃烧产物不会使澄清石灰水变浑浊,说明该气体X不是CO,为氢气;有红色
沉淀生成,根据反应中涉及的元素,红色沉淀可能是Cu O或Cu或二者的混合物,由于Cu O溶于氨水生
2 2
成 , 易被氧化生成 得到蓝色溶液,而实验中发现红色沉淀用浓氨
水充分浸取后未明显减少,得到蓝色溶液,因此红色沉淀为Cu O和Cu的混合物,据此分析解答。
2
(1)①“控制温度40-50℃”的常用加热方法是水浴加热,故答案为:水浴加热;
②结合反应中涉及的元素,能够燃烧的气体可能为氢气和CO,气体X能燃烧且完全燃烧产物不会使澄清
石灰水变浑浊,说明该气体不是CO,则X为氢气,故答案为:H;
2
(2)①根据图示,仪器a是分液漏斗,故答案为:分液漏斗;
②甲酸易挥发,生成的气体中会混有HCOOH蒸汽,因此b中NaOH溶液的作用是除去CO中混有的
HCOOH蒸汽,故答案为:除去CO中混有的HCOOH蒸汽;
③c中,银氨溶液中出现黑色沉淀,是CO将银氨溶液还原成的银单质,反应中氧化剂是 ,Ag
的化合价由+1价变成0价,还原剂是CO,C的化合价由+2价变成+4价,根据化合价升降守恒,氧化剂与
还原剂的物质的量之比为(4-2)∶(1-0)=2∶1,故答案为:2∶1;
(3)①根据反应中涉及的元素,红色沉淀可能是Cu O或Cu或二者的混合物,Cu O溶于氨水生成
2 2
,由于 没有颜色,易被氧化生成 得到蓝色溶液,故答案为:;
②1.00g红色沉淀,用适量稀盐酸、双氧水溶解完全,加热煮沸溶液4-5min,冷却后加入过量的碘化钾溶
液和淀粉指示剂,用1.000 mol/L Na SO 溶液滴定,消耗NaSO 溶液15.50mL,消耗的NaSO 的物质的
2 2 3 2 2 3 2 2 3
量为1.000 mol/L×0.01550L=0.01550mol,根据 , 有2Cu~
2Cu2+~I~2 S O ,则红色沉淀中Cu元素的物质的量=0.01550mol。设Cu O的物质的量为x,Cu的物质
2 2 2
的量为y,则144g/mol×x+64g/mol×y=1.000g,x+y=0.01550mol,解得:x=0.001mol,y=0.0145mol,则沉淀
中Cu单质的质量分数 ×100%=92.8%,故答案为:92.8%;
(4)若最终测得实验中Cu单质和氢气的物质的量比为1∶1,该条件下甲醛与新制氢氧化铜反应的化学方程
式主要为 ,故答案为:
。