文档内容
第三章 烃的衍生物
第四节 羧酸 羧酸衍生物
第1课时 羧酸
本节课学习羧酸的性质,以乙酸为代表物,了解羧酸的组成与结构,理解羧酸的化学性质及应
用。学生能够基于官能团、化学键的特点分析羧酸的化学性质,能描述和分析羧酸的重要反应,能
书写相应的化学方程式。通过实验探究乙酸、碳酸、苯酚的酸性强弱及乙酸乙酯的制备,认识反应
条件控制的重要性,了解同位素示踪法在酯化反应反应机理分析中的应用,逐渐形成科学探究与创
新意识的学科素养。
课程目标 学科素养
1. 认识羧酸的官能团与组成,能对简单羧酸 1. 宏观辨识与微观探析:基于官能团、化学键的特点
进行分类。
分析羧酸的化学性质,
2. 认识羧酸的结构特点与物理性质、化学性
2. 科学探究与创新意识:通过实验探究乙酸、碳酸、
质。
苯酚的酸性强弱及乙酸乙酯的制备,认识反应条件控制
的重要性,了解同位素示踪法在酯化反应反应机理分析
中的应用。
3. 科学态度与社会责任:通过结合生产、生活实际了
解羧酸在生活和生产中的应用。
教学重点:羧酸的结构及性质
教学难点:羧酸酸性强弱的比较,酯化反应中有机化合物的断键规律
讲义 教具
【导入新课】
[展示]乳酸和柠檬酸的结构
[过渡]
自然界的许多动植物中含有有机酸,例如,蚁酸(甲酸)、安息香酸(苯甲酸)、草酸(乙二酸)等。
有些有机酸分子中既含有羧基也含有羟基,所以又叫做羟基酸,它们既具有羟基的性质,也具有羧
基的性质。例如,乳酸、柠檬酸、苹果酸等。任务一:认识羧酸
阅读课本,完成下列问题
1. 羧酸的定义及官能团
2. 饱和一元脂肪酸的通式
3. 羧酸的分类
4. 列举生活中常见的羧酸,总结其性质及其用途。
5. 阅读表3-4,总结羧酸的物理性质及其递变规律。
【讲解】
1. 羧酸:由烃基(或氢原子)与羧基相连而构成的化合物,其官能团简式为—COOH。
2. 饱和一元脂肪酸的通式:C H O。
n 2n 2
3. 羧酸的分类
4.蚂蚁和蜜蜂分泌物中的甲酸;衣服上沾上蓝墨水可用草酸洗涤;在食品包装袋的配料表上经常出
现的食品防腐剂苯甲酸钠和山梨酸钾;以下消炎药中也含有羧酸或羧酸盐。
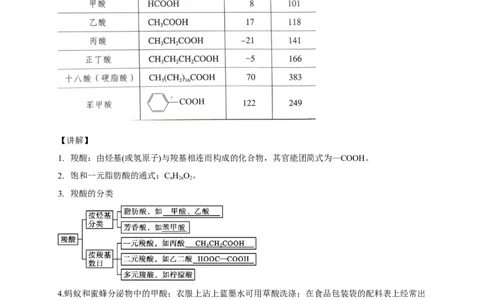
名称 甲酸 苯甲酸 乙二酸
俗称 蚁酸 安息香酸 草酸
结构简式 HCOOH无色、有刺激性气味的液 无色晶体,易升华, 无色晶体,通常含有两
物理性质 体,有腐蚀性,能与水、乙 微溶于水,易溶于乙 分子结晶水,可溶于水
醇等互溶 醇 和乙醇
既表现羧酸的性质,又表现
化学性质 表现羧酸的性质 表现羧酸的性质
醛的性质
工业上可用作还原剂,也是 用于合成香料、药物 化学分析中常用的还原
用途 合成医药、农药和染料等的 等,它的钠盐是常用 剂,也是重要的化工原
原料 的食品防腐剂 料
5.羧酸的物理性质及其递变规律
(1)甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。
(2)随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水,其沸点也逐渐
升高。
(3)高级脂肪酸是不溶于水的蜡状固体。
(4)羧酸与相对分子质量相当的其他有机化合物相比,沸点较高,这与羧酸分子间可以形成氢键有
关。
任务二:羧酸的化学性质
复习回顾:乙酸的分子式、结构式、结构简式、分子结构模型、核磁共振氢谱
探究一:羧酸的酸性
1、设计实验证明羧酸具有酸性
甲酸、苯甲酸和乙二酸的酸性
实验对象 甲酸 苯甲酸 乙二酸
① 分别取0.01 mol·L-1三种酸溶液,滴入紫色石蕊溶液
实验操作
② 分别取0.01 mol·L-1三种酸溶液,测pH
现象 ①紫色石蕊溶液变红色;②pH大于2
结论 甲酸、苯甲酸和乙二酸具有弱酸性
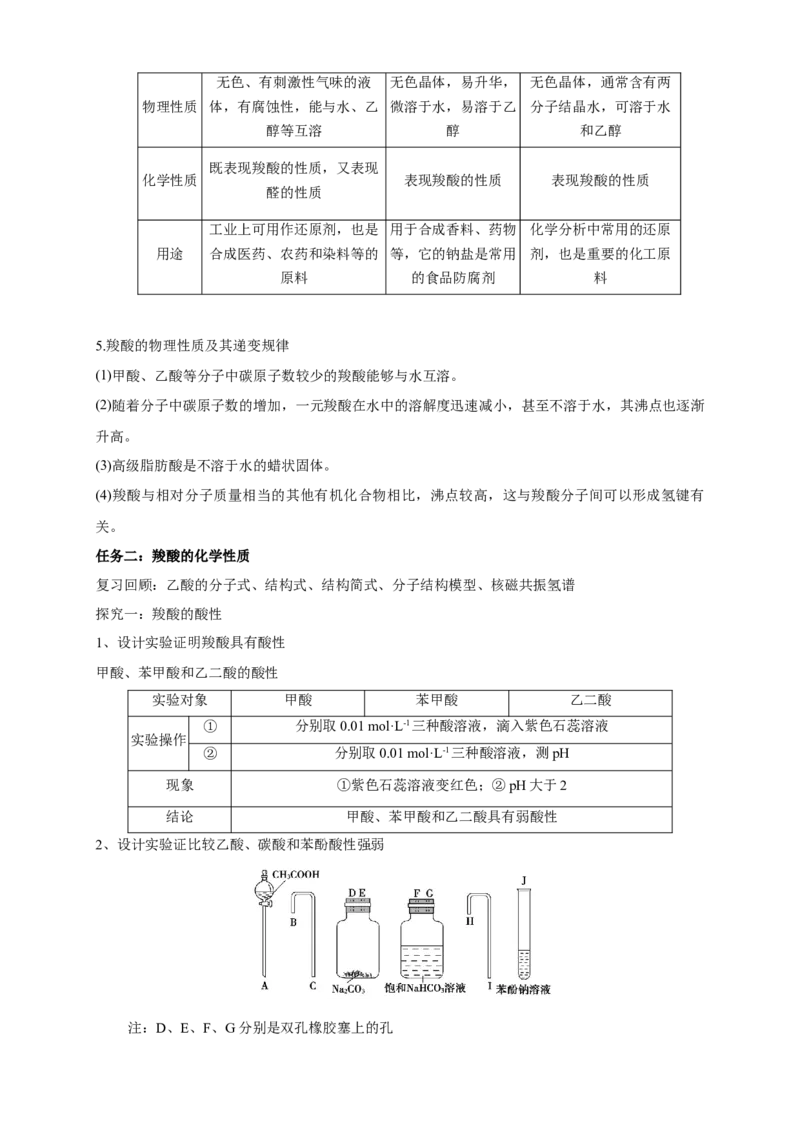
2、设计实验证比较乙酸、碳酸和苯酚酸性强弱
注:D、E、F、G分别是双孔橡胶塞上的孔[实验方案]
实验装置
实验现象 B中:有气泡产生;C中:溶液变浑浊
实验结论 结合现象,根据强酸制弱酸的规律可知,酸性:乙酸>碳酸>苯酚
[思考与讨论]
1. 上述装置中饱和NaHCO 溶液的作用是什么?可否将其撤去?
3
2. 写出各装置中反应的化学方程式。
3. 甲酸除了具有酸性,还可能有哪些化学性质?请从分子结构的角度进行分析。
4. 甲酸和乙酸的鉴别方法
[提示]
1. 饱和NaHCO 溶液的作用是除去CO 中的乙酸蒸气,防止对碳酸酸性大于苯酚的检验产生干
3 2
扰,故不能撤去。
2. 2CHCOOH+NaCO―→2CHCOONa+CO↑+HO,
3 2 3 3 2 2
探究二:酯化反应
环节一:酯化反应原理探究
[思考与讨论]
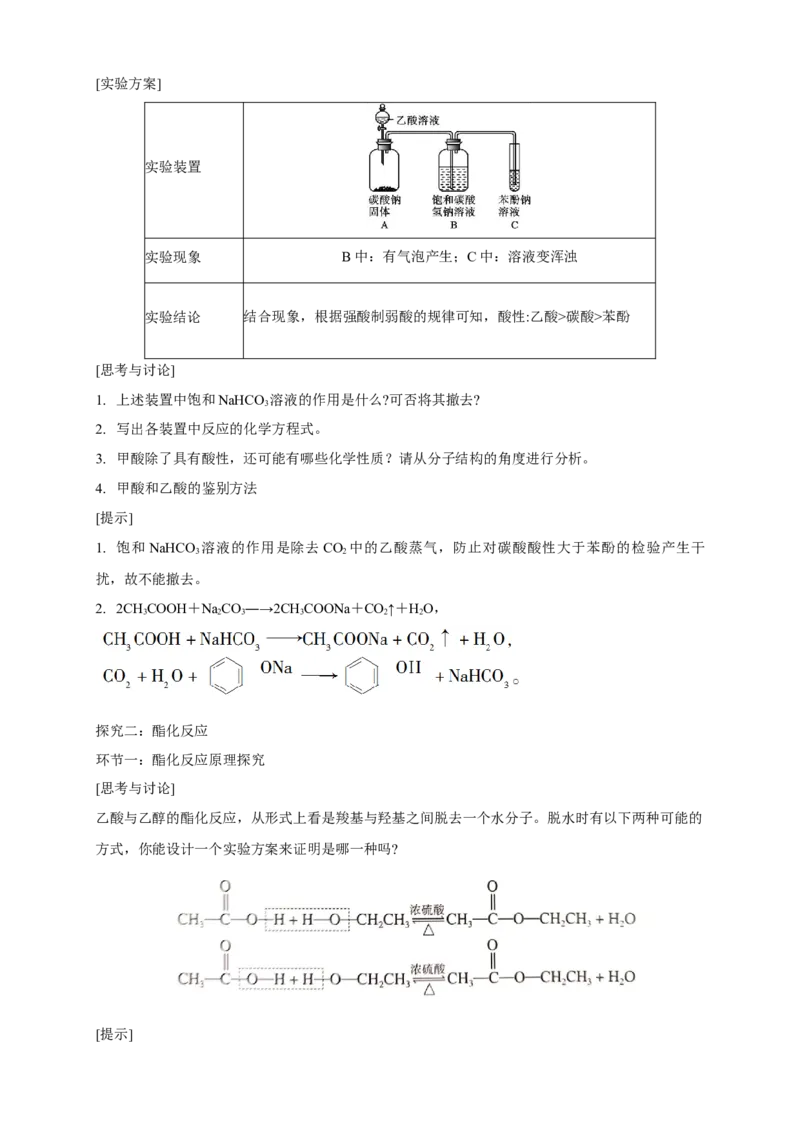
乙酸与乙醇的酯化反应,从形式上看是羧基与羟基之间脱去一个水分子。脱水时有以下两种可能的
方式,你能设计一个实验方案来证明是哪一种吗?
[提示]1. 方法:同位素示踪法是利用同位素对研究对象进行标记的微量分析方法,可以利用探测仪器随
时追踪标记的同位素在产物中的位置和数量。
2. 解释:我们可以使用同位素示踪法,证实乙酸与乙醇的酯化反应是乙酸分子中羧基的羟基与乙
醇分子中羟基的氢原子结合成水,其余部分相互结合成酯,其反应可用化学方程式表示如下:
3. 酯化反应反应规律:羧基脱—OH,醇羟基脱H。
环节二:酯化反应产率探究
[思考与讨论]
在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?请结合化学反
应原理的有关知识进行说明。
[提示]
1、浓硫酸的作用:吸水剂和催化剂,吸收生成的水,有利于平衡正向移动,提高产率。
2、加热,乙酸乙酯挥发,减少生成物的浓度,平衡正向移动,提高产率。
3、冷凝回流,提高产率。
任务三: 羧酸的化学性质探究
1、理解羧酸的化学性质取决于羧基官能团
[提示]
羧酸的化学性质主要取决于羧基官能团。由于受氧原子电负性较大等因素的影响,当羧酸发生化学
反应时,羧基结构中下面两个部位的化学键容易断裂。
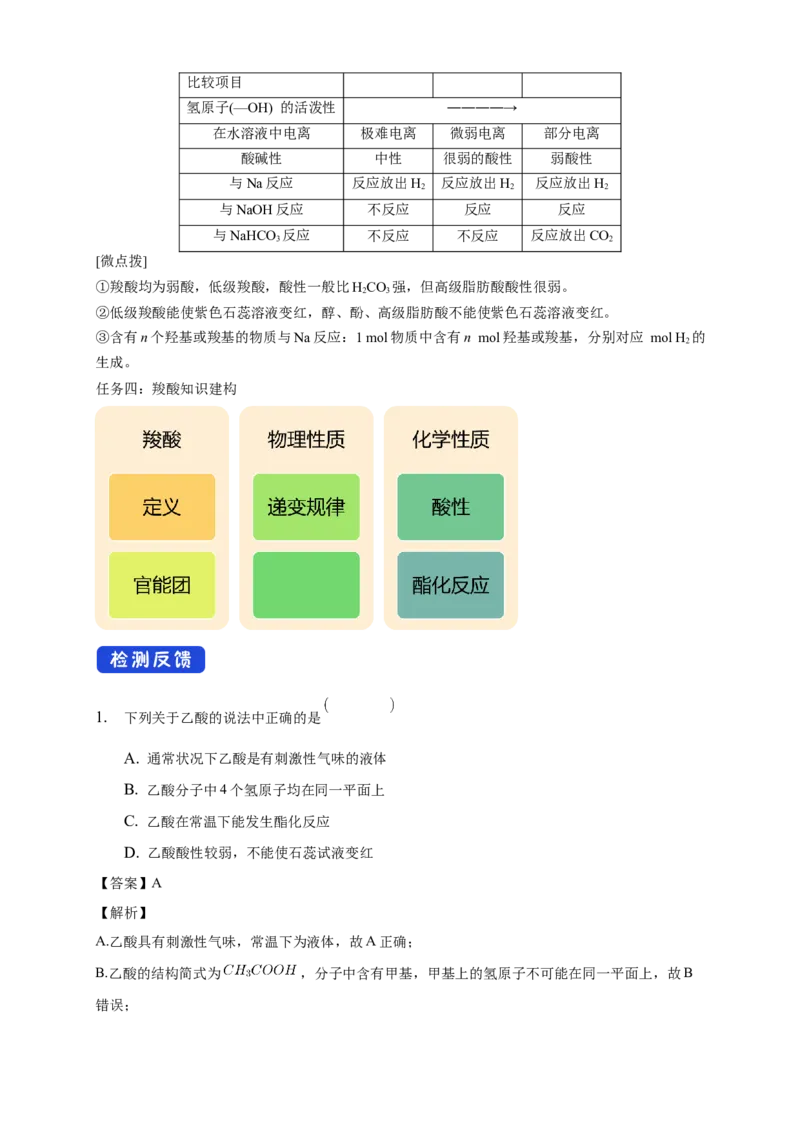
1. 羧基、酚羟基、醇羟基酸性强弱的比较
醇、酚、羧酸的结构中均有—OH,由于这些—OH所连的基团不同,—OH受相连基团的影响就不
同。故羟基上的氢原子的活泼性也就不同,表现在性质上也相差较大,其比较如下:
含—OH结构的
醇 酚 羧酸
物质比较项目
氢原子(—OH) 的活泼性 ――――→
在水溶液中电离 极难电离 微弱电离 部分电离
酸碱性 中性 很弱的酸性 弱酸性
与Na反应 反应放出H 反应放出H 反应放出H
2 2 2
与NaOH反应 不反应 反应 反应
与NaHCO 反应 不反应 不反应 反应放出CO
3 2
[微点拨]
①羧酸均为弱酸,低级羧酸,酸性一般比HCO 强,但高级脂肪酸酸性很弱。
2 3
②低级羧酸能使紫色石蕊溶液变红,醇、酚、高级脂肪酸不能使紫色石蕊溶液变红。
③含有n个羟基或羧基的物质与Na反应:1 mol物质中含有n mol羟基或羧基,分别对应 mol H 的
2
生成。
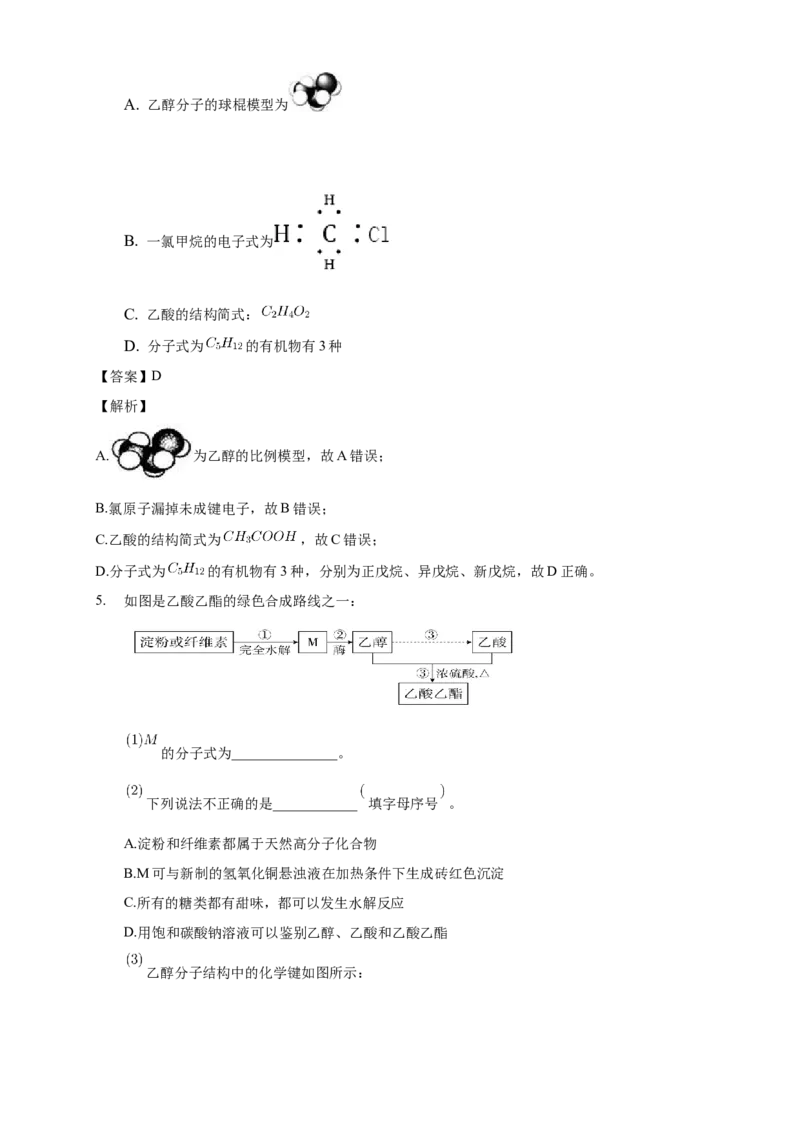
任务四:羧酸知识建构
1. 下列关于乙酸的说法中正确的是
A. 通常状况下乙酸是有刺激性气味的液体
B. 乙酸分子中4个氢原子均在同一平面上
C. 乙酸在常温下能发生酯化反应
D. 乙酸酸性较弱,不能使石蕊试液变红
【答案】A
【解析】
A.乙酸具有刺激性气味,常温下为液体,故A正确;
B.乙酸的结构简式为 ,分子中含有甲基,甲基上的氢原子不可能在同一平面上,故B
错误;C.乙酸在浓硫酸作用下加热发生酯化反应,故C错误;
D.乙酸为弱酸,但可使石蕊试液变红,故D错误。
2. 下列关于乙酸的说法不正确的是
A. 乙酸是一种重要的有机酸,且具有强烈的刺激性气味
B. 乙酸分子中含有4个H原子,所以乙酸不是一元酸
C. 无水乙酸又称冰醋酸,它是纯净物
D. 乙酸易溶于水和乙醇
【答案】B
【解析】
A.乙酸是一种重要的有机酸,是有刺激性气味的液体,故A正确;
B.化学上根据酸电离出的 数目将酸分为一元酸、二元酸和多元酸,乙酸分子中 中的氢原
子不能电离出来,含有一个 ,只能电离出1个 ,故乙酸为一元酸,故B错误;
C.无水乙酸又称冰醋酸,为一种物质,它属于纯净物,故C正确;
D.乙酸中的 能与水或乙醇形成氢键,所以乙酸易溶于水和乙醇,故D正确。
3. 酒精和醋酸是生活里的常用品,下列方法不能将二者鉴别开的是
A. 闻气味
B. 分别用来浸泡水壶中的水垢看是否溶解
C. 分别滴加NaOH溶液
D. 分别滴加紫色石蕊溶液
【答案】C
【解析】
A.酒精和醋酸气味不同,可用闻气味的方法鉴别,故A不选;
B.水垢的主要成分是 和 ,溶于醋酸但不与酒精反应,故B不选;
C.酒精和NaOH溶液不反应,醋酸和NaOH溶液反应,但无明显现象,不能鉴别,故C选;
D.醋酸使紫色石蕊试液变红,酒精不能,可鉴别,故D不选。
故选C。
4. 下列有关化学用语的表示中正确的是A. 乙醇分子的球棍模型为
B. 一氯甲烷的电子式为
C. 乙酸的结构简式:
D. 分子式为 的有机物有3种
【答案】D
【解析】
A. 为乙醇的比例模型,故A错误;
B.氯原子漏掉未成键电子,故B错误;
C.乙酸的结构简式为 ,故C错误;
D.分子式为 的有机物有3种,分别为正戊烷、异戊烷、新戊烷,故D正确。
5. 如图是乙酸乙酯的绿色合成路线之一:
的分子式为_______________。
下列说法不正确的是____________ 填字母序号 。
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜悬浊液在加热条件下生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
乙醇分子结构中的化学键如图所示:乙醇与乙酸反应时,断裂的化学键是___________ 填字母序号 ,
反应的化学方程式为__________。反应类型:_______________________
乙醇在铜作催化剂时与氧气反应,断裂的化学键是________ 填字母序号 ,反应的化学方程
式为__________,
乙醇和乙酸在一定条件下制备乙酸乙酯。
乙酸中官能团的名称是______________________ 。
生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是_______ 填
序号 。
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
乙酸乙酯和丁酸互为同分异构体,丁酸有______________________种结构。
【答案】
; 酯 化 反 应 ; ad ;羧基;
【解析】
淀粉或纤维素完全水解得到 M为葡萄糖,分子式为 ,葡萄糖在酒化酶作用下得到
, 发生氧化反应得到 , 与 发生酯
化反应得到 ;
淀粉和纤维素化学式均可表示为 ,都属于天然高分子化合物,故A正确;
B.M为葡萄糖,含有醛基,可与新制氢氧化铜悬浊液在加热条件下生成砖红色沉淀,故B正确;
C.糖类分为单糖,双塘,多糖,单糖不能发生水解反应,并不是所有的糖都有甜味,故C错误;
D.乙酸乙酯在碳酸钠溶液中分层,乙醇、乙酸均溶于碳酸钠溶液,且乙酸与碳酸钠反应生成二氧化
碳,现象各不同,可以进行鉴别,故D正确;
答案选C;
乙醇,乙酸发生酯化反应生成乙酸乙酯,酸失去羟基,醇失去羟基上的氢原子,乙醇中
间断裂,即a断裂;反应为
;反应类型为酯化反应
乙醇发生催化氧化生成乙醛,反应方程式为 ,乙醇
中 键断裂、羟基连接的碳原子中的 键断裂,即ad断裂
乙酸的结构简式为 ,官能团的名称为羧基;
单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应方向速率,故A错误;
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸,表示正逆反应速率相等,故B正确;
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应方向速率,故C错误;
D.正反应的速率与逆反应的速率相等,达到化学平衡,故D正确;
E.混合物中各物质的物质的量相等,不能表示达到平衡状态,故E错误;
答案选BD;乙酸乙酯和丁酸互为同分异构体,分子式为 ,丁酸有正丁酸和异丁酸两种结构。
本节课学习羧酸的性质,以乙酸为代表物,了解羧酸的组成与结构,理解羧酸的化学性质及应
用,培养“变化观念与平衡思想”的核心素养。学生能够基于官能团、化学键的特点分析羧酸的化
学性质,能描述和分析羧酸的重要反应,能书写相应的化学方程式,逐渐形成宏观辨识与微观探析
的学科素养。通过实验探究乙酸、碳酸、苯酚的酸性强弱及乙酸乙酯的制备,认识反应条件控制的
重要性,了解同位素示踪法在酯化反应反应机理分析中的应用,逐渐形成科学探究与创新意识的学
科素养。通过结合生产、生活实际了解羧酸在生活和生产中的应用,形成科学态度与社会责任的学
科素养。