文档内容
3.4 羧酸 羧酸的衍生物(精练)
题组一 羧酸
1.(2021·全国·高二课时练习)苯甲酸是一种重要的羧酸,以下关于苯甲酸的说法不正确的是
A.在通常条件下为无色晶体
B.苯甲酸钠水溶液的pH小于7
C.苯甲酸能与乙醇发生酯化反应
D.苯甲酸及其钠盐可用作食品防腐剂
【答案】B
【解析】A.苯甲酸为无色晶体,故A正确;
B.苯甲酸是弱酸,所以苯甲酸钠为强碱弱酸盐,呈碱性,故B错误;
C.苯甲酸中有羧基能与乙醇的羟基发生酯化反应,故C正确;
D.苯甲酸及其钠盐可用作防腐剂,在酸性环境下能抑制微生物生长,故D正确;
故选B。
2.(2022·广西钦州·高二期末)下列各组溶液,只用新制氢氧化铜悬浊液(可以加热)不能鉴别的是
A.甲酸溶液和醋酸溶液 B.甲酸钠溶液和醋酸钠溶液
C.甲酸溶液和葡萄糖溶液 D.甲酸钠溶液和乙醛溶液
【答案】D
【解析】A.甲酸分子中含有醛基、羧基,醋酸分子中只含有羧基。甲酸溶液中加入新制氢氧化铜悬浊液,
二者都会发生酸碱中和反应产生可溶性物质,看到沉淀溶液变为蓝色溶液。由于甲酸分子中含有醛基,在
加热煮沸时会产生砖红色沉淀,而醋酸分子中只有羧基,表现酸性,因此向醋酸溶液中加入新制氢氧化铜
悬浊液时,只能看到沉淀溶液变为蓝色溶液,二者实验现象不同,可以鉴别,A不符合题意;
B.甲酸钠中含有醛基,而醋酸钠中无醛基,因此向甲酸钠溶液和醋酸钠溶液中分别加入新制氢氧化铜悬
浊液并加热,前者产生砖红色沉淀,后者无明显现象,可以鉴别,B不符合题意;
C.甲酸分子中含有醛基、羧基,葡萄糖分子中含有多个羟基、醛基。向二者的水溶液中分别加入新制氢
氧化铜悬浊液,前者首先溶解,变为蓝色溶液,后者无明显现象;然后都加热煮沸,都产生砖红色沉淀,
二者的实验现象不同,可以鉴别,C不符合题意;
D.甲酸钠和乙醛中都含有醛基,向两种物质的溶液分别加入新制氢氧化铜悬浊液,无现象,再加热煮沸,
都产生砖红色沉淀,实验现象相同,不能鉴别,D符合题意;
故合理选项是D。3.(2022·河南郑州·一模)有机物M是合成药物ZJM—289的中间体,其结构简式如图所示。下列有关M
的叙述错误的是
A.分子中含有四种官能团
B.苯环上的一氯代物有2种
C.可以发生加成反应,也可以发生加聚反应
D.既能和Na反应生成H,又能和NaHCO 反应生成CO
2 3 2
【答案】B
【解析】A.分子中含有酯基,羧基,醚键,碳碳双键四种官能团,A正确;
B.苯环上有三种不化学环境的氢,所以的苯环上一氯代物也有3种,B错误;
C.分子中碳碳双键可以发生加成反应,也可以发生加聚反应,C正确;
D.分子中羧基既能和Na反应生成H,又能和NaHCO 反应生成CO,D正确;
2 3 2
故选B。
4.(2022·湖北·十堰市教育科学研究院高二期末)苹果酸(α-羟基丁二酸)是苹果醋饮料的主要酸性物质,
苹果酸的结构如下图所示,下列相关说法不正确的是
A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.苹果酸在一定条件下能反应生成环酯
D.1 mol苹果酸与足量NaCO 溶液反应生成2 mol CO
2 3 2
【答案】D
【解析】A.苹果酸分子中含有羧基、羟基,因此在一定条件下可以发生酯化反应,A正确;
B.在苹果酸分子中由于羟基连接的C原子上含有H原子,因此在一定条件下能发生催化氧化反应,形成
羰基,B正确;
C.苹果酸分子中含有羧基、羟基,因此在一定条件下可以发生分子内的酯化反应,形成环酯和水,酯化
反应发生时脱水方式为:酸脱羟基醇脱氢,C正确;D.只有羧基能够与NaCO 发生反应,由于反应时物质的量关系为2-COOH~CO ,苹果酸分子中只有1个
2 3 2
羧基,所以1 mol苹果酸与足量NaCO 溶液反应生成0.5 mol CO ,D错误;
2 3 2
故合理选项是D。
5.(2021·黑龙江·铁人中学高二期末)有机物M的结构简式如下。下列说法错误的是
A.M的分子式为C H O
10 12 3
B.M分子中所有碳原子可能共平面
C.M分子可发生酯化反应生成环状酯
D.1molM与足量金属钠反应可生成2mol氢气
【答案】D
【解析】A.通过M的结构简式可知M的分子式为C H O,A正确;
10 12 3
B.与苯环直接相连的碳和苯环在同一个平面上,苯环左边的碳链可以通过旋转碳碳单键,而使所有的碳
在同一个平面上,B正确;
C.M分子中含有羟基和羧基,则M分子可发生酯化反应生成环状酯,C正确;
D.M中的羟基和羧基可以和钠反应生成氢气,则1molM与足量金属钠反应可生成1mol氢气,D错误;
故选D。
6.(2021·内蒙古·北京八中乌兰察布分校高二阶段练习)某有机物的结构如图所示,该有机物可能具有的
性质是
①能使酸性KMnO 溶液褪色;②能跟NaHCO 溶液反应;③能发生酯化反应;④能发生消去反应;⑤能发
4 3
生水解反应
A.①②③ B.②⑤ C.②④⑤ D.①②③④
【答案】A
【解析】①含双键、-OH,能使酸性KMnO 溶液褪色,故正确;
4
②含-COOH,具有酸性,可与碳酸氢钠溶液反应,故正确;
③含-OH、-COOH,能发生酯化反应,故正确;④羟基邻位无氢原子,不能发生消去反应,故错误;
⑤不含能水解的官能团,不能发生水解反应,故错误;
故选:A。
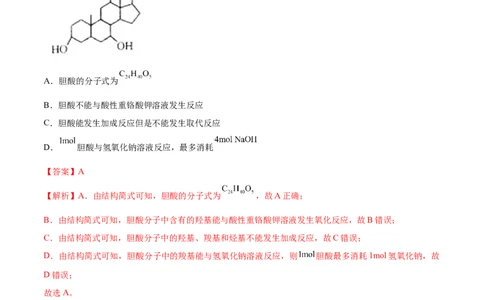
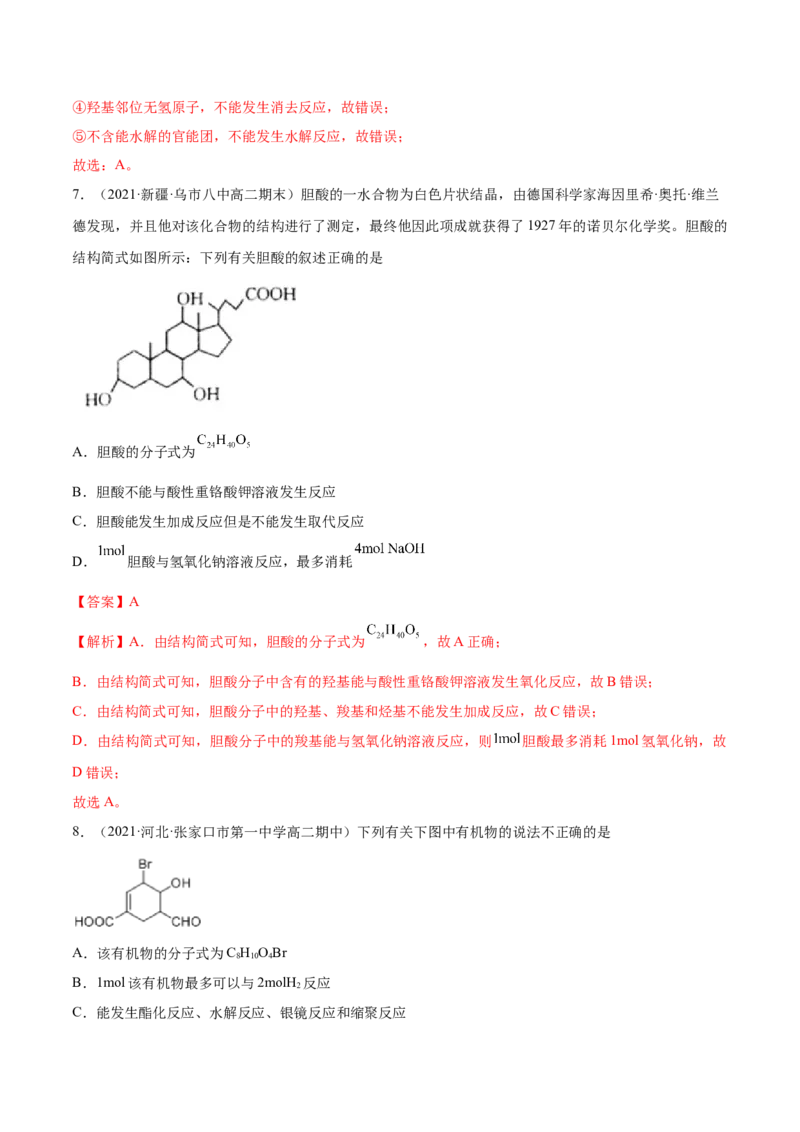
7.(2021·新疆·乌市八中高二期末)胆酸的一水合物为白色片状结晶,由德国科学家海因里希·奥托·维兰
德发现,并且他对该化合物的结构进行了测定,最终他因此项成就获得了1927年的诺贝尔化学奖。胆酸的
结构简式如图所示:下列有关胆酸的叙述正确的是
A.胆酸的分子式为
B.胆酸不能与酸性重铬酸钾溶液发生反应
C.胆酸能发生加成反应但是不能发生取代反应
D. 胆酸与氢氧化钠溶液反应,最多消耗
【答案】A
【解析】A.由结构简式可知,胆酸的分子式为 ,故A正确;
B.由结构简式可知,胆酸分子中含有的羟基能与酸性重铬酸钾溶液发生氧化反应,故B错误;
C.由结构简式可知,胆酸分子中的羟基、羧基和烃基不能发生加成反应,故C错误;
D.由结构简式可知,胆酸分子中的羧基能与氢氧化钠溶液反应,则 胆酸最多消耗1mol氢氧化钠,故
D错误;
故选A。
8.(2021·河北·张家口市第一中学高二期中)下列有关下图中有机物的说法不正确的是
A.该有机物的分子式为C H OBr
8 10 4
B.1mol该有机物最多可以与2molH 反应
2
C.能发生酯化反应、水解反应、银镜反应和缩聚反应D.1mol该有机物与NaOH溶液反应时,最多消耗2molNaOH
【答案】A
【解析】A.根据有机物的结构可知,该有机物的分子式为C HOBr,A错误;
8 9 4
B.该物质中碳碳双键和醛基能与H 发生加成反应,故1mol该有机物最多可以与2molH 反应,B正确;
2 2
C.该物质中羟基和羧基能发生酯化反应,碳卤键能发生水解反应,醛基能发生银镜反应,碳碳双键能发
生缩聚反应,C正确;
D.该物质中羧基能与NaOH发生中和反应,碳卤键能与NaOH发生水解反应,故1mol该有机物与NaOH
溶液反应时,最多消耗2molNaOH,D正确;
故选A。
题组二 乙酸
1.(2021·云南·盐津县第一中学高一阶段练习)下列有关乙酸的叙述错误的是
A.是一种生活中常见的烃的衍生物
B.分子中含有4个氢原子,它是四元有机酸
C.分子中含有1个羧基,它是一元有机羧酸
D.分子中含有碳氧双键,不能使溴水褪色
【答案】B
【解析】A.烃是只含C、H元素的有机化合物,乙酸除了含C、H元素还有O元素,属于烃的衍生物,故
A正确;
B.只有羧基上的氢原子可以电离,是一元酸,故B错误;
C.分子中含有1个羧基,只有羧基上的氢原子可以电离,属于一元酸,故C正确;
D.分子中含有碳氧双键,但不能与溴水加成,所以不能使溴水褪色,故D正确;
故答案为B。
2.(2022·重庆)下图是某市售乙酸试剂瓶标签上的部分数据。则该乙酸的物质的量浓度为
乙酸
化学式: 相对分子质量:60
密度: 溶质的质量分数:36%
A.6.12mol/L B.10.2mol/L C.3.06mol/L D.3.6mol/L
【答案】A
【解析】 ,答案选A。
3.(2022·辽宁辽阳·高二期末)乙酸是一种一元有机弱酸,为食醋的主要成分。下列实验事实不能证明乙酸是弱酸的是
A.乙酸钠溶液显碱性
B.等体积、等 的盐酸和乙酸溶液分别与同样大小的锌粒反应,最初产生氢气的速率相等
C.常温下,测得 的乙酸溶液的
D.相同条件下,等浓度的盐酸和乙酸溶液的导电性:盐酸>乙酸溶液
【答案】B
【解析】A. 乙酸钠溶液显碱性,则乙酸钠为强碱弱酸盐,能说明乙酸是弱酸,A不选;
B. 等体积、等 的盐酸和乙酸溶液分别与同样大小的锌粒反应,因氢离子浓度相同,因此最初产生氢
气的速率相等,不能说明乙酸是弱酸,B选;
C. 常温下,测得 的乙酸溶液的 ,氢离子浓度为 ,乙酸不完全电
离,能说明乙酸是弱酸,C不选;
D. 相同条件下,等浓度的盐酸和乙酸溶液的导电性:盐酸>乙酸溶液,自由离子浓度盐酸>乙酸溶液,乙
酸不完全电离,能说明乙酸是弱酸,D不选;
答案选B。
4.(2022·云南·高二学业考试)下列物质中能用来鉴别乙醇和乙酸的是
A.碳酸钠溶液 B.氯化钠溶液
C.氢氧化钠溶液 D.葡萄糖溶液
【答案】A
【解析】A.碳酸钠溶液和乙醇不反应、和乙酸生成二氧化碳气体,可以鉴别,A正确;
B.氯化钠溶液和乙醇不反应、和乙酸不反应,B错误;
C.氢氧化钠溶液和乙醇不反应、和乙酸反应无明显现象,C错误;
D.葡萄糖溶液和乙醇不反应、和乙酸不反应,D错误;
故选A。
5.(2022·甘肃靖远·高二期末)乙酸是一种一元有机弱酸,为食醋的主要成分。下列实验事实不能证明乙
酸是弱酸的是
A.等体积、等pH的盐酸和乙酸溶液分别与同样大小的锌粒反应,最初产生氢气的速率相等
B.相同条件下,等浓度的盐酸和乙酸溶液的导电性:盐酸>乙酸溶液
C.常温下,测得0.01mol/L的乙酸溶液的D.乙酸钠溶液显碱性
【答案】A
【解析】A.等pH的盐酸和乙酸溶液起始氢离子浓度相同,与锌粒反应产生氢气的速率相等,到不能说明
乙酸是弱酸,故A符合题意;
B.相同条件下等浓度的盐酸和乙酸导电能力盐酸大于乙酸,可说明盐酸中离子浓度大于乙酸,可知乙酸
不能完全电离,属于弱酸,故B不符合题意;
C.常温下,测得0.01mol/L的乙酸溶液的 ,可知乙酸溶液中氢离子浓度小于溶质浓度,可知乙酸不
能完全电离,其属于弱酸,故C不符合题意;
D.乙酸钠溶液显碱性,可知能发生水解,为强碱弱酸盐,乙酸为弱酸,故D不符合题意;
故选:A。
6.(2022·江苏省前黄高级中学高二学业考试)下列关于乙醇和乙酸的说法中,正确的是
A.乙醇和乙酸分子所含官能团相同
B.乙酸和钠发生置换反应,乙醇与钠不反应
C.乙醇和乙酸均能使紫色石蕊试液变红
D.乙醇和乙酸在一定条件下能发生酯化反应
【答案】D
【解析】A.乙醇中官能团为羟基,乙酸中官能团为羧基,A错误;
B.乙酸、乙醇均能与Na反应,且均属于置换反应,B错误;
C.乙酸有酸性,能使紫色石蕊变红,乙醇呈中性,不能使石蕊变红,C错误;
D.乙酸与乙醇在浓硫酸加热条件下能发生酯化反应,生成乙酸乙酯,D正确;
故答案选D。
7.(2022·山东·日照青山学校高三阶段练习)现有乙酸蒸气与氧气(足量)的混合气体11.0g,当乙酸完全燃
烧后的产物被足量过氧化钠固体吸收时,固体质量增加了3.0g。下列说法错误的是
A.乙酸完全燃烧的产物均属于非极性分子
B.乙酸完全燃烧时,分子中的C-H键完全断裂
C.混合气体中乙酸的质量为3.0g
D.混合气体的平均相对分子质量约为36.7
【答案】A
【解析】A.乙酸完全燃烧的产物是CO 和HO,HO为V型结构,属于非极性分子,CO 结构式为
2 2 2 2
O=C=O,为直线形,结构对称,正负电荷重心重合,为非极性分子,故A错误;
B.乙酸完全燃烧时生成CO 和HO,,分子中的C-H键完全断裂生成C=O键和O-H键,故B正确;
2 2C.乙酸分子式C HO 改写为(CO) (H ),则固体质量增加了3.0g为乙酸质量,故C正确;
2 4 2 2 2 2
D.3.0g为乙酸质量,其物质的量为 ,11.0g-3.0g=8.0g为氧气的质量,其物质的
量为 ,混合气体的摩尔质量 ,而平均相对分
子质量在数值上等于摩尔质量,故混合气体的平均相对分子质量为36.7,故D正确;
故选:A。
题组三 乙酸乙酯
1.(2022·山东枣庄·高三期末)某同学在实验室制备乙酸乙酯,操作如下:检查气密性后,在试管中按比
例依次加入浓硫酸、乙醇、乙酸,连接好装置后,用酒精灯小心均匀的加热试管,将产生的气体通到饱和
溶液的液面下。实验中存在的错误有几处?
A.2 B.3 C.4 D.15
【答案】B
【解析】实验室制备乙酸乙酯,操作如下:检查气密性后,在试管中先加入乙醇,再加浓硫酸,最后加乙
酸,连接好装置后,试管中加入碎瓷片,用酒精灯小心均匀的加热试管,将产生的气体通到饱和
溶液的液面上,所以上述实验中共存在3处错误,答案选B。
2.(2021·全国·高三专题练习)乙酸与乙醇的酯化反应。某同学设计了甲、乙两套实验装置,对乙酸与乙
醇进行了酯化反应的研究:
(1)乙酸和乙醇(CHCHOH)发生酯化反应的化学方程式为___________。
3 2
(2)实验过程中选用的药品及试剂有:浓HSO 、乙醇、乙酸还有___________、___________两种必备用品。
2 4
(3)某同学用装有饱和氢氧化钠溶液的三颈瓶接收乙酸乙酯,几乎没有收集到产物,请给予合理的解释:
___________。【答案】(1)CH COOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(2)沸石 饱和NaCO 溶液
2 3
(3)NaOH溶液的碱性较强,乙酸乙酯在NaOH溶液中发生水解
【解析】
(1)乙酸和乙醇(CHCHOH)发生酯化反应生成乙酸乙酯(CHCOOCH CH)和水,反应的化学方程式为
3 2 3 2 3
CHCOOH+CH CHOH CHCOOCH CH+H O。
3 3 2 3 2 3 2
(2)实验过程中为防止液体暴沸,还需加入沸石,同时需用饱和NaCO 溶液吸收乙醇,中和乙酸,降低乙
2 3
酸乙酯的溶解度。
(3)用装有饱和氢氧化钠溶液的三颈瓶接收乙酸乙酯,由于NaOH溶液的碱性较强,乙酸乙酯在NaOH溶液
中发生水解,因此几乎没有收集到产物。
3.(2021·内蒙古·北京八中乌兰察布分校高二阶段练习)红葡萄酒密封储存时间越长,质量越好,原因之
一是储存过程中生成了有香味的酯。在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题。
(1)试管a中加入几块碎瓷片的目的是:___________。
(2)浓硫酸的作用是:___________。
(3)若加的是C H18OH写出制乙酸乙酯的方程式:___________。
2 5
(4)试管b中加入饱和碳酸钠的作用是:
①___________ ;
②___________ ;
③___________ 。
(5)试剂加入的先后顺序:___________、 ___________、 ___________。
【答案】(1)防止暴沸
(2)催化剂和吸水剂
(3)
(4)吸收乙酸 溶解乙醇 降低乙酸乙酯在水中的溶解度(5)乙醇 浓硫酸 乙酸
【解析】(1)试管a中加入几块碎瓷片的目的是防止暴沸;
(2)浓硫酸的作用是催化剂和吸水剂;
(3)酯化反应中酸脱羟基、醇脱氢,C H18OH与乙酸反应得到乙酸乙酯,标记氧在酯中,反应的方程式:
2 5
;
(4)饱和碳酸钠溶液的作用为中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分层;
(5)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸,故答案
为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加乙酸。
4.(2021·陕西·长安一中高二阶段练习)某化学小组采用类似制乙酸乙酯的装置(如图1所示),用环己醇
制备环己烯。
已知: +H O
2
相对分子质量 密度/g•cm-3 熔点/℃ 沸点/℃ 溶解性
环己醇 100 0.96 25 161 能溶于水
环己烯 82 0.81 ﹣103 83 难溶于水
(1)制备粗品
将12.5mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得
到环己烯粗品。
①在试管中混合环己醇和浓硫酸操作时,加入药品的先后顺序为___________。
②导管B除了导气外还具有的作用是___________。
③将试管C置于冰水中的目的是___________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在___________层(填“上”或“下”),分液后用___________(填字母)洗涤。
a.酸性KMnO 溶液 b.稀硫酸 c.Na CO 溶液
4 2 3
②再将提纯后的环己烯按如图2所示装置进行蒸馏。图中仪器a的名称是___________。蒸馏时要加入生石
灰,目的是___________。收集产品时,控制的温度应在___________左右。
(3)本实验所得到的环己烯质量为6.25g,则产率是___________。
【答案】(1) 先加入环己醇,再加入浓硫酸 冷凝 防止环己烯挥发
(2)上 C 蒸馏烧瓶 吸收剩余的水 83℃
(3)63.5%
【解析】(1)混合环己醇和浓硫酸时,因为浓硫酸密度较大,应向环己醇中加入浓硫酸,故填先加入环己醇,
再加入浓硫酸;
②长导管B除了可以导气以外,还可以起到冷凝的作用,故填冷凝;
③乙烯的沸点较低,相反其液化点也低,冰水可以使其快速液化,防止挥发,故填防止环己烯挥发;
(2) ①环己烯密度小于水,且不溶于水,与水溶液混合时在上层;为了出去其中的酸性物质,可以用碱性
溶液,如碳酸钠溶液,故填上、c;
②如图2为蒸馏装置,仪器a为蒸馏烧瓶;蒸馏时加入生石灰是为了除了有机物中含有的少量水;如表所
示,环己烯产品的沸点为83℃,蒸馏时,控制温度在83℃即可,故填蒸馏烧瓶、吸收剩余的水、83℃;
(3)实验所用环己醇为12.5mL,其密度为0.96 ,根据 可计算其质量为 。设环
己烯的理论产量为xg,根据反应,可得 ,解得x=9.84g,则环己烯的产率为
63.5%。故填63.5%。
5.(2021·全国·高三专题练习)为探究乙酸乙酯的实验室制备方法,某实验小组设计主要步骤如下:
①在大试管A中配制反应混合液;②按图甲所示连接装置(装置气密性良好),用小火均匀加热大试管
;③待试管B(内装滴有酚酞的饱和碳酸钠溶液)收集到一定量产物后停止加热,撤去导管并用
力振荡,然后静置待分层;④分离出乙酸乙酯层,洗涤、干燥.乙醇可与氯化钙反应,生成微溶于水的 .有关试剂部分数据如下:
物质 熔点/ 沸点/ 密度/( )
乙醇 78.5 0.789
乙酸 16.6 117.9 1.05
乙酸乙酯 77.5 0.90
浓硫酸( ) — 338.0 1.84
(1)配制反应混合液的主要操作步骤为___________________(不必指出液体体积);写出制取乙酸乙酯的化学
方程式____________________________.
(2)步骤②必须小火均匀加热,一个主要原因是温度过高会发生副反应,另一个原因是
___________________.
(3)写出步骤③中观察到的实验现象____________________.
(4)分离出乙酸乙酯层后,一般用饱和 溶液洗涤.通过洗涤可除去的杂质是____________________(填
名称);干燥乙酸乙酯最适宜的干燥剂为____________ (填字母).
a. b.无水硫酸钠 c.碱石灰 d. 固体
(5)某化学课外小组设计了图乙所示的装置(图中铁架台,铁夹,加热装置均已略去)制取乙酸乙酯,与图甲
装置相比,图乙装置的主要优点有______________.
a.增加了温度计,有利于控制反应温度 b.增加了分液漏斗,能随时补充反应混合液
c.增加了冷凝装置,有利于收集产物 d.反应容器容积大,容纳反应物的量多
【答案】(1)在大试管A中加入乙醇,再分别慢慢加入浓硫酸和乙酸,边加边振荡试管使之混合均匀(2)反应物中乙醇、乙酸的沸点较低,若用大火加热,大量反应物会随产物蒸发而损失
(3)试管B中的液体分为上下两层,上层为无色油状液体,可闻到水果香味,下层为红色液体,振荡后颜色
变浅,有气泡产生
(4)乙醇 b
(5)abc
【解析】(1)配制反应混合液的主要操作步骤为在大试管A中加入乙醇,再分别慢慢加入浓硫酸和乙酸,边
加边振荡试管使之混合均匀(不必指出液体体积);乙醇与乙酸在浓硫酸作用下加热制取乙酸乙酯的化学方
程式 .故答案为:在大试管A中加入乙醇,再分别慢慢
加入浓硫酸和乙酸,边加边振荡试管使之混合均匀; ;
(2)步骤②必须小火均匀加热,一个主要原因是温度过高会发生副反应,另一个原因是反应物中乙醇、乙酸
的沸点较低,若用大火加热,大量反应物会随产物蒸发而损失.故答案为:反应物中乙醇、乙酸的沸点较
低,若用大火加热,大量反应物会随产物蒸发而损失;
(3)步骤③中观察到的实验现象试管B中的液体分为上下两层,上层为无色油状液体,可闻到水果香味,下
层为红色液体,振荡后颜色变浅,有气泡产生.故答案为:试管B中的液体分为上下两层,上层为无色油
状液体,可闻到水果香味,下层为红色液体,振荡后颜色变浅,有气泡产生;
(4)分离出乙酸乙酯层后,一般用饱和 溶液洗涤,乙醇可与氯化钙反应,生成微溶于水的
,通过洗涤可除去的杂质是乙醇(填名称);干燥乙酸乙酯最适宜的干燥剂为a. 与水
反应生成酸催化酯水解,故不符;b.无水硫酸钠与水生成硫酸钠晶体,故符合; c.碱石灰促进酯水解,
故不符;d. 固体促进酯水解,故不符;故选b;故答案为:乙醇;b;
(5)与图甲装置相比,图乙装置的主要优点有a.增加了温度计,有利于控制反应温度,减少副反应的发生,
故符合; b.增加了分液漏斗,能随时补充反应混合液,促进平衡正向移动,故符合;c.增加了冷凝
装置,更快地冷凝液体,有利于收集产物,故符合;d.题中没有指出反应容器的大小,故不符;故答案
为:abc。
6.(2021·湖南·模拟预测)下面为甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙
酸乙酯的实验过程。
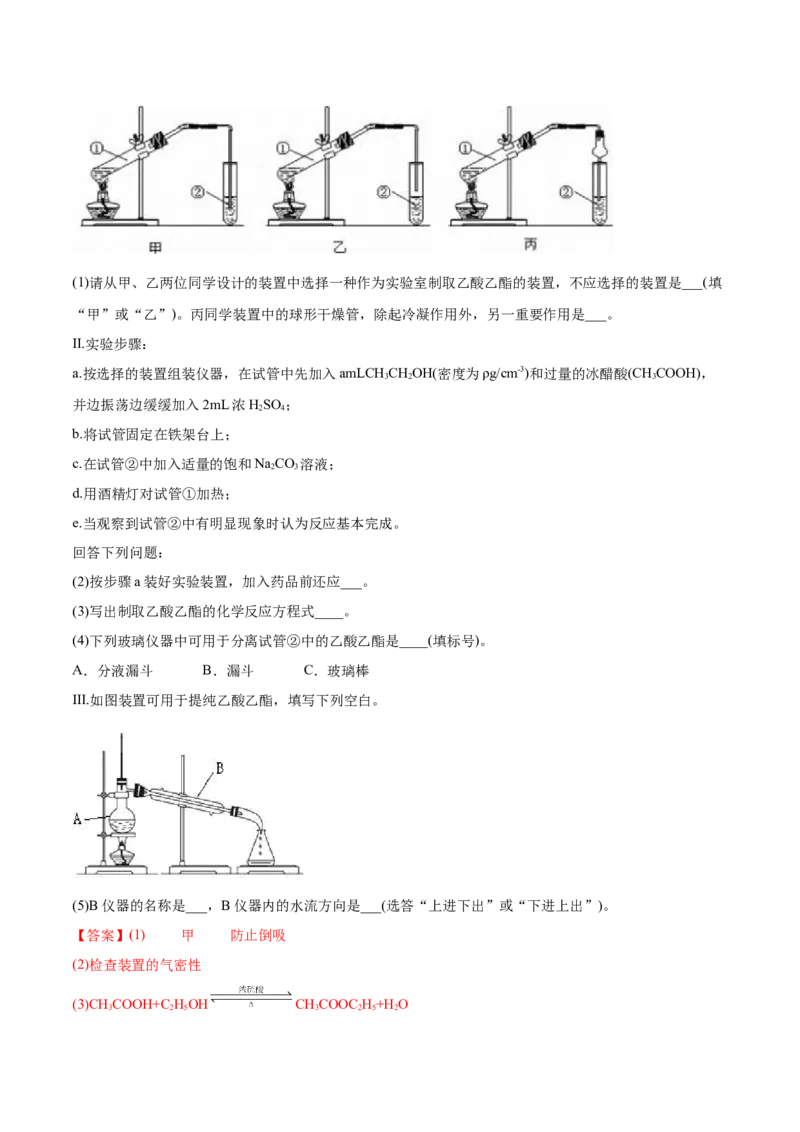
Ⅰ.装置设计:甲、乙、丙三位同学分别设计了下列三套实验装置:(1)请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,不应选择的装置是___(填
“甲”或“乙”)。丙同学装置中的球形干燥管,除起冷凝作用外,另一重要作用是___。
Ⅱ.实验步骤:
a.按选择的装置组装仪器,在试管中先加入amLCH CHOH(密度为ρg/cm-3)和过量的冰醋酸(CHCOOH),
3 2 3
并边振荡边缓缓加入2mL浓HSO ;
2 4
b.将试管固定在铁架台上;
c.在试管②中加入适量的饱和NaCO 溶液;
2 3
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象时认为反应基本完成。
回答下列问题:
(2)按步骤a装好实验装置,加入药品前还应___。
(3)写出制取乙酸乙酯的化学反应方程式____。
(4)下列玻璃仪器中可用于分离试管②中的乙酸乙酯是____(填标号)。
A.分液漏斗 B.漏斗 C.玻璃棒
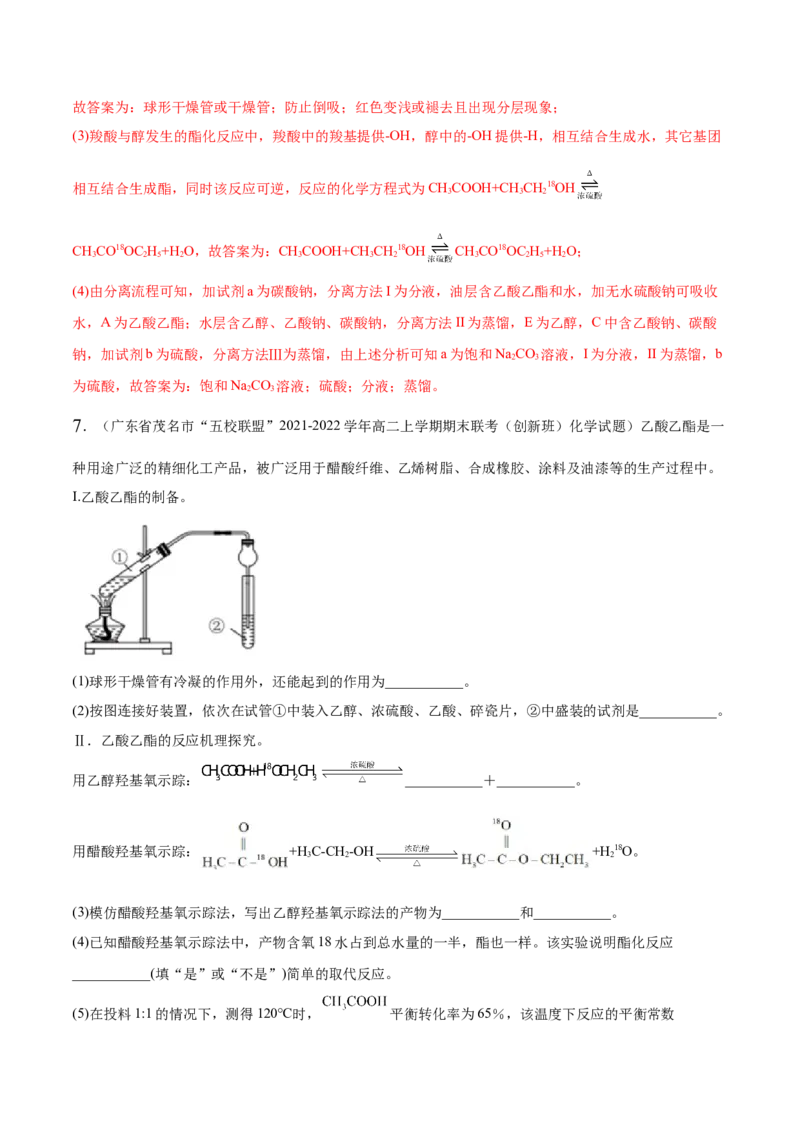
Ⅲ.如图装置可用于提纯乙酸乙酯,填写下列空白。
(5)B仪器的名称是___,B仪器内的水流方向是___(选答“上进下出”或“下进上出”)。
【答案】(1) 甲 防止倒吸
(2)检查装置的气密性
(3)CH COOH+C HOH CHCOOC H+H O
3 2 5 3 2 5 2(4)A
(5)直型冷凝管(或冷凝管) 下进上出
【解析】(1)实验室制取乙酸乙酯的反应物是乙酸和乙醇,乙酸和乙醇易挥发,乙酸和乙醇溶于水时易倒吸,
装置中②导管不插入液面下,而甲装置中②试管中导管在液面下,易发生倒吸,则不合理,丙同学装置中
的球形干燥管,除起冷凝作用外,另一重要作用是防止倒吸;答案为甲;防止倒吸。
(2)该实验中乙醇、乙酸易挥发,装置不能漏气,则步骤a装好实验装置,加入样品前还应检查装置的气密
性;答案为检查装置的气密性。
(3)乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,化学方程式为CHCOOH+C HOH
3 2 5
CHCOOC H+H O;答案为CHCOOH+C HOH CHCOOC H+H O。
3 2 5 2 3 2 5 3 2 5 2
(4)乙酸乙酯不溶于饱和碳酸钠溶液,混合液会分层,分离可通过分液操作分离出乙酸乙酯,即选用分液漏
斗进行分液,A选项符合题意;答案为A。
(5)由题中图示装置 可知,B仪器的名称是直型冷凝管(或冷凝管),蒸
馏操作中,冷凝管采用逆向通水,即下进上出通水,冷凝效果较好;答案为直型冷凝管(或冷凝管);下进
上出。
6.(2021·河北·任丘市第一中学高二开学考试)某课外小组设计的实验室制取乙酸乙酯的装置如图1:
已知:A中放有浓硫酸;B中放有乙醇、乙酸;D中放有饱和碳酸钠溶液。
有关有机物的沸点如表:
试剂 乙醚 乙醇 乙酸 乙酸乙酯
沸点/℃ 34.7 78.5 118 77.1请回答:
(1)浓硫酸的作用:____。
(2)仪器C的名称是___,其作用有冷凝乙酸乙酯和___,若反应前向D中加入几滴酚酞,溶液呈红色。实验
完毕后,将烧杯D中的溶液充分振荡、静置,现象为___。
(3)若用同位素18O标记乙醇中的氧原子以确定反应产物水分子中氧原子的提供者,写出能表示18O位置的
化学方程式:___。
(4)现拟分离含少量乙醇和乙酸的乙酸乙酯粗产品,如图2是分离操作步骤流程图:
则试剂a是___,试剂b是___,分离方法Ⅰ是___,分离方法Ⅱ是___。
【答案】(1)催化剂和吸水剂
(2)球形干燥管或干燥管 防止倒吸 红色变浅或褪去且出现分层现象
(3)CH COOH+CH CH18OH CHCO18OC H+H O
3 3 2 3 2 5 2
(4)饱和NaCO 溶液 硫酸 分液 蒸馏
2 3
【解析】(1)乙酸与乙醇发生酯化反应,该反应为可逆反应,需浓硫酸作催化剂,浓硫酸吸水利于平衡向生
成乙酸乙酯方向移动,故浓硫酸的作用为催化剂、吸水剂,增加乙醇的量平衡正向移动,提高乙酸的转化
率,故答案为:催化剂和吸水剂;
(2)仪器C具有球形特征,为球形干燥管或干燥管,乙酸、乙醇易溶于碳酸钠溶液,会导致装置内气体减小,
容易发生倒吸,球形干燥管的管口伸入液面下可能发生倒吸,但球形干燥管体积大,可冷凝乙酸乙酯,也
可以防止倒吸,碳酸钠为强碱弱酸盐,水解生成碳酸氢根离子和氢氧根离子,离子方程式: +H O
2
+OH-;碳酸钠溶液显碱性,遇到酚酞变红,实验完毕后,将烧杯D中的溶液充分振荡、静止,乙酸
和碳酸钠反应而使溶液红色变浅,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油
体液体,故答案为:球形干燥管或干燥管;防止倒吸;红色变浅或褪去且出现分层现象;
(3)羧酸与醇发生的酯化反应中,羧酸中的羧基提供-OH,醇中的-OH提供-H,相互结合生成水,其它基团
相互结合生成酯,同时该反应可逆,反应的化学方程式为CHCOOH+CH CH18OH
3 3 2
CHCO18OC H+H O,故答案为:CHCOOH+CH CH18OH CHCO18OC H+H O;
3 2 5 2 3 3 2 3 2 5 2
(4)由分离流程可知,加试剂a为碳酸钠,分离方法I为分液,油层含乙酸乙酯和水,加无水硫酸钠可吸收
水,A为乙酸乙酯;水层含乙醇、乙酸钠、碳酸钠,分离方法II为蒸馏,E为乙醇,C中含乙酸钠、碳酸
钠,加试剂b为硫酸,分离方法Ⅲ为蒸馏,由上述分析可知a为饱和NaCO 溶液,I为分液,II为蒸馏,b
2 3
为硫酸,故答案为:饱和NaCO 溶液;硫酸;分液;蒸馏。
2 3
7.(广东省茂名市“五校联盟”2021-2022学年高二上学期期末联考(创新班)化学试题)乙酸乙酯是一
种用途广泛的精细化工产品,被广泛用于醋酸纤维、乙烯树脂、合成橡胶、涂料及油漆等的生产过程中。
Ⅰ.乙酸乙酯的制备。
(1)球形干燥管有冷凝的作用外,还能起到的作用为___________。
(2)按图连接好装置,依次在试管①中装入乙醇、浓硫酸、乙酸、碎瓷片,②中盛装的试剂是___________。
Ⅱ.乙酸乙酯的反应机理探究。
用乙醇羟基氧示踪: ___________+___________。
用醋酸羟基氧示踪: +H C-CH-OH +H 18O。
3 2 2
(3)模仿醋酸羟基氧示踪法,写出乙醇羟基氧示踪法的产物为___________和___________。
(4)已知醋酸羟基氧示踪法中,产物含氧18水占到总水量的一半,酯也一样。该实验说明酯化反应
___________(填“是”或“不是”)简单的取代反应。
(5)在投料1:1的情况下,测得120℃时, 平衡转化率为65%,该温度下反应的平衡常数K=___________。(保留三位有效数字)
Ⅲ.乙酸乙酯的催化水解(酯化反应的逆反应)探究。
已知:①乙酸乙酯的沸点约77℃;
②酸和碱均可用作酯水解的催化剂。
实验步骤:向试管中加入 溶液,再加入2mL乙酸乙酯,量出乙酸乙酯的高度。再把试管放入
70℃的水浴中,每隔1min将其取出,振荡,静置,立即测量并记录剩余酯层的高度,再迅速放回水浴中
继续加热,如此反复进行。改变NaOH溶液的浓度,重复实验。乙酸乙酯水解后剩余高度/mm数据如下:
时间/min
组别
0 1 2 3 4 5 6 7 8
1 0.5 10.0 9.0 8.0 7.5 7.0 6.5 6.5 6.5 6.5
2 1.0 10.0 8.5 7.0 6.0 5.0 4.5 4.5 4.5 4.5
3 2.0 10.0 8.0 6.0 4.5 3.0 2.0 1.5 1.5 1.5
回答下列问题:
(6)分析上述数据,得到乙酸乙酯水解速率的规律是:
①NaOH溶液浓度越大,水解速率越___________;
②___________。
(7)结论②的理论解释是___________。
(8)该实验必须严格控制NaOH溶液的体积、乙酸乙酯的用量和反应的温度。为了达到实验的目的,有同学
建议用___________代替NaOH溶液重复试验,对数据进行修正。
【答案】(1)防倒吸
(2)饱和 溶液
(3)
(4)不是
(5)3.45
(6)快 乙酸乙酯水解速率先快后慢,一段时间后停止水解
(7)NaOH能与水解产物醋酸发生中和反应,随着反应的进行,NaOH浓度逐渐减小直到完全消耗,其催化
作用也逐渐减弱直到没有催化作用
(8)蒸馏水
【解析】(1)球形干燥管除了有冷凝的作用外,还能起到防倒吸的作用。(2)②中盛装的试剂是饱和碳酸钠溶液,用来溶解乙醇、消耗乙酸等。
(3)由醋酸羟基氧示踪法可知,醋酸脱去羟基、醇脱去羟基氢,因此乙醇羟基氧示踪法的产物为
、 。
(4)用醋酸羟基氧示踪法中,产物含氧18水占到总水量的一半,酯也一样,说明酯化反应的历程可能是首
先乙酸分子中含有碳氧双键打开,发生加成反应,氧上连氢原子,碳上连乙氧基,连在同一个碳上的两个
羟基不稳定,会脱水,脱水有两种情况,从而使得产物含氧18水占到总水量的一半,酯也一样,说明酯化
反应不是简单的取代反应。
(5)在投料1:1的情况下,测得120℃时, 平衡转化率为65%,则
。
(6)①由表中数据可知:氢氧化钠溶液浓度越大,相同时间内剩余乙酸乙酯的量越少,则乙酸乙酯的水解速
率越快。
②氢氧化钠溶液浓度一定时,随着水解反应的进行,相同时间内乙酸乙酯的变化量越来越少,并且最终不
变化,即乙酸乙酯水解速率先快后慢,一段时间后达到平衡状态。
(7)乙酸乙酯水解生成乙酸和乙醇,由于氢氧化钠在反应中起催化作用,浓度较大时,催化作用效果明显,
随着乙酸乙酯水解反应的进行,生成乙酸和乙醇的量逐渐增加,氢氧化钠因与醋酸发生中和反应,导致氢
氧化钠溶液的浓度逐渐减小、直至消耗完全,其催化作用也逐渐减弱、直到没有,则乙酸乙酯的水解反应
达到平衡状态,乙酸乙酯的剩余量不变。
(8)在实验中,乙酸乙酯水解过程中部分挥发,为体现氢氧化钠的催化作用,可以用蒸馏水代替氢氧化钠溶
液来进行空白对照实验,推算乙酸乙酯的挥发损耗,便于对数据进行修正。
题组四 酯类
1.(2021·黑龙江·哈尔滨市第六中学校高二阶段练习)使9g乙二酸与一定量的二元醇完全酯化,生成wg
酯和3.6g水,则该醇的相对分子质量可表示为
A. B. C. D.
【答案】B
【解析】3.6g水的物质的量为0.2mol,乙二酸与二元醇完全酯化反应脱去2分子HO,即乙二酸+二元醇→
2
酯+2H O,故二元醇的物质的量为0.1mol,根据质量守恒可知,二元醇的质量为:Wg+3.6g-9g=(W+3.6-
29)g,该二元醇的摩尔质量为: = g/mol,故该二元醇的相对分子质量为 ;
综上所述答案为B。
2.(2021·云南·昆明八中高二期中)分子式为C H O 的酯水解,得到A和B两种物质,A氧化可转变
10 20 2
为B,符合上述性质的酯的结构有
A.4种 B.8种 C.16种 D.32种。
【答案】A
【解析】分子式为C H O 的有机物能水解生成A和B,A氧化可转变为B,则A为醇,B为酸,A能被
10 20 2
氧化为酸,则A中含有—CHOH,因A在一定条件下可氧化为B,则A为C HCHOH,B为
2 4 9 2
C HCOOH,而—C H 有四种结构,故选A。
4 9 4 9
3.(2021·全国·高二课时练习)下列关于油脂的叙述不正确的是。
A.油脂属于酯类 B.油脂没有固定的熔点和沸点
C.油脂是高级脂肪酸的甘油酯 D.油脂都不能使溴水褪色
【答案】D
【解析】A.油脂是高级脂肪酸与甘油形成的酯,油脂属于酯,故A正确;
B.油脂属于混合物,没有固定的熔沸点,故B正确;
C.油脂是高级脂肪酸与甘油形成的酯,故C正确;
D.油脂中含有碳碳双键,能与溴水发生加成反应,使溴水褪色,故D错误;
故选D。
4.(2022·全国·高二课时练习)实验室制备乙酸异戊酯的有关信息如下表所示。
物质 相对分子质量 密度/(g·cm-3) 沸点/℃ 水溶性
乙酸异戊酯 130 0.867 142 难溶
在洗涤、分液操作中,应充分振荡,然后静置,待分层后操作正确的是
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
【答案】D
【解析】乙酸异戊酯的密度比水的小且难溶于水,分层后水层在下面,应先将下面的水层从分液漏斗的下
口放出,再将上层的乙酸异戊酯从上口倒出;不能将密度小的液体从下口放出,若水层和乙酸异戊酯都从
下口放出,附着在分液漏斗下口的少量水层又会混入乙酸异戊酯中,导致分离失败。答案选D。
5.(2021·广西·桂林十八中高二期中)已知某有机物C H O 能发生水解反应生成A和B,B能氧化成
8 16 2
A,则C H O 符合条件的结构简式有(不考虑立体异构)
8 16 2
A.2种 B.3种 C.4种 D.5种
【答案】A
【解析】根据题意,有机物 为酯类化合物,不饱和度为 ,结构中除了碳氧双键以外没有
其它的不饱和键;其水解产物为羧酸和醇,又B能氧化成A,所以A、B含有的碳原子数相同,且A为伯
醇,则A为C HCHOH;B为C HCOOH,其中 可能的结构有 、 ,
3 7 2 3 7
共两种,故选A。
6.(2021·湖北·麻城市实验高级中学高二阶段练习)乙酸橙花酯是一种食用香料,其结构如图所示。下列
有关该物质的说法中正确的是
A.该有机物的分子式为
B. 该有机物最多可与 反应
C.能发生加成、取代、氧化、加聚反应
D.在碱性条件下水解, 该有机物最多消耗
【答案】C
【解析】A.由结构简式可知,乙酸橙花酯的分子式C H O,故A错误;
12 20 2
B.由结构简式可知,乙酸橙花酯分子中含有的碳碳双键能与氢气发生加成反应,则1mol乙酸橙花酯最多
消耗2 mol氢气,故B错误;
C.由结构简式可知,乙酸橙花酯分子中含有碳碳双键和酯基,其中碳碳双键能发生加成反应、氧化反应
和加聚反应,酯基能发生水解反应,故C正确;
D.由结构简式可知,乙酸橙花酯分子中含有的酯基能与氢氧化钠溶液反应,则1mol乙酸橙花酯最多消耗
1 mol氢氧化钠,故D错误;故选C。
7(2021·陕西蓝田·高二期末)某酯C H O 经水解后可得到相同碳原子数的羧酸和醇,再把醇氧化可得到
6 12 2
丙酮( ),该酯是
A. B.
C. D.
【答案】B
【解析】某酯分子式是C H O,该物质经水解后可得到相同碳原子数的羧酸和醇,说明形成酯的酸与醇
6 12 2
分子中都含有3个C原子。若再把醇氧化得到丙酮,则该醇为2-丙醇,结构简式是 ,故酯是
丙酸异丙酯,结构简式是 ,故合理选项是B。
8.(2021·全国·高二)某羧酸酯的分子式为C H O,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,
18 26 5
该羧酸的分子式为
A.C H O B.C H O C.C H O D.C H O
14 18 5 14 16 4 14 22 5 14 10 5
【答案】A
【解析】某羧酸酯的分子式为C H O,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,说明酯中含有
18 26 5
2个酯基,设羧酸为M,则反应的方程式为C H O+2H O→M+2C HO,由质量守恒可知M的分子式为
18 26 5 2 2 6
C H O。
14 18 5
故选A。
9.(2022·全国·高二专题练习)下列物质中,不属于酯类的是
A.硬脂酸钠 B.醋酸纤维 C.乙酸乙酯 D.牛油
【答案】A
【解析】A.硬脂酸钠属于盐,A符合题意;
B.醋酸纤维是醋酸和纤维素形成的酯类,B不符合题意;
C.乙酸乙酯属于酯类,C不符合题意;
D.牛油属于酯类,D不符合题意;
故选A。10.(2021·全国·高三专题练习)关于酯类物质,下列说法不正确的是
A.三油酸甘油酯可表示为
B.酯类物质只能由含氧酸和醇类通过酯化反应获得
C.1mol乙酸苯酚酯( )与足量NaOH溶液反应,最多消耗2molNaOH
D.酯类物质在酸性或碱性条件下都可以发生水解反应
【答案】B
【解析】A.甘油是丙三醇、油酸是C H COOH,两者发生酯化反应得到三油酸甘油酯,结构简式为
17 33
,A正确;
B.若羟基直接连接在苯环上,类别属于酚类,即羧酸和苯酚类也可通过酯化反应得到酯类物质,B错误;
C. 与NaOH溶液反应先断裂酯基的键,得到羟基是连接在苯环上,即为苯酚,其具有酸性,可
再消耗NaOH,所以1mol乙酸苯酚酯最多消耗2molNaOH,C正确;
D.酯类物质在酸性条件如浓硫酸加热下可发生水解得到羧酸类和醇类,在碱性条件下如NaOH溶液加热
下可得到钠盐,两种条件下都可以发生水解反应,D正确;
故选:B。
11.(2021·重庆市清华中学校高二阶段练习)有机物 有多种同分异构体,其中含有苯环且属
于酯类的有
A.6种 B.5种 C.4种 D.3种
【答案】A
【解析】含有1个侧链时,侧链分别为-COOCH 、HCOOCH -,CHOOC-,有3种;含有2个侧链时,侧
3 2 3
链为-OOCH和-CH,有邻间对3种;共3+3=6种,A正确;
3
选A。
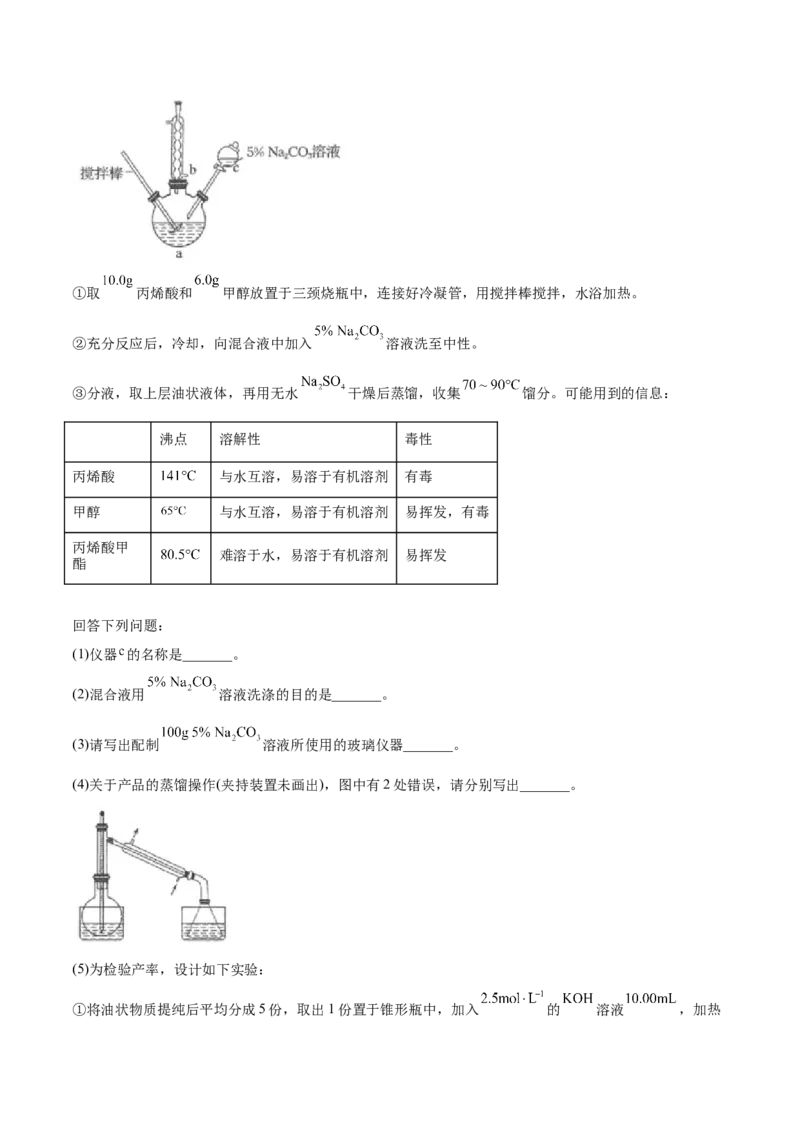
12.(2021·江苏常熟·高二开学考试)丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的
装置如图所示:①取 丙烯酸和 甲醇放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热。
②充分反应后,冷却,向混合液中加入 溶液洗至中性。
③分液,取上层油状液体,再用无水 干燥后蒸馏,收集 馏分。可能用到的信息:
沸点 溶解性 毒性
丙烯酸 与水互溶,易溶于有机溶剂 有毒
甲醇 与水互溶,易溶于有机溶剂 易挥发,有毒
丙烯酸甲
难溶于水,易溶于有机溶剂 易挥发
酯
回答下列问题:
(1)仪器 的名称是_______。
(2)混合液用 溶液洗涤的目的是_______。
(3)请写出配制 溶液所使用的玻璃仪器_______。
(4)关于产品的蒸馏操作(夹持装置未画出),图中有2处错误,请分别写出_______。
(5)为检验产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入 的 溶液 ,加热使之完全水解。
②用酚酞作指示剂,向冷却后的溶液中滴加 的 溶液,中和过量的 ,滴到终点时共消耗
盐酸 。计算本次酯化反应丙烯酸的转化率_______。
【答案】(1)分液漏斗
(2)除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度)
(3)烧杯、玻璃棒、量筒、胶头滴管
(4)温度计水银球位置、接液管与锥形瓶接口密封
(5)
【解析】利用该实验装置制备并提纯丙烯酸甲酯,装置a中将10.0g丙烯酸、6.0g甲醇和浓硫酸混合用搅拌
棒搅拌,水浴加热发生反应制取丙烯酸甲酯,制得的粗品丙烯酸甲酯用5%Na CO 溶液洗去混合液中丙烯
2 3
酸、甲醇和浓硫酸至中性,经干燥过滤,利用水浴加热蒸馏分离出丙烯酸甲酯,蒸馏操作时,冷凝水的方
向与蒸汽的流动方向相反,温度计测定蒸汽的温度,水银球在蒸馏烧瓶的支管口处,将制得的丙烯酸甲酯
利用中和滴定的原理进行含量的测定并计算含量,据此分析解答。
(1)根据仪器的构造可判断仪器 的名称是分液漏斗;
(2)混合液中有丙烯酸甲酯、丙烯酸、甲醇、浓硫酸,浓硫酸、丙烯酸能与NaCO 溶液反应,甲醇能溶于
2 3
碳酸钠溶液中,所以用5%Na CO 溶液洗涤的目的是除去混合液中的丙烯酸、浓硫酸和甲醇(降低丙烯酸
2 3
甲酯的溶解度);
(3)配制100g 5% Na CO 溶液通常用的玻璃仪器是烧杯、玻璃棒、量筒、胶头滴管;
2 3
(4)根据装置以及以上分析可知可判断两处错误 温度计水银球位置、接液管与锥形瓶接口密封;
(5)中和过量的KOH,滴到终点时共消耗盐酸20.00mL,物质的量为0.5mol/L×0.02L=0.01mol,所以用于水
解的KOH的物质的量为0.025mol-0.01mol=0.015mol,所以用于生成CH=CHCOOCH 的CH=CHCOOH的
2 3 2
质量为:0.015mol×72g/mol=1.08g,参加实验的样品为原样品的 ,则丙烯酸的转化率为:
×100%=54.0%。
题组五 酰胺
1.(2021·全国·高二课时练习)油脂是人体重要的能源物质,胺和酰胺是重要的化工原料,下列关于羧酸
衍生物的叙述正确的是
A.油脂的主要成分是高级脂肪酸 B.胺类化合物不能与盐酸反应C.酰胺基中碳原子采取 杂化 D.油脂可以在碱性条件下水解,用于制取肥皂
【答案】D
【解析】A.油脂的主要成分是高级脂肪酸甘油酯,A错误;
B.胺类化合物具有碱性,能与盐酸反应生成盐,B错误;
C.酰胺基中碳原子采取 杂化,C错误;
D.油脂在碱性条件下的水解反应又叫皂化反应,生成的高级脂肪酸盐可以用来制取肥皂,D正确;
故选D。
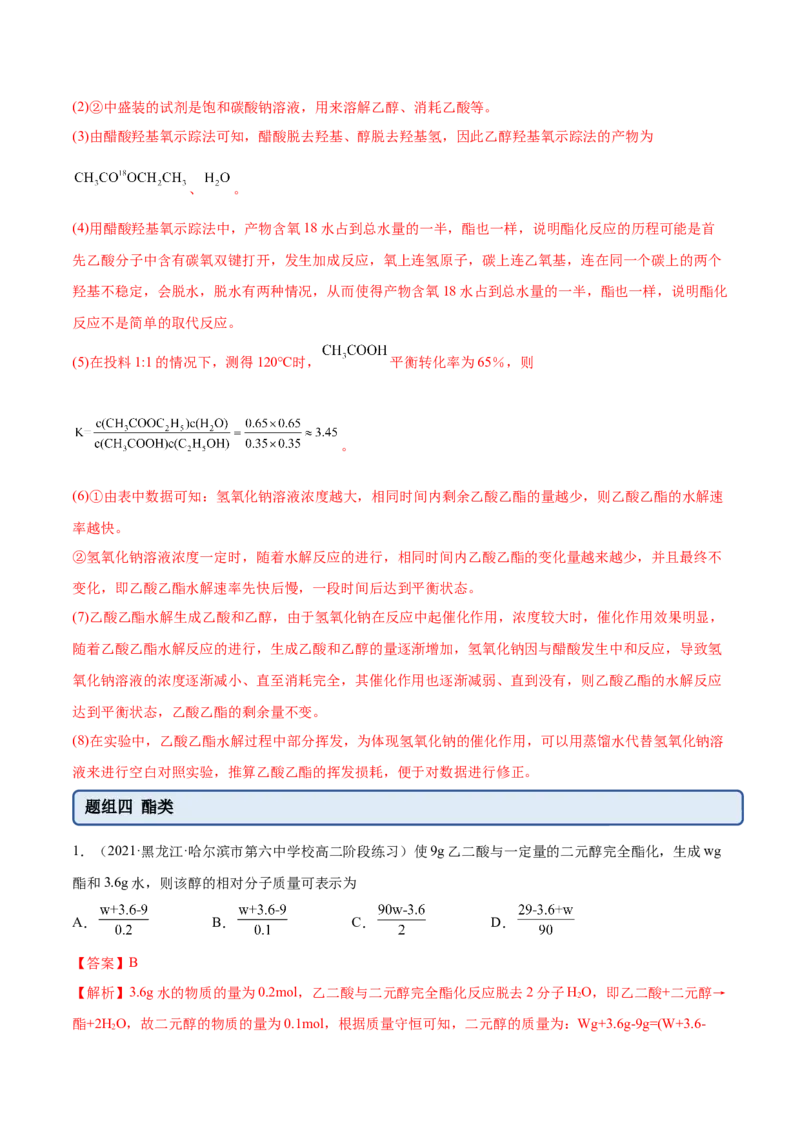
2.(2021·山东潍坊·模拟预测)乙氧酰胺苯甲酯常用于氨丙啉等抗球虫药的增效剂,其结构简式如图所示,
下列说法错误的是
A.元素的第一电离能: B.与该物质苯环上取代基相同的芳香族化合物有6种
C.分子中含有三种含氧官能团 D.其水解产物一定条件下都能发生聚合反应
【答案】BD
【解析】A.同周期随原子序数增大第一电离能呈增大趋势,但N元素原子2p轨道为半充满稳定状态,第
一电离能高于氧元素的,故第一电离能: ,A正确;
B. 含有3个不同的取代基,分别用a、b、c表示3个不同的取代基,其取代基相同的芳香族化合物共有10种,分别为 ,B错误;
C.该分子中含氧官能团有肽键、醚键、酯基3种,C正确;
D. 在酸性条件下水解一定产物为 、甲酸、甲醇,甲酸、甲醇不能发生聚合反应,
D错误;
故选BD。
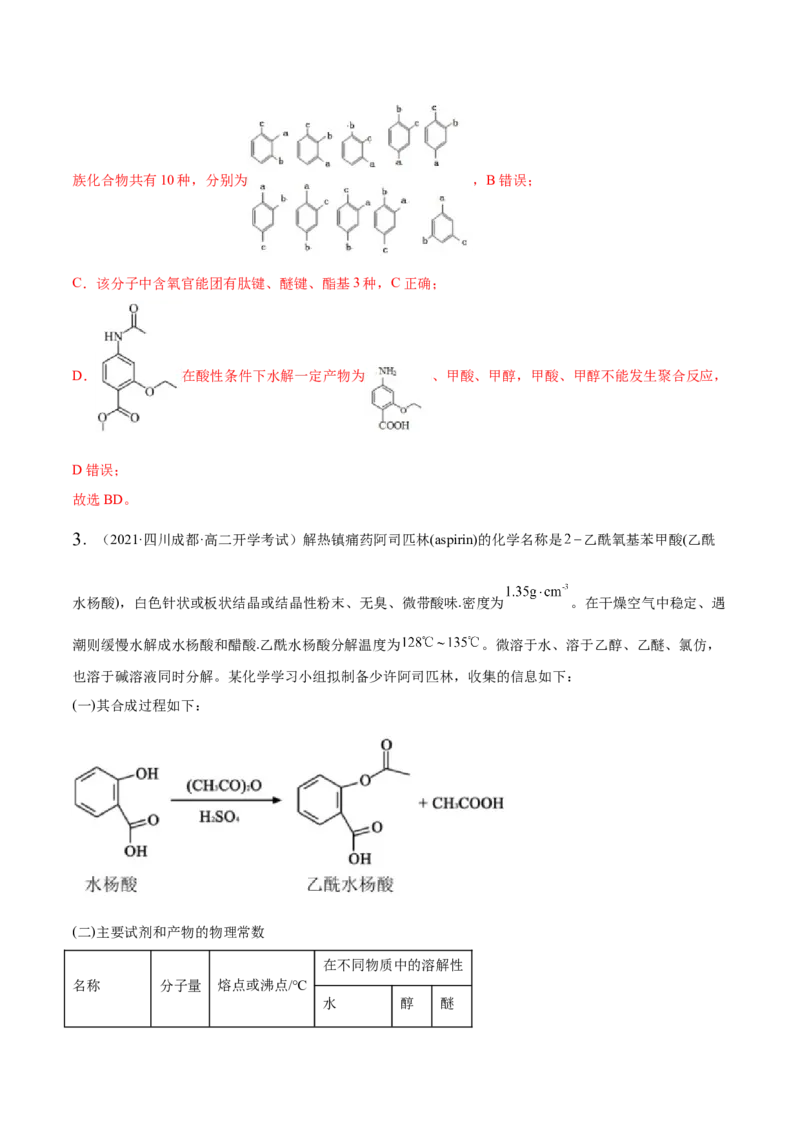
3.(2021·四川成都·高二开学考试)解热镇痛药阿司匹林(aspirin)的化学名称是 乙酰氧基苯甲酸(乙酰
水杨酸),白色针状或板状结晶或结晶性粉末、无臭、微带酸味.密度为 。在干燥空气中稳定、遇
潮则缓慢水解成水杨酸和醋酸.乙酰水杨酸分解温度为 。微溶于水、溶于乙醇、乙醚、氯仿,
也溶于碱溶液同时分解。某化学学习小组拟制备少许阿司匹林,收集的信息如下:
(一)其合成过程如下:
(二)主要试剂和产物的物理常数
在不同物质中的溶解性
名称 分子量 熔点或沸点/℃
水 醇 醚水杨酸 138 158(s) 微 易 易
醋酐 102.09 139.35(1) 易 溶 ∞
乙酰水杨
180.17 135(s) 溶、热 溶 微
酸
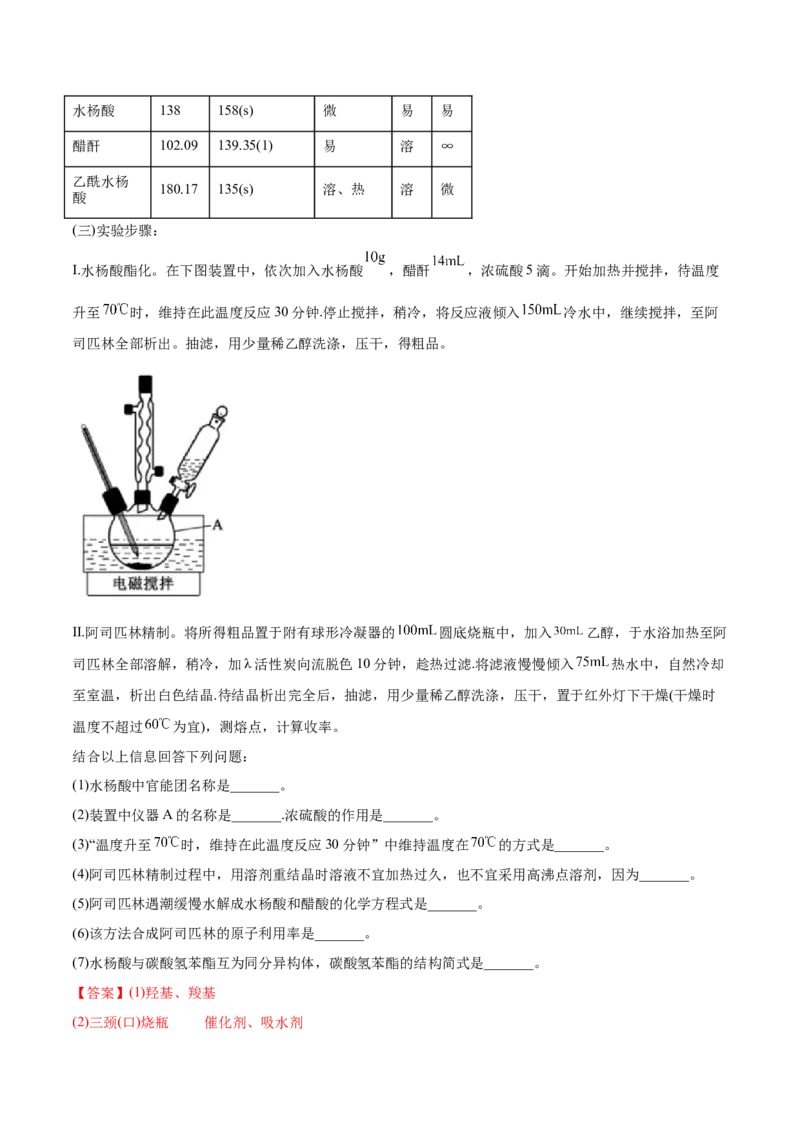
(三)实验步骤:
Ⅰ.水杨酸酯化。在下图装置中,依次加入水杨酸 ,醋酐 ,浓硫酸5滴。开始加热并搅拌,待温度
升至 时,维持在此温度反应30分钟.停止搅拌,稍冷,将反应液倾入 冷水中,继续搅拌,至阿
司匹林全部析出。抽滤,用少量稀乙醇洗涤,压干,得粗品。
Ⅱ.阿司匹林精制。将所得粗品置于附有球形冷凝器的 圆底烧瓶中,加入 乙醇,于水浴加热至阿
司匹林全部溶解,稍冷,加λ活性炭向流脱色10分钟,趁热过滤.将滤液慢慢倾入 热水中,自然冷却
至室温,析出白色结晶.待结晶析出完全后,抽滤,用少量稀乙醇洗涤,压干,置于红外灯下干燥(干燥时
温度不超过 为宜),测熔点,计算收率。
结合以上信息回答下列问题:
(1)水杨酸中官能团名称是_______。
(2)装置中仪器A的名称是_______.浓硫酸的作用是_______。
(3)“温度升至 时,维持在此温度反应30分钟”中维持温度在 的方式是_______。
(4)阿司匹林精制过程中,用溶剂重结晶时溶液不宜加热过久,也不宜采用高沸点溶剂,因为_______。
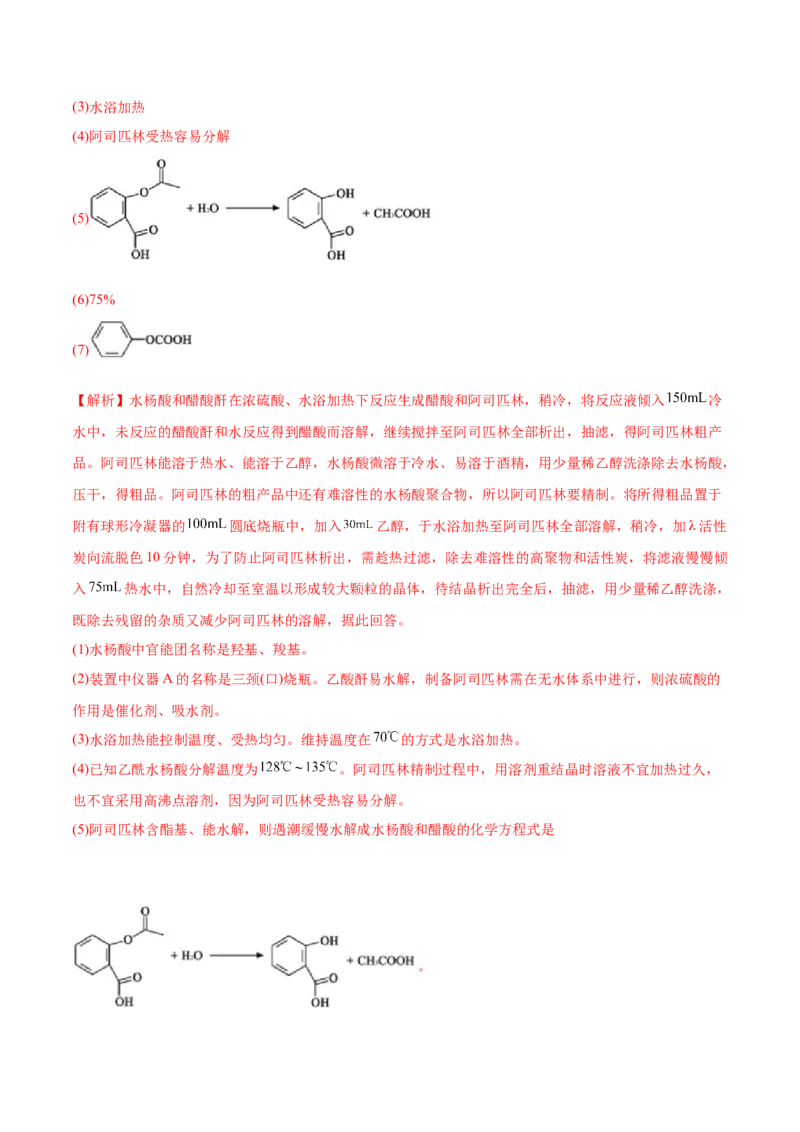
(5)阿司匹林遇潮缓慢水解成水杨酸和醋酸的化学方程式是_______。
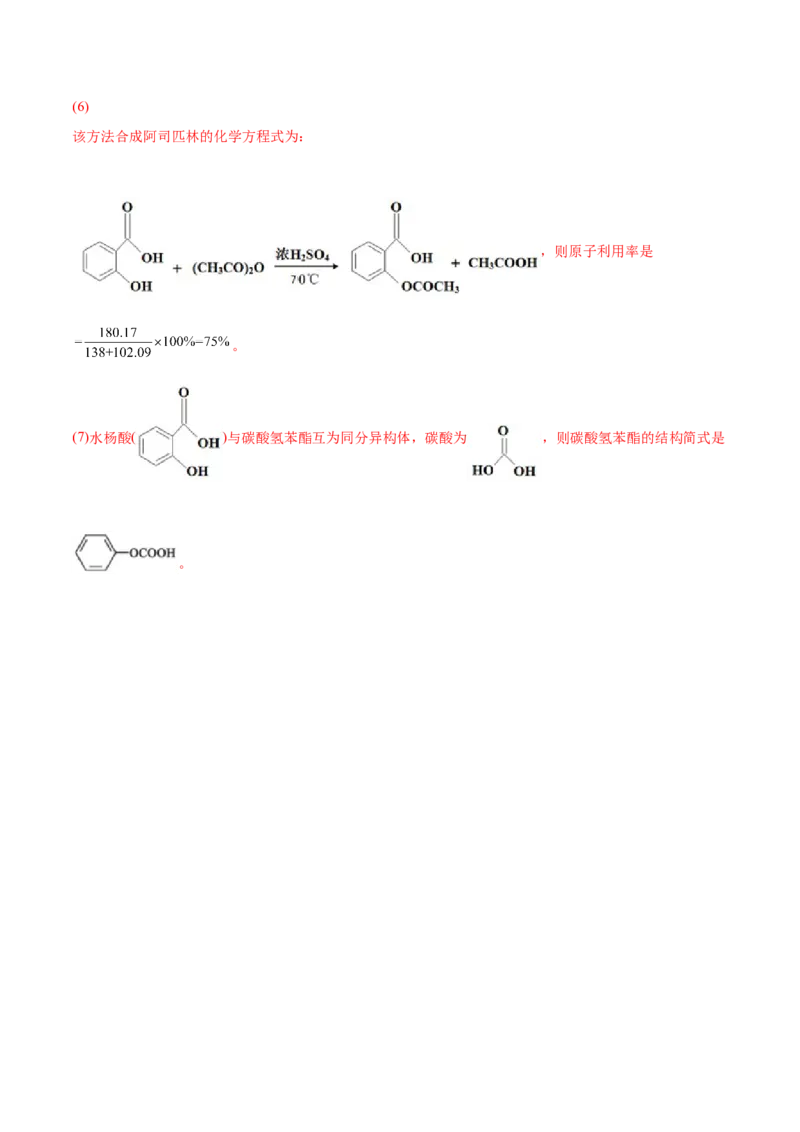
(6)该方法合成阿司匹林的原子利用率是_______。
(7)水杨酸与碳酸氢苯酯互为同分异构体,碳酸氢苯酯的结构简式是_______。
【答案】(1)羟基、羧基
(2)三颈(口)烧瓶 催化剂、吸水剂(3)水浴加热
(4)阿司匹林受热容易分解
(5)
(6)75%
(7)
【解析】水杨酸和醋酸酐在浓硫酸、水浴加热下反应生成醋酸和阿司匹林,稍冷,将反应液倾入 冷
水中,未反应的醋酸酐和水反应得到醋酸而溶解,继续搅拌至阿司匹林全部析出,抽滤,得阿司匹林粗产
品。阿司匹林能溶于热水、能溶于乙醇,水杨酸微溶于冷水、易溶于酒精,用少量稀乙醇洗涤除去水杨酸,
压干,得粗品。阿司匹林的粗产品中还有难溶性的水杨酸聚合物,所以阿司匹林要精制。将所得粗品置于
附有球形冷凝器的 圆底烧瓶中,加入 乙醇,于水浴加热至阿司匹林全部溶解,稍冷,加λ活性
炭向流脱色10分钟,为了防止阿司匹林析出,需趁热过滤,除去难溶性的高聚物和活性炭,将滤液慢慢倾
入 热水中,自然冷却至室温以形成较大颗粒的晶体,待结晶析出完全后,抽滤,用少量稀乙醇洗涤,
既除去残留的杂质又减少阿司匹林的溶解,据此回答。
(1)水杨酸中官能团名称是羟基、羧基。
(2)装置中仪器A的名称是三颈(口)烧瓶。乙酸酐易水解,制备阿司匹林需在无水体系中进行,则浓硫酸的
作用是催化剂、吸水剂。
(3)水浴加热能控制温度、受热均匀。维持温度在 的方式是水浴加热。
(4)已知乙酰水杨酸分解温度为 。阿司匹林精制过程中,用溶剂重结晶时溶液不宜加热过久,
也不宜采用高沸点溶剂,因为阿司匹林受热容易分解。
(5)阿司匹林含酯基、能水解,则遇潮缓慢水解成水杨酸和醋酸的化学方程式是
。(6)
该方法合成阿司匹林的化学方程式为:
,则原子利用率是
。
(7)水杨酸( )与碳酸氢苯酯互为同分异构体,碳酸为 ,则碳酸氢苯酯的结构简式是
。