文档内容
第三节 化学键
第2课时 共价键
基础巩固
1.(2022·全国·高一专题练习)下列关于共价键的叙述中正确的是
A.只有不同种元素的原子之间才能形成共价键
B.由A失去电子,B接受电子的过程形成了共价键
C.原子核外有几个电子就一定能形成几个共价键
D.共用电子对必然偏向吸引电子能力强的一方
2.(2022·宁夏·贺兰县景博中学高一阶段练习)下列说法中正确的是
A.H O 中既有极性键,又含有非极性键
2 2
B.非金属元素只能形成共价键
C.共价化合物H O 只含共价键,离子化合物Na O 只含离子键
2 2 2 2
D.金属元素与非金属元素只能形成离子键
3.下列物质中化学键类型完全相同的是( )
A.HS,NaS B.NaBr,CaF C.NaCl,CO D.SO ,KCl
2 2 2 2 2
4.下列物质中,既有离子键又有共价键的是( )
A.KOH B.O C.NaBr D.HO
2 2
5.下列电子式,正确的是( )
A. B.
C. D.
6.下列表示电子式的形成过程正确的是( )
A.
B.
C.
D.
7.下列说法正确的是( )
A.分子间作用力与化学键的大小相当
B.分子间作用力的大小远大于化学键,是一种很强的作用力
C.分子间作用力主要影响物质的化学性质
D.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作用,称为分子间作用
学科网(北京)股份有限公司力
8.下列说法正确的是( )
A.HO的沸点较高是因为水分子间存在较强的化学键
2
B.HCl气体溶于水后,共价键被破坏,形成了 和
C.HS分子中所有原子最外电子层都具有8电子的稳定结构
2
D.NaOH和MgCl 所含化学键类型完全相同
2
9.下面是同学们熟悉的物质:
①O ②金刚石 ③NaBr ④HSO ⑤NaCO
2 2 4 2 3
⑥NH Cl ⑦NaHSO ⑧Ne ⑨NaO ⑩NaOH
4 4 2 2
(1)这些物质中,只含有共价键的是________;只含有离子键的是________;既含有共价键又含有离子键
的是________;不存在化学键的是________。
(2)属于共价化合物的是________;属于离子化合物的是________。
(3)将NaHSO 溶于水,破坏了NaHSO 中的________,写出其电离方程式_________________;
4 4
NaHSO 在熔融状态下电离,破坏了________,写出其电离方程式___________________________。
4
10.(2020·河南·辉县市第二高级中学高一阶段练习)有A、B、C、D四种短周期元素,它们的原子序数
由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空
气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色
固态化合物,试根据以上叙述回答:
(1)请写出元素A的名称______,B的简单离子示意图______;D的简单离子的电子式_____;
(2)D元素位于周期表中____周期_______族,C B 的电子式:____,所含化学键____。
2 2
(3)电子式表示化合物C D的形成过程:______________。
2
能力提升
11.(2022·四川·威远中学校高一阶段练习)工业上用 和 制“漂白液”,反应的化学方程式为
,下列关于该反应的说法错误的是
A. 中存在离子键和极性键
B.此反应过程中既有离子键、共价键断裂,也有离子键和共价键形成
C. 含 键, 含2mol共用电子对
D.像 、 这样含金属元素的化合物一定属于离子化合物
12.(2022·陕西·周至县第四中学高一期中)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意
义的N 气体分子。N 分子结构如图所示,下列说法正确的是
4 4
A.N 分子属于一种新型的化合物
4
学科网(北京)股份有限公司B.N 分子中只含有非极性键
4
C.1 mol N 分子所含共价键数为4N
4 A
D.N 分子中只含有极性键
4
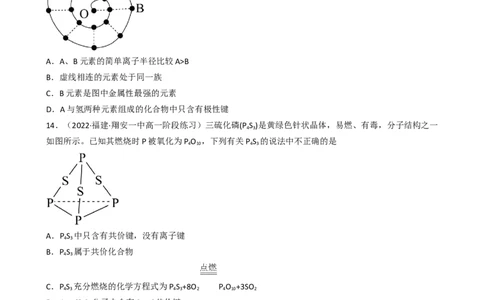
13.(2022·浙江省普陀中学高三阶段练习)门捷列夫周期表是常见的经典形式,人们在研究前18号元素
时发现,还可以将它们排成如图所示的“海螺”形状,图中每个“·”代表一种元素,其中0点代表氢元素,
下列说法错误的是
A.A、B元素的简单离子半径比较A>B
B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素
D.A与氢两种元素组成的化合物中只含有极性键
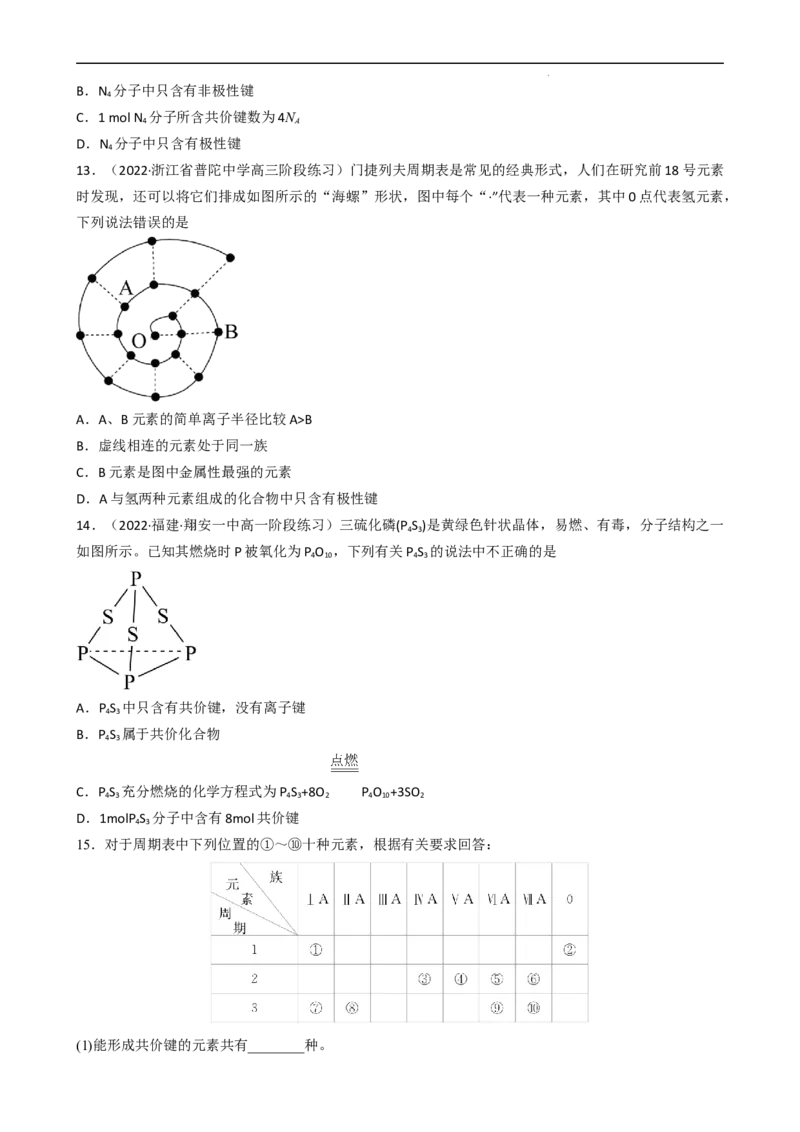
14.(2022·福建·翔安一中高一阶段练习)三硫化磷(P S )是黄绿色针状晶体,易燃、有毒,分子结构之一
4 3
如图所示。已知其燃烧时P被氧化为P O ,下列有关P S 的说法中不正确的是
4 10 4 3
A.P S 中只含有共价键,没有离子键
4 3
B.P S 属于共价化合物
4 3
C.P S 充分燃烧的化学方程式为P S +8O P O +3SO
4 3 4 3 2 4 10 2
D.1molP S 分子中含有8mol共价键
4 3
15.对于周期表中下列位置的①~⑩十种元素,根据有关要求回答:
(1)能形成共价键的元素共有________种。
学科网(北京)股份有限公司(2)只需形成一个共价单键就能达到稳定结构的元素有_______(填元素符号)。
(3)气态氢化物溶于水生成的呈碱性的化合物是____________(填化学式)。
(4)⑩号元素最高正价含氧酸只含有________键。
(5)①⑤⑦形成的化合物的电子式为________。
(6)某元素的气态氢化物为HB,其最高价氧化物中B的质量分数为40%,则其气态氢化物的电子式为
2
__________,它与③的化合物的分子式为__________,含有的化学键类型有__________。
(7)④⑩元素之间能形成两种化合物,其中一种化合物中每个原子都达到8电子稳定结构,该化合物的电
子式为__________。
学科网(北京)股份有限公司学科网(北京)股份有限公司