文档内容
高清视频学案
1 / 4
中考总复习——综合计算技巧
魏国福
一、思维导图:
二、主要题型:
1、化学方程式与溶液综合的计算
2、表格型数据分析题
3、坐标型数据分析题
4、标签型计算应用题
5、实验型计算应用题
三、解题技巧:
1、找纯量:反应生成的气体或沉淀的质量。
2、看反应程度:根据反应是恰好完全反应还是某种反应物完全反应,是否
有物质已经过量。
3、标签中的信息:物质名称、主要成份、化学式、含量等。
4、看坐标:起点、终点、变化趋势、转折点(拐点)等。
5、反应后溶液质量的求算:
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687高清视频学案
2 / 4
守恒法:加入的物质总质量—沉淀(或气体)质量
组成法:溶质质量+溶剂质量
习题
1、实验室用过氧化氢溶液与二氧化锰混合制氧气。现将1.0 g二氧化锰放
入盛有20.0 g过氧化氢溶液的锥形瓶中,立即塞紧带导管的橡胶塞,反应
结束,共收集到559 mL气体。计算:(结果保留1位小数)
(1)反应结束后,过滤,滤渣的质量为________g。
(2)反应产生氧气的质量为__________g。(标准状况下氧气的密度约为
1.43 g/L)
(3)过氧化氢溶液中溶质的质量分数(百分数)。
2、为测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的含量,取12g样品
放入烧杯中,加入100g稀盐酸,恰好完全反应。经测定,所得溶液常温下
为不饱和溶液,其质量为107.6 g(产生的气体全部逸出)。试计算:
(1)反应生成二氧化碳的质量为 g。
(2)12g样品中碳酸钠的质量为 g。
(3)稀盐酸中溶质的质量分数(写出计算过程)。
3、某同学为了测定NaCl和MgCl 固体混合物中MgCl 的质量分数,进行
2 2
如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相
同质量分数的NaOH溶液,获得如下实验数据:
问:
(1)表中m的值为 ;
(2)原固体混合物中MgCl 的质量分数是多少?(要求写出计算过程)
2
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687高清视频学案
3 / 4
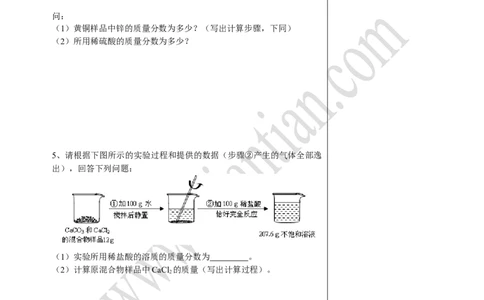
4、某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取
10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,充分反应,实
验数据如下:
问:
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
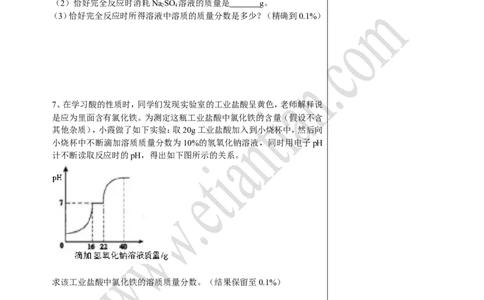
5、请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸
出),回答下列问题:
(1)实验所用稀盐酸的溶质的质量分数为 。
(2)计算原混合物样品中CaCl 的质量(写出计算过程)。
2
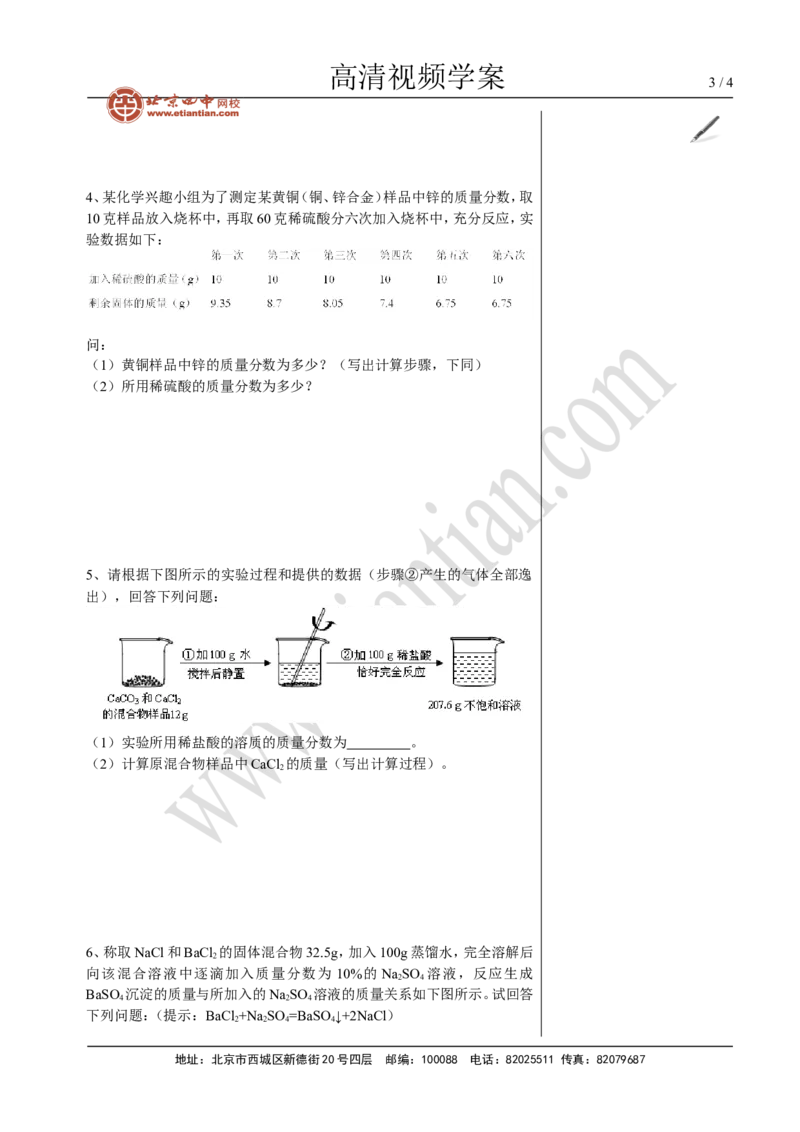
6、称取NaCl和BaCl 的固体混合物32.5g,加入100g蒸馏水,完全溶解后
2
向该混合溶液中逐滴加入质量分数为 10%的 NaSO 溶液,反应生成
2 4
BaSO 沉淀的质量与所加入的NaSO 溶液的质量关系如下图所示。试回答
4 2 4
下列问题:(提示:BaCl +Na SO =BaSO ↓+2NaCl)
2 2 4 4
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687高清视频学案
4 / 4
(1)完全反应后生成BaSO 沉淀 g。
4
(2)恰好完全反应时消耗NaSO 溶液的质量是 g。
2 4
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)
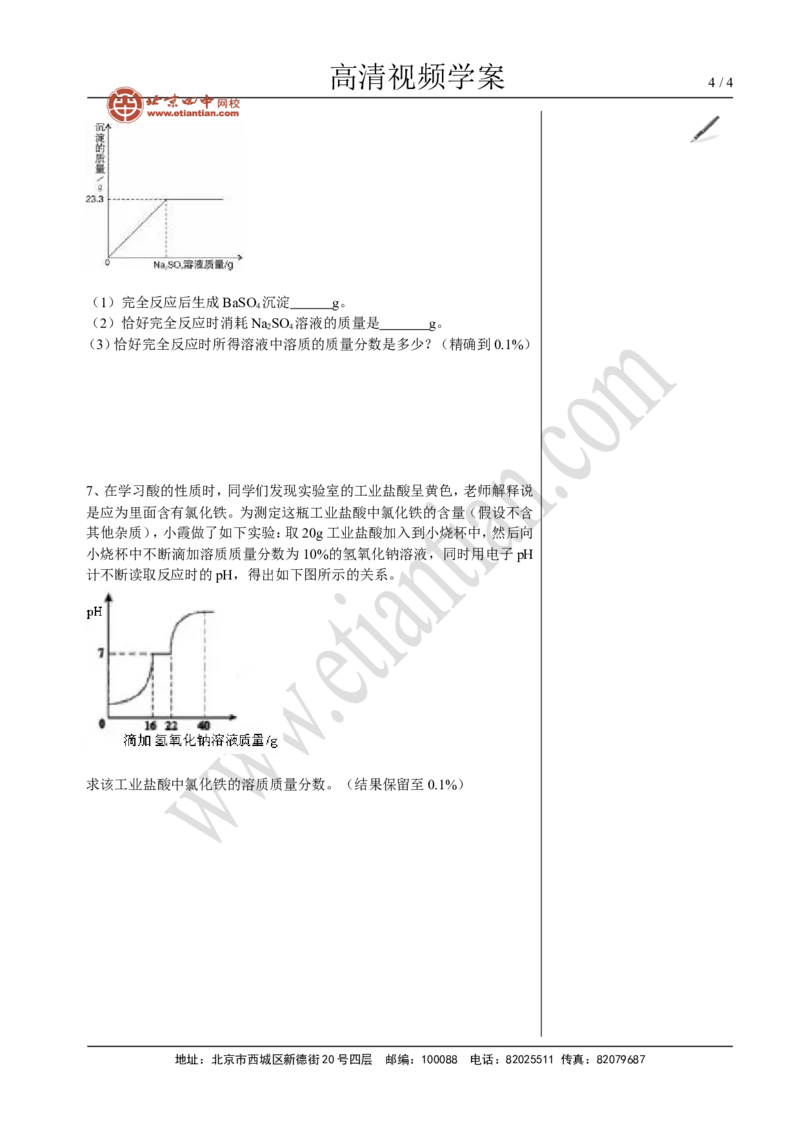
7、在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说
是应为里面含有氯化铁。为测定这瓶工业盐酸中氯化铁的含量(假设不含
其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向
小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH
计不断读取反应时的pH,得出如下图所示的关系。
求该工业盐酸中氯化铁的溶质质量分数。(结果保留至0.1%)
地址:北京市西城区新德街20号四层 邮编:100088 电话:82025511 传真:82079687