文档内容
第 16 讲 气体摩尔体积
知识导航
课前引入
冰,水,水蒸气,都是HO分子构成的物质。
2
为什么冰有固定的形状,水和水蒸气却没有呢?
知识精讲
一、不同聚集状态物质的微观结构
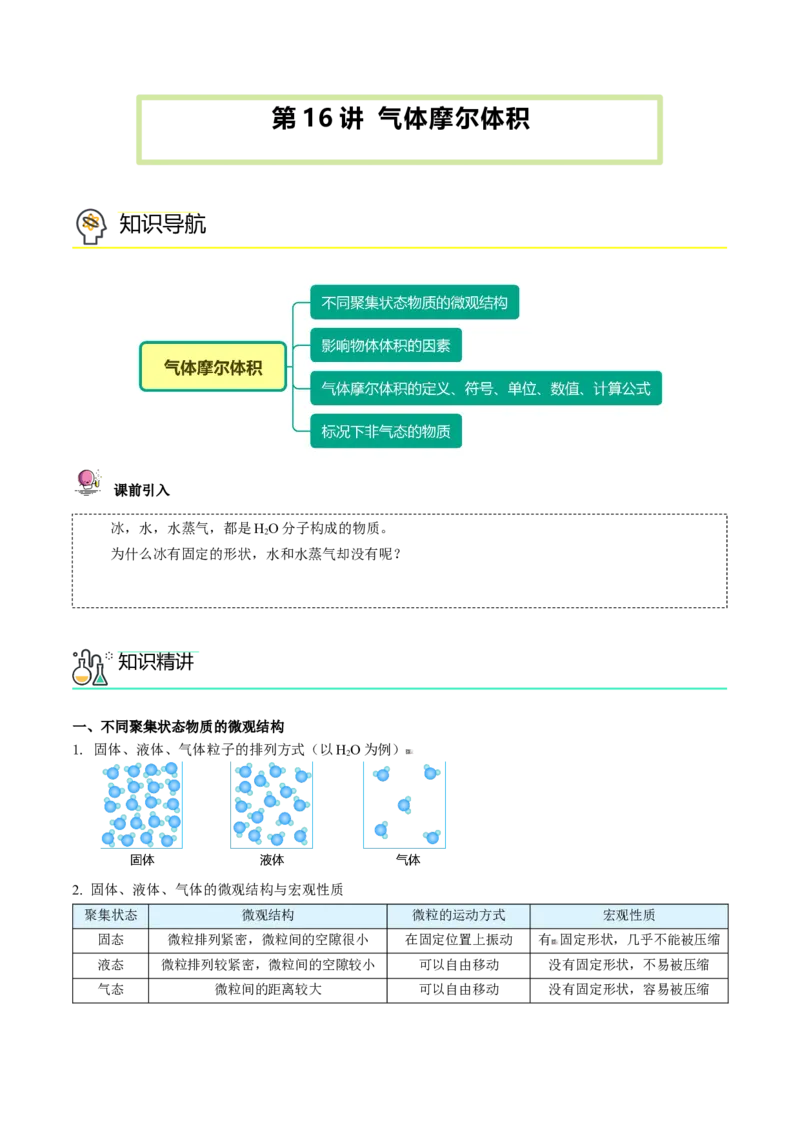
1. 固体、液体、气体粒子的排列方式(以HO为例)
2
2. 固体、液体、气体的微观结构与宏观性质
聚集状态 微观结构 微粒的运动方式 宏观性质
固态 微粒排列紧密,微粒间的空隙很小 在固定位置上振动 有 固定形状,几乎不能被压缩
液态 微粒排列较紧密,微粒间的空隙较小 可以自由移动 没有固定形状,不易被压缩
气态 微粒间的距离较大 可以自由移动 没有固定形状,容易被压缩二、影响物体体积的因素
从微观来角度来看,物质体积的大小取决于构成这种物质的粒子的数目、粒子的大小和粒子之间的距离。
1. 固态、液态物质粒子之间的距离是非常小的,因此决定固体或液体体积的主要因素是构成物质的粒子的
数目和粒子的大小。
2. 气态分子之间的距离远远大于分子本身的大小,因此决定气体体积的主要因素则是构成气体的分子的数
目和分子之间的距离。分子间的距离与温度、压强有关:温度越高,距离越大;压强越大,距离越小。
三、气体摩尔体积
1. 定义:单位物质的量的气体所占有的体积,叫做气体摩尔体积。
2. 符号:V
m
3. 单位:L·mol-1(或L/mol)
4. 数值:在标准状况(温度为0℃,压强为101 kPa)下,气体摩尔体积为22.4L/mol
5. 计算公式:V=n·V
m
及时小练——填写下表
物质 物质的量 分子数 质量 体积(标况)
CO 1.5 mol
2
O 64g
2
Cl N
2 A
【答案】1.5N 66g 33.6L 2mol 2N 44.8L 1 mol 71g 22.4L
A A
对点训练
题型一:决定物质体积大小的因素
【例1】(2021·江苏苏州市·周市高级中学高一月考)在一定温度和压强下的气体,影响其所占气体大小的
最主要因素是
A.分子直径大小 B.分子间距离的大小C.分子间作 用力的大小 D.分子数的大小
【答案】D
【详解】
影响气体体积大小的因素有分子直径的大小、分子间距离的大小、分子数的大小,在一定温度和压强下,
气体分子间的距离相等,因分子间距离远大于气体分子大小,则影响其所占体积大小的主要因素是分子数
的大小,D选项符合题意;答案为D。题型二:气体摩尔体积的适用范围
【例2】(2021·全国高一课时练习)设N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,22.4 L SO 的物质的量是1 mol B.标准状况下,11.2 L HO的物质的量是0.5 mol
2 2
C.标准状况下,44.8 LCO 含有的分子数为2N D.1 mol任何气体的体积都约是22.4 L
2 A
【答案】C
【详解】
A.常温常压V 大于22.4L/mol,22.4L SO 的物质的量小于1mol,故A错误;
m 2
B.标况下水是液体,不能使用气体摩尔体积,故B错误;
C.标准状况下,44.8L CO 含有的分子数为2N ,故C正确;
2 A
D.气体状况未知,应该是标况下1 mol任何气体的体积都约是22.4 L,故D错误;
故答案为C。
题型三:气体摩尔体积的计算
【例3】(2021·北京首师大附中通州校区高一期末)1g氮气所 占有的体积为VL,则该条件下氮气的摩尔
体积为
A.22.4L·mol-1 B.28V L·mol-1 C.28/V L·mol-1 D.V/28 L·mol-1
【答案】B
【详解】
1g氮气的物质的量为 ,氮气的摩尔体积 ,故B正确。
故选B。
题型四:基于方程式的气体摩尔体积计算
【例4】(2020·贵州高二学业考试)24g Mg与足量的稀硫酸反应,生成的 在标准状况下的体积约为
A.1L B.0.1L C.22.4L D.11.2L
【答案】C
【详解】
24g Mg的物质的量为 =1mol,由Mg+HSO =MgSO +H ↑可知,1mol Mg完全反应后生成H 的物
2 4 4 2 2
质的量为1mol,其在标准状况的体积为1mol×22.4L/mol=22.4L,故答案为C。
题型五:气体摩尔体积的应用【例5】(2020·福建省南安市柳城中学高一期中)标准状况下,等质量的下列气体所 占有的体积最大的
是
A.O B.CH C.CO D.N
2 4 2 2
【答案】B
【分析】
标准状况下,各种气体的温度和压强相同,同温同压下,气体体积比等于物质的量之比,气体体积最大,
则物质的量n最大,根据 可知,质量相等的气体,M越小,n越大
【详解】
O 摩尔质量为32 g∙mol−1,CH 摩尔质量为16 g∙mol−1,CO 摩尔质量为44 g∙mol−1,N 摩尔质量为28
2 4 2 2
g∙mol−1,CH 摩尔质量最小,故B符合题意。
4
答案选B。
题型六:化学计量综合计算
【例6】(2021·河南安阳三十五中高一开学考试)在标准状况下,18gCO与CO 的混合气体,体积为
2
11.2L。则:
(1)混合气体的密度是________;
(2)混合气体的平均摩尔质量是_______;
(3)CO与CO 的体积之比是_________;
2
(4)CO与CO 的质量之比是__________;
2
(5)混合气体中所含碳原子的物质的量是________。
【答案】1.6g/L 36g/mol 1∶1 7∶11 0.5mol
【分析】
根据ρ= 、n= 、 = ,结合质量及物质的量和质量守恒定律分析解答。
【详解】
在标准状况下,18g CO与CO 的混合气体,体积为11.2L。
2
(1)混合气体的密度为:ρ= =1.6 g/L,故答案为:1.6 g/L;
(2)混合气体的物质的量为 =0.5mol,混合气体平均摩尔质量为 =36g/mol,故答案为:
36g/mol;
(3)设CO与CO 的物质的量分别为xmol、ymol,根据二者质量及物质的量,则x+y=0.5、28x+44y=18,解
2
得:x=0.25、y=0.25,故CO 和CO的体积之比等于物质的量之比为0.25mol∶0.25mol=1∶1,故答案为:
2
1∶1;(4)CO 和CO的质量之比为(0.25mol×44g/mol)∶(0.25 mol×28g/mol)=7∶11,故答案为:7∶11;
2
(5)根据分子式CO、CO 可知,碳原子的物质的 量与混合气体的物质的量相等,所以混合气体中碳原子的
2
物质的量为0.5mol,故答案为:0.5mol。
【例7】(2021·全国高一课时练习)按要求回答下列问题:
(1)H SO 的相对分子质量为_____。
2 4
(2)在标准状况下,0.5 mol 任何气体的体积都约为_____。
(3)4 g H 与 22.4 L(标准状况)CO 相比,所含分子数目较多的是 _____。
2 2
(4)0.01 mol 某气体的质量为 0.28 g,该气体的摩尔质量为_____。
(5)0.3 mol NH 分子中所含氢原子数与___________个 HO 分子中所含氢原子数相等。
3 2
(6)含 0.4 mol Al3+的 Al (SO ) 中所含的 SO 的物质的量是_____。
2 3
(7)已知 16 g A 和 20 g B 恰好完全反应生成 0.04 mol C 和 31.76 g D,则 C 的摩尔质量为_____
(8)2.3 g Na 中含电子的物质的量为_____mol。
【答案】98 11.2 L H 28 g·mol-1 0.45NA 0.6 mol 106 g·mol-1 1.1
2
【详解】
(1)H SO 的相对分子质量=1×2+32+16×4=98;
2 4
(2)标准状况下,任何气体的气体摩尔体积都近似为22.4 L/mol,则V(气体)=22.4 L/mol×0.5 mol=11.2 L;
(3)n(H )= ,n(CO)= ,故所含分子数较多的为H;
2 2 2
(4)M= ,故此处填28 g/mol;
(5)由题意列式得:3n(NH )=2n(H O),代入数据计算得n(H O)=0.45 mol,故此处填0.45N ;
3 2 2 A
(6)由化学式知: ,故n( )= ×n(Al3+)=0.6 mol;
(7)由质量守恒得:m(C)=(16+20-31.76) g=4.24 g,则M(C)= ;
(8)1个Na含有11个电子,则2.3 g Na所含电子= 。
提分特训
【题1】(2021·全国)相同物质的量的各固体或液体的体积并不相同,其主要原因是
A.粒子大小不同
B.粒子质量不同C.粒子间距离不同
D.粒子的状态不同
【答案】A
【详解】
影响固体或液体体积的主要因素是微粒的数目和微粒的大小,A正确;
答案选A。
【题2】(2020·浙江高一期末)下列叙述正确的是
A.1 mol任何物质均含有约6.02×1023个原子
B.摩尔质量等于该物质的相对分子质量
C.气体的摩尔体积为22.4 L∙mol-1
D.同温、同压下,不同气体的摩尔体积近似相等
【答案】D
【详解】
A.物质不一定是由原子构成,还可能是由分子或离子构成,故A不符合题意;
B.摩尔质量单位为g/mol,相对分子质量单位为1,摩尔质量数值上等于相对分子质量,故B不符合题意;
C.气体摩尔体积的数值和状态有关,在标况下,气体摩尔体积为22.4 L∙mol-1,故C不符合题意;
D.气体摩尔体积的大小取决于温度和压强,故在同温同压下,气体摩尔体积近似相等,故D符合题意;
答案选D。
【题3】(2020·浙江高一期中)下列说法正确的是
A.1mol H 的体积是22. 4L
2
B.1mol HO在标准状况下的体积是22. 4L
2
C.1mol 任何气体的体积在标准状况下都约是22. 4L
D.温度为室温,压强为101kPa时,CO 气体的气体摩尔体积是22. 4L·mol-1
2
【答案】C
【详解】
A.未指明标准状况,不能用22.4L/mol计算体积,A错误;
B.HO在标准状况下不是气体,不能用22.4L/mol计算体积,B错误;
2
C.标准状况下的气体摩尔体积为22.4L/mol,则1mol 任何气体的体积在标准状况下都约是22. 4L,C正
确;
D.室温,压强为101kPa不是标准状况,气体摩尔体积不是22.4L/mol,D错误;
答案选C。
【题4】(2021·河南南阳市·南阳中学高一月考)同温同压下,下列关于氢气和氯气的叙述中,正确的是
①等体积的氢气和氯气所含的分子数相同
②氢分子间的平均距离和氯分子间的平均距离几乎是相等的
③氢分子与氯分子的大小相同
④氢分子和氯分子本身大小对于气体体积影响可以忽略不计
A.①②④ B.①②③④ C.①②③ D.①④【答案】A
【详解】
①同温同压下,体积之比等于物质的量之比,则体积的氢气和氯气所含的分子数相同,①项正确;
②气体分子间的距离主要受温度和压强的影响,同温同压下氢分子间的平均距离和氧分子间的平均距离几
乎是相等的,②项正确;
③氢原子和氧原子大小不同,则氢分子与氧分子大小也是不相同的,③项错误;
④对于气体来说,粒子之间的距离远远大于粒子本身的直径,则氢分子和氧分子本身的大小对气体体积的
影响可以忽略不计,④项正确;
答案选A。
【题5】(2021·甘肃张掖·高一期末)请回答下列问题:
(1)现有质量比为11:14的CO 和CO的混合气体,则该混合气体中碳原子和氧原子的个数比为_______,该
2
混合气体的平均摩尔质量为_______。(该空的最后结果保留一位小数)
(2)12.4gNa X中含Na+0.4 mol,则X的相对原子质量是_______。
2
(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下11.2L“人造空
气”的质量是4.8g,其中氧气和氦气的分子数之比是_______,氧气的质量是_______。
【答案】3:4 33.3 g∙mol−1 16 1:4 3.2g
【详解】
(1)现有质量比为11:14的CO 和CO的混合气体,假设CO 和CO的质量分别为11g和14g,则两者物质的
2 2
量之比为 ,则该混合气体中碳原子和氧原子的个数比为3:4,该混合气体的平均摩
尔质量为 ;故答案为:3:4;33.3 g∙mol−1。
(2)12.4gNa X中含Na+0.4 mol,则NaX物质的量为0.2mol,NaX的摩尔质量为
2 2 2
,则X的相对原子质量是16;故答案为:16。
(3)根据题意,在标准状况下11.2L“人造空气”,其物质的量为 ,质量是4.8g,
n(O )+n(He)=0.5mol,n(O )×32 g∙mol−1+n(He)×4g∙mol−1=4.8g,解得n(O )=0.1mol,n(He)=0.4mol,其
2 2 2
中氧气和氦气的分子数之比是1:4,氧气的质量是0.1mol×32 g∙mol−1=3.2g;故答案为:1:4;3.2g。
【题6】(2021·土默特左旗第三中学高一期末)对一定量气体体积的探究。已知1mol气体在不同条件下
的体积:
化学式 条件 1mol气体体积/LH 0℃,101kPa 22.4
2
O 0℃,101kPa 22.4
2
CO 0℃,101kPa 22.4
H 0℃,202kPa 11.2
2
CO 0℃,202kPa 11.2
2
N 273℃,202kPa 22.4
2
NH 273℃,202kPa 22.4
3
(1)从上表分析得出的结论:
①1mol任何气体,在标准状况下的体积都约为_______L。
②1mol不同的气体,在不同的条件下,体积_______(填“一定”“一定不”或“不一定”)相等。
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:
①气体分子数目_______(填“相等”或“不等”)
②相同条件下,气体分子间的平均距离_______(填“差距较大”“几乎相等”或“无法确定”)。
(3)应用:在标准状况下,4gO 的体积为_______L(写出计算过程)。
2
【答案】22.4 不一定 相等 几乎相等 2.8
【详解】
(1)①从上表中可以看出,1mol任何气体在标况下的体积约为22.4L,故填22.4;
②从上表数据可以看出,1mol不同气体,在不同条件下体积不一定相等,故填不一定;
(2)①根据 ,相同条件下,1mol气体的分子数目相等,故填相等;
②相同条件下,气体分子间的平均距离几乎相等,故填几乎相等;
(3)4g氧气的物质的量为 = = ,标况下 ,根据 = =2.8L,
故填2.8。
【题7】(2020·城固县第一中学高一月考)(1)在标准状况下,由 CO 和 CO 组成的混合气体 8.96L,质
2
量是 16g。此混合物中 CO 和 CO 的物质的量比是 ______________ ,CO 的体积分数是 __________,
2
CO 的质量分数是 ___________,C 和 O 的原子个数比是 _____________,混合气体的平均摩尔质量是
_____________。
(2)19g 某二价金属的氯化物 ACl 中含有 0.4mol Cl-离子,ACl 的摩尔质量是 _____,相对分子质量是
2 2
____________,A 的相对原子质量是 __________。
【答案】1:3 25% 17.5% 4:7 40g/mol 95g/mol 95 24
【详解】(1)设混合气体中CO为xmol,CO 为ymol,则 ,解得x=0.1,y=0.3,此混合物中CO和
2
CO 的物质的量比是0.1:0.3=1:3;CO的体积分数=物质的量分数= ×100%=25%;CO的质量分数是
2
×100%=17.5%;C和O的原子个数比是(0.1+0.3):(0.1+2×0.3)=4:7;混合气体的平均摩尔
质量是 =40g/mol,故答案为:1:3;25%;17.5%;4:7;40g/mol;
(2)由ACl 化学式可知,19g ACl 中含有0.2mol ACl ,因此ACl 的摩尔质量是 =95g/mol;相对分
2 2 2 2
子质量与摩尔质量数值相等,因此相对分子质量为95;A的相对原子质量是95-35.5×2=24,故答案为:
95g/mol;95;24。
提分作业
【练1】(2021·浙江高一月考)一定温度、压强条件下,决定气体体积大小的主要因素是
A.粒子数目 B.粒子大小 C.粒子间距 D.粒子种类
【答案】A
【详解】
在一定温度、压强条件下,气体分子之间的距离不变,这时影响气体体积的主要因素是气体分子数目的多
少。气体分子数越多,气体体积就越大,故此时决定气体体积大小的主要因素是粒子数目,合理选项是
A。
【练2】(2021·全国高一课时练习)下列有关气体体积的叙述正确的是
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.气体摩尔体积指1mol任何气体所占的体积,约为22.4L
【答案】B
【详解】
A.相同条件下,气体的体积由气体的分子数决定,故A错误;
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定,故B正确;
C.气体的体积不同时,所含的分子数可能相同,故C错误;
D.气体的摩尔体积的单位是L/mol,且在标注状况下气体体积为22.4L/mol,其数值随温度和压强的改变
而改变,故D错误。
故选B。【练3】(2021·上海市新场中学高二期中)下列说法正确的是
A.1mol任何气体的体积都约为22.4L
B.在标准状况下,1mol任何物质的体积都约为22.4L
C.在标准状况下,1molH O所占的体积都约为22.4L
2
D.在标准状况下,22.4LH 的物质的量约为1mol
2
【答案】D
【详解】
A.没有指明气体所处的温度、压强,故A错误;
B.标准状况下,1mol液态物质或固态物质的体积不为22.4L,故B错误;
C.水在标准状况下不是气体,故C错误;
D.标准状况下, 1mol任何气体的体积都是22.4L,故D正确;
答案选D。
【练4】(2020·浙江高一课时练习)下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5 mol H 所占体积为11.2 L
2
③标准状况下,1 mol HO的体积为22.4 L
2
④标准状况下,28 g CO与N 混合气体的体积约为22.4 L
2
⑤各种气体的气体摩尔体积都约为22.4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①②⑤ B.④⑥ C.③④⑥ D.①④⑥
【答案】B
【详解】
①标准状况下,6.02×1023个分子为1mol,但该物质不一定是气体,故所占的体积不一定是22.4L,错误;
②0.5 mol H 所处的状态不一定是标准状况,气体摩尔体积不一定是22.4L/mol,所占体积不一定是11.2
2
L,错误;
③标准状况下,HO不是气体,1 mol HO的体积不是22.4 L,错误;
2 2
④标准状况下,28 g CO与N 混合气体物质的量为1mol,体积约为22.4 L,正确;
2
⑤影响气体摩尔体积的因素有温度、压强、气体所处的状态不确定,各气体的气体摩尔体积不一定是
22.4L/mol,错误;
⑥标准状况下,体积相同的气体的分子数相同,正确;
故选B。
【练5】(2021·福建厦门双十中学高一月考)判断下列正误:
(1)①标准状况下,0.2mol任何物质的体积均为4.48L。______。
(2)②若1mol气体的体积为22.4L,则它一定处于标准状况下。______。
(3)③标准状况下,1LHCl和1LHO的物质的量相同。______。
2
(4)④常温常压下,1gH 和14gN 的体积相同。______。
2 2
(5)⑤28gCO的体积为22.4L。______。(6)⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同。______。
(7)⑦在同温同体积时,气体物质的物质的量越大,则压强越大。______。
(8)⑧同温同压下,气体的密度与气体的相对分子质量成正比。______。
(9)⑨1g氮气所占有的体积为VL,则氮气的气体摩尔体积为28VL·mol-1。______。
(10))⑩标准状况下,0.4molH 和0.6molO 的混合气体的体积约为22.4L。______。
2 2
【答案】
(1)错误
(2)错误
(3)错误
(4)正确
(5)错误
(6)错误
(7)正确
(8)正确
(9)正确
(10)正确
【分析】
(1)
标准状况下,0.2mol任何气体物质的体积均为4.48L,但所有物质并不都是气体,故错误;
(2)
若1mol气体的体积为22.4L,由于温度、压强影响气体摩尔体积,则它可能处于标准状况下,也可能不是
标况下,故错误;
(3)
标准状况下,HCl为气体,而HO不是气体,二者体积相等,它们物质的量不相等,故错误;
2
(4)
1g H 物质的量为 ,14g N 的物质的量为 ,二者物质的量相
2 2
等,标况下,二者体积相等,故正确;
(5)
28g CO为1mol,不是标况下,CO的体积不一定为22.4L ,故错误;
(6)
标况下,两种物质不一定都是气体,它们物质的量相等,占有的体积不一定相等,故错误;
(7)
在同温同体积时,气体压强与物质的量成正比,则气体物质的物质的量越大,压强越大,故正确;
(8)
同温同压下,气体的密度之比等于摩尔质量之比,也等于相对分子质量之比,即气体的密度与气体的相对分子质量成正比,故正确,
(9)
1g氮气的物质的量为 ,氮气的气体摩尔体积为VL÷ =28VL·mol-1,故正确;
(10)
混合气体的总物质的量为0.4+0.6=1mol,标准状况下体积V=nVm=1mol×22.4L/mol=22.4L,故正确。
【练6】(2021·全国高一课时练习)(1)标准状况下,0.5mol N 的体积约为___________,1.5mol O 的体积
2 2
约为___________。
(2)标准状况下,33.6L N 的物质的量为___________,8.96L CO 气体的物质的量为___________。
2 2
(3)标准状况下,2g H 的体积约为___________,11.2L CH 的质量为___________。
2 4
【答案】11.2L 33.6L 1.5mol 0.4mol 22.4L 8g
【详解】
(1)标准状况下,0.5mol N 的体积约为 11.2L,1.5mol O 的体积约为
2 2
33.6L;
(2)标准状况下,33.6L N 的物质的量为 =1.5mol,8.96L CO 气体的物质的量为
2 2
=0.4mol;
(3)标准状况下,2g H 的体积约为 22.4L,11.2L CH 的质量为 8g。
2 4
【练7】(2021·全国高一课时练习)(1)同温同压下的两个容积相同的容器中分别装有O 和O 气体,则两
2 3
瓶气体中分子数之比是___________,原子数之比是___________,密度之比是___________,质量之比是
___________。
(2)下列所给出的几组物质中:含有分子数最多的是___________;含有原子数最多的是___________;标准
状况下体积最大的是___________;质量最大的是___________。(填序号)
① 1gH ; ② 2.408×1023个CH;③ 10.8gH O; ④ 标准状况下6.72LCO
2 4 2 2
【答案】1∶1 2∶3 2∶3 2∶3 ③ ② ① ④
【详解】
(1)同温同压下的两个容积相同的容器中分别装有O 和O 气体,则两瓶气体中分子数之比是1:1,原子数
2 3
之比是 1×2:1×3=2:3,质量之比是1×32:1×48=2:3,密度之比是2:3, 故答案为:1:1;2:3;2:
3;2:3;
(2)①1gH 的物质的量为 ;②2.408×1023个CH 的物质的量为 ,原子的
2 4
物质的量为0.4mol×5=2mol,原子数最多;③10.8gH O的物质的量为 ,但标准状态下水为
2液态;④标准状况下6.72LCO 的物质的量为 ,质量为 ;则含有
2
分子数最多的是③;含有原子数最多的是②;标准状况下体积最大的是①;质量最大的是④;故答案为:
③;②;①;④。
【练8】(2019·宜昌市人文艺术高中高一月考)(1)0.5 mol CH 的质量是_____________,在标准状况下的
4
体积为____________;含电子的物质的量是_____________。
(2)同温同压下,等质量的O 和CO ,物质的量之比为______________,原子个数比为_____________,密
2 2
度比为_______________。
(3)下列数量的各物质所含原子数按由大到小的顺序排列是____________________。
①0.5 mol氨气 ②标准状况下22.4 L氦气
③4 ℃时9 mL水 ④0.2 mol磷酸钠(Na PO )
3 4
【答案】8g 11.2L 5mol 11:8 11:12 8:11 ①④③②
【分析】
(1)利用m=n M,V=n Vm进行计算;
× ×
(2)利用阿伏伽德罗定律及其推论进行分析,同温同压下,分子数之比等于物质的量之比,密度与摩尔
质量成正比;
(3)利用以物质的量为核心的有关计算公式进行计算。
【详解】
(1)m=n×M=0.5mol×16g/mol=8g;在标准状况下的体积为V=n×Vm=0.5mol×22.4L/mol=11.2L;含电子的
物质的量是0.5mol×10=5mol;
(2)同温同压下,等质量的O 和CO ,物质的量之比为 : =11:8;原子个数之比
2 2
=11:12,同温同压下密度与摩尔质量成正比,故密度之比是32:44=8:11;
(3)①0.5mol氨气中含原子为0.5mol×4=2.0mol;
②标准状况下22.4L氦气含原子为 =1.0mol;
③4℃时9mL水中含原子为 ×3=1.5mol;
④0.2mol磷酸钠(NaPO )中含原子为0.2mol×8=1.6mol;
3 4
则所含原子数按由大到小的顺序为①④③②。关注更新免费领取,淘宝唯一每月更新店铺:知二教育