文档内容
2007年江苏省初中学生化学素质和实验能力竞赛初赛试题(调研测试)
(120分钟满分100分)
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23
S-32 C1-35.5 K-39 Ca-40 Mn-55 Fe-56 Cu-64
一、选择题(本题包括16个小题,每小题2分,共32分。每小题有1个或2个选项符合题意。
若有两个答案的错选1个不得分,漏选1个扣1分)
1.从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事,
这个先后顺序跟下列哪些因素有关:①地壳中金属元素的含量,②金属活动性顺序,
③金属的导电性能,④金属冶炼的难易程度,⑤金属的延展性 ( )
A.①③ B.②⑤ C.③⑤ D.②④
2.根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论。下列说法正确
的是 ( )
A.水是由氢分子和氧分子构成的
B.水是由氢原子和氧原子直接构成的
C.试管a、b中所得气体的质量比约为2∶1
D.试管a、b中所得气体的体积比约为2∶1
3.若用右图装置来制取气体,应满足下列条件中的
( )
①反应物是固体②反应需要加热③制得的气体不易溶于
水④制得的气体密度比空气大
A.①② B.②④
C.①②③ D.①②③④
4.人体内含有多种元素,其中许多元素都是人体所需的。但有些元素尚未证实其生理功
能,在食品中它们的含量稍高会引起毒性反应。我国食品卫生法对这些元素在食品中的含量
的最高标准有极严格的规定,这些元素是 ( )
①Na ②Mg ③As ④Cd ⑤Ca ⑥Zn ⑦Hg ⑧Pb ⑨Fe ⑩ K
A.⑥⑦⑧⑨ B.②④⑥⑧ C.③④⑦⑧ D.②④⑥⑦⑧
5.世界卫生组织(WHO)将某氧化物RO 列为A级高效安全灭菌消毒剂,它在食品保鲜、
2
饮用水消毒等方面有着广泛应用。实验测得该氧化物中R与O的质量比为71∶64,则RO 的
2
化学式为 ( )
A.CO B.ClO C.SO D. NO
2 2 2 2
6.葡萄糖(C H O)供给人体活动和维持体温所需能量的反应可表示为:
6 12 6
C H O6 +6O 6CO + 6HO
6 12 2 2 2
下列分析错误的是 ( )
A.医疗上可用一定质量分数的葡萄糖溶液给病人输液以补充能量
B.葡萄糖缓慢氧化转变成二氧化碳和水,同时产生能量
C.人呼出的气体和吸人的空气的成分相比,CO 和HO的含量增加,O 的含量减少
2 2 2
D.葡萄糖氧化产生的CO 如不能及时排出人体,则血液的pH将增大
2
7.室温下,在pH= 13的溶液中不可能大量共存的是 ( )
A. Fe3+、C1一、SO 2一、Na + K+、SO 2一、CO2一、Cl一
4 4 3
C. K+、 Na+、Ba2+、NO 一 D. H +、CO2一、C1一、Ca2+
3 3
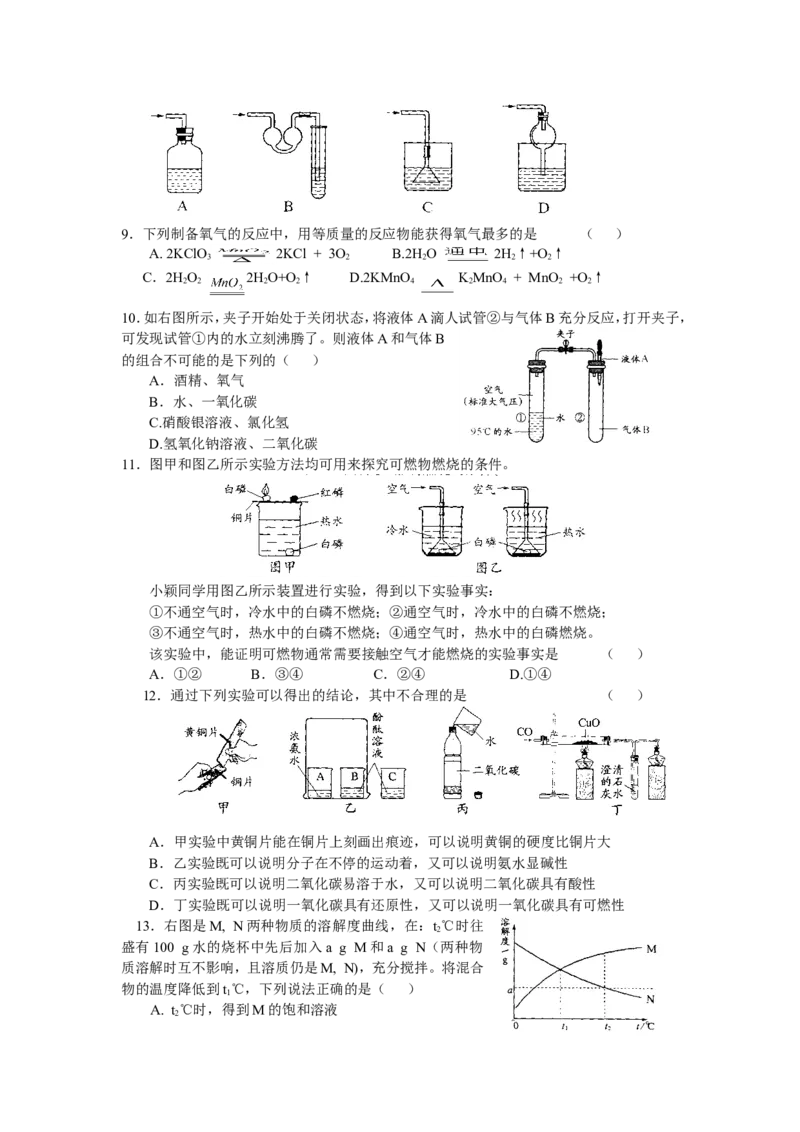
8.以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是( )9.下列制备氧气的反应中,用等质量的反应物能获得氧气最多的是 ( )
A. 2KClO 2KCl + 3O B.2H O 2H↑+O ↑
3 2 2 2 2
C.2HO 2HO+O↑ D.2KMnO KMnO + MnO +O ↑
2 2 2 2 4 2 4 2 2
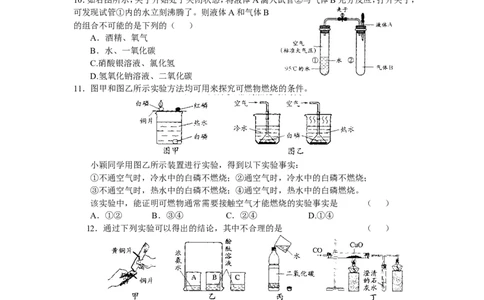
10.如右图所示,夹子开始处于关闭状态,将液体A滴人试管②与气体B充分反应,打开夹子,
可发现试管①内的水立刻沸腾了。则液体A和气体B
的组合不可能的是下列的( )
A.酒精、氧气
B.水、一氧化碳
C.硝酸银溶液、氯化氢
D.氢氧化钠溶液、二氧化碳
11.图甲和图乙所示实验方法均可用来探究可燃物燃烧的条件。
小颖同学用图乙所示装置进行实验,得到以下实验事实:
①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;
③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。
该实验中,能证明可燃物通常需要接触空气才能燃烧的实验事实是 ( )
A.①② B.③④ C.②④ D.①④
12.通过下列实验可以得出的结论,其中不合理的是 ( )
A.甲实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大
B.乙实验既可以说明分子在不停的运动着,又可以说明氨水显碱性
C.丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性
D.丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性
13.右图是M, N两种物质的溶解度曲线,在:t℃时往
2
盛有100 g水的烧杯中先后加入a g M和a g N(两种物
质溶解时互不影响,且溶质仍是M, N),充分搅拌。将混合
物的温度降低到t℃,下列说法正确的是( )
1
A. t℃时,得到M的饱和溶液
2B. t℃时,得到N的不饱和溶液
2
C.温度降低到t℃时,M, N的溶质质量分数相等,得到M, N的不饱和溶液
l
D.温度降低到t℃时,M, N的溶解度相等,得到M, N的饱和溶液
1
14.学习化学时会遇到一些与“相等”有关的规律,不列有关“相等”的说法中错误的是
( )
A.微粒中的质子总数和电子总数一定相等
B.中和反应中参加反应的酸和碱的质量一定相等
C.溶液稀释前后,溶质的质量一定相等
D.物质发生化学变化前后,元素的种类数一定相等
15.超临界CO 流体是一种和水相似、能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶
2
剂”。下列说法正确的是 ( )
①超临界CO 流体性质特殊,因此,与干冰的化学组成不同②CO 是自然界中存在的
2 2
物质,它参与自然界的碳元素循环③超临界CO 流体是一种特殊的物质,容易燃烧④超临界
2
CO 流体可代替许多有害、有毒、易燃的溶剂
2
A.①② B.②④ C.①③ D.①②③④
16.将下列各组中的物质混合,若每组中最后一种物质过量,充分反应后过滤,则滤纸上仅
留下一种不溶物(纯净物)的是 ( )
①NaOH溶液、MgCl 溶液、硝酸 ②BaC1 溶液、NaNO 溶液、稀硫酸
2 2 3
③CuCl 溶液、FeCl 溶液、锌粒 ④NaCl溶液、AgNO 溶液、盐酸
2 3 3
⑤Fe (SO ) 溶液、NaNO 溶液、Ba(OH) 溶液
2 4 3 3 2
A.①④ B.②③ C.③⑤ D.②④
二、填空题(本题包括9小题,共35分)
17.(4分)钨(W)是我国丰产元素,广泛用作灯泡的灯丝,有“光明使者”的美誉。
(1)钨用作灯丝,主要利用它的 (填物理性质);
(2)钨的原子结构示意图如右图所示,则钨原子核外电子总数为 ;
(3)冶炼钨的一个阶段是用炭、氢气等还原剂在高温条件下把氧化钨
(WO)还原为金属钨。为了获得纯度较高的钨,应选择 (选填“氢气”或“炭”)
3
作还原剂,写出所选物质还原氧化钨的化学方程式 。
18.(3分)某同学探究盐溶液发生复分解反应的规律,做了以下实验:
实验 现象
①向5mLCuSO 溶液中加入5mL NaCl溶液 无明显现象
4
②向5mLCuSO 溶液中加入5mL BaCl 溶液 有白色沉淀产生
4 2
由上述实验分析,生成的白色沉淀与 离子和 离子有关。用硫酸钠和硝
酸钡混合也得到了这种白色沉淀,请写出该反应的化学方程式 。
19.(3分)取一定质量的某可燃物在足量氧气中充分燃烧得到44 g二氧化碳和36 g水。
则 (1)该可燃物的质量至少 g;
(2)另取该可燃物16g在氧气中完全燃烧,消耗氧气 24 g。该可燃物的组成元素为
,各元素的质量比为 。
20.(4分)某品牌脱脂奶粉包装上标出的配料如下:①白砂糖;②脱脂乳;③乳酸亚铁;④
维生素A;⑤维生素D等,请写出(填序号)
(1)配料中能产生能量的物质是 ;
(2)该产品配料中属于营养素的有 ;
(3)人体中缺少铁元素会引起贫血,该奶粉中可以补充铁的物质是 ;(4)蛋白质是重要的营养物质,处于生长发育期的青少年需要量很大。除奶制品外,很
多食物也能提供丰富的蛋白质,下列食物a.大米、b.花生油、c。鱼、d大豆、e.萝
卜。能提供丰富蛋白质的食物有 。
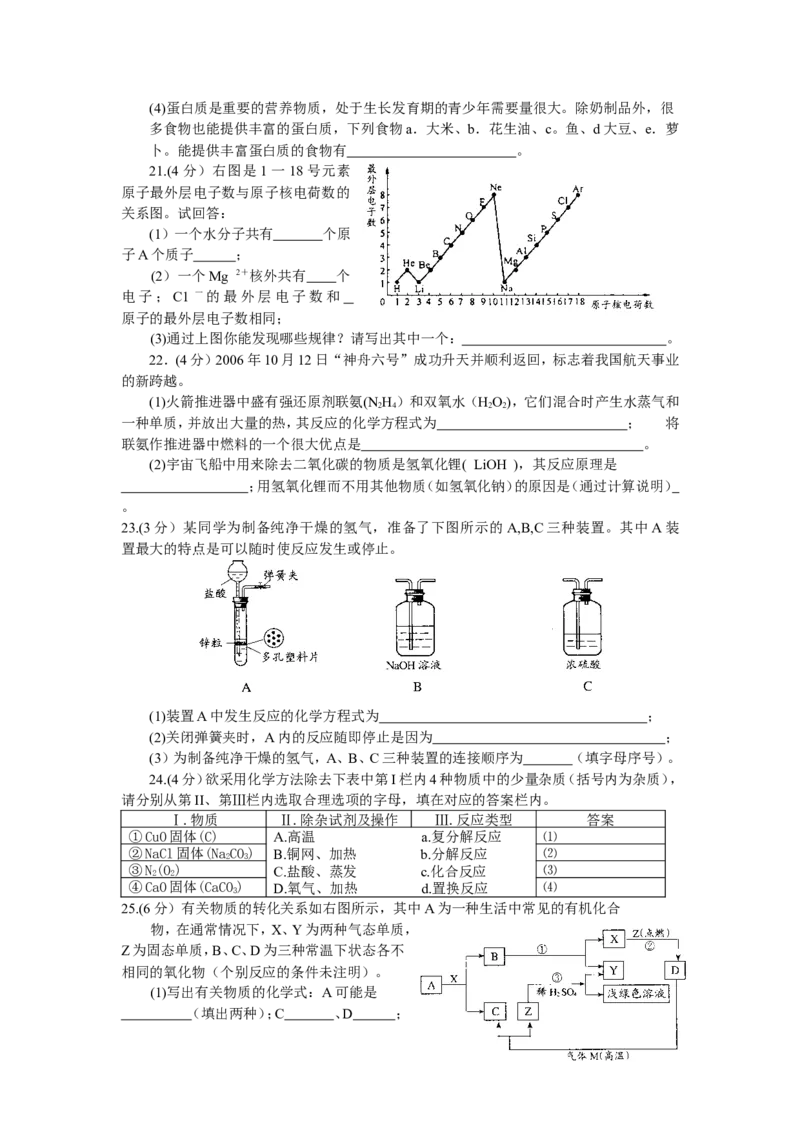
21.(4分)右图是1一18号元素
原子最外层电子数与原子核电荷数的
关系图。试回答:
(1)一个水分子共有 个原
子A个质子 ;
(2)一个Mg 2+核外共有 个
电子;C1 一的最外层电子数和
原子的最外层电子数相同;
(3)通过上图你能发现哪些规律?请写出其中一个: 。
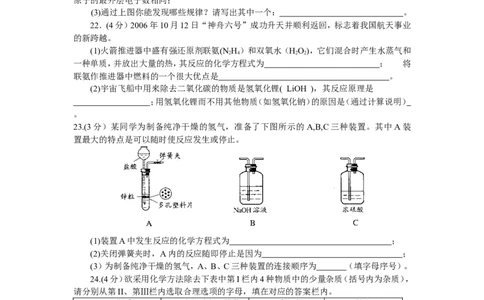
22.(4分)2006年10月12日“神舟六号”成功升天并顺利返回,标志着我国航天事业
的新跨越。
(1)火箭推进器中盛有强还原剂联氨(N H)和双氧水(HO),它们混合时产生水蒸气和
2 4 2 2
一种单质,并放出大量的热,其反应的化学方程式为 ; 将
联氨作推进器中燃料的一个很大优点是 。
(2)宇宙飞船中用来除去二氧化碳的物质是氢氧化锂( LiOH ),其反应原理是
;用氢氧化锂而不用其他物质(如氢氧化钠)的原因是(通过计算说明)
。
23.(3分)某同学为制备纯净干燥的氢气,准备了下图所示的A,B,C三种装置。其中A装
置最大的特点是可以随时使反应发生或停止。
(1)装置A中发生反应的化学方程式为 ;
(2)关闭弹簧夹时,A内的反应随即停止是因为 ;
(3)为制备纯净干燥的氢气,A、B、C三种装置的连接顺序为 (填字母序号)。
24.(4分)欲采用化学方法除去下表中第I栏内4种物质中的少量杂质(括号内为杂质),
请分别从第II、第Ⅲ栏内选取合理选项的字母,填在对应的答案栏内。
Ⅰ.物质 Ⅱ.除杂试剂及操作 Ⅲ.反应类型 答案
①CuO固体(C) A.高温 a.复分解反应 ⑴
②NaCl固体(NaCO) B.铜网、加热 b.分解反应 ⑵
2 3
③N
2
(O
2
) C.盐酸、蒸发 c.化合反应 ⑶
④CaO固体(CaCO
3
) D.氧气、加热 d.置换反应 ⑷
25.(6分)有关物质的转化关系如右图所示,其中A为一种生活中常见的有机化合
物,在通常情况下,X、Y为两种气态单质,
Z为固态单质,B、C、D为三种常温下状态各不
相同的氧化物(个别反应的条件未注明)。
(1)写出有关物质的化学式:A可能是
(填出两种);C 、D ;(2)写出M的一种用途 ;
(3)写出反应①的化学方程式 。
三、实验题 (本题共3小题,共23分)
26.(6分)已知木炭粉和Fe O 反应的化学方程式
2 3
为:2Fe O + 3C 高温 4Fe+3CO ↑。某同学设计一个
2 3 2
实验,证明氧化铁中含有氧元素,并测定氧化铁中氧
元素的质量分数,实验装置如右图。
(1)实验中,盛放澄清石灰水的烧杯中出现的现象是 ,
原因是 ;
(2)实验中通入的气体是纯净干燥的N,写出不用空气的主要理由
2
,实验也不能用潮湿的氮气,原因是
。
(3)如用3.2g氧化铁与木炭粉的混合物反应,测的澄清石灰水增重1.32g,则氧化铁中氧元
素的质量分数为 。
27.(8分)化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸
反应,测定反应后生成的CO 质量,再根据CO 的质量求出样品中碳酸钙的质量。
2 2
(1)为测定CO 的质量,他们想出了以下a、b、c三种方案,请填空以帮助他们完成设计方
2
案:
a.可称量反应前后物质总质量的减小量。
b.可称量吸收CO 前后盛有氢氧化钠溶液容器质量的 (选填“增大”或“减小”)
2
量。
c.选用右图 装置可测量产生的
CO 的 ,再利用此时CO 的 ,可计
2 2
算CO 的质量。图中瓶内水面上油层的作用
2
是 。
(2)下表是五组学生按方案 a 所测得的数
据。
小组 取用石灰石样品质量 测得CO 的质量 碳酸钙的质量分数
2
① 1.0g 0.90g 204%
② 2.0g 0.80g 91%
③ 2.5g 1.0g 93%
④ 3.0g 1.2g 92%
⑤ 4.0g 1.5g 85.7%
根据上表所得数据,该样品中碳酸钙质量分数的平均值为 ;在此实验
中,导致碳酸钙质量分数比室际值偏高的可能原因 ,
碳酸钙质量分数比实际值偏低的可能原因有 。
28.(9分)请你参与某学习小组进行研究性学习的过程,并协助完成相关任务。
【研究课题】探究热水壶底部水垢的主要成分;
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含有Ca2+、Mg2+、HCO 一等离子,
3
在加热条件下,这些离子趋于生成溶解度更小的物质—水垢,水垢的主要成分是碳酸盐和碱。
同时,他们还查阅到下列有关物质的溶解性:
物质 Ca(HCO ) Mg(HCO ) Ca(OH) Mg(OH) CaCO MgCO
3 2 3 2 2 2 3 3
溶解性 可溶 可溶 微溶 不溶 不溶 微溶
【提出猜想】水垢的主要成分一定含有Mg(OH) 和 ,可能含有Ca(OH) 和 。
2 2
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加人适量蒸馏水充分搅拌,取 上
层清液加入 ,没有白色沉淀,说明水垢中无Ca(OH) 。
2(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分。其主要实验步 骤
如下:
①按下图组装仪器,将50 g水垢试样放入锥形瓶中,加入足量某酸溶液;
②测量一定时间内干燥管内物质增加的质量(见下列曲线);
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变。
讨论:
a.步骤①加入样品前还应检查 ,所加的酸溶液是 。
b.装置Ⅱ的作用是 ;从导管A处缓缓鼓入一定的空气时,装
置Ⅰ的作用是 。
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO 的理由是
3
。
【实验结论】通过上述探究可知:水垢的主要成分有 。
四、计算题(本题共2小题,共10分)
29.(5分)某化学兴趣小组在做Fe和CuSO 溶液反应实验时,发现生成Cu的同时有气泡产
4
生。为了进一步研究做了如下实验:
①取8.5 g Fe粉放入一定量的CuSO 中,
4
反应完成后,滤出固体,洗涤、干燥后称量,固
体质量为9.2 g 。
②将 9.2g固体与一定质量分数的稀盐酸
充分反应,消耗盐酸50.0g,根据实验绘制反应
产生氢气的质量与反应时间的关系见右图。求:
(1)稀盐酸的质量分数、与稀盐酸反应的Fe的质量。
(2)与CuSO 反应的Fe的质量。
4
(3)与CuSO 反应的Fe的质量及与盐酸反应的Fe的质量之和 8.5g(选填“>”、
4
“<”或“=”)。对此结果作出你的解释。
30.(5分)航天技术中的火箭推进剂可用醇类为燃料,液态氧为氧化剂,但后者的沸点较
低(-183℃),需要额外的隔热装置,因而增加了火箭的重量。为了避免此缺点,可用过 氧
化氢(H O)代替液态氧,它具有相对高的沸点和较低的凝固点,而且没有毒性,和醇反应时
2 2
也能放出很高的能量。现有一液体推进剂以醇(含碳52%、含氢13%、含氧35%)为燃料,质
量分数为90%的过氧化氢做氧化剂,欲使1 kg该醇燃料完全燃烧,计算需消耗质量分数为
90%的过氧化氢的质量(提示:可按2 HO→2HO + O↑得到的氧气与醇反应来计算)。
2 2 2 22007年江苏省初中学生化学素质和实验能力竞赛初赛试题(调研测试)
参考答案及评分标准
一、选择题(每题2分,共32分)
1、D 2、D 3、C 4、C 5、B 6、D 7、AD 8、BD 9、B 10、AB 11、B 12、C
13、C 14、AB 15、B 16、D
二、填空题(共35分)
17.(4分)
(1)熔点高(1分)(2)74 (1分)(3)氢气(1分)(4) 3H+ WO 高温 3HO + W ( 1分)
2 3 2
18.(3分)
(1) SO 2一(1分)(2)Ba2 +(1分)(3) NaSO + Ba(NO ) = BaSO↓+2NaNO(1分)
4 2 4 3 2 4 3
19.(3分)
(1)16(1分)(2)C、H、O(1分)m (C):m (H):m (O)=3:1:4(1分)
20.(4分)
(1)①②(1分)(2) ①②③④⑤(1分)(3) ③(1分)(4)c, d(1分)
21.(4分)
(1)3、10(1分) (2)10 Ar(或Ne)(1分)
(3)随着原子核电荷数的递增,元素原子最外层电子数呈现周期性变化(2分)
22.(4分)
(1)N H+2H O==N + 4HO (1分)高能(或污染少)(1分)
2 4 2 2 2 2
(2) CO +2LiOH=Li CO+ HO (1分)吸收等质量的CO 所需要的LiOH比NaOH少得
2 2 3 2 2
多(由反应式可知.吸收等质量的CO 所需LiOH和NaOH的质量比为24/40= 3/5) (1分)
2
23.(3分)
(1) Zn+2HCl= ZnCl+ H↑(1分)
2 2
(2)反应产生的氢气使试管A内压强增大,盐酸被压进长颈漏斗与锌粒脱离接触,反应即
停止((1分)
(3)A→B→C(1分)
24.(4分)
(1)D c(1分)(2)C a(1分) (3)B c(1分) (4 )A b(1分)
25.(6分)
(1)CH 、C HOH(其他合理答案亦可)(2分)CO (1分)Fe O (l分)
4 2 5 2 2 3
(2)作燃料(其他合理答案均给分)(1分)
(3)2 HO通电 2H↑+O ↑ (1分)
2 2 2
三、实验题(共23分)
26.(6分)
(1)澄清石灰水变浑浊(1分)石灰水与二氧化碳反应生成碳酸钙(1分)
(2)空气中含有O,能与碳反应生成CO ,会影响实验的准确性(( 1分)潮湿的N 中有
2 2 2
水蒸气,影响实验结果(1分)
(3) 30% (2分)
27.(8分)
(1)增大(1分)甲(1分)体积(1分)密度(1分)防止二氧化碳溶于水(2分)
(2)92% (1分)泡沫溢出或样品粉末撒落(1分)(其它合理答案亦可)试样未充分反应或搅
拌不充分((1分)(其它合理答案亦可)28.(9分)
[提出猜想]CaCO ( 1分)Mg CO(1分)
3 3
[设计方案](1)Na CO 溶液(1分)
2 3
(2)装置的气密性(1分)稀盐酸(1分)
吸收CO 中的水蒸气((l分)除去空气中的CO (1分)
2 2
即使50 g水垢全部为CaCO ,产生CO 的质量应为22 g,而实验测得生
3 2
成的CO 质量为 24 g,大于22 g (1分)
2
[实验结论]Mg(OH) ,、CaCO 、MgCO (1分)
2 3 3
四、计算题(共10分)
29.(5分)
解:(l)设9.2 g固体中Fe的质量为x,盐酸的质量分数为w。
Fe+2HC1===== FeC1 +H↑*
2 2
56 73 2
x 50.0g×w 0.10g
56:2=x:0.10g x=2.8 g(1分)
73:2=50.0g×w :0. 10 g w =7.3% (1分)
(2)设与CuSO 反应的Fe的质量为y
4
Fe+ CuSO ==FeSO +Cu
4 4
56 64
y (9.2一2.8)g
56:64= y:(9.2一2.8) g y=5.6g (1分)
(3) < (1分)因为有少量Fe与CuSO 溶液中的酸性物质发生了反应(1分)
4
30.(5分)
解:设1 kg该醇燃料的碳和氢完全燃烧,分别消耗氧气的质量为x和y
则:C ~ O 4H ~ O
2 2
12 32 4 32
1000 g×52% x 1000 g ×13% y
x=32 ×1000 g×52%/12=1387 g(1分)
y=32× 1000 g ×13%/4=1040 g (1分)
则1 kg该醇燃料完全燃烧消耗氧气的质量为1387g +1040 - 1000g×35% = 2077 g (1
分)
设需HO 2的质量为w
2 2
2HO==2 HO+O↑
2 2 2 2
2 ×34 32
w 2077 g
w=2×34×2077 g/32=4414 g-(1分)
需质量分数为90%的HO 的质量为:4414 g/90%==4904 g ( 1分)
2 2