文档内容
2009年全国初中学生化学素质和实验能力竞赛
河南赛区预赛试卷
(时间:120分钟 满分:100分)
题 号 一 二 三 四 总分
得 分
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 Cl:35.5
K:39 Ca:40 Mn:55 Fe :56 Cu:64 Zn :65
一、选择题(本题包括20个题,每题1分,共20分。每题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
答案
1.运用2008年诺贝尔化学奖的研究成果,可依据生物发光现象检测超微量钙的存在。这里
的“钙”是指
A.分子 B.原子 C.元素 D.单质
2.下列过程中主要只涉及物理变化的是
A.浓硫酸使白纸变黑 B.用灼烧法鉴别羊毛和合成纤维
C.生石灰遇水变成熟石灰 D.用酒精浸泡紫罗兰花自制酸碱指示剂
3.食品安全与人体健康密切相关。下列做法不会损害人体健康的是
A.用含小苏打的发酵粉焙制糕点 B.用甲醛浸泡水产品
C.用含NaNO 的工业盐烹调食品 D.用霉变花生制成压榨花生油
2
4.前者属于混合物,后者属于纯净物的一组物质是
A.干冰、空气 B.食醋、加碘食盐 C.甲烷、烧碱 D.汽水、冰水共存物
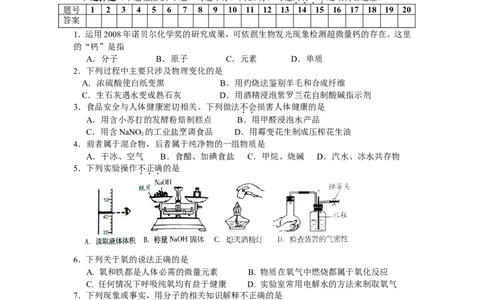
5.下列实验操作不正确的是
6.下列关于氧的说法正确的是
A. 氧和铁都是人体必需的微量元素 B. 物质在氧气中燃烧都属于氧化反应
C. 任何情况下呼吸纯氧均有益于健康 D. 实验室常用电解水的方法来制取氧气
7.下列现象或事实,用分子的相关知识解释不正确的是
A.一滴水中大约有1.67×1021个水分子,说明分子很小
B.石油气加压后可贮存在钢瓶中,说明分子之间有间隙
C.水沸腾时可掀起壶盖,说明分子大小随温度升高而增大
D.湿衣服晾在太阳下干得快,说明分子运动速率与温度有关
8.下列化学方程式符合题意且书写正确的是
A.用盐酸除铁锈:FeO+2HCl == FeCl +H O
2 2
B.正常雨水的pH约为5.6的原因:CO + H O == HCO
2 2 2 3
C.医疗上用碱性物质中和过多胃酸:NaOH + HCl == NaCl + H O
2
D.除去氯化钠中少量的碳酸钠:NaCO+H SO == NaSO +H O +CO↑
2 3 2 4 2 4 2 2
9.下列实验现象和对应的结论描述都正确的是A.向某固体上滴加稀盐酸,有气泡产生一一该固体一定是碳酸盐
B.向某无色溶液中滴入酚酞试液,溶液变红色——该溶液一定是碱溶液
C.某固态化肥与熟石灰混合研磨后产生氨味——该化肥一定是铵态氮肥
D.把燃着的木条伸入某无色气体中,木条熄灭——该气体一定是二氧化碳
10.课本中的图表、数据等可以提供很多信息。下面有关的说法不正确的是
A. 根据相对分子质量可比较气体的密度大小
B. 根据某元素的原子结构示意图可判断该元素原子核内中子的数目
C. “酸、碱和盐溶解性表”是判断复分解反应能否发生的依据之一
D. 根据不同物质的溶解度曲线图,可确定混合溶液的分离方法
11.已知甲、乙、丙、丁四种物质在化学反应中的关系为:甲+乙→丙+丁。下列有关说法正确
的是
A.若取10g甲和20g乙反应,则生成的丙和丁的质量总和一定为30g
B.若丙和丁分别为盐和水,则甲和乙一定属于酸和碱
C.若该反应为复分解反应,则生成物中一定有水生成
D.若甲和丁均为单质,乙和丙均为化合物,则该反应一定属于置换反应
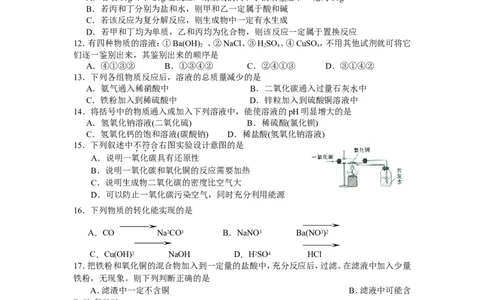
12.有四种物质的溶液:①Ba(OH) 、②NaCl、③HSO 、④CuSO ,不用其他试剂就可将它
2 2 4 4
们逐一鉴别出来,其鉴别出来的顺序是
A.④①③② B.①③④② C.②④①③ D.③①④②
13.下列各组物质反应后,溶液的总质量减少的是
A.氨气通入稀硝酸中 B.二氧化碳通入过量石灰水中
C.铁粉加入到稀硫酸中 D.锌粒加入到硫酸铜溶液中
14.将括号中的物质通入或加入下列溶液中,能使溶液的pH明显增大的是
A.氢氧化钠溶液(二氧化硫) B.稀硫酸(氯化钡)
C.氢氧化钙的饱和溶液(碳酸钠) D.稀盐酸(氢氧化钠溶液)
15.下列叙述中不符合右图实验设计意图的是
A.说明一氧化碳具有还原性
B.说明一氧化碳和氧化铜的反应需要加热
C.说明生成物二氧化碳的密度比空气大
D.可以防止一氧化碳污染空气,同时充分利用能源
16.下列物质的转化能实现的是
A.CO Na2CO3 B.NaNO3 Ba(NO3)2
C.Cu(OH)2 NaOH D.H2SO4 HCl
17.把铁粉和氧化铜的混合物加入到一定量的盐酸中,充分反应后,过滤。在滤液中加入少量
铁粉,无现象。则下列判断正确的是
A.滤渣中一定不含铜 B.滤液中可能含
FeCl 和HCl
2
C.滤渣可能是铜和铁的混合物 D.滤液中一定含FeCl 和CuCl
2 2
18.4.6g某有机物完全燃烧需9.6g氧气,可生成8.8gCO 和5.4gH O,则该有机物
2 2
A.只含碳、氢两种元素 B.含有碳、氢、氧三种元素
C.含有碳、氢两种元素,可能含氧元素 D.含有碳、氢两种元素,不含氧元素
19.下列各物质无论以何种比例混合,其氯元素的质量分数不变的是
A.HClO、KClO B.NaClO、KCl C.KClO、KCl D.NaCl、KCl
4 3
20.在托盘天平两边各放一只烧杯并注入相同的足量稀盐酸,调节至平衡,然后向左、右两边
烧杯中分别投入等质量的镁和铝,则天平指针的偏转情况是
A.先偏向左,最后偏向右 B.先偏向右,最后平衡
C.先偏向右,最后偏向左 D.先偏向左,最后平衡
3
+NaOH +BaCO
2
+NaCl +BaCl二、填空题(本题包括8个题,共30分)
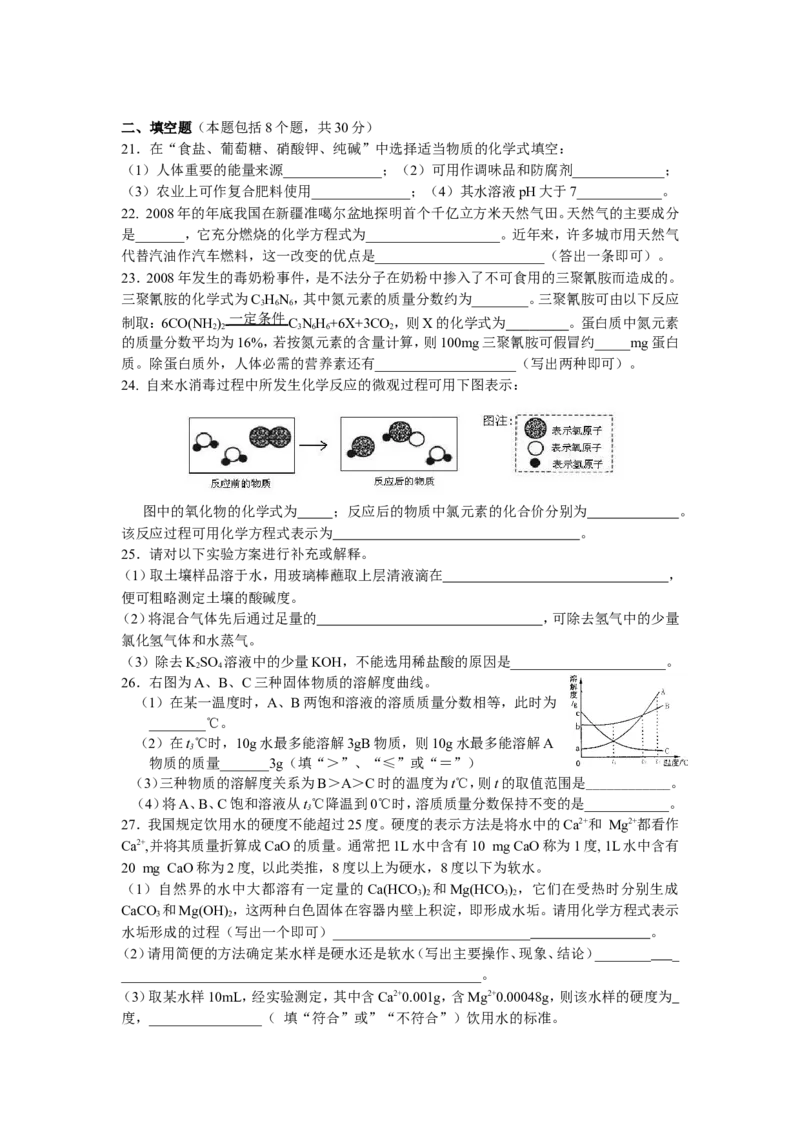
21.在“食盐、葡萄糖、硝酸钾、纯碱”中选择适当物质的化学式填空:
(1)人体重要的能量来源______________;(2)可用作调味品和防腐剂_____________;
(3)农业上可作复合肥料使用______________;(4)其水溶液pH大于7____________。
22. 2008年的年底我国在新疆准噶尔盆地探明首个千亿立方米天然气田。天然气的主要成分
是_______,它充分燃烧的化学方程式为___________________。近年来,许多城市用天然气
代替汽油作汽车燃料,这一改变的优点是________________________(答出一条即可)。
23.2008年发生的毒奶粉事件,是不法分子在奶粉中掺入了不可食用的三聚氰胺而造成的。
三聚氰胺的化学式为C HN,其中氮元素的质量分数约为________。三聚氰胺可由以下反应
3 6 6
制取:6CO(NH)
一定条件
C NH+6X+3CO ,则X的化学式为________。蛋白质中氮元素
2 2 3 6 6 2
的质量分数平均为16%,若按氮元素的含量计算,则100mg三聚氰胺可假冒约_____mg蛋白
质。除蛋白质外,人体必需的营养素还有____________________(写出两种即可)。
24. 自来水消毒过程中所发生化学反应的微观过程可用下图表示:
图中的氧化物的化学式为 ;反应后的物质中氯元素的化合价分别为 。
该反应过程可用化学方程式表示为 。
25.请对以下实验方案进行补充或解释。
(1)取土壤样品溶于水,用玻璃棒蘸取上层清液滴在 ,
便可粗略测定土壤的酸碱度。
(2)将混合气体先后通过足量的 ,可除去氢气中的少量
氯化氢气体和水蒸气。
(3)除去KSO 溶液中的少量KOH,不能选用稀盐酸的原因是______________________。
2 4
26.右图为A、B、C三种固体物质的溶解度曲线。
(1)在某一温度时,A、B两饱和溶液的溶质质量分数相等,此时为
________℃。
(2)在t℃时,10g水最多能溶解3gB物质,则10g水最多能溶解A
3
物质的质量_______3g(填“>”、“≤”或“=”)
(3)三种物质的溶解度关系为B>A>C时的温度为t℃,则t的取值范围是____________。
(4)将A、B、C饱和溶液从t℃降温到0℃时,溶质质量分数保持不变的是____________。
3
27.我国规定饮用水的硬度不能超过25度。硬度的表示方法是将水中的Ca2+和 Mg2+都看作
Ca2+,并将其质量折算成CaO的质量。通常把1L水中含有10 mg CaO称为1度, 1L水中含有
20 mg CaO称为2度, 以此类推,8度以上为硬水,8度以下为软水。
(1)自然界的水中大都溶有一定量的Ca(HCO ) 和Mg(HCO ) ,它们在受热时分别生成
3 2 3 2
CaCO 和Mg(OH) ,这两种白色固体在容器内壁上积淀,即形成水垢。请用化学方程式表示
3 2
水垢形成的过程(写出一个即可)____________________________ 。
(2)请用简便的方法确定某水样是硬水还是软水(写出主要操作、现象、结论)________ _
___________________________________________________。
(3)取某水样10mL,经实验测定,其中含Ca2+0.001g,含Mg2+0.00048g,则该水样的硬度为
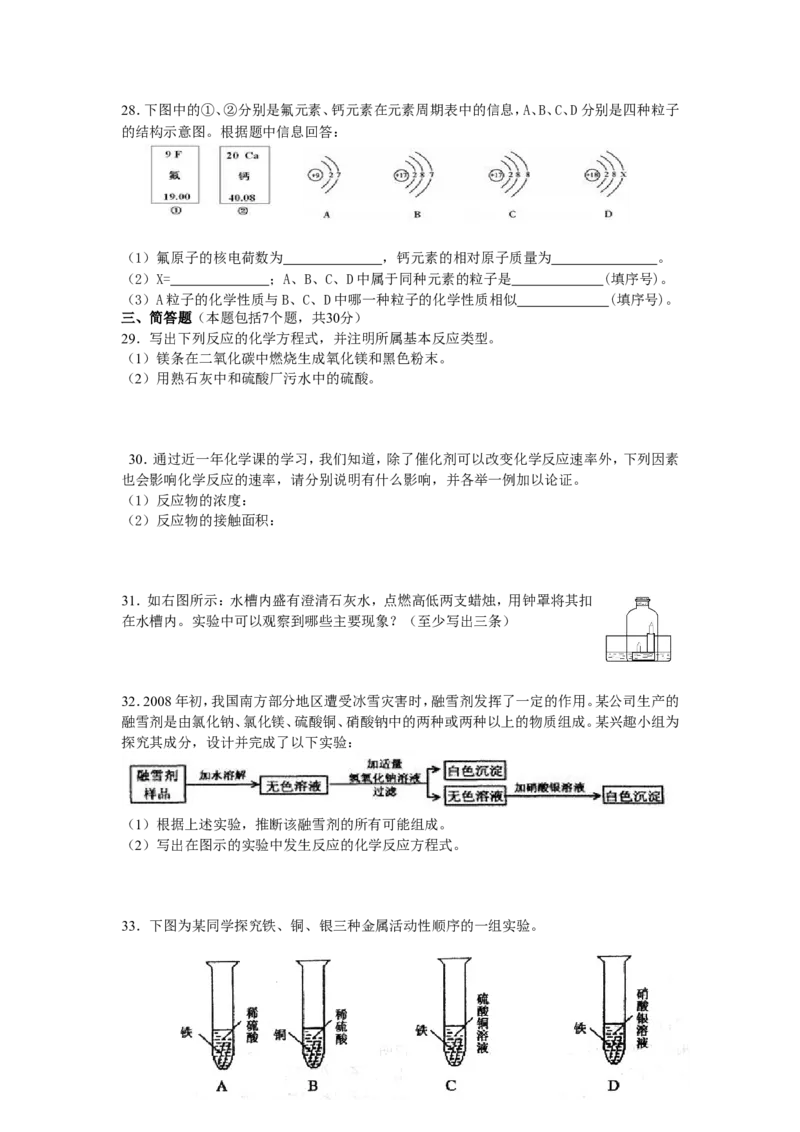
度,________________( 填“符合”或”“不符合”)饮用水的标准。28.下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子
的结构示意图。根据题中信息回答:
(1)氟原子的核电荷数为 ,钙元素的相对原子质量为 。
(2)X= ;A、B、C、D中属于同种元素的粒子是 (填序号)。
(3)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 (填序号)。
三、简答题(本题包括7个题,共30分)
29.写出下列反应的化学方程式,并注明所属基本反应类型。
(1)镁条在二氧化碳中燃烧生成氧化镁和黑色粉末。
(2)用熟石灰中和硫酸厂污水中的硫酸。
30.通过近一年化学课的学习,我们知道,除了催化剂可以改变化学反应速率外,下列因素
也会影响化学反应的速率,请分别说明有什么影响,并各举一例加以论证。
(1)反应物的浓度:
(2)反应物的接触面积:
31.如右图所示:水槽内盛有澄清石灰水,点燃高低两支蜡烛,用钟罩将其扣
在水槽内。实验中可以观察到哪些主要现象?(至少写出三条)
32.2008年初,我国南方部分地区遭受冰雪灾害时,融雪剂发挥了一定的作用。某公司生产的
融雪剂是由氯化钠、氯化镁、硫酸铜、硝酸钠中的两种或两种以上的物质组成。某兴趣小组为
探究其成分,设计并完成了以下实验:
(1)根据上述实验,推断该融雪剂的所有可能组成。
(2)写出在图示的实验中发生反应的化学反应方程式。
33.下图为某同学探究铁、铜、银三种金属活动性顺序的一组实验。(1)上述实验中,有气泡产生的是哪个实验?
(2)我国古代“湿法冶金”就是利用了C中的反应原理,请写出该反应的化学方程式。
(3)通过上述实验,还不能证明铁、铜、银三种金属的金属活动性顺序,请你在此基础上补充
一个实验帮助这位同学达到实验目的(写出实验步骤、现象及结论)。
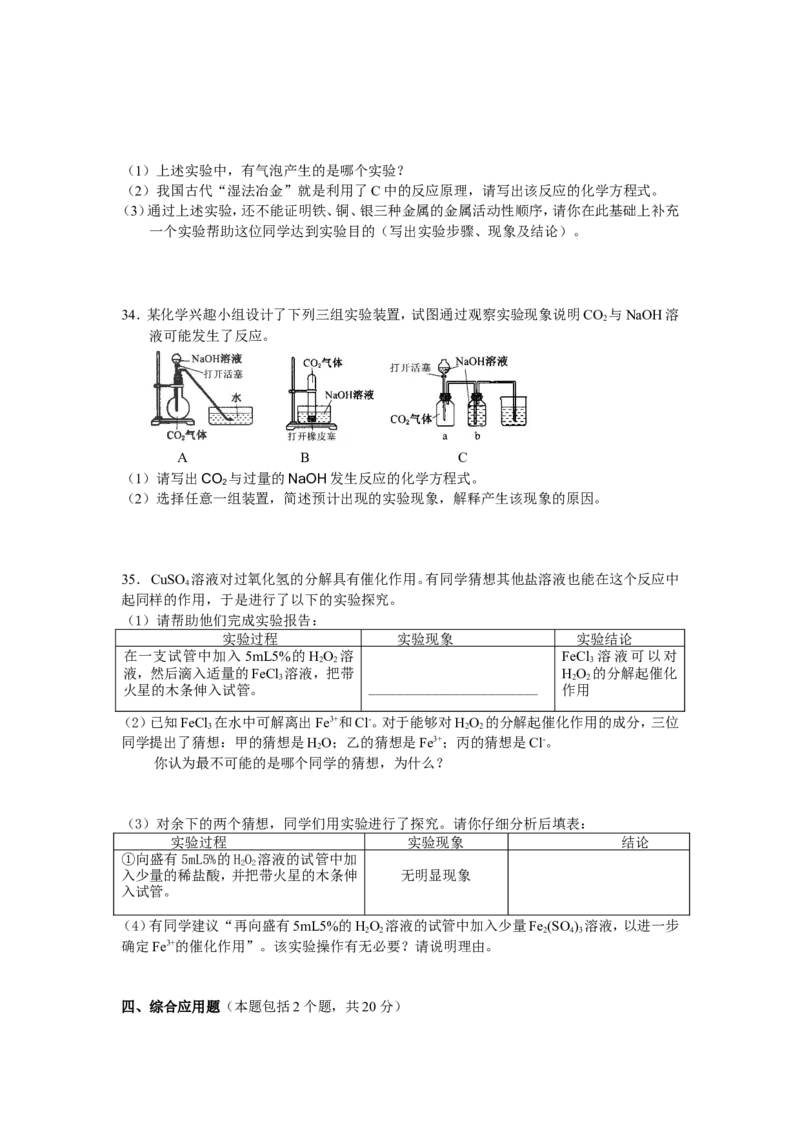
34.某化学兴趣小组设计了下列三组实验装置,试图通过观察实验现象说明CO 与NaOH溶
2
液可能发生了反应。
A B C
(1)请写出CO 与过量的NaOH发生反应的化学方程式。
2
(2)选择任意一组装置,简述预计出现的实验现象,解释产生该现象的原因。
35. CuSO 溶液对过氧化氢的分解具有催化作用。有同学猜想其他盐溶液也能在这个反应中
4
起同样的作用,于是进行了以下的实验探究。
(1)请帮助他们完成实验报告:
实验过程 实验现象 实验结论
在一支试管中加入5mL5%的HO 溶 FeCl 溶液可以对
2 2 3
液,然后滴入适量的FeCl 溶液,把带 HO 的分解起催化
3 2 2
火星的木条伸入试管。 ________________________ 作用
(2)已知FeCl 在水中可解离出Fe3+和Cl-。对于能够对HO 的分解起催化作用的成分,三位
3 2 2
同学提出了猜想:甲的猜想是HO;乙的猜想是Fe3+;丙的猜想是Cl-。
2
你认为最不可能的是哪个同学的猜想,为什么?
(3)对余下的两个猜想,同学们用实验进行了探究。请你仔细分析后填表:
实验过程 实验现象 结论
①向盛有5mL5%的HO 溶液的试管中加
2 2
入少量的稀盐酸,并把带火星的木条伸 无明显现象
入试管。
(4)有同学建议“再向盛有5mL5%的HO 溶液的试管中加入少量Fe (SO ) 溶液,以进一步
2 2 2 4 3
确定Fe3+的催化作用”。该实验操作有无必要?请说明理由。
四、综合应用题(本题包括2个题,共20分)点 燃
36 . 下 列 化 学 反 应 都 能 产 生 二 氧 化 碳 气 体 : ① C+O CO
2 2
点燃 加热
②CaCO +2HCl==CaCl +CO ↑+H O ③2CO+O 2CO ④CO+CuO Cu+2CO 。
3 2 2 2 2 2 2
(1)以上化学反应中,最适用于实验室制取二氧化碳气体的反应是________________。
(2)根据你所选择的化学反应,如下图所示中可以制取二氧化碳气体的装置是___________;
利用该装置还可以制取的一种气体是________,反应的化学方程式为___________________。
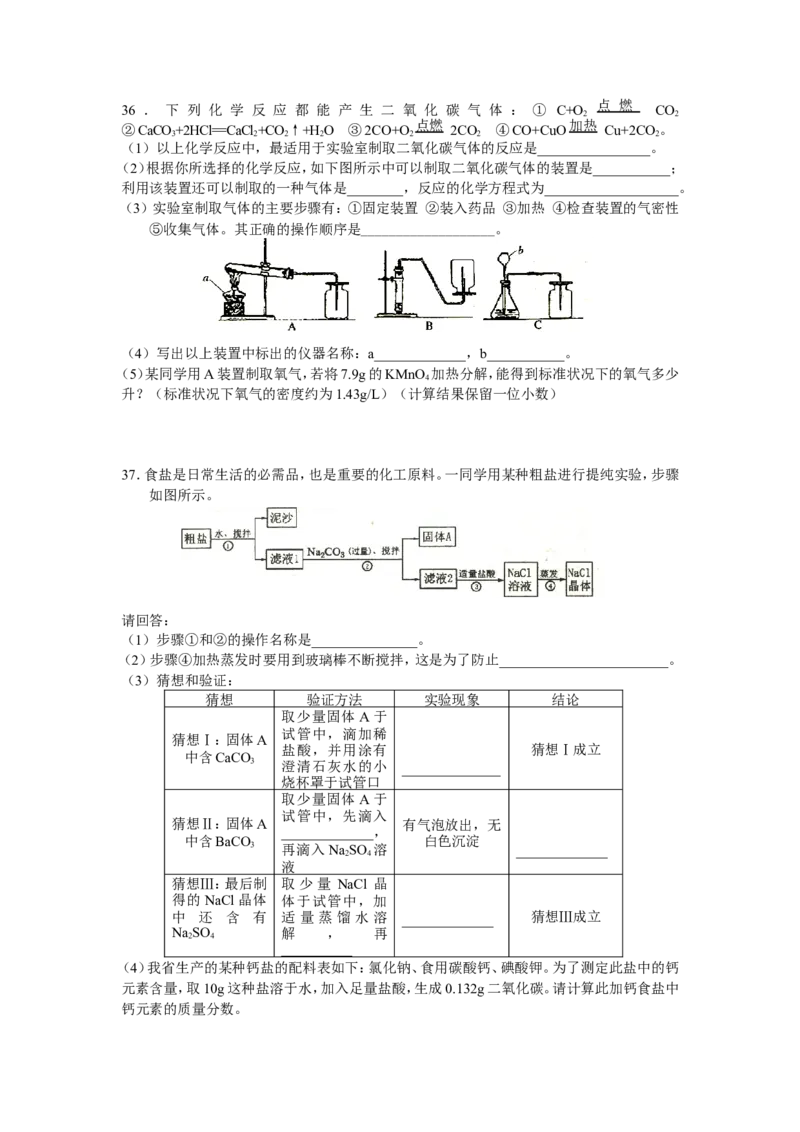
(3)实验室制取气体的主要步骤有:①固定装置 ②装入药品 ③加热 ④检查装置的气密性
⑤收集气体。其正确的操作顺序是___________________。
(4)写出以上装置中标出的仪器名称:a_____________,b___________。
(5)某同学用A装置制取氧气,若将7.9g的KMnO 加热分解,能得到标准状况下的氧气多少
4
升?(标准状况下氧气的密度约为1.43g/L)(计算结果保留一位小数)
37.食盐是日常生活的必需品,也是重要的化工原料。一同学用某种粗盐进行提纯实验,步骤
如图所示。
请回答:
(1)步骤①和②的操作名称是_______________。
(2)步骤④加热蒸发时要用到玻璃棒不断搅拌,这是为了防止________________________。
(3)猜想和验证:
猜想 验证方法 实验现象 结论
取少量固体A于
试管中,滴加稀
猜想Ⅰ:固体A
盐酸,并用涂有 猜想Ⅰ成立
中含CaCO
3 澄清石灰水的小 ______________
烧杯罩于试管口
取少量固体A于
试管中,先滴入
猜想Ⅱ:固体A 有气泡放出,无
_____________,
中含BaCO 白色沉淀
3 再滴入NaSO 溶 _____________
2 4
液
猜想Ⅲ:最后制 取少量 NaCl 晶
得的NaCl晶体 体于试管中,加
中 还 含 有 适 量 蒸 馏 水 溶 _____________ 猜想Ⅲ成立
NaSO 解 , 再
2 4
__________
(4)我省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾。为了测定此盐中的钙
元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳。请计算此加钙食盐中
钙元素的质量分数。2009年全国初中学生化学素质和实验能力竞赛
河南赛区预赛试卷参考答案
一、选择题(每题1分,共20分)
1.C 2.D 3.A 4. D 5. B 6.B 7.C 8.B 9.C 10.B 11.D 12.A 13.B 14.D 15.C
16.D 17.C 18.B 19.B 20.C
二、填空题(每空1分,共30分)
21.C H O NaCl KNO NaCO
6 12 6 3 2 3
22.甲烷或CH CH+2O CO+2H O 减少有害气体对大气的污染等
4 4 2 2 2
23.66.7% NH 417 糖类、油脂、维生素等
3
24.H O –1和+1 Cl+HO ==HCl+HClO
2 2 2
25.(1)pH试纸上,把试纸显示的颜色与标准比色卡比较
(2)氢氧化钠溶液和浓硫酸
(3)会生成KCl,从而引入新的杂质
26.(1)t (2)> (3)t~t (4)C
2 1 2
加热 加热
27.(1)Ca(HCO )=CaCO ↓+H O+CO↑或Mg(HCO )=Mg(OH) ↓+2CO ↑
3 2 3 2 2 3 2 2 2
(2)取少量的水样,向水样中加入适量的肥皂水,若泡沫少浮渣多则是硬水,反之是软水
(3)20.7 符合
28.(1)9 40.08 (2)8 BC (3) B
三、简答题(共30分)
29.(4分)
(1)2Mg+ CO C+2MgO(1分) 置换反应(1分)
2
(2)Ca(OH) +H SO ==CaSO +H O(1分) 复分解反应(1分)
2 2 4 4 2
30.(4分)
(1)反应物的浓度越大,反应速率越快;如物质在氧气中燃烧比在空气中快得多。
(2)反应物的接触面积越大,反应速率越快;如煤粉的燃烧比煤块快得多。
31.(3分)钟罩内澄清的石灰水变浑浊;高处蜡烛先熄灭,低处蜡烛后熄灭;钟罩内液面上升
等
32.(5分)
(1)①氯化镁、氯化钠(1分) ②氯化镁、硝酸钠(1分)
③氯化镁、氯化钠、硝酸钠(1分)
(2)MgCl +2NaOH===Mg(OH) ↓+2NaCl(1分)
2 2
NaCl + AgNO === AgCl↓ + NaNO (1分)
3 3
33.(4分)
(1)A(1分) (2)Fe+CuSO==Cu+FeSO (1分)
4 4
(3)将铜放入到AgNO 溶液中,若铜表面有银白色固体析出,说明铜比银活泼(2分)
3
34.(4分)(1)CO +2NaOH=NaCO+HO(1分)
2 2 3 2
(2)A:水槽中的水进入烧瓶中(1分) CO 与NaOH溶液发生反应,使烧瓶内的气体压强减
2
小(2分)(或B:试管内液面上升,水槽内的液面下降 CO 与的NaOH溶液反应,使试管
2
内的气体压强减小;或C:烧杯内的水进入广口瓶b中, 广口瓶b中的水进入广口瓶a中
CO 与的NaOH溶液发生反应,使瓶a内的气体压强减小)
2
35.(6分)
(1)试管中快速产生大量气泡,能使带火星的木条复燃。(1分)
(2)甲同学的猜想(1分)
因为HO 溶液中含有大量水,但HO 并没有快速分解。(1分)
2 2 2 2
(3)能催化HO 分解的不是Cl—和H+。(1分)
2 2
(4)没有必要(1分) 因为Fe Cl 溶液本身含有Fe3+、Cl—、HO、H+,前面实验和推断已经证
2 3 2
明Cl—、HO、H+对HO 的分解无催化作用,说明只有Fe3+对HO 的分解有催化作用。(1分)
2 2 2 2 2
四、综合应用题(共20分)
36.(共10分,第(5)小题3分,其余每空1分)
(1)② (2)C O 2HO 二氧化锰 2HO+ O↑
2 2 2 2 2
(3)④②①③⑤
(4)酒精灯 长颈漏斗
(5)解:设生成氧气的质量为x。
△
2KMnO K MnO +MnO +O ↑ …………………1分
4 2 4 2 2
316 32
7.9g x
316 / 32 ==7.9 g / x x=0.8 g …………………1分
标准状况下氧气的体积为:0.8 g/(1.43 g/L )≈0.6 L …………………1分
答:略。
37.(共10分)
(1)过滤(1分) (2)溶液局部过热而飞溅(1分)
(3)猜想Ⅰ:产生气泡,烧杯内壁有白色固体生成(1分) 猜想Ⅱ:盐酸或硝酸(1分) 猜
想Ⅱ不成立(1分) 猜想Ⅲ:加BaCl 或Ba(NO ) 溶液(1分) 有白色沉淀生成(1分)
2 3 2
(4)解: 设此加钙食盐中碳酸钙的质量为x。
CaCO + 2HCl == CaCl + H O + CO ↑
3 2 2 2
100 44
x 0.132g
100 ∶ 44 = x∶0.132g
x=0.3g ………………1分
碳酸钙中钙的质量为0.3g×40/100=0.12g ………………1分
此加钙食盐中钙元素的质量分数为: 0.12g/10g ×100% = 1.2% …………1分
答:略。