文档内容
第三章 烃的衍生物
第二节 醇 酚
第 1 课时 醇
【即时训练】
一、元素或物质推断题
1.已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色
无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
(1)写出下列物质的化学式:A:______,D:______,R:______。
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:______;
②向N中通足量CO 时反应的离子方程式:______;
2
③D与盐酸反应的离子方程式:______。
(3)简述检验气体C的方法:______。
2.已知A、B、C、D、E、F、G、H、X、Y是中学化学常见物质,E、F、H、X、Y中含有同种元素,F
是一种红棕色气体;反应①是置换反应,A是一种活泼金属,D是一种黑色固体。它们之间在一定条件下
存在下列转化关系:
根据图,完成下列问题:(1)写出指定物质的化学式:C___,E___,H___。
(2)反应①的化学方程式为___,实验现象为___。
(3)反应②中每转移2mole-,标况下产生的还原产物与氧化产物的体积差为___L。
(4)D和G在高温下反应可制取工业原料气,反应的化学方程式为___。
(5)要确定反应④的生成物,在反应后的溶液中加入过量NaOH浓溶液,看到有白色沉淀出现,其成分是
___;然后过滤出沉淀并对滤液加热,闻到有刺激性气味气体产生,为确定气体的成分用湿润的红色石蕊
试纸检验,发现试纸变蓝。根据上述现象写出反应④的化学方程式:__。
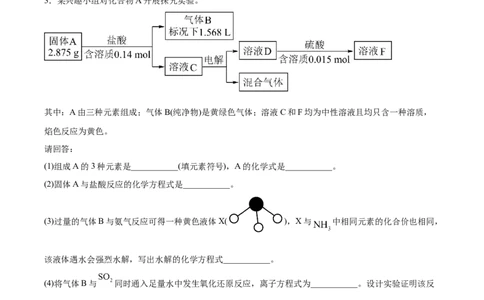
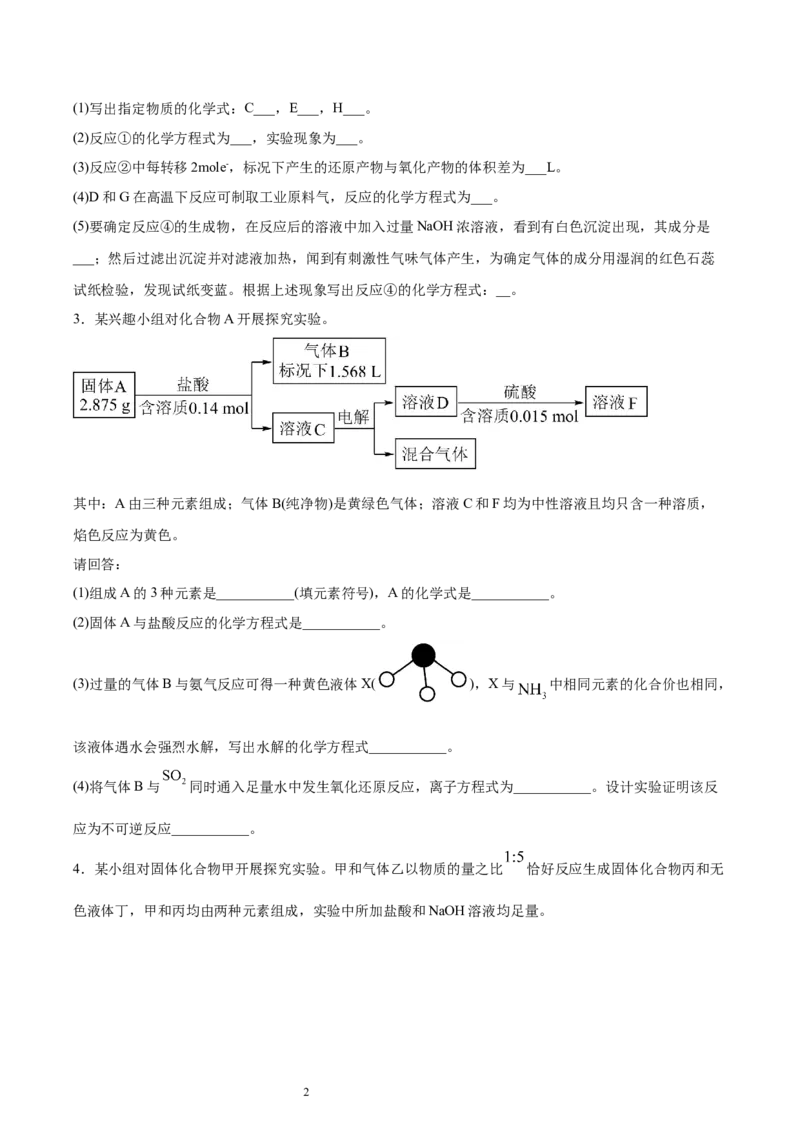
3.某兴趣小组对化合物A开展探究实验。
其中:A由三种元素组成;气体B(纯净物)是黄绿色气体;溶液C和F均为中性溶液且均只含一种溶质,
焰色反应为黄色。
请回答:
(1)组成A的3种元素是___________(填元素符号),A的化学式是___________。
(2)固体A与盐酸反应的化学方程式是___________。
(3)过量的气体B与氨气反应可得一种黄色液体X( ),X与 中相同元素的化合价也相同,
该液体遇水会强烈水解,写出水解的化学方程式___________。
(4)将气体B与 同时通入足量水中发生氧化还原反应,离子方程式为___________。设计实验证明该反
应为不可逆反应___________。
4.某小组对固体化合物甲开展探究实验。甲和气体乙以物质的量之比 恰好反应生成固体化合物丙和无
色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
22
请回答:
(1)组成甲的元素是___________(填元素符号),甲的化学式是___________。
(2)甲与乙反应的化学方程式是___________。
(3)丙与盐酸反应的离子方程式是___________。
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去。褪色的原因是___________,请设计实验方案
证明之___________。
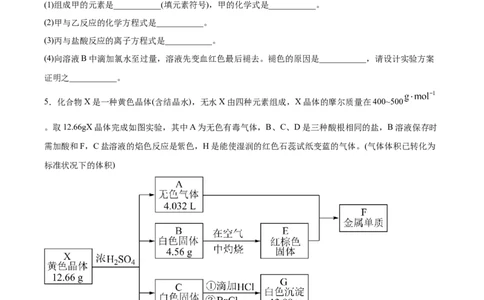
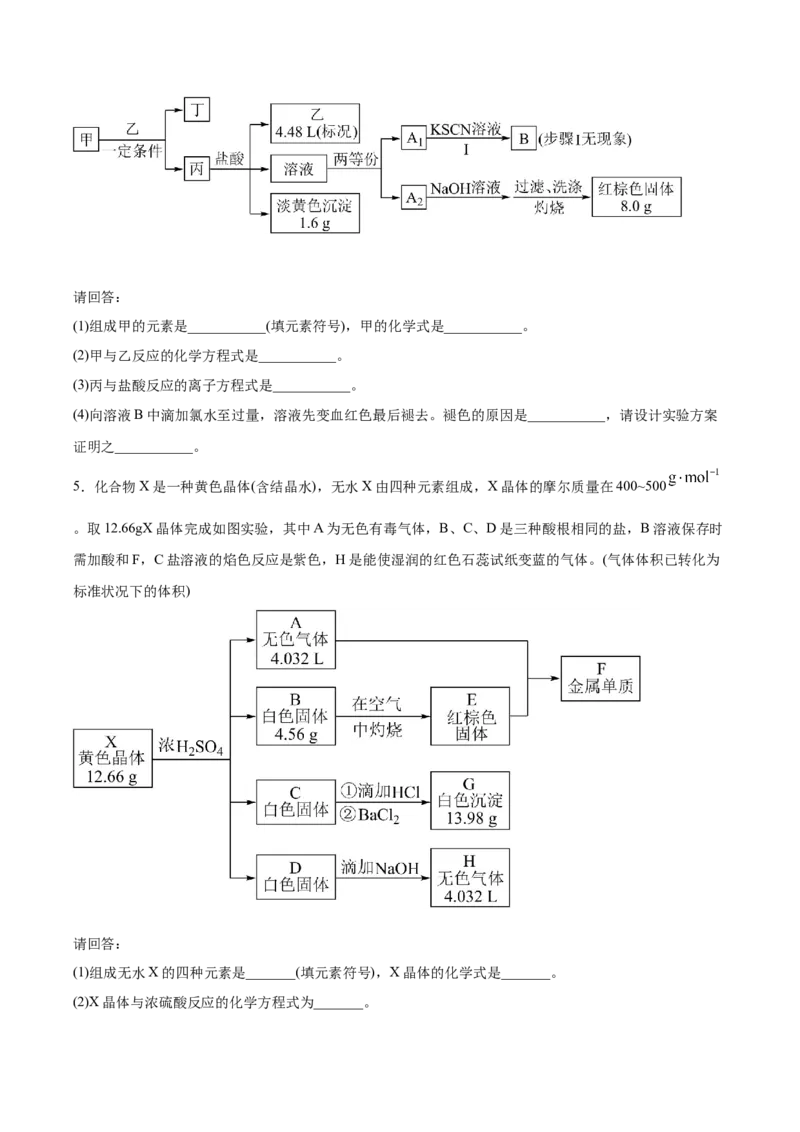
5.化合物X是一种黄色晶体(含结晶水),无水X由四种元素组成,X晶体的摩尔质量在400~500
。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液保存时
需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已转化为
标准状况下的体积)
请回答:
(1)组成无水X的四种元素是_______(填元素符号),X晶体的化学式是_______。
(2)X晶体与浓硫酸反应的化学方程式为_______。(3)无水X可被 氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为_______。
(4)可利用X来鉴别 和 ,原因是_______。
(5)设计实验方案检验B在空气中灼烧的产物:_______。
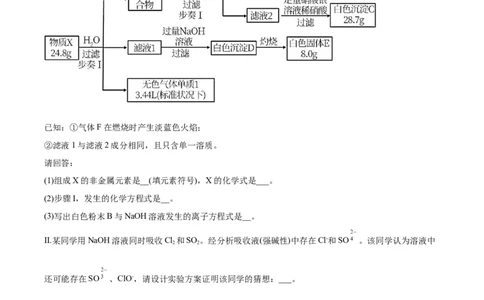
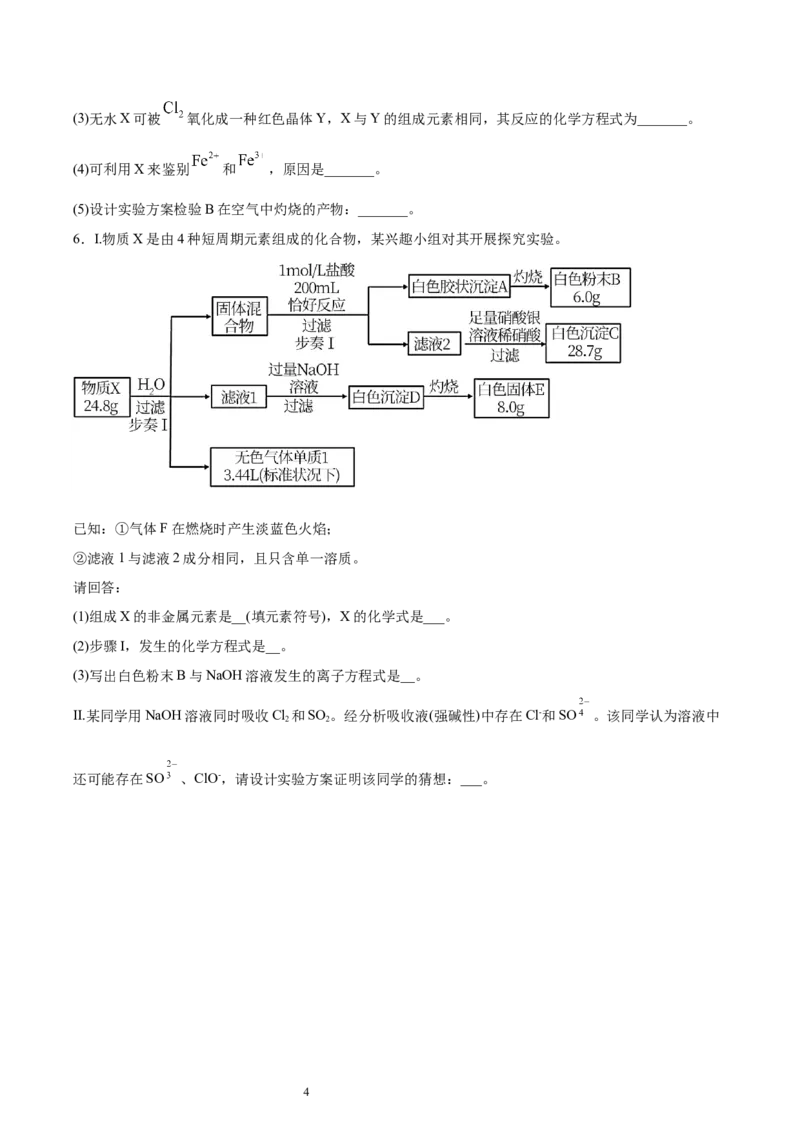
6.I.物质X是由4种短周期元素组成的化合物,某兴趣小组对其开展探究实验。
已知:①气体F在燃烧时产生淡蓝色火焰;
②滤液1与滤液2成分相同,且只含单一溶质。
请回答:
(1)组成X的非金属元素是__(填元素符号),X的化学式是___。
(2)步骤I,发生的化学方程式是__。
(3)写出白色粉末B与NaOH溶液发生的离子方程式是__。
II.某同学用NaOH溶液同时吸收Cl 和SO 。经分析吸收液(强碱性)中存在Cl-和SO 。该同学认为溶液中
2 2
还可能存在SO 、ClO-,请设计实验方案证明该同学的猜想:___。
44
参考答案
1.NaO Fe O Al 4Fe(OH) +O+2HO=4Fe(OH) AlO +CO+2HO=Al(OH) ↓+HCO
2 2 3 4 2 2 2 3 2 2 3
Fe O+8H+=Fe2++2Fe3++4HO 用带火星的木条伸入试管口,若带火星的木条复燃,说明有氧气生成
3 4 2
【详解】
A为淡黄色固体,且A能和水反应,则A是NaO,A和水反应生成NaOH和O,C是无色无味的气体,
2 2 2
则C是O、B是NaOH;D是具有磁性的黑色晶体,是Fe O,Fe在氧气中燃烧生成四氧化三铁,则T是
2 3 4
Fe,R和氧气反应生成氧化物Q,Q能和NaOH溶液反应,则Q是Al O、R是Al,N是NaAlO ,H是白
2 3 2
色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M,则H是Fe(OH) 、M是Fe(OH) ,
2 3
Fe O 和HCl、足量Fe反应后得到E,E为FeCl ,Fe(OH) 和HCl反应生成W,则W是FeCl 。
3 4 2 3 3
(1)根据以上分析可知: A:NaO,D:Fe O,R:Al。
2 2 3 4
(2)①H是请氧化亚铁,在潮湿空气中变成氢氧化铁的化学方程式:4Fe(OH) +O+2HO=4Fe(OH) ;
2 2 2 3
②向偏铝酸钠中通足量CO 时反应生成氢氧化铝和碳酸氢钠,离子方程式:AlO +CO+2HO=Al(OH) ↓
2 2 2 3
+HCO ;
③四氧化三铁和盐酸反应生成氯化铁和氯化亚铁和水,离子方程式:Fe O+8H+=Fe2++2Fe3++4HO。
3 4 2
(3)气体C为氧气,检验的方法:用带火星的木条伸入试管口,若带火星的木条复燃,说明有氧气生成。
2.MgO HNO NO 2Mg+CO 2MgO+C 剧烈燃烧,发出耀眼白光放出大量热,
3 2
生成白色固体和黑色固体 33.6 C+H O CO+H Mg(OH)
2 2 2
4Mg+10HNO =4Mg(NO )+NHNO +3H O
3 3 2 4 3 2
【分析】
推断F是红棕色气体NO ,A是一种活泼金属,并且A在B中燃烧属于置换反应,D是一种黑色固体,能
2
与E反应产生NO ,则E应该是浓HNO,D是碳;故A是Mg,B是CO,C是MgO。C和浓HNO 反应,
2 3 2 3
产生CO、NO 和HO,故G是HO,又由于E、F、H、X、Y中含有同种元素,故H是NO。
2 2 2 2
【详解】
(1)根据分析可知C是MgO,E是浓HNO,H是NO;
3
11
(2)镁在CO 中剧烈燃烧,发出耀眼的白光并放出大量的热,生成黑色的碳和白色的MgO,化学方程式为
2
2Mg+CO 2MgO+C;
2
(3)反应②为:C+4HNO (浓) CO↑+4NO↑+2H O,根据反应可知,每转移4mole-生成5mol气体;则转移
3 2 2 2
2mol电子生成2.5mol气体,且n(NO )=2mol,n(CO)=0.5mol;其中NO 是还原产物,CO 是氧化产物,故
2 2 2 2
二者的体积差ΔV=(2.0mol-0.5mol)×22.4L·mol-1=33.6L;
(4)C和HO在高温下生成水煤气,反应为:C+H O CO+H;
2 2 2
(5)Mg和HNO 反应肯定生成Mg(NO),故加入NaOH产生的白色沉淀是Mg(OH) ;将沉淀过滤后加热产
3 3 2 2
生NH ,说明HNO 被还原成 ,故反应为:4Mg+10HNO ==4Mg(NO)+NHNO +3H O。
3 3 3 3 2 4 3 2
3.Na、O、Cl
向氯水中通入过量 ,
充分反应后再加入淀粉碘化钾溶液,不变蓝色,说明该反应为不可逆反应
【分析】
固体A和盐酸反应生成溶液C,溶液C为中性溶液且只含一种溶质,焰色反应为黄色,则含有Na元素,
则C中溶质为NaCl,A中含有Na元素;气体B(纯净物)是黄绿色气体,气体B为Cl,
2
,电解NaCl溶液生成NaOH、Cl、H,生成的溶液D和硫酸反应生成F
2 2
溶液,溶液F为中性溶液且只含一种溶质,则溶液F为NaSO 溶液,溶液D为NaOH溶液,硫酸中含有溶
2 4
质0.015mol,则NaOH的物质的量为0.03mol,则A中Na元素的物质的量为0.03mol,根据Na元素守恒,
则溶液C中NaCl的物质的量为0.03mol,盐酸中溶质的物质的量为0.14mol,根据Cl元素守恒,则A中Cl
元素的物质的量为 ,A由三种元素组成,其中两种元素为Na元
素、Cl元素,则另一种元素为O元素,A中含有Na、Cl的总质量为
22
,则A中含有O元素的物质的量为
,则A的化学式为 。
【详解】
(1)由分析可知,组成A的3种元素是Na、O、Cl,A的化学式为 ;
(2)2.875g固体A和0.14mol HCl反应生成0.07molCl 、0.03molNaCl和HO,由此得出化学方程式为
2 2
;
(3)过量的Cl 和氨气反应可得一种黄色液体X( ),X与 中相同元素的化合价也相同,由此
2
推测X为NCl ,NCl 水解生成 和HClO,水解方程式为: ;
3 3
(4)Cl 与 同时通入足量水中反应生成HCl和HSO ,离子方程式为:
2 2 4
;若该反应为可逆反应,反应中会有Cl 的存在,因此只需检验
2
是否含有Cl,即可证明该反应是否为可逆反应,检验方法为:向氯水中通入过量 ,充分反应后再加
2
入淀粉碘化钾溶液,不变蓝色,说明该反应为不可逆反应。
4.Fe、O
过量的氯水将 氧化 向溶液中加入足量的KSCN溶液,若溶液变成血红色即证明
【分析】
根据转化的框图可知,红棕色固体为Fe O,n(Fe)=2n(Fe O)=2× =0.1mol,A1中加入KSCN
2 3 2 3
溶液无现象,说明溶液中只含Fe2+,故说明丙中含有Fe元素,其物质的量为0.2mol,淡黄色沉淀为S,其
33
物质的量为:n(S)= ,说明化合物丙中含有S元素,故推测乙气体为HS,物质的量
2
为n(H S)= ,故丙中含有的S为0.25mol,故丙中n(Fe):n(S)=0.2mol:0.25mol=4:5,
2
其化学是为:Fe S,无色液体常见的有HO,故丁为HO,则甲中含有Fe和O元素,根据甲和气体乙以
4 5 2 2
物质的量之比 恰好反应生成固体化合物丙和无色液体丁,其反应方程式为:
,据此分析解题。
【详解】
(1)由分析可知,组成甲的元素是Fe、O,甲的化学式是Fe O,故答案为:Fe、O;Fe O;
4 5 4 5
(2)由分析可知,甲与乙反应的化学方程式是 ,故答案为:
;
(3)由分析可知,丙的化学式为Fe S,生成的HS和S的物质的量之比为:0.2mol:0.05mol=4:1,且溶液
4 5 2
中无Fe3+,故其与盐酸反应的离子方程式是 ,故答案为:
;
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去,由于Cl 能将亚铁离子氧化为铁离子,故显血
2
红色,但由于Cl 有强氧化性,能将SCN-氧化,故又褪色,要想验证猜想只需向反应后的溶液中加入足量
2
的KSCN看是否重新变为血红色,若变则说明猜想正确,若不变则猜想错误,故答案为:过量的氯水将
氧化;向溶液中加入足量的KSCN溶液,若溶液变成血红色即证明。
5.K、 、C、N
44
能与 反应生成蓝色沉淀,不能与
反应生成沉淀 取少量灼烧后的固体粉末溶于足量稀硫酸中,滴加几滴 溶液,若溶液变成
血红色,说明有 产生,反之则无;把灼烧过程中产生的气体依次通过装有盐酸酸化的 溶液、
品红溶液的洗气瓶,如果盐酸酸化的 溶液变浑浊,则说明有 产生,反之则无;若品红褪色,取
少量褪色后的溶液加热后又恢复品红的颜色,则说明有 产生,反之则无
【分析】
题中信息显示,C盐溶液的焰色反应呈紫色,则含有K+,C中滴加盐酸、BaCl 后,有白色沉淀生成,则G
2
为BaSO,C为KSO ;B溶液保存时需加酸和F,而B为硫酸盐,在空气中灼烧生成红棕色固体E,则E
4 2 4
为Fe O、F为Fe、A为CO、B为FeSO ;白色固体D中滴加NaOH溶液,产生的无色气体H能使湿润的
2 3 4
红色石蕊试纸变蓝,则其为NH ,所以D为(NH )SO ,从而得出由四种元素组成的无水X中含有K、Fe、
3 4 2 4
C、N元素。n(FeSO )= ,n(BaSO)= ,n(NH )=
4 4 3
,n(CO)= ,从而得出无水X中含有Fe2+、CN-、K+,依据电
荷守恒,可求出n(K+)=0.18mol-0.03mol 2=0.12mol,n(K+): n(Fe2+): n(CN-)=0.12:0.03:0.18=4:1:6,从而
×
得出X的无水盐的化学式为K[Fe(CN) ];n(H O)=
4 6 2
,故X的化学式为 。
【详解】
55
(1)由分析可知,组成无水X的四种元素是K、 、C、N,X晶体的化学式是 。答
案为:K、 、C、N; ;
(2)由框图推知, 晶体与浓硫酸反应,生成FeSO 、CO、(NH )SO 、KSO ,化学方
4 4 2 4 2 4
程式为 。答案为:
;
(3)无水K[Fe(CN) ]可被 氧化成一种红色晶体Y,X与Y的组成元素相同,则X中[Fe(CN) ]4-被氧化为
4 6 6
[Fe(CN) ]3-,从而得出其反应的化学方程式为 。答案为:
6
;
(4)可利用 来鉴别 和 ,则只能与Fe3+发生反应生成蓝色沉淀,原因是
能与 反应生成蓝色沉淀,不能与 反应生成沉淀。答案为: 能与
反应生成蓝色沉淀,不能与 反应生成沉淀;
(5) B在空气中灼烧的产物为Fe O,可能有SO 、SO 等,检验Fe O 时,可先加酸溶液,再加入KSCN溶
2 3 2 3 2 3
液;检验SO 时,可通入品红溶液中;检验SO 时,可通入BaCl 溶液中。实验方案为:取少量灼烧后的固
2 3 2
体粉末溶于足量稀硫酸中,滴加几滴 溶液,若溶液变成血红色,说明有 产生,反之则无;把
灼烧过程中产生的气体依次通过装有盐酸酸化的 溶液、品红溶液的洗气瓶,如果盐酸酸化的
溶液变浑浊,则说明有 产生,反之则无;若品红褪色,取少量褪色后的溶液加热后又恢复品红的颜色,
66
则说明有 产生,反之则无。答案为:取少量灼烧后的固体粉末溶于足量稀硫酸中,滴加几滴
溶液,若溶液变成血红色,说明有 产生,反之则无;把灼烧过程中产生的气体依次通过装有盐酸酸
化的 溶液、品红溶液的洗气瓶,如果盐酸酸化的 溶液变浑浊,则说明有 产生,反之则无;
若品红褪色,取少量褪色后的溶液加热后又恢复品红的颜色,则说明有 产生,反之则无。
【点睛】
检验SO 时,通入品红溶液,品红褪色还不能说明气体为SO ,还应加热无色溶液,看溶液是否恢复红色。
2 2
6.Si、H、Cl 3MgH ·SiCl 3MgH ·SiCl +6H O=Mg(OH)+2MgCl +6H ↑+H SiO(或
2 4 2 4 2 2 2 2 4 4
3MgH ·SiCl +5H O=Mg(OH)+2MgCl +6H ↑+H SiO) SiO+2OH-=SiO +H O 取一定量吸收液,加
2 4 2 2 2 2 2 3 2 2
入足量氯化钡溶液,过滤;往滤渣中加入稀盐酸,若沉淀的量减少且产生刺激性气味的气体,则说明含有
SO ,反之则无;往滤液中加入足量的稀盐酸呈酸性,再加入紫色石蕊试液,先变红后褪色,则说明有
ClO-,反之则无
【分析】
根据题给信息可知:气体F在燃烧时产生淡蓝色火焰,F为氢气;物质的量为 =0.6mol;固体
混合物中加入1mol/L盐酸200mL恰好反应,过滤得到白色胶状沉淀A,A为硅酸沉淀,灼烧后得到二氧
化硅粉末,物质的量的为 =0.1mol;滤液2中(只含单一溶质)加入足量的硝酸银和稀硝酸产生氯化
银白色沉淀,物质的量为 =0.2mol;短周期元素形成的离子中,不溶于强碱的白色沉淀为氢氧
化镁,滤液1(只含单一溶质),加入足量的氢氧化钠溶液,产生白色沉淀,所以白色沉淀D为氢氧化镁,
77
灼烧后得到氧化镁E,物质的量为 =0.2mol;根据②滤液1与滤液2成分相同,且只含单一溶质,
所以滤液1与滤液2的溶质为MgCl ,滤液2为氢氧化镁与盐酸反应所得,说明固体混合物中含有氢氧化
2
镁和硅酸两种物质,且硅酸的量为0.1mol,根据盐酸与氢氧化镁的反应关系可知,氢氧化镁的量为
0.1mol;根据镁原子守恒及氯化镁的组成可知,滤液1中氯化镁的量为0.2mol,氯离子的量为0.4mol;
结合以上分析可知,物质X中含有元素镁的物质的量为:0.2mol+0.1mol=0.3mol;含有硅元素的物质的量
为0.1mol;氯元素的量为0.4mol;根据质量守恒可知,含有氢元素的质量为24.8-0.3×24-0.1×28-
0.4×35.5=0.6g,则含有氢元素的物质的量0.6mol;所以四种元素的量之比:n(Mg):n(Si):n(H):
n(Cl)=0.3mol:0.1mol:0.6mol:0.4mol=3:1:6:4,所以X的化学式为:3MgH ·SiCl ;据以上分析解答。
2 4
【详解】
(1)结合以上分析可知,组成X的非金属元素是Si、H、Cl;X的化学式是3MgH ·SiCl ;
2 4
(2)结合以上分析可知,步骤I中,X与水发生反应,生成氢氧化镁、氢气、硅酸、氯化镁四种物质,反应
的化学方程式为:3MgH ·SiCl +6H O=Mg(OH)+2MgCl +6H ↑+H SiO(或
2 4 2 2 2 2 4 4
3MgH ·SiCl +5H O=Mg(OH)+2MgCl +6H ↑+H SiO);
2 4 2 2 2 2 2 3
(3)白色粉末B为二氧化硅,与NaOH溶液反应生成硅酸钠与水,离子方程式是:SiO+2OH-=SiO +H O;
2 2
II.亚硫酸钡与硫酸钡均为白色沉淀,但是亚硫酸钡能够溶于稀盐酸,产生刺激性气味的二氧化硫气体;
次氯酸具有强氧化性,能够漂白酸碱指示剂,而盐酸没有漂白性;如果吸收液(强碱性)中除了存在Cl-和
SO 外,还可能存在SO 、ClO-,为证明猜想,设计实验方案如下:取一定量吸收液,加入足量氯化钡
溶液,过滤;往滤渣中加入稀盐酸,若沉淀的量减少且产生刺激性气味的气体,则说明含有SO ,反之
则无;往滤液中加入足量的稀盐酸呈酸性,再加入紫色石蕊试液,先变红后褪色,则说明有ClO-,反之则
无。
8