文档内容
第三章 烃的衍生物
第二节 醇 酚
第 1 课时 醇
学习导航 1. 通过认识羟基的结构,了解醇类的结构特点;进而从化学键、官能团的角度理解醇类消
去反应、催化氧化反应的特征和规律。
2. 通过乙醇性质的学习,能利用反应类型的规律判断、说明和预测醇类物质的性质。
教学过程 一、醇的概述
1.醇的概念、分类及命名
(1)概念
醇是羟基与饱和碳原子相连的化合物。
饱和一元醇通式为C H OH或C H O(n≥1,n为整数)。
n 2n+1 n 2n+2
(2)分类
(3)命名
①步骤原则
—选择含有与羟基相连的碳原子的最长碳链为,主链,根据碳原子数目称为某醇
|
—从距离羟基最近的一端给主链碳原子依次编号
|
—醇的名称前面要用阿拉伯数字标出羟基的位置;羟基的个数用“二”“三”等表示
②实例
CHCHCHOH 1-丙醇; 2-丙醇;
3 2 2
1,2,3-丙三醇。
③注意:用系统命名法命名醇,确定最长碳链时不能把—OH看作链端,只能看作取代基,
但选择的最长碳链必须连有—OH。
2.物理性质
(1)沸点①相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
②饱和一元醇,随分子中碳原子个数的增加,醇的沸点升高。
③碳原子数相同时,羟基个数越多,醇的沸点越高。
(2)溶解性:甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例混溶。
(3)密度:醇的密度比水的密度小。
3.几种重要的醇
名称 结构简式 性质 用途
无色透明、易挥发的液体;能
与水及多种有机溶剂混溶;有
甲醇 CHOH 毒、误服少量(10 mL)可致人 化工原料、燃料
3
失明,多量(30 mL)可致人死
亡
无色、黏稠的液体,有甜味、 发动机防冻液的主要化学
乙二醇 能与水混溶,能显著降低水的 成分,也是合成涤纶等高
凝固点 分子化合物的主要原料
吸水能力——配制印泥、
无色、黏稠、具有甜味的液
丙三醇 化妆品;凝固点低——作
体,能与水以任意比例混溶,
(甘油) 防冻剂;三硝酸甘油酯俗
具有很强的吸水能力
称硝化甘油——作炸药等
二、醇的化学性质——以乙醇为例
乙醇发生化学反应时,可断裂不同的化学键。如
1.与钠反应
分子中a键断裂,化学方程式为
2CHCHOH+2Na―→2CHCHONa+H↑。
3 2 3 2 2
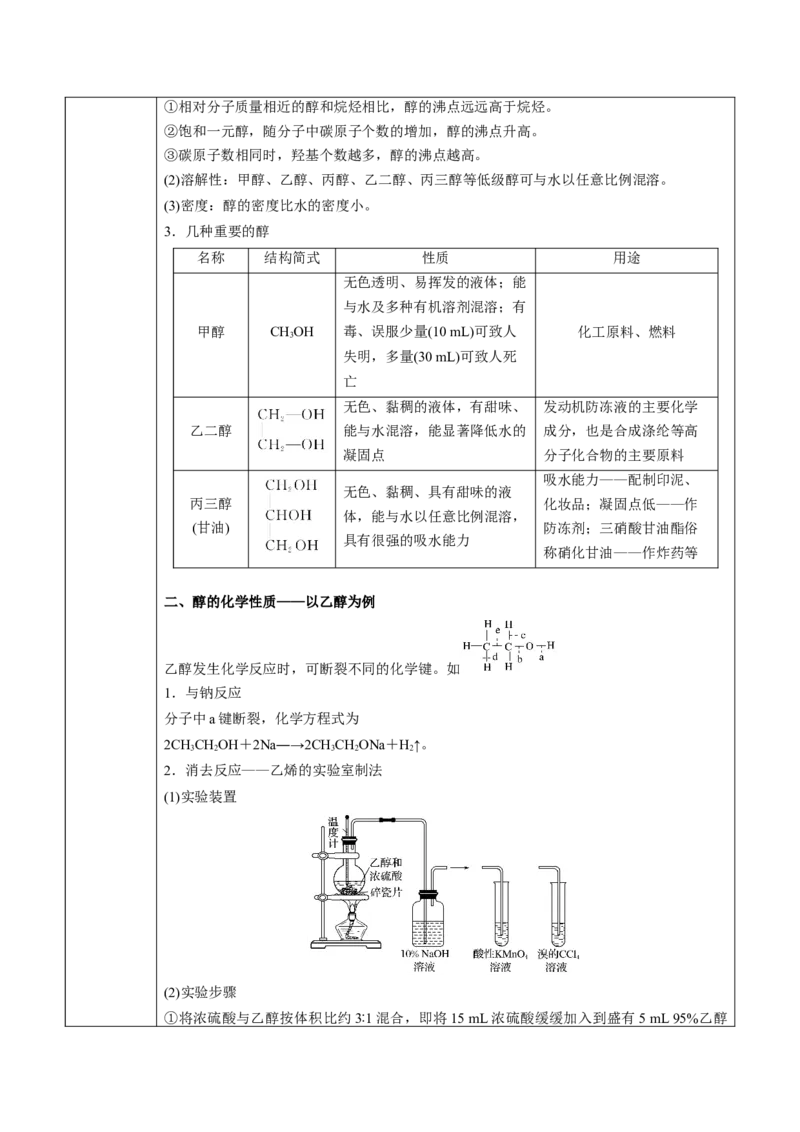
2.消去反应——乙烯的实验室制法
(1)实验装置
(2)实验步骤
①将浓硫酸与乙醇按体积比约3∶1混合,即将15 mL浓硫酸缓缓加入到盛有5 mL 95%乙醇的烧杯中混合均匀,冷却后再倒入长颈圆底烧瓶中,并加入碎瓷片防止暴沸;
②加热混合溶液,迅速升温到170 ℃,将生成的气体分别通入酸性KMnO 溶液和溴的四氯
4
化碳溶液中,观察现象。
(3)实验现象
酸性KMnO 溶液、溴的四氯化碳溶液褪色。
4
(4)实验结论
乙醇在浓硫酸作用下,加热到170 ℃,发生了消去反应,生成乙烯。
分子中b、d键断裂,化学方程式为
CHCHOH―――→CH==CH ↑+HO。
3 2 2 2 2
3.取代反应
(1)与HX发生取代反应
分子中b键断裂,化学方程式为
C HOH+HX――→C HX+HO。
2 5 2 5 2
(2)分子间脱水成醚
一分子中a键断裂,另一分子中b键断裂,化学方程式为
2CHCHOH―――→CHCHOCH CH+HO。
3 2 3 2 2 3 2
[醚类简介] (1)醚的概念和结构
像乙醚这样由两个烃基通过一个氧原子连接起来的化合物叫做醚。醚的结构可用 R—O—R′
来表示,R和R′都是烃基,可以相同,也可以不同。
(2)乙醚的物理性质
乙醚是一种无色、易挥发的液体,沸点34.5 ℃,有特殊气味,具有麻醉作用。乙醚易溶于
有机溶剂,它本身是一种优良溶剂,能溶解多种有机化合物。
4.氧化反应
(1)燃烧反应:C HOH+3O――→2CO+3HO。
2 5 2 2 2
(2)催化氧化
乙醇在铜或银作催化剂加热的条件下与空气中的氧气反应生成乙醛,分子中 a、c键断裂,
化学方程式为
2CHCHOH+O―――→2CHCHO+2HO。
3 2 2 3 2
(3)醇被酸性KMnO 溶液或酸性KCr O 溶液氧化
4 2 2 7
Ⅰ.实验装置
Ⅱ.实验步骤:
①在试管中加入少量酸性重铬酸钾溶液。②滴加少量乙醇,充分振荡,观察并记录实验现象。
Ⅲ.实验现象:溶液由黄色变为墨绿色。
乙醇能被酸性重铬酸钾溶液氧化,其氧化过程分为两个阶段:
CH3CH2OH――→CH3CHO――→CH3COOH。
【归纳总结】
1.醇消去反应的规律
(1)醇消去反应的原理如下:
(2)若醇分子中只有一个碳原子或与—OH相连碳原子的相邻碳原子上无氢原子,则不能发生
消去反应。如CHOH、 、 等。
3
(3)某些醇发生消去反应,可以生成不同的烯烃,如: 有三种消去反应
有机产物。
2.醇催化氧化反应的规律
(1)RCHOH被催化氧化生成醛:
2
2RCHOH+O――→2RCHO+2HO
2 2 2
(2) 被催化氧化生成酮:
+O――→ +2HO
2 2
(3) 一般不能被催化氧化。
课时训练
1.下列各组物质中,一定互为同系物的是
A.C HO、C HO B.C H、C H
3 6 4 8 3 8 2 6
C. 和 D.C HO、C HO
3 8 2 62.下列关于醇类物质的物理性质的说法,不正确的是
A.沸点:乙二醇>乙醇>丙烷
B.乙醇是常用的有机溶剂,可用于萃取碘水中的碘
C.交警对驾驶员进行呼气酒精检测,利用了酒精易挥发的性质
D.甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为这些醇与水形成了氢键,且烃基体积小
3.下列说法错误的是
A.葡萄糖和麦芽糖可以用新制氢氧化铜悬浊液鉴别
B.乙醇与氢卤酸的反应中乙醇分子断裂碳氧键而失去羟基
C.分子式为 的有机物的两种同分异构体可以利用红外光谱区别
D.醇分子中的氢氧键不如水分子中的氢氧键容易断裂,这是因为醇分子中的烷基具有推电子作用
4.下列说法正确的是
A.化妆品中添加甘油不能起到保湿作用
B.红外光谱法与核磁共振氢谱可用于有机物分子结构的鉴定
C.当液态有机物与杂质的沸点相差较小时可以用蒸馏的方法提纯
D. 乙醇完全氧化成乙醛,转移电子数为
5.某有机物的结构简式为CH-CH=CH-CH OH,现有①溴水②金属钠③灼热的CuO④酸性高锰酸钾溶
3 2
液,在一定条件下,能与该有机物反应的物质是
A.只有①②④ B.只有①④ C.只有①② D.①②③④
6.有机物分子中原子(或原子团)间的相互影响会导致它们化学性质改变。下列叙述能说明上述观点的是
A.乙烯可发生加成反应,而乙烷不能
B.乙醇分子能发生消去反应,而2,2-二甲基-1-丙醇不行
C.甲苯能与酸性高锰酸钾溶液反应,而甲烷不行
D.等物质的量的丙三醇和乙醇分别与足量金属钠反应,丙三醇产生的H 多
2
7.正丁醚常用作有机反应的溶剂,不溶于水,密度比水小,在实验室中可利用反应
制备,反应装置如图所示。下列
说法正确的是
A.装置B中a为冷凝水进水口
B.为加快反应速率可将混合液升温至170℃以上C.若分水器中水层超过支管口下沿,应打开分水器旋钮放水
D.本实验制得的粗醚经碱液洗涤、干燥后即可得纯醚
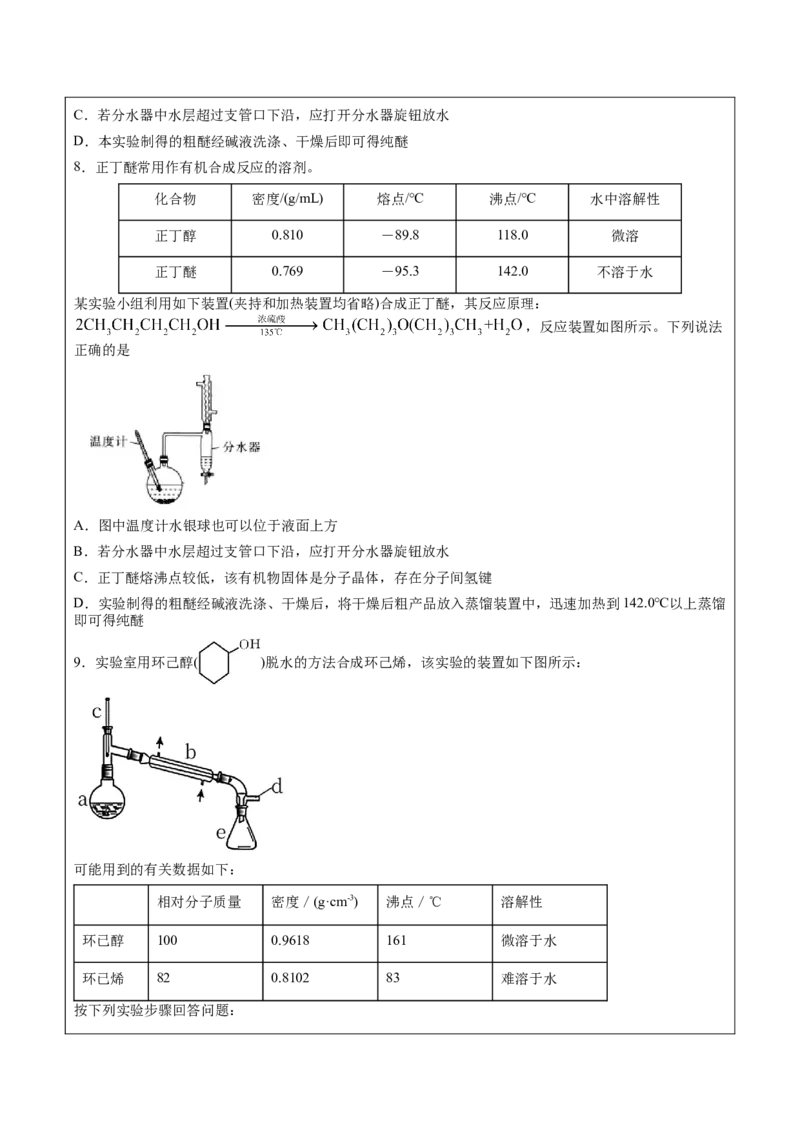
8.正丁醚常用作有机合成反应的溶剂。
化合物 密度/(g/mL) 熔点/℃ 沸点/℃ 水中溶解性
正丁醇 0.810 -89.8 118.0 微溶
正丁醚 0.769 -95.3 142.0 不溶于水
某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚,其反应原理:
,反应装置如图所示。下列说法
正确的是
A.图中温度计水银球也可以位于液面上方
B.若分水器中水层超过支管口下沿,应打开分水器旋钮放水
C.正丁醚熔沸点较低,该有机物固体是分子晶体,存在分子间氢键
D.实验制得的粗醚经碱液洗涤、干燥后,将干燥后粗产品放入蒸馏装置中,迅速加热到142.0℃以上蒸馏
即可得纯醚
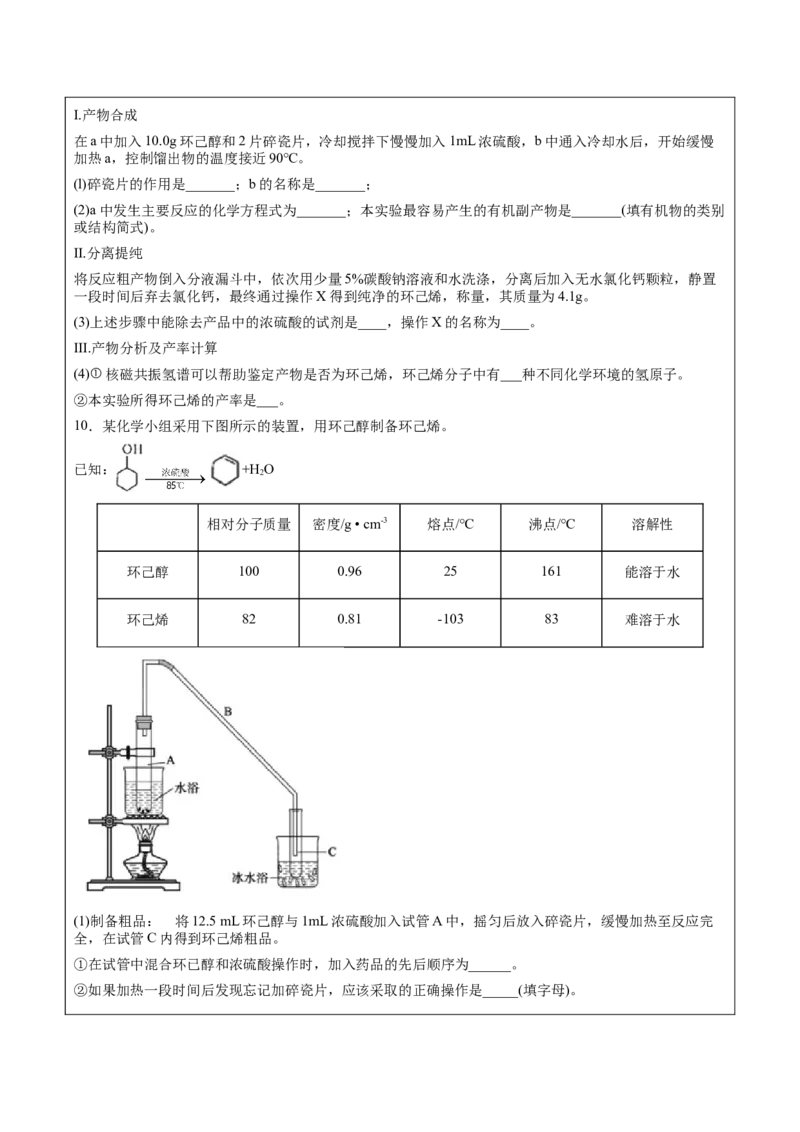
9.实验室用环己醇( )脱水的方法合成环己烯,该实验的装置如下图所示:
可能用到的有关数据如下:
相对分子质量 密度/(g·cm-3) 沸点/℃ 溶解性
环已醇 100 0.9618 161 微溶于水
环已烯 82 0.8102 83 难溶于水
按下列实验步骤回答问题:I.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢
加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是_______;b的名称是_______;
(2)a中发生主要反应的化学方程式为_______;本实验最容易产生的有机副产物是_______(填有机物的类别
或结构简式)。
II.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置
一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)上述步骤中能除去产品中的浓硫酸的试剂是____,操作X的名称为____。
III.产物分析及产率计算
(4)①核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有___种不同化学环境的氢原子。
②本实验所得环己烯的产率是___。
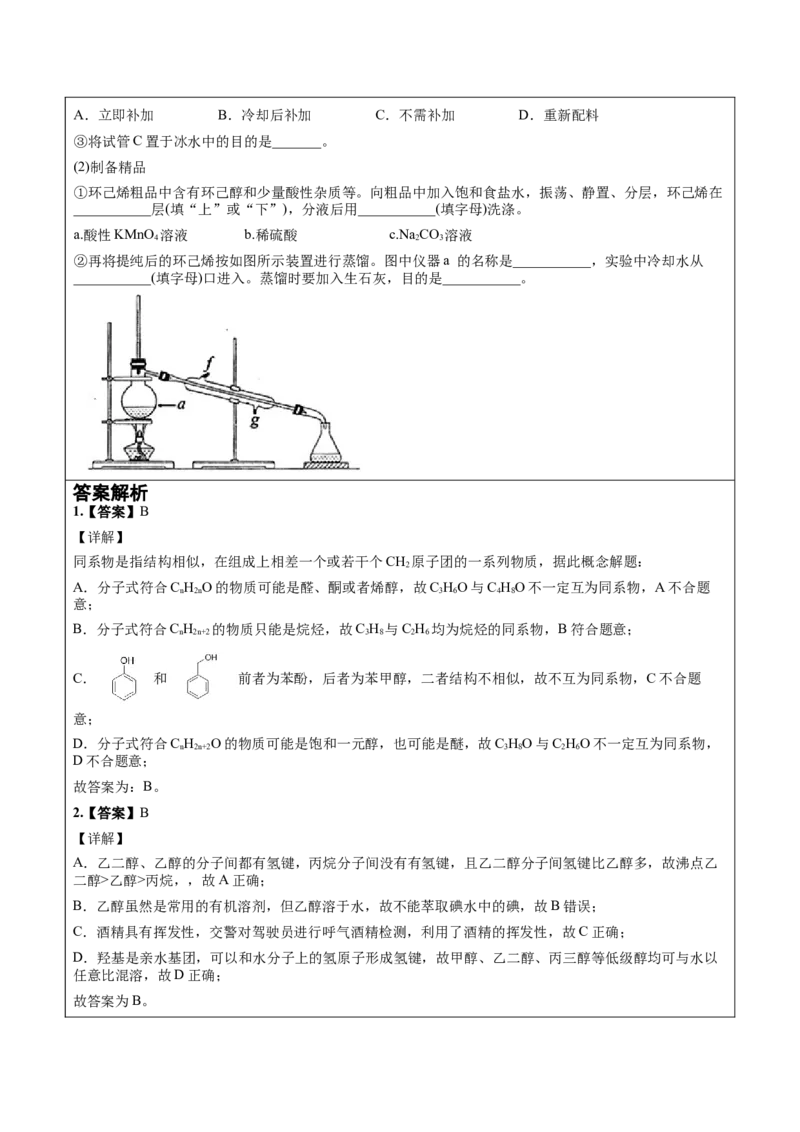
10.某化学小组采用下图所示的装置,用环己醇制备环己烯。
已知: +H O
2
相对分子质量 密度/g • cm-3 熔点/℃ 沸点/℃ 溶解性
环己醇 100 0.96 25 161 能溶于水
环己烯 82 0.81 -103 83 难溶于水
(1)制备粗品: 将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完
全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为______。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_____(填字母)。A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在
___________层(填“上”或“下”),分液后用___________(填字母)洗涤。
a.酸性KMnO 溶液 b.稀硫酸 c.Na CO 溶液
4 2 3
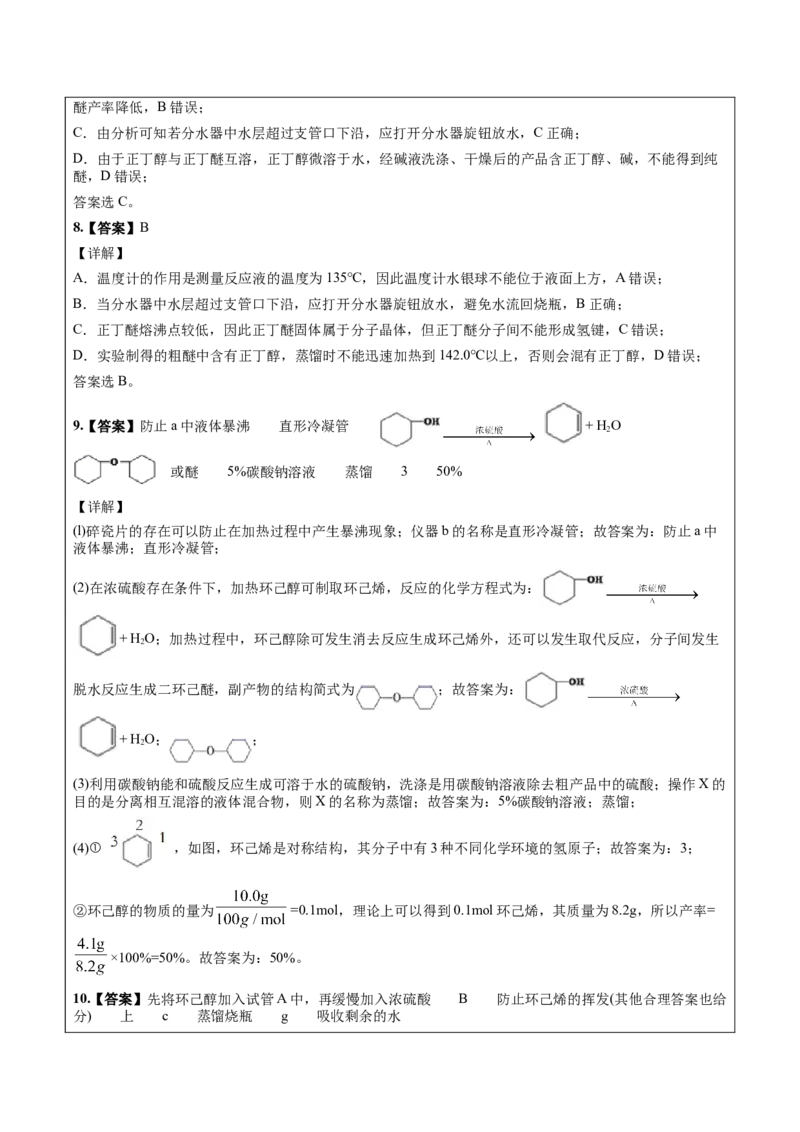
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是___________,实验中冷却水从
___________(填字母)口进入。蒸馏时要加入生石灰,目的是___________。
答案解析
1.【答案】B
【详解】
同系物是指结构相似,在组成上相差一个或若干个CH 原子团的一系列物质,据此概念解题:
2
A.分子式符合C H O的物质可能是醛、酮或者烯醇,故C HO与C HO不一定互为同系物,A不合题
n 2n 3 6 4 8
意;
B.分子式符合C H 的物质只能是烷烃,故C H 与C H 均为烷烃的同系物,B符合题意;
n 2n+2 3 8 2 6
C. 和 前者为苯酚,后者为苯甲醇,二者结构不相似,故不互为同系物,C不合题
意;
D.分子式符合C H O的物质可能是饱和一元醇,也可能是醚,故C HO与C HO不一定互为同系物,
n 2n+2 3 8 2 6
D不合题意;
故答案为:B。
2.【答案】B
【详解】
A.乙二醇、乙醇的分子间都有氢键,丙烷分子间没有有氢键,且乙二醇分子间氢键比乙醇多,故沸点乙
二醇>乙醇>丙烷,,故A正确;
B.乙醇虽然是常用的有机溶剂,但乙醇溶于水,故不能萃取碘水中的碘,故B错误;
C.酒精具有挥发性,交警对驾驶员进行呼气酒精检测,利用了酒精的挥发性,故C正确;
D.羟基是亲水基团,可以和水分子上的氢原子形成氢键,故甲醇、乙二醇、丙三醇等低级醇均可与水以
任意比混溶,故D正确;
故答案为B。3.【答案】A
【详解】
A.葡糖糖和麦芽糖都含有醛基,属于还原性糖,都能与新制氢氧化铜反应,故不能鉴别,故A错误;
B.乙醇能与氢卤酸发生取代,断裂碳氧键而失去羟基,故B正确;
C.C HO可能的结构是乙醇和甲醚,两者化学键不同的是乙醇中含有氢氧键,而甲醚中没有氢氧键,故
2 6
可以利用红外光谱区别,故C正确;
D.醇分子中的烷基具有推电子作用,导致醇分子中的氢氧键不容易断裂,故D正确;
故选A。
4.【答案】B
【详解】
A. 甘油能以任意比例和水互溶,故甘油能起到保湿作用,A错误;
B.红外光谱仪用于测定有机分子中所含的化学键或官能团,核磁共振氢谱用于测定有机物分子中氢原子
的种类和相对数目,所以红外光谱法与核磁共振氢谱可用于有机物分子结构的鉴定,B正确;
C. 蒸馏用于分离互溶的沸点相差大的液体混合物,故当液态有机物与杂质的沸点相差较大时可以用蒸馏
的方法提纯,C错误;
D. 乙醇催化氧化为乙醛,反应方程式为: ,每有2mol乙醇发
生反应、转移4mol电子,则 乙醇(即0.1mol)完全氧化成乙醛,转移电子数为 ,D错误;
答案选B。
5.【答案】D
【详解】
CH-CH=CH-CH OH含有碳碳双键,能与溴水发生加成反应,能被酸性高锰酸钾溶液氧化,CH-CH=CH-
3 2 3
CHOH含有羟基,能与钠反应,与羟基相连的碳原子上有氢,能与CuO反应,也能被酸性高锰酸钾溶液
2
氧化,所以①溴水②金属钠③灼热的CuO④酸性高锰酸钾溶液,在一定条件下,均能与该有机物反应,故
选D。
6.【答案】C
【详解】
A.乙烯含有碳碳双键,乙烯可发生加成反应,而乙烷不能,是因为官能团不同,故不选A;
B.乙醇分子能发生消去反应生成乙烯,2,2-二甲基-1-丙醇不能发生消去反应是因为与羟基相连碳原子的
邻碳原子上没有H原子,故不选B;
C.甲烷不能与酸性高锰酸钾反应,甲苯能与酸性高锰酸钾溶液反应,是因为苯环对甲基产生影响,故选
C;
D.等物质的量的丙三醇和乙醇分别与足量金属钠反应,丙三醇产生的H 多,是因为丙三醇中羟基个数
2
多,故不选D;
选C。
7.【答案】C
【详解】
A.B的作用是冷凝,为保证冷凝管充满水,得到最好的冷凝效果,则b为冷凝水进水口,A错误;
B.由反应方程式可知温度应控制在135℃,温度达到170℃正丁醇可能发生消去反应,副产物增多,正丁醚产率降低,B错误;
C.由分析可知若分水器中水层超过支管口下沿,应打开分水器旋钮放水,C正确;
D.由于正丁醇与正丁醚互溶,正丁醇微溶于水,经碱液洗涤、干燥后的产品含正丁醇、碱,不能得到纯
醚,D错误;
答案选C。
8.【答案】B
【详解】
A.温度计的作用是测量反应液的温度为135℃,因此温度计水银球不能位于液面上方,A错误;
B.当分水器中水层超过支管口下沿,应打开分水器旋钮放水,避免水流回烧瓶,B正确;
C.正丁醚熔沸点较低,因此正丁醚固体属于分子晶体,但正丁醚分子间不能形成氢键,C错误;
D.实验制得的粗醚中含有正丁醇,蒸馏时不能迅速加热到142.0℃以上,否则会混有正丁醇,D错误;
答案选B。
9.【答案】防止a中液体暴沸 直形冷凝管 + H O
2
或醚 5%碳酸钠溶液 蒸馏 3 50%
【详解】
(l)碎瓷片的存在可以防止在加热过程中产生暴沸现象;仪器b的名称是直形冷凝管;故答案为:防止a中
液体暴沸;直形冷凝管;
(2)在浓硫酸存在条件下,加热环己醇可制取环己烯,反应的化学方程式为:
+ H O;加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应,分子间发生
2
脱水反应生成二环己醚,副产物的结构简式为 ;故答案为:
+ H O; ;
2
(3)利用碳酸钠能和硫酸反应生成可溶于水的硫酸钠,洗涤是用碳酸钠溶液除去粗产品中的硫酸;操作X的
目的是分离相互混溶的液体混合物,则X的名称为蒸馏;故答案为:5%碳酸钠溶液;蒸馏;
(4)① ,如图,环己烯是对称结构,其分子中有3种不同化学环境的氢原子;故答案为:3;
②环己醇的物质的量为 =0.1mol,理论上可以得到0.1mol环己烯,其质量为8.2g,所以产率=
×100%=50%。故答案为:50%。
10.【答案】先将环己醇加入试管A中,再缓慢加入浓硫酸 B 防止环己烯的挥发(其他合理答案也给
分) 上 c 蒸馏烧瓶 g 吸收剩余的水【详解】
(1)①浓硫酸密度大于环己醇,混合环已醇和浓硫酸操作时,先将环己醇加入试管A中,再缓慢加入浓硫
酸;
②碎瓷片的作用是防爆沸,如果加热一段时间后发现忘记加碎瓷片,应该冷却后补加;
③试管C收集环己烯,环己烯的沸点83℃,易挥发,将试管C置于冰水中的目的是防止环己烯的挥发;
(2)①环己烯难溶于水、密度小于水,向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在上层;环己
烯粗品中含有少量酸性杂质,分液后用有关加入碱性溶液洗涤,所以用NaCO 溶液,故选c。
2 3
②根据图示,仪器a 的名称是蒸馏烧瓶,冷却水应该“低进高出”,实验中冷却水从 g口进入。氧化钙和
水反应生成氢氧化钙,蒸馏时加入生石灰,目的是吸收剩余的水。