文档内容
第三章 烃的衍生物
第一节 卤代烃
学 习 1.从卤代烃的官能团及其转化角度,认识卤代烃取代反应、消去反应的特点和规律,了解有机
反应类型与有机化合物分子结构特点之间的关系。
导航
2.了解某些卤代烃对环境和人身健康的影响,基于绿色化学的思想,摒弃卤代烃的使用或寻找
卤代烃替代品。
教 学 一、卤代烃
过程 1.概念与分类
2.卤代烃的命名
卤代烃的命名一般用系统命名法,与烃类的命名相似。例如:
、CH==CH—Cl、
2
2-氯丁烷 氯乙烯 1,2-二溴乙烷
3.物理性质
4.几种卤代烃的密度和沸点
名称 结构简式 沸点/℃
氯甲烷 CHCl 0.916 -24
3
氯乙烷 CHCHCl 0.898 12
3 2
1-氯丙烷 CHCHCHCl 0.890 46
3 2 2
1-氯丁烷 CHCHCHCHCl 0.886 78
3 2 2 2
1-氯戊烷 CHCHCHCHCHCl 0.882 108
3 2 2 2 2
二、取代反应 消去反应
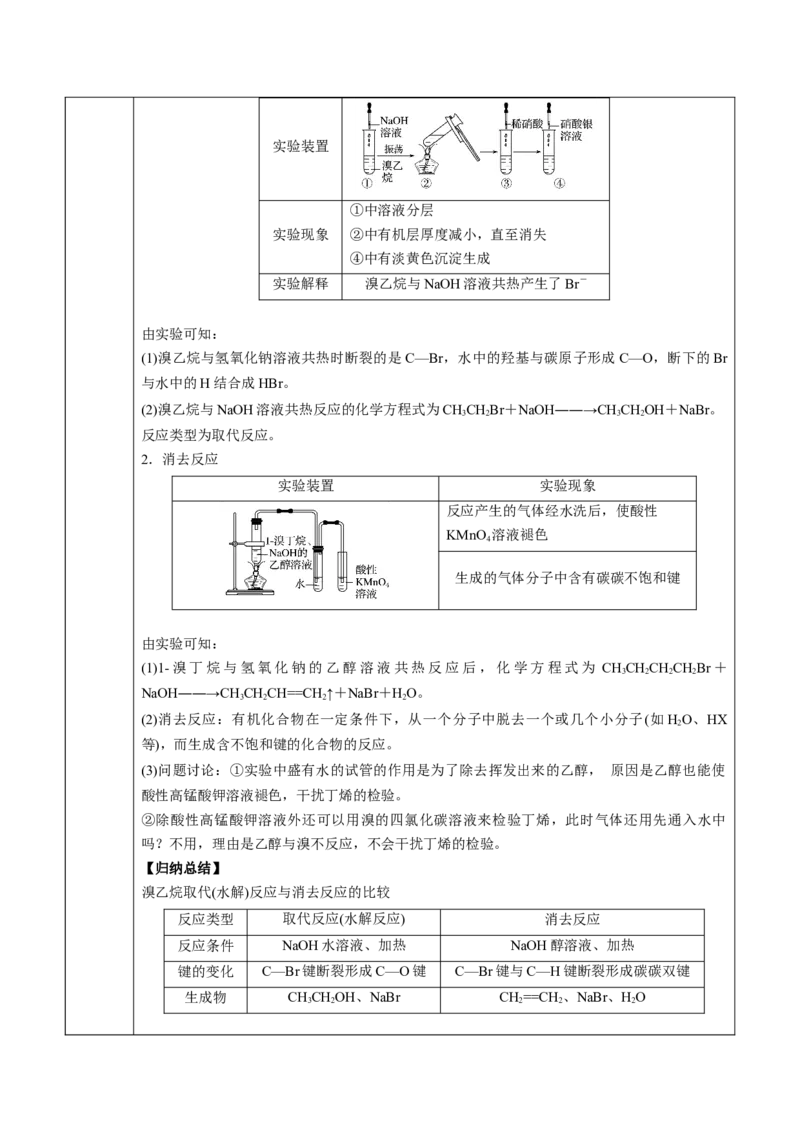
1.取代反应(水解反应)实验装置
①中溶液分层
实验现象 ②中有机层厚度减小,直至消失
④中有淡黄色沉淀生成
实验解释 溴乙烷与NaOH溶液共热产生了Br-
由实验可知:
(1)溴乙烷与氢氧化钠溶液共热时断裂的是C—Br,水中的羟基与碳原子形成C—O,断下的Br
与水中的H结合成HBr。
(2)溴乙烷与NaOH溶液共热反应的化学方程式为CHCHBr+NaOH――→CHCHOH+NaBr。
3 2 3 2
反应类型为取代反应。
2.消去反应
实验装置 实验现象
反应产生的气体经水洗后,使酸性
KMnO 溶液褪色
4
生成的气体分子中含有碳碳不饱和键
由实验可知:
(1)1-溴丁烷与氢氧化钠的乙醇溶液共热反应后,化学方程式为 CHCHCHCHBr+
3 2 2 2
NaOH――→CHCHCH==CH ↑+NaBr+HO。
3 2 2 2
(2)消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如HO、HX
2
等),而生成含不饱和键的化合物的反应。
(3)问题讨论:①实验中盛有水的试管的作用是为了除去挥发出来的乙醇, 原因是乙醇也能使
酸性高锰酸钾溶液褪色,干扰丁烯的检验。
②除酸性高锰酸钾溶液外还可以用溴的四氯化碳溶液来检验丁烯,此时气体还用先通入水中
吗?不用,理由是乙醇与溴不反应,不会干扰丁烯的检验。
【归纳总结】
溴乙烷取代(水解)反应与消去反应的比较
反应类型 取代反应(水解反应) 消去反应
反应条件 NaOH水溶液、加热 NaOH醇溶液、加热
键的变化 C—Br键断裂形成C—O键 C—Br键与C—H键断裂形成碳碳双键
生成物 CHCHOH、NaBr CH==CH 、NaBr、HO
3 2 2 2 2三、卤代烃的化学性质及卤代烃中卤素原子的检验
1.卤代烃的化学性质
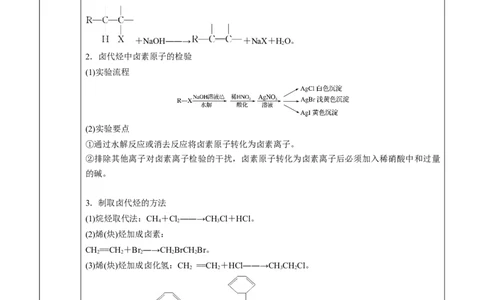
(1)取代反应(水解反应)
R—X+NaOH――→R—OH+NaX。
反应机理:在卤代烃分子中,由于卤素原子的电负性比碳原子的大,使 C—X的电子向卤素原
子偏移,进而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性
较强的共价键:Cδ+—Xδ-。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他
原子或原子团所取代,生成负离子而离去。
(2)消去反应
+NaOH――→ +NaX+HO。
2
2.卤代烃中卤素原子的检验
(1)实验流程
(2)实验要点
①通过水解反应或消去反应将卤素原子转化为卤素离子。
②排除其他离子对卤素离子检验的干扰,卤素原子转化为卤素离子后必须加入稀硝酸中和过量
的碱。
3.制取卤代烃的方法
(1)烷烃取代法:CH+Cl――→CHCl+HCl。
4 2 3
(2)烯(炔)烃加成卤素:
CH==CH +Br ―→CHBrCHBr。
2 2 2 2 2
(3)烯(炔)烃加成卤化氢:CH ==CH +HCl――→CHCHCl。
2 2 3 2
(4)芳香烃取代法: +Br ――→ +HBr。
2
特别提醒 工业上制备氯乙烷时,常用CH==CH 与 HCl发生加成反应制取,因为乙烯与氯
2 2
化氢反应产物纯净,易分离、提纯。
4.卤代烃的用途与危害
(1)用途:制冷剂、灭火剂、溶剂、麻醉剂、合成有机化合物。
(2)危害:含氯、溴的氟代烷可对臭氧层产生破坏作用,形成臭氧空洞,危及地球上的生物。
5.卤代烯烃
卤代烯烃的某些化学性质与烯烃的相似,能发生加成反应和加成聚合反应。例如,氯乙烯能加成聚合生成聚氯乙烯,四氟乙烯加成聚合生成聚四氟乙烯。聚氯乙烯和聚四氟乙烯都是用途广
泛的高分子材料。
nCF==CF ―→CF —CF
2 2 2 2
四氟乙烯 聚四氟乙烯
课时训练
1.四氯化碳常常用于灭火,若按官能团分类,四氯化碳应该属于
A.烷烃 B.烯烃 C.卤代烃 D.羧酸
2.由CHCH→CHCHCl→CH = CH→CHCHOH的转化过程中,经过的反应是
3 3 3 2 2 2 3 2
A.取代→消去→加成 B.裂解→取代→消去
C.取代→加成→氧化 D.取代→消去→水解
3.据调查,劣质的家庭装饰材料会释放出近百种能引发疾病的有害物质,其中一种有机物分子的球棍模
型如图,图中“棍”代表单键或双键或三键,不同大小的球代表不同元素的原子,且三种元素位于不同的
短周期。下面关于该有机物的叙述不正确的是
A.有机物化学式为
B.分子中所有原子在同一个平面内
C.该有机物难溶于水
D.可由乙炔和氯化氢加成得到
4.化学知识在生产生活中有广泛的应用,下列物质的性质与应用有对应关系的是
A.石墨的熔点很高,可用作干电池电极材料
B.Fe的金属性比Cu强,FeCl 浓溶液可腐蚀Cu用于刻制印刷电路板
3
C.溴能与很多有机物反应,在药物合成方面有广泛应用
D.NH 断键时要吸收能量,工业上常用液氨作制冷剂
3
5.由2—氯丙烷制取少量1,2—丙二醇( )时,需要经过下列哪几步反应
A.加成反应→消去反应→取代反应 B.消去反应→加成反应→消去反应
C.消去反应→加成反应→取代反应 D.取代反应→消去反应→加成反应
6.下列实验装置不能达到相应实验目的的是A.用甲装置验证NH 在水中的溶解度大
3
B.用乙装置验证牺牲阳极保护法
C.用丙装置将CuC1 溶液蒸干制备CuC1
2 2
D.用丁装置验证溴乙烷的消去产物是乙烯
7.下列操作能达到实验目的的是
实验目的 实验操作
A 验证可溶性 为强酸强碱盐 25℃,测得可溶性正盐 溶液的
B 除去 中的 气体 依次通过盛有饱和 溶液和浓硫酸的洗气瓶
C 除去 中的 加入足量 浓溶液充分反应后过滤,洗涤
先滴加 水溶液,加热,再加入 溶液有白色沉
D 检验氯乙烷中的氯原子
淀生成
A.A B.B C.C D.D
8.实验室由叔丁醇(沸点82℃)与浓盐酸反应制备2-甲基-2-氯丙烷(沸点52℃)路线如下:
下列说法错误的是
A.室温搅拌的目的是为了加快反应速率
B.用5%NaCO 溶液洗涤分液时,先将上层的有机相由分液漏斗上口放出
2 3
C.两次水洗主要目的是分别除去有机相中的盐酸与钠盐
D.蒸馏收集2-甲基-2-氯丙烷时,应选用直形冷凝管
9.(1)写出下列物质的分子式①含有18个氢原子的烷烃___________
②含有6个碳原子的单环烷烃___________
(2)用系统命名法命名下列有机化合物(CH)C(CH)C(CH)___________; ___________
3 3 2 5 3 3
(3)分子式为C HCl的卤代烃的所有同分异构体的结构简式___________
3 7
(4)画出下列烷烃的键线式
2,5-二甲基-3-乙基庚烷___________;1,1,4-三甲基环己烷___________
(5)烷烃分子式为C H ,写出分结子构中主链有6个碳原子,支链有一个甲基和一个乙基的所有同分异构
9 20
体的结构简式___________
10.实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理为:
; 。有关实验装
置(省去加热装置)和数据如下:
乙醇 溴乙烷 溴
状态 无色液体 无色液体 深红棕色液体
密度/ 0.79 1.44 3.1
沸点/℃ 78.5 38.4 59
相对分子质量 46 109 160
请回答:
(1)仪器B的名称是___________,进水口是___________(填“a”或“b”)。
(2)装置A中加入沸石的作用是___________,如果加热一段时间后发现忘记加沸石,应该釆取的正确操作
是___________(填字母)。
A.不需补加 B.立即补加 C.冷却后补加 D.重新配料
(3)装置C的作用是___________。(4)支管D接橡皮管导入 溶液,其目的是吸收溴蒸气和另一种污染性气体,请写出产生该气体的化
学方程式___________。
(5)将试管中收集到的液体,经除杂、分液、蒸馏等操作,得到35~40℃的馏分约 ,则所得溴乙烷的
产率约为___________(精确到0.1%)。
答案解析
1.【答案】C
【详解】
A.烷烃中不含官能团,故A不选;
B.烯烃的官能团为碳碳双键,故B不选;
C.卤代烃的官能团为卤素原子,则四氯化碳属于卤代烃,故C选;
D.羧酸的官能团为-COOH,故D不选;
故选C。
2.【答案】A
【详解】
乙烷和氯气在光照的条件下发生取代反应,生成氯乙烷,氯乙烷通过消去反应生成乙烯,乙烯和水发生加
成反应生成乙醇。
故选A。
3.【答案】D
【分析】
结构中间的两个球型代表C原子,那么,最小的原子应该是H原子,剩下三个半径比C原子模型还大的球
型应该是代表Cl原子。
【详解】
A.根据分析信息,确定模型代表的有机物分子中有两个C,一个H,三个Cl,化学式是 ,描述
正确,不符题意;
B.根据原子个数,可以推测出两个碳原子之间是碳碳双键,故该分子空间结构应与乙烯相同,所以所有
原子处于同一平面,描述正确,不符题意;
C.该有机物属于卤代烃,卤代烃均难溶于水,描述正确,不符题意;
D.乙炔加成一分子氯化氢,得到的产物是 ,描述错误,符合题意;
综上,本题选D。
4.【答案】C
【详解】
A.石墨具有导电性,可用作干电池电极材料,与其熔点高无关,A不符合题意;
B.FeCl 腐蚀Cu刻制印刷电路板,是因为Fe3+具有氧化性,与铁和铜的活泼性大小无关,不能说明铁比铜
3
金属性强,B不符合题意;
C.溴能与很多有机物发生取代反应和加成反应等从而形成溴代物,在药物合成方面有广泛应用,C符合
题意;
D.液氨汽化时吸收大量的热,使周围的温度急剧降低,工业上可使用液氨作制冷剂,与其化学键无关,
D不符合题意;故选C。
5.【答案】C
【详解】
由2-氯丙烷制取少量的1,2-丙二醇,可用逆推法判断:
CHCHOHCH OH→CH CHBrCH Br→CHCH=CH→CHCHClCH ,则2-氯丙烷应首先发生消去反应生成
3 2 3 2 3 2 3 3
CHCH=CH,CHCH=CH 发生加成反应生成CHCHBrCH Br,CHCHBrCH Br发生取代反应可生成1,2-
3 2 3 2 3 2 3 2
丙二醇。故选:C。
6.【答案】C
【详解】
A.氨气极易溶于水,挤压甲装置中的胶头滴管,气球会膨胀,故A正确;
B.乙装置为原电池装置,酸性条件下,Zn作负极,Fe作正极被保护,为牺牲阳极的阴极保护法,正极区
域无明显现象,故B正确;
C.氯化铜为挥发性酸的强酸弱碱盐,直接加热蒸干时会发生水解反应,最终得到氧化铜固体,故C错
误;
D.溴乙烷在NaOH的醇溶液中,加热时发生消去反应,生成乙烯,能使溴的四氯化碳溶液褪色,故D正
确;
故选C。
7.【答案】C
【详解】
A.25℃,测得可溶性正盐 溶液的 ,不能证明验证可溶性 为强酸强碱盐,也可能是水解程
度相同的弱酸弱碱盐,A不合题意;
B.由于碳酸钠溶液与二氧化碳会反应,故不能依次通过盛有饱和 溶液和浓硫酸的洗气瓶来除去
中的 气体,应该依次通过盛有饱和 溶液和浓硫酸的洗气瓶来除去,B不合题意;
C.由于Ca(OH) +MgCl =Mg(OH) ↓+CaCl ,故可以用加入足量 浓溶液充分反应后过滤,洗涤的操
2 2 2 2
作来除去 中的 ,C符合题意;
D.由于NaOH过量, 与NaOH会反应将生成黑色的氧化银,掩盖白色的氯化银,故检验氯乙烷
中的氯原子,应先滴加 水溶液,加热,再加入过量的HNO 将溶液先酸化再加入 溶液有白
3
色沉淀生成,D不合题意;
故答案为:C。
8.【答案】B
【分析】
叔丁醇与浓盐酸常温搅拌反应15min可得2-甲基-2-氯丙烷与HO,分液后向有机相中加入水进行洗涤分
2
液,继续向有机相中加入,5%Na CO 溶液洗涤,由于有机物2-甲基-2-氯丙烷的密度小于水,分液后获得
2 3
上层有机相,有机相中加入少量无水CaCl 干燥,蒸馏即得有机物2-甲基-2-氯丙烷。
2
【详解】
A.室温搅拌可以加快反应速率,A项正确;
B.5%Na CO 溶液洗涤,有机物2-甲基-2-氯丙烷的密度小于水,上层为有机相,下层为水相,先放掉下
2 3
层液体,再将上层的有机相由分液漏斗上口放出,B项错误;C.第一次水洗是为了除去有机相中的盐酸,第二次水洗是为了除去有机相中碳酸钠,C项正确;
D.蒸馏时,应选用直形冷凝管,D项正确;
答案选B。
9.【答案】C H C H 2,2,8,8-四甲基壬烷 3-甲基-3-乙基戊烷 CHCHCHCl和
8 18 6 12 3 2 2
CHCHClCH (CH )CHCH(C H)CHCHCH、
3 3 3 2 2 5 2 2 3
(CH)CHCH CH(C H)CHCH、(C H)C(CH)CHCHCH、CHCHCH(CH )CH(C H)
3 2 2 2 5 2 3 2 5 2 3 2 2 3 3 2 3 2 5 2
【详解】
(1)①链状烷烃的通式为C H ,含有18个氢原子的烷烃,即2n+2=18,解得n=8,所以分子式为
n 2n+2
C H ;
8 18
②单环烷烃的通式为C H ,含有6个碳原子的单环烷烃的分子式为C H ;
n 2n 6 12
(2)(CH )C(CH)C(CH) 属于链状烷烃,主链含有9个碳原子,4个甲基作支链,其名称是2,2,8,8-四
3 3 2 5 3 3
甲基壬烷; 属于链状烷烃,主链含有5个碳原子,1个甲基和1个乙基作支链,其名
称是3-甲基-3-乙基戊烷;
(3)丙烷分子中含有2类氢原子,则分子式为C HCl的卤代烃的所有同分异构体的结构简式为
3 7
CHCHCHCl和CHCHClCH ;
3 2 2 3 3
(4)2,5-二甲基-3-乙基庚烷属于链状烷烃,其键线式为 ;1,1,4-三甲基环己烷属于
环烷烃,键线式为 ;
(5)烷烃分子式为C H ,分子结构中主链有6个碳原子,支链有一个甲基和一个乙基,由于乙基只能放在3
9 20
或4号碳原子上,则所有同分异构体的结构简式为(CH)CHCH(C H)CHCHCH、
3 2 2 5 2 2 3
(CH)CHCH CH(C H)CHCH、(C H)C(CH)CHCHCH、CHCHCH(CH )CH(C H)。
3 2 2 2 5 2 3 2 5 2 3 2 2 3 3 2 3 2 5 2
10.【答案】(球形)冷凝管 b 防止暴沸 C 冷凝并减少溴乙烷的挥发
53.4%
【详解】
(1)根据装置图可知,仪器B的名称为(球形)冷凝管;为使冷凝效果更佳,冷凝管中冷凝水应装满,因此冷
凝水为b进a出,故答案为:(球形)冷凝管;b;
(2)液体加热加入沸石,可以防止液体暴沸;如果加热一段时间后发现忘记加沸石,应该釆取的正确操作是
冷却后补加,故答案为:防止暴沸;C;
(3)由表格数据可知,溴乙烷的沸点相对较低,蒸馏而得的气流中含有溴乙烷、乙醇、HBr等,利用装置C
中冷水进行冷凝,可减少溴乙烷的挥发,故答案为:冷凝并减少溴乙烷的挥发;
(4)浓硫酸具有强氧化性,HBr具有还原性,在加热条件下二者能够发生氧化还原生成SO 、Br ,反应方程
2 2式为 ;
(5)将试管中收集到的液体,经除杂、分液、蒸馏等操作,得到35~40℃的馏分约10.0g,该馏分为溴乙
烷,10.0mL 乙醇的质量为 10.0mL×0.79g/cm3=7.9g,设溴乙烷理论产量为 x,根据质量守恒可知
,解得x=18.72g,则所得溴乙烷的产率约为 ×100%=53.4%。