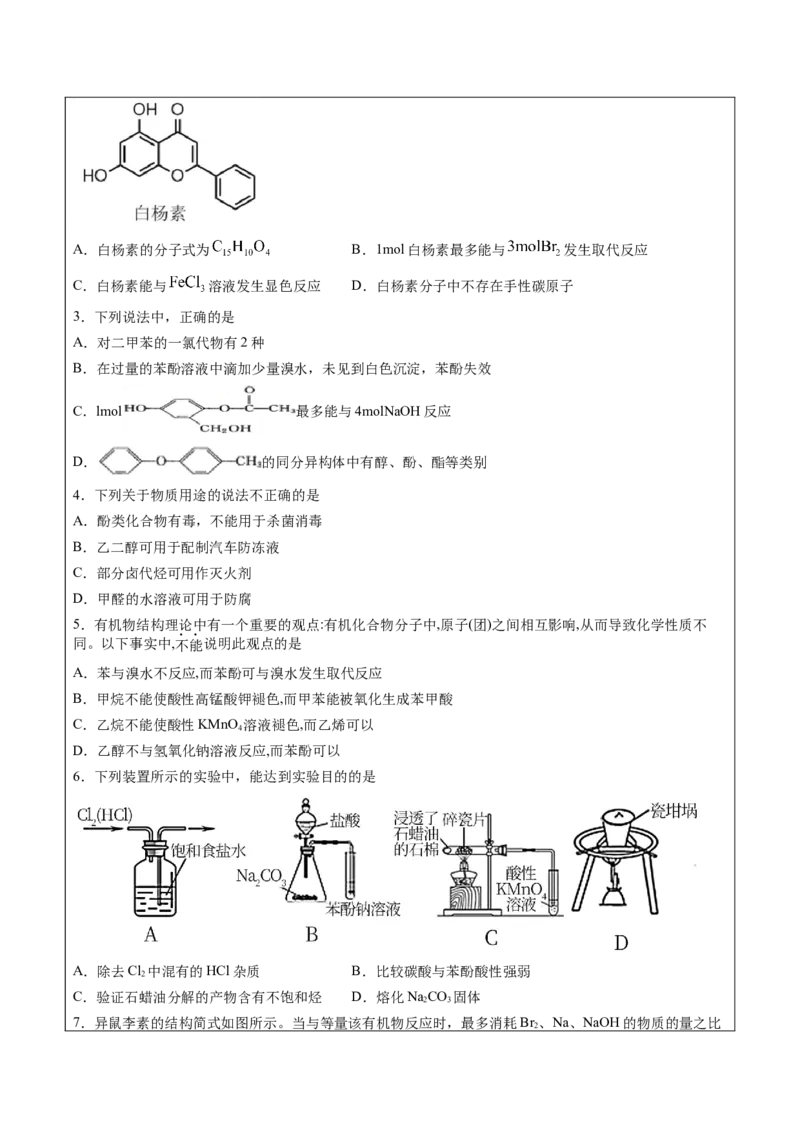
文档内容
第三章 烃的衍生物
第二节 醇 酚
第 2 课时 酚
学习导航 1.通过认识酚分子中羟基连接方式的不同,了解苯酚的主要性质,理解羟基和苯环的相互
影响,形成物质结构决定性质的核心理念。
2.通过苯酚性质的学习,了解苯酚及酚类毒性及其对环境的危害,要合理应用。
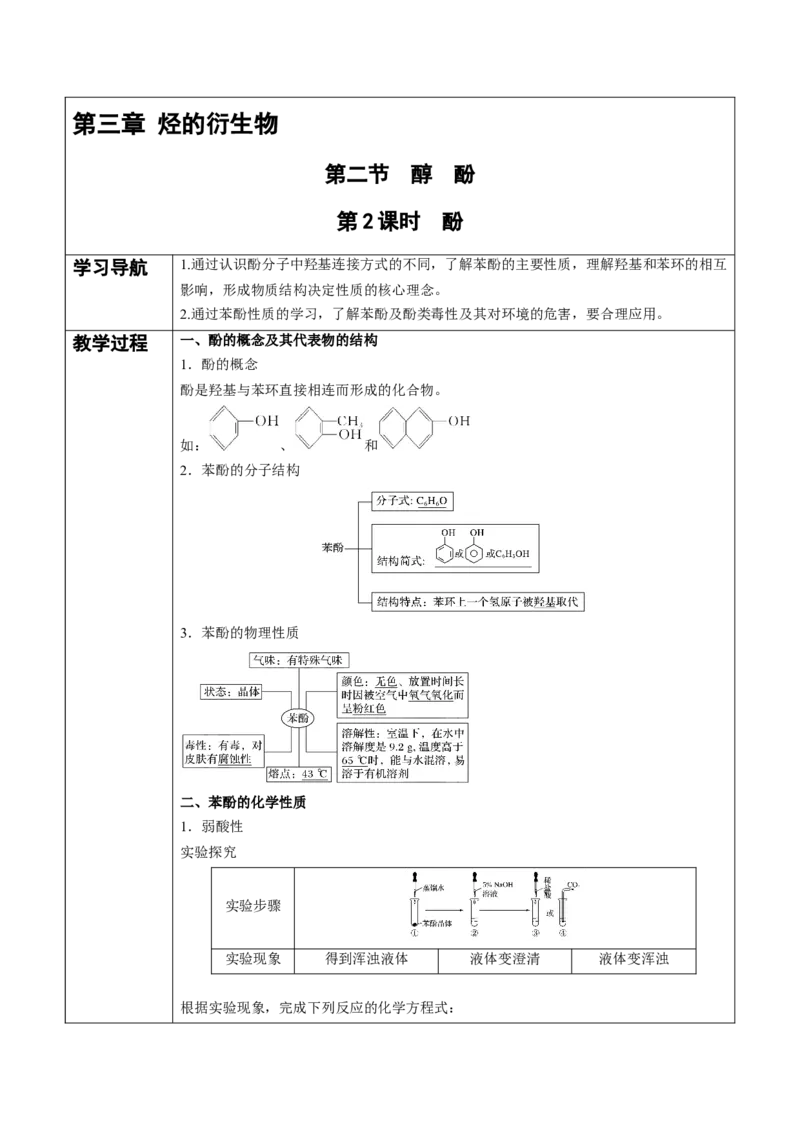
教学过程 一、酚的概念及其代表物的结构
1.酚的概念
酚是羟基与苯环直接相连而形成的化合物。
如: 、 和
2.苯酚的分子结构
3.苯酚的物理性质
二、苯酚的化学性质
1.弱酸性
实验探究
实验步骤
实验现象 得到浑浊液体 液体变澄清 液体变浑浊
根据实验现象,完成下列反应的化学方程式:试管②: +NaOH―→ +HO。
2
试管③: +HCl―→ +NaCl。
试管④: +CO+HO―→ +NaHCO 。
2 2 3
2.取代反应
实验探究
实验步骤:向盛有少量苯酚稀溶液的试管中滴加过量的饱和溴水。
现象:有白色沉淀生成。
反应的化学方程式:
+3Br ―→ +3HBr,在此反应中,苯酚分子中苯环上的氢原子
2
被溴原子取代,发生了取代反应。
3.显色反应
实验探究
实验过程:在少量苯酚溶液中滴加氯化铁溶液。
现象:溶液显紫色。
4.氧化反应
苯酚是无色晶体,但放置时间过长往往显粉红色,其原因是部分苯酚被空气中的氧气氧
化。
5.苯、苯酚与Br 反应的比较
2
类别 苯 苯酚
溴的状态 液溴 饱和溴水
条件 催化剂 无催化剂
取代
产物
反应
特点 苯酚与溴的取代反应比苯易进行
原因 酚羟基对苯环的影响使苯环上的邻、对位氢原子变得活泼,易被取代
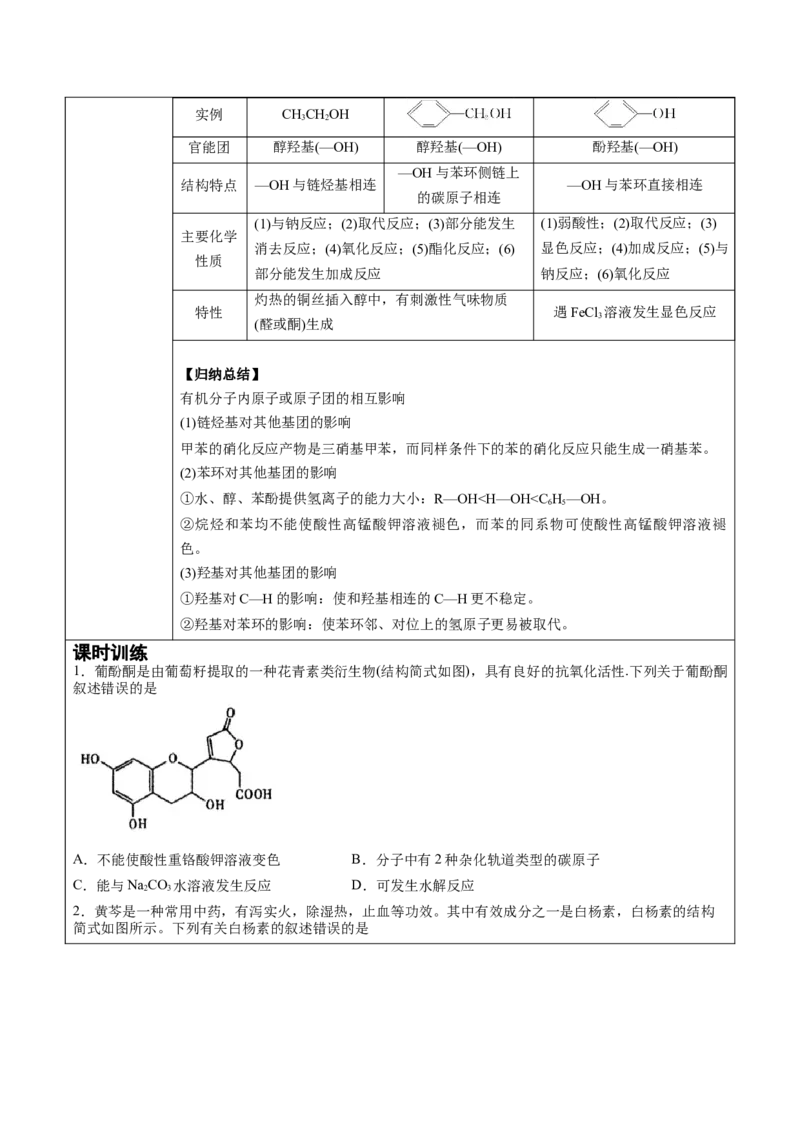
6.脂肪醇、芳香醇和酚的比较
类别 脂肪醇 芳香醇 酚实例 CHCHOH
3 2
官能团 醇羟基(—OH) 醇羟基(—OH) 酚羟基(—OH)
—OH与苯环侧链上
结构特点 —OH与链烃基相连 —OH与苯环直接相连
的碳原子相连
(1)与钠反应;(2)取代反应;(3)部分能发生 (1)弱酸性;(2)取代反应;(3)
主要化学
消去反应;(4)氧化反应;(5)酯化反应;(6) 显色反应;(4)加成反应;(5)与
性质
部分能发生加成反应 钠反应;(6)氧化反应
灼热的铜丝插入醇中,有刺激性气味物质
特性 遇FeCl 溶液发生显色反应
3
(醛或酮)生成
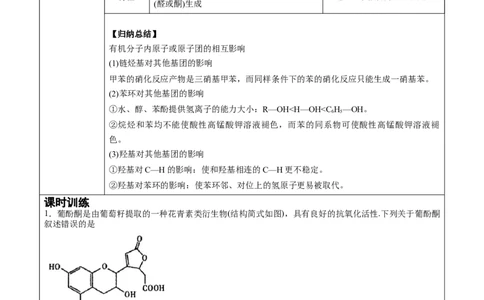
【归纳总结】
有机分子内原子或原子团的相互影响
(1)链烃基对其他基团的影响
甲苯的硝化反应产物是三硝基甲苯,而同样条件下的苯的硝化反应只能生成一硝基苯。
(2)苯环对其他基团的影响
①水、醇、苯酚提供氢离子的能力大小:R—OH