文档内容
第三节 醛 酮
发 展 目 标 体 系 构 建
1.以乙醛为例,了解醛类的组成、
结构特点,理解醛的主要化学性
质及应用,培养“微观探析与变
化观念”的核心素养。
2.知道酮的结构特点、主要性质及
应用,培养“宏观辨识与社会责
任”的核心素养。
3.了解醛、酮在有机合成中的重要
应用,培养“科学态度和社会责
任”的核心素养。
一、乙醛
1.醛的定义与通式
(1)定义:由 烃基 ( 或氢原子 )与醛基相连而构成的化合物,其官能团的结构简
式为 ,简写为 — CHO 。
(2)通式:饱和一元醛的通式为C H O。
n 2n
微点拨:醛基的结构简式为—CHO,不能写成—COH。
2.乙醛的物理性质与结构
(1)物理性质
乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥
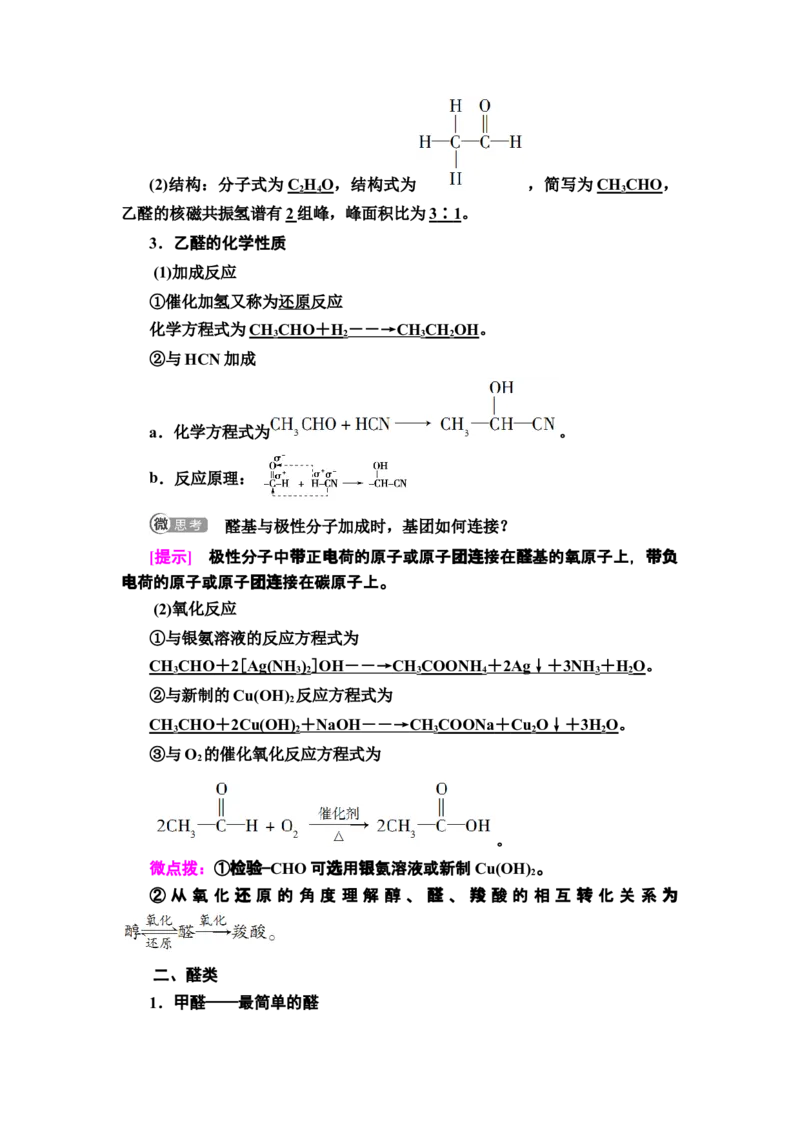
发,易燃烧,能与水、乙醇等互溶。(2)结构:分子式为C H O,结构式为 ,简写为CH CHO,
2 4 3
乙醛的核磁共振氢谱有2 组峰,峰面积比为 3 ∶ 1 。
3.乙醛的化学性质
(1)加成反应
①催化加氢又称为还原反应
化学方程式为CH CHO + H ――→ CH CH OH。
3 2 3 2
②与HCN加成
a.化学方程式为 。
b.反应原理:
醛基与极性分子加成时,基团如何连接?
[提示] 极性分子中带正电荷的原子或原子团连接在醛基的氧原子上,带负
电荷的原子或原子团连接在碳原子上。
(2)氧化反应
①与银氨溶液的反应方程式为
CH CHO + 2 [ Ag(NH ) ] OH ――→ CH COONH + 2A g ↓ + 3NH + H O。
3 3 2 3 4 3 2
②与新制的Cu(OH) 反应方程式为
2
CH CHO + 2Cu(OH) + NaOH ――→ CH COONa + Cu O ↓ + 3H O。
3 2 3 2 2
③与O 的催化氧化反应方程式为
2
。
微点拨:①检验—CHO可选用银氨溶液或新制Cu(OH) 。
2
② 从 氧 化 还 原 的 角 度 理 解 醇 、 醛 、 羧 酸 的 相 互 转 化 关 系 为
二、醛类
1.甲醛——最简单的醛甲醛又叫蚁醛,是一种无色、有强烈刺激性气味的气味,易溶于水。其水
溶液又称福尔马林,具有杀菌、防腐性能,可用于消毒和制作生物标本。
2.苯甲醛是最简单的芳香醛,俗称苦杏仁油,是一种有苦杏仁气味的无色
液体。苯甲醛是制造染料、香料及药物的重要原料。
微点拨:桂皮中含肉桂醛( );杏仁中含苯甲醛(
)。
三、酮
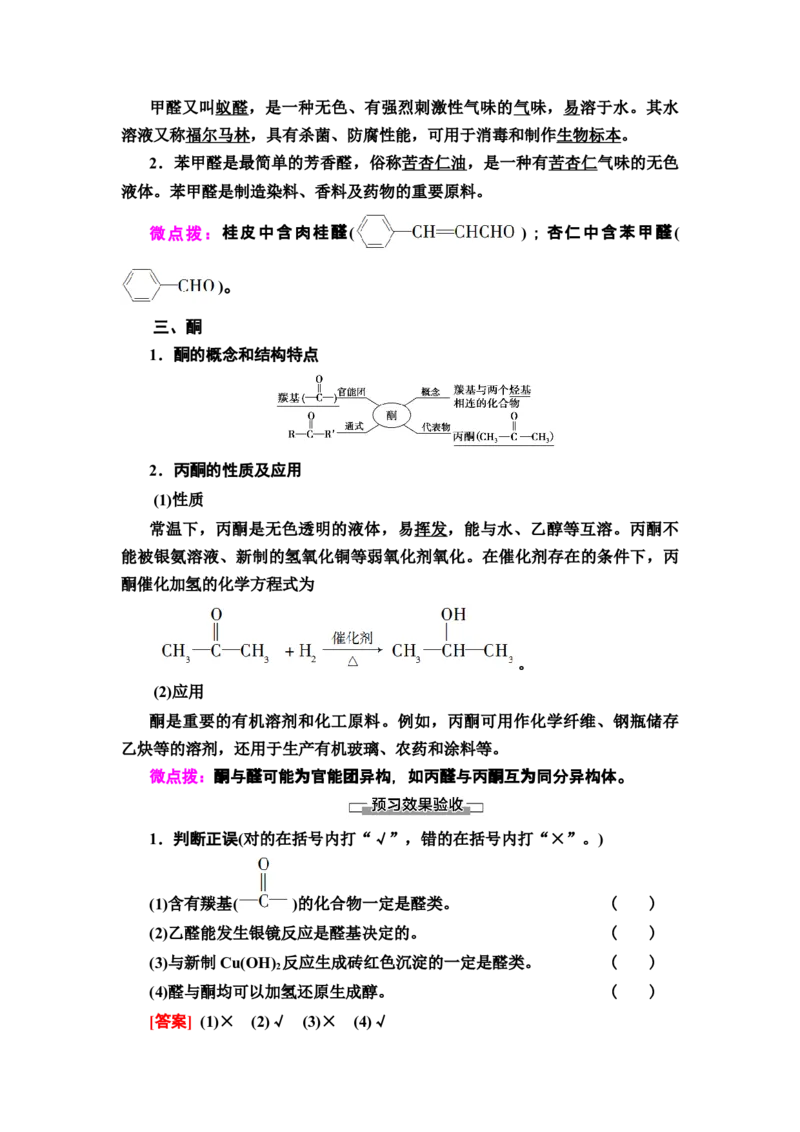
1.酮的概念和结构特点
2.丙酮的性质及应用
(1)性质
常温下,丙酮是无色透明的液体,易挥发,能与水、乙醇等互溶。丙酮不
能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化。在催化剂存在的条件下,丙
酮催化加氢的化学方程式为
。
(2)应用
酮是重要的有机溶剂和化工原料。例如,丙酮可用作化学纤维、钢瓶储存
乙炔等的溶剂,还用于生产有机玻璃、农药和涂料等。
微点拨:酮与醛可能为官能团异构,如丙醛与丙酮互为同分异构体。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)含有羰基( )的化合物一定是醛类。 ( )
(2)乙醛能发生银镜反应是醛基决定的。 ( )
(3)与新制Cu(OH) 反应生成砖红色沉淀的一定是醛类。 ( )
2
(4)醛与酮均可以加氢还原生成醇。 ( )
[答案] (1)× (2)√ (3)× (4)√2.下列物质中不能发生银镜反应的是( )
[答案] D
3.分别写出丙醛与下列物质反应的化学方程式。
(1)与银氨溶液反应___________________________________
_____________________________________________________。
(2)与新制的氢氧化铜反应_____________________________
_____________________________________________________。
(3)与氢气反应__________________________________________
_____________________________________________________。
(4)与氰化氢反应________________________________________
_____________________________________________________。
[答案] (1)CH CH CHO+2[Ag(NH ) ]OH――→CH CH COONH +2Ag↓
3 2 3 2 3 2 4
+3NH +H O
3 2
(2)CH CH CHO+2Cu(OH) +NaOH――→CH CH COONa+Cu O↓+
3 2 2 3 2 2
3H O
2
(3)CH CH CHO+H ――→CH CH CH OH
3 2 2 3 2 2
醛的主要性质及醛基的检验
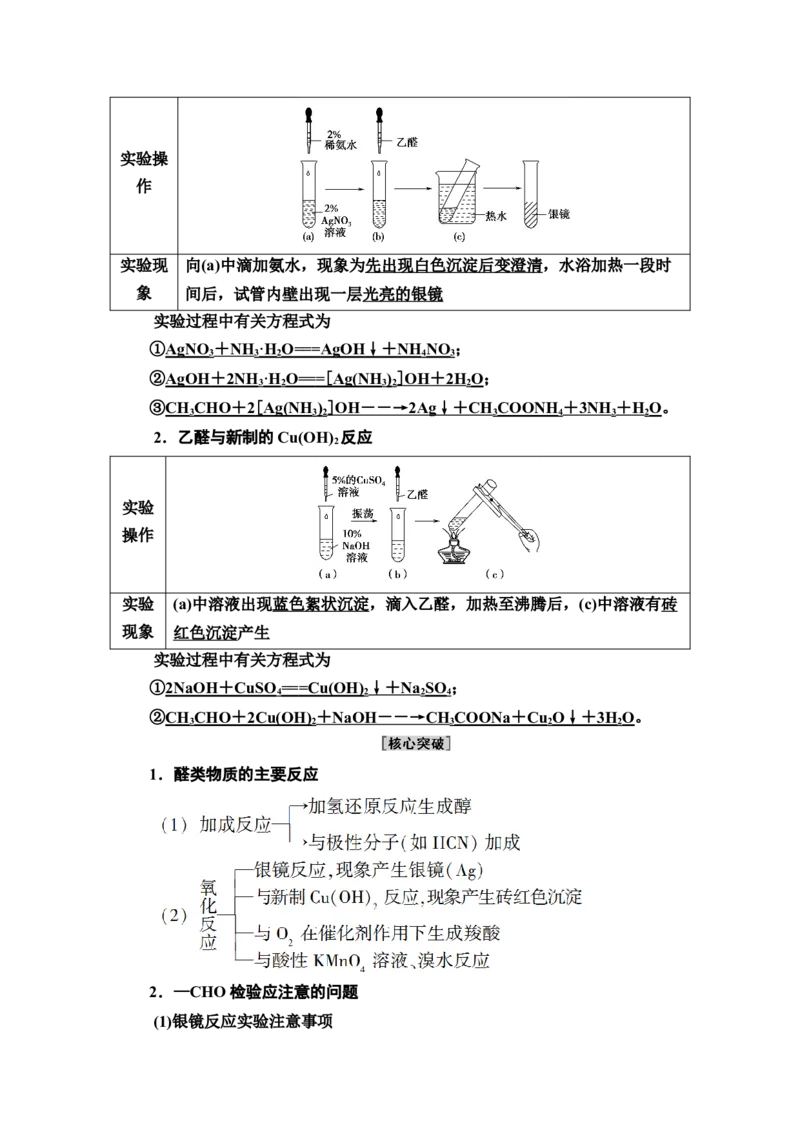
1.乙醛的银镜反应实验操
作
实验现 向(a)中滴加氨水,现象为先出现白色沉淀后变澄清,水浴加热一段时
象 间后,试管内壁出现一层光亮的银镜
实验过程中有关方程式为
①AgNO + NH ·H O == = AgOH ↓ + NH NO ;
3 3 2 4 3
② AgOH + 2NH ·H O == = [ Ag(NH ) ] OH + 2H O;
3 2 3 2 2
③CH CHO + 2 [ Ag(NH ) ] OH ――→ 2A g ↓ + CH COONH + 3NH + H O。
3 3 2 3 4 3 2
2.乙醛与新制的Cu(OH) 反应
2
实验
操作
实验 (a)中溶液出现蓝色絮状沉淀,滴入乙醛,加热至沸腾后,(c)中溶液有砖
现象 红色沉淀产生
实验过程中有关方程式为
① 2NaOH + CuSO == = Cu(OH) ↓ + N a SO ;
4 2 2 4
②CH CHO + 2Cu(OH) + NaOH ――→ CH COONa + Cu O ↓ + 3H O。
3 2 3 2 2
1.醛类物质的主要反应
2.—CHO检验应注意的问题
(1)银镜反应实验注意事项①试管要洁净,否则单质银不易附着在试管内壁上,会生成黑色的银沉淀,
而得不到光亮的银镜。洗涤试管时一般要先用热的NaOH溶液洗,再用水洗。
②银氨溶液必须现用现配,不可久置,否则会生成易爆物质。
③配制银氨溶液时,氨水、硝酸银溶液都必须是稀溶液,且是将稀氨水逐
滴加入稀硝酸银溶液中(顺序不能颠倒),直到最初生成的沉淀恰好溶解为止,
氨水不能过量,否则也会生成易爆物质。
④银镜反应的条件是水浴加热,不能直接加热,加热时不可振荡或摇动试
管,以防生成黑色的银,而不能在试管内壁形成光亮的银镜。
⑤实验结束后,试管内壁附着的银镜,可用稀硝酸浸泡,待银溶解后再用
自来水、蒸馏水洗涤干净。
(2)乙醛与新制Cu(OH) 反应实验注意事项
2
①所用Cu(OH) 悬浊液必须是新制备的。
2
②配制Cu(OH) 悬浊液时,必须保证NaOH溶液过量,即保证所得溶液呈
2
碱性。
③用酒精灯直接加热试管至溶液沸腾,才有明显的砖红色沉淀产生。
④加热煮沸时间不能过久,否则会导致Cu(OH) 分解成CuO而出现黑色沉
2
淀。
1.丙烯醛的结构简式为 CH ===CH—CHO。下列关于它的性质的叙述中
2
错误的是 ( )
A.能使溴水褪色,也能使酸性高锰酸钾溶液褪色
B.在一定条件下与H 充分反应,生成1丙醇
2
C.能发生银镜反应,且反应过程中表现出氧化性
D.在一定条件下能被空气中的氧气氧化
C [丙烯醛(CH ===CH—CHO)分子中含碳碳双键,能使溴水褪色,也能
2
使酸性高锰酸钾溶液褪色,故 A正确;碳碳双键、—CHO均能与氢气发生加成
反应,丙烯醛在一定条件下与H 充分反应生成1丙醇,故B正确;丙烯醛含—
2
CHO,能发生银镜反应,表现出还原性,故 C错误;—CHO在催化剂、加热条
件下能被空气中的氧气氧化,故D正确。]
2.某学生将2 mL 1 mol·L-1的CuSO 溶液和4 mL 0.5 mol·L-1的NaOH溶
4
液混合,然后加入0.5 mL 40%的乙醛溶液,加热到沸腾,未见砖红色沉淀,失
败的主要原因是( )
A.乙醛的量太少 B.硫酸铜的量太少C.NaOH的量太少 D.加热时间短
C [由题中数据可知CuSO 和NaOH的物质的量之比为1∶1,表明CuSO
4 4
过量,碱不足;而醛与新制Cu(OH) 悬浊液反应时碱必须过量。]
2
3.醛类因易被氧化为羧酸,而易使酸性KMnO 溶液或溴水褪色。向乙醛
4
中滴加酸性KMnO 溶液, 可观察到的现象是
4
_____________________________________________________。
现已知柠檬醛的结构简式为
若要检验其中的碳碳双键,能否直接加入酸性KMnO 溶液或溴水?为什么?
4
______________________________________________
_____________________________________________________。
经常使用的实验方法是什么?___________________________
_______________________________________________________
_____________________________________________________。
[解析] 乙醛的结构简式为 CH CHO,官能团是醛基,向乙醛中滴加酸性
3
高锰酸钾溶液,乙醛被氧化,所以可观察到酸性高锰酸钾溶液褪色;检验碳碳
双键的存在,常用方法是取少量待测物于试管中,向其中加入溴水或酸性高锰
酸钾溶液,若溴水或酸性高锰酸钾溶液褪色,则该物质的分子结构中含有碳碳
双键。但柠檬醛的分子结构中不仅含有碳碳双键,还含有醛基,醛基具有还原
性,也能使溴水或酸性高锰酸钾溶液褪色,因此要检验柠檬醛分子结构中的碳
碳双键,必须把醛基转变为不具有还原性的基团,方法是取少量柠檬醛与足量
新制银氨溶液混合,并置于热水浴中加热,充分反应后,取少量上层清液置于
另一试管中,并滴加溴水或酸性高锰酸钾溶液,充分振荡,若溴水或酸性高锰
酸钾溶液褪色,则可证明柠檬醛分子结构中含有碳碳双键。
[答案] 酸性KMnO 溶液紫色褪去 不能直接加入酸性 KMnO 溶液或溴
4 4
水,因为醛基(—CHO)也易被氧化,使酸性KMnO 溶液或溴水褪色 应先用银
4
氨溶液将醛基氧化成羧基,再滴加溴水或酸性 KMnO 溶液,若溴水或酸性
4
KMnO 溶液褪色,说明柠檬醛分子中含有
4含醛基物质中碳碳双键或三键的检验模型先加银氨溶液或新制 CuOH 加
2
热→再用酸性KMnO 溶液或溴水检验,确定。
4
醛的有关转化应用与定量计算
1.设计以乙醇为原料,其他试剂自选,合成乙二酸的合成路线图示,并注
明试剂与条件。
[提示]
2.1 mol乙醛与足量银氨溶液反应,理论上应生成多少g Ag?
[提示] CH CHO ~ 2Ag↓
3
1 mol 2 mol
故m(Ag)=2 mol×108 g·mol-1=216 g。
1.常见有机物的衍变关系
2.相关定量计算
(1)一元醛发生银镜反应或与新制的Cu(OH) 悬浊液反应时,量的关系如下:
2
(2)甲醛发生氧化反应时,可理解为所以,甲醛分子中相当于有 2 个—CHO,当与足量的银氨溶液或新制的
Cu(OH) 悬浊液作用时,可存在如下量的关系:
2
1 mol HCHO~4 mol [Ag(NH ) ]OH~4 mol Ag
3 2
1 mol HCHO~4 mol Cu(OH) ~2 mol Cu O
2 2
(3)二元醛
1 mol二元醛~4 mol [Ag(NH ) ]OH~4 mol Ag
3 2
1 mol二元醛~4 mol Cu(OH) ~2 mol Cu O
2 2
两种饱和一元脂肪醛的混合物,其平均相对分子质量为51。取4.08 g混合
物与足量银氨溶液共热,生成银21.6 g。试通过计算判断这两种醛是什么醛,
并求它们各自的物质的量。
[解析] 混合醛的物质的量==0.08 mol,生成银的物质的量==0.2
mol>0.08 mol×2,由此可知:混合物中必含有甲醛。设甲醛的物质的量为 x,
另一种醛A的物质的量为y,则有:
⇒
M(A)==58 g·mol-1
根据题意,醛A应符合通式C H O,故12n+2n+16=58,n=3,所以A
n 2n
为丙醛。
综上可知,这两种醛是甲醛和丙醛,物质的量分别是 0.02 mol 和 0.06
mol。
[答案] 这两种醛是甲醛和丙醛,物质的量分别是0.02 mol和0.06 mol。
1 mol有机物与足量银氨溶液反应时,若生成Ag的物质的量大于2 mol,
则说明有机物中含甲醛或多元醛。
1.科学家研制出多种新型杀虫剂代替 DDT,化合物A是其中的一种,其
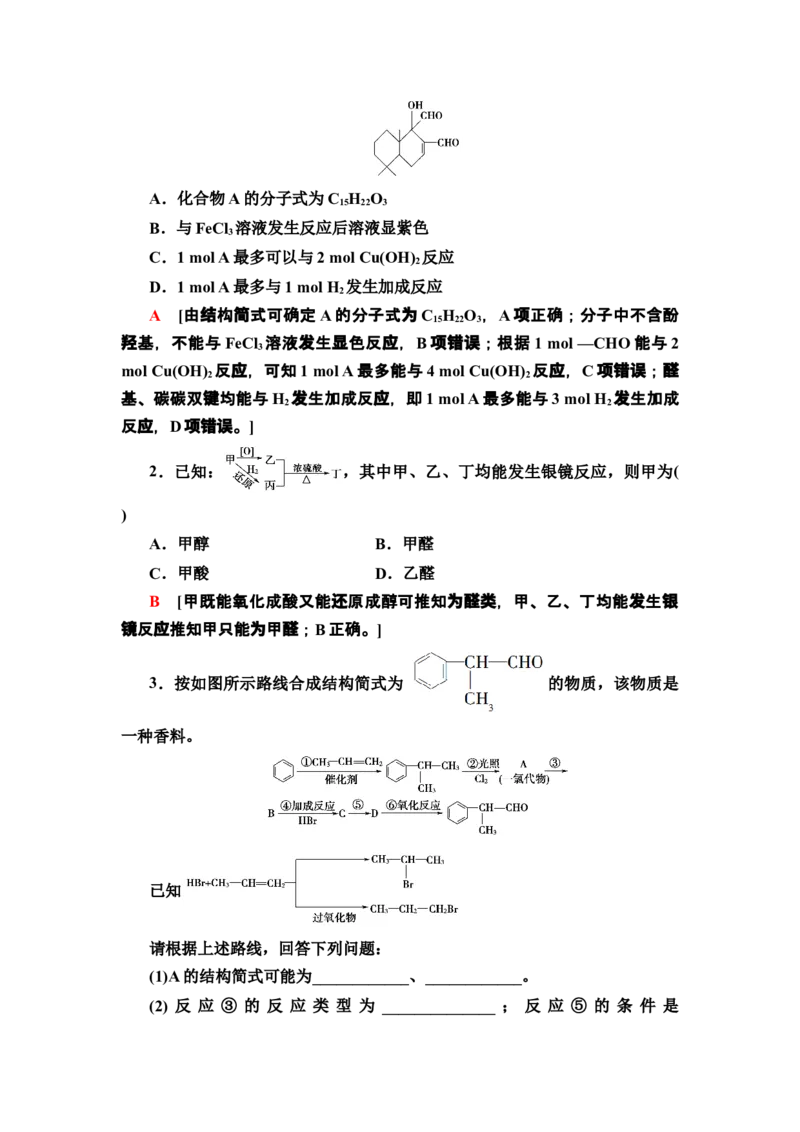
结构如下。下列关于A的说法中正确的是 ( )A.化合物A的分子式为C H O
15 22 3
B.与FeCl 溶液发生反应后溶液显紫色
3
C.1 mol A最多可以与2 mol Cu(OH) 反应
2
D.1 mol A最多与1 mol H 发生加成反应
2
A [由结构简式可确定A的分子式为C H O ,A项正确;分子中不含酚
15 22 3
羟基,不能与FeCl 溶液发生显色反应,B项错误;根据1 mol —CHO能与2
3
mol Cu(OH) 反应,可知1 mol A最多能与4 mol Cu(OH) 反应,C项错误;醛
2 2
基、碳碳双键均能与H 发生加成反应,即1 mol A最多能与3 mol H 发生加成
2 2
反应,D项错误。]
2.已知: ,其中甲、乙、丁均能发生银镜反应,则甲为(
)
A.甲醇 B.甲醛
C.甲酸 D.乙醛
B [甲既能氧化成酸又能还原成醇可推知为醛类,甲、乙、丁均能发生银
镜反应推知甲只能为甲醛;B正确。]
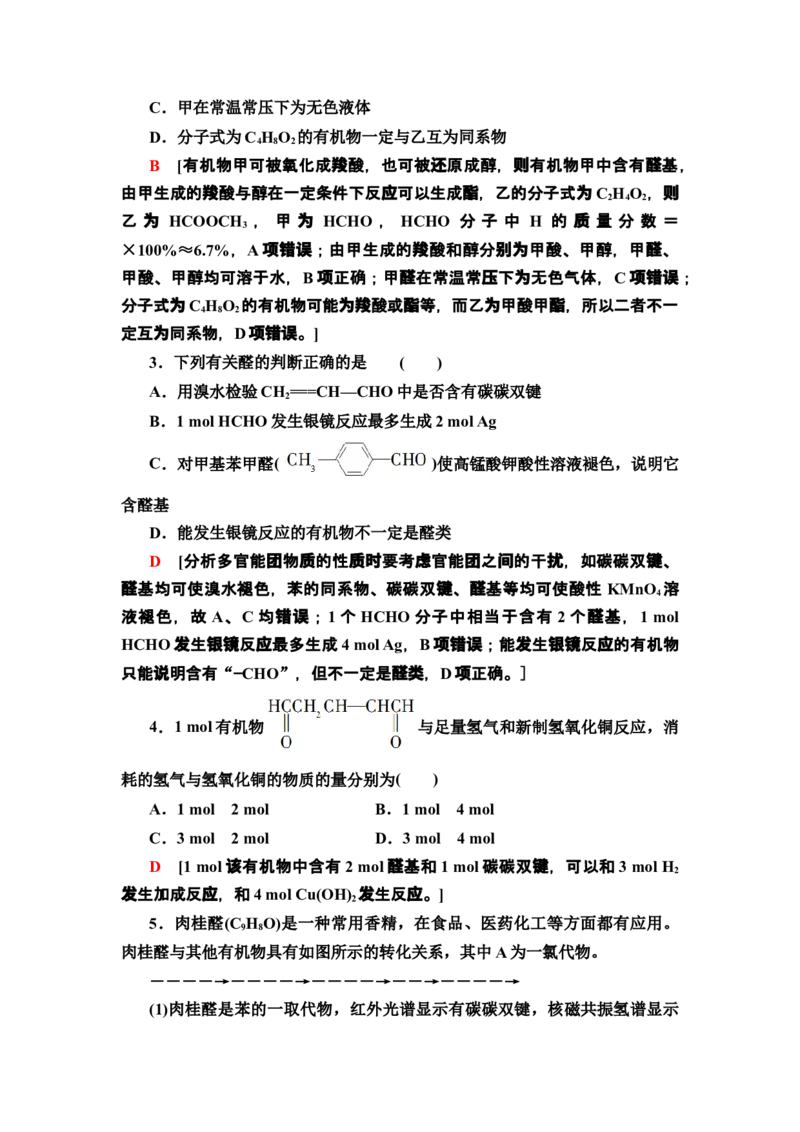
3.按如图所示路线合成结构简式为 的物质,该物质是
一种香料。
已知
请根据上述路线,回答下列问题:
(1)A的结构简式可能为____________、____________。
(2) 反 应 ③ 的 反 应 类 型 为 ______________ ; 反 应 ⑤ 的 条 件 是________________。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):
______________________________________________________。
[解析] 根据“光照、Cl ”反应条件,应是烷烃基上氢原子的氯代产物,
2
其一氯代物有两种;B与HBr加成,可知B为烯烃,C为溴代烃;根据最终产
物 的 结 构 可 以 确 定 , D 为
[答案] (1)
(2)消去反应 氢氧化钠水溶液、加热
(3)
1.下列关于醛的说法正确的是 ( )
A.甲醛是甲基跟醛基相连而构成的醛
B.醛的官能团是—COH
C.饱和一元脂肪醛的分子式符合C H O(n≥1)
n 2n
D.甲醛、乙醛、丙醛均有同分异构体
C [甲醛是H与—CHO相连构成的化合物;醛的官能团是—CHO;甲醛、
乙醛不存在同分异构体,而丙醛和丙酮互为同分异构体。]
2.有机物甲可被氧化成羧酸,也可被还原成醇。由甲生成的羧酸与醇在一
定条件下反应可以生成化合物乙,其分子式为C H O 。下列说法正确的是(
2 4 2
)
A.甲分子中H的质量分数为40%
B.甲和由甲生成的羧酸与醇均可溶于水C.甲在常温常压下为无色液体
D.分子式为C H O 的有机物一定与乙互为同系物
4 8 2
B [有机物甲可被氧化成羧酸,也可被还原成醇,则有机物甲中含有醛基,
由甲生成的羧酸与醇在一定条件下反应可以生成酯,乙的分子式为C H O ,则
2 4 2
乙 为 HCOOCH , 甲 为 HCHO , HCHO 分 子 中 H 的 质 量 分 数 =
3
×100%≈6.7%,A项错误;由甲生成的羧酸和醇分别为甲酸、甲醇,甲醛、
甲酸、甲醇均可溶于水,B项正确;甲醛在常温常压下为无色气体,C项错误;
分子式为C H O 的有机物可能为羧酸或酯等,而乙为甲酸甲酯,所以二者不一
4 8 2
定互为同系物,D项错误。]
3.下列有关醛的判断正确的是 ( )
A.用溴水检验CH ===CH—CHO中是否含有碳碳双键
2
B.1 mol HCHO发生银镜反应最多生成2 mol Ag
C.对甲基苯甲醛( )使高锰酸钾酸性溶液褪色,说明它
含醛基
D.能发生银镜反应的有机物不一定是醛类
D [分析多官能团物质的性质时要考虑官能团之间的干扰,如碳碳双键、
醛基均可使溴水褪色,苯的同系物、碳碳双键、醛基等均可使酸性 KMnO 溶
4
液褪色,故 A、C 均错误;1 个 HCHO 分子中相当于含有 2 个醛基,1 mol
HCHO发生银镜反应最多生成4 mol Ag,B项错误;能发生银镜反应的有机物
只能说明含有“—CHO”,但不一定是醛类,D项正确。]
4.1 mol有机物 与足量氢气和新制氢氧化铜反应,消
耗的氢气与氢氧化铜的物质的量分别为( )
A.1 mol 2 mol B.1 mol 4 mol
C.3 mol 2 mol D.3 mol 4 mol
D [1 mol该有机物中含有2 mol醛基和1 mol碳碳双键,可以和3 mol H
2
发生加成反应,和4 mol Cu(OH) 发生反应。]
2
5.肉桂醛(C H O)是一种常用香精,在食品、医药化工等方面都有应用。
9 8
肉桂醛与其他有机物具有如图所示的转化关系,其中A为一氯代物。
――――→――――→――――→――→――――→
(1)肉桂醛是苯的一取代物,红外光谱显示有碳碳双键,核磁共振氢谱显示有6组峰,则肉桂醛的结构简式是________________。
(2)反应A→B的化学方程式是_____________________________
_____________________________________________________。
(3)Z不能发生的反应类型是________(填字母)。
A.取代反应 B.加聚反应
C.加成反应 D.消去反应
(4)肉桂醛→X的化学方程式是____________________________
_____________________________________________________。
[解析] 由题意可知,肉桂醛中含有一个苯环,苯环上只有一个侧链。根据
肉桂醛分子式为C H O,可推得苯环侧链含有3个碳原子,红外光谱显示有碳
9 8
碳 双 键 , 核 磁 共 振 氢 谱 显 示 有 6 组 峰 , 则 肉 桂 醛 的 结 构 简 式 是
。A为一氯代物,根据反应条件可知,A→B为水解
反应,B→C为醇的催化氧化反应,再根据已经推得的肉桂醛的结构可知,A为
。由题中的相互转化关系,Y为肉桂酸,Z的结构
简式为 ,其中,苯环可发生加成反应,溴原子和羧
基可发生取代反应,溴原子可发生消去反应。