文档内容
第八单元 金属和金属材料
知能优化训练
中考回顾
1.(2017广州中考)下列有关金属材料说法正确的是( )
A.铁片在海水中不易生锈
B.钢是纯铁
C.铝片表面易生成一层致密的氧化膜
D.纯铜硬度高于黄铜(铜锌合金)
答案:C
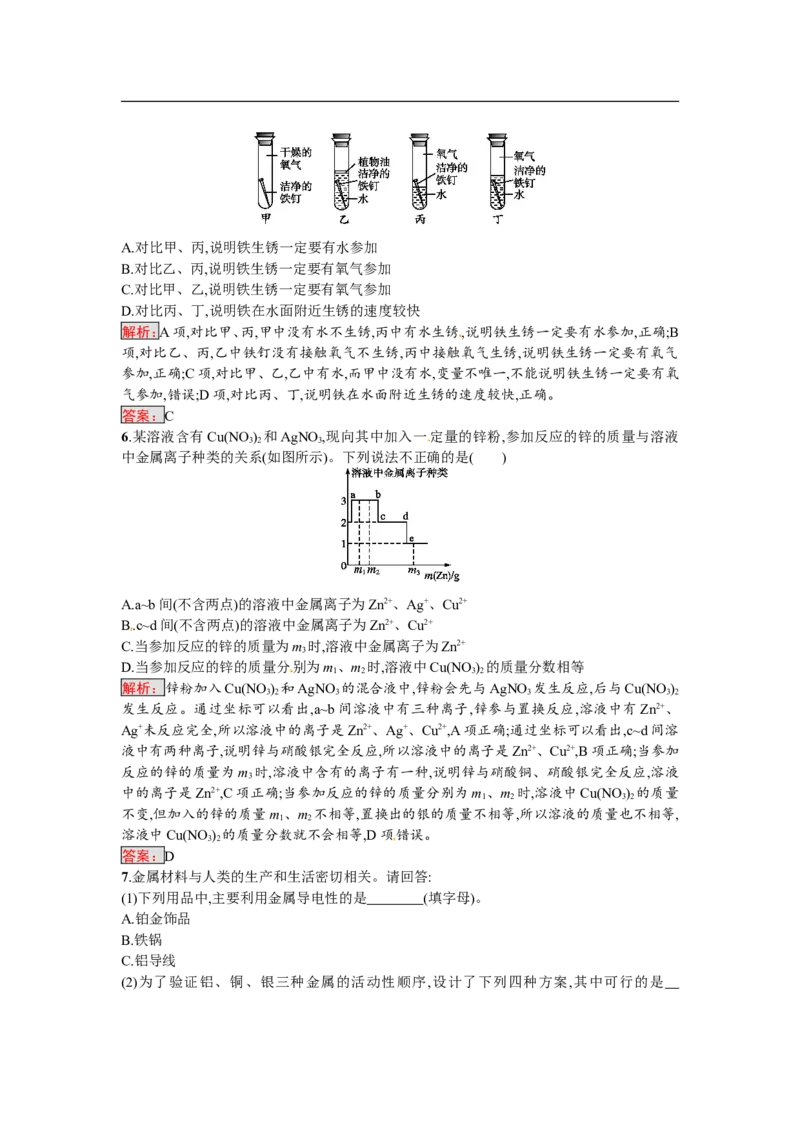
铝丝与硫酸铜
溶液反应
2.(2017成都中考)右图所示反应,有关说法错误的是( )
A.铝丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:Al>Cu
D.反应的化学方程式为Al+CuSO Cu+AlSO
4 4[来源:学,科,网]
答案:D
3.(2017山东青岛中考)下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
答案:B
4.(2017广州中考)化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方
案。下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
[来源:学+科+网Z+X+X+K]
D.实验甲中的CuSO 改为CuCl 不能完成本实验探究
4 2
答案:D
5.(2017湖南邵阳中考)下列根据实验目的所设计的实验方案中,正确的是( )
选
实验目的 实验方案
项
除去稀硫酸中的
A 加入适量铁粉
FeSO
4
除 去 CO 中 的将 气 体 通 入
B 2
CO NaOH溶液
除去 CaCl 溶液加 过 量 CaCO ,
C 2 3
中的HCl 过滤
除去铝粉中的铜加适量稀硫酸,
D
粉 过滤
答案:C
6.(2017天津中考)金属材料广泛应用于生产生活中。
(1)铝块能制成铝箔是利用了铝的 (填“导电”或“延展”)性。
(2)为探究铝、铜的金属活动性顺序,某同学选用了下列药品进行实验,其中可行的是
(填字母)。
A.铝丝、铜丝、氯化镁溶液
B.铝丝、铜丝、硫酸铜溶液
(3)A~G是初中化学常见的物质。已知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单
质,它们的转化关系如图所示,回答问题。
[来源:学*科*网Z*X*X*K]
①写出化学式:A ;B 。
②反应Ⅱ的化学方程式为 。
③反应Ⅲ的化学方程式为 。
(4)用1 600 t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量为
t(结果保留至0.1)。答案:(1)延展
(2)B
(3)①C Fe O ②CO+C 2CO ③Fe+CuSO FeSO +Cu
2 3 2 4 4
(4)933.3
7.(2016天津中考)金属具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是 (填字母)。
A.金属硬币
B.铝制导线
C.铜制火锅
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器
配制波尔多液的原因是 (用化学方程式表示)。
(3)防止金属锈蚀是保护金属资源的有效途径之一。洁净的铁钉在下列情况下容易生锈的是
(填字母)。
A.在干燥的空气中
B.在潮湿的空气中
C.浸没在植物油中
(4)铝具有良好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝
薄膜,从而阻止铝进一步氧化。氧化铝难溶于水,却能溶于酸。写出氧化铝与稀硫酸反应生成
硫酸铝和水的化学方程式:
。
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得滤渣和滤
液。向滤液中加一洁净铁片,未看到铁片有任何变化。则滤液中含有的溶质是
(填化学式),滤渣中一定含有的物质是 (填化学式)。
答案:(1)C
(2)Fe+CuSO FeSO +Cu
4 4
(3)B
(4)AlO+3H SO Al (SO )+3H O
2 3 2 4 2 4 3 2
(5)FeSO Cu
4
模拟预测
1.下列说法不符合事实的是( )
A.金属大多数都是银白色的
B.钢的性能优良,所以钢是很纯的铁
C.多数合金的抗腐蚀性能比组成它们的纯金属更好
D.“真金不怕火炼”说明金的化学性质不活泼
解析:钢是含碳0.03%~2%的铁合金,是混合物,B项错误。
答案:B2.下列有关金属资源的利用和保护不合理的是( )
A.车船表面涂油漆可防止生锈
B.炼铁的主要原料有铁矿石、焦炭、石灰石
C.银是导电性最好的金属,应该全面取代铜、铝做导线
D.废旧金属的回收利用是保护金属资源的有效途径之一
解析:银是导电性最好的金属,但价格昂贵,因此无法全面取代铜、铝做导线,C项错误。
答案:C
3.先取质量相等的甲、乙、丙、丁四种金属粉末,分别投入相同浓度的稀盐酸中,只有甲、乙能
产生气体,乙反应更剧烈;再取一小块丁投入丙的硝酸盐溶液中,丁的表面有丙析出。则甲、乙、
丙、丁四种金属的活动性顺序为( )
A.甲>乙>丙>丁
B.乙>甲>丙>丁
C.丁>丙>乙>甲
D.乙>甲>丁>丙
解析:由题意可知:将这四种金属粉末分别投入相同浓度的盐酸中,只有甲、乙发生反应并产
生气体,而且乙反应更剧烈,说明甲和乙排在氢前,且乙排在甲的前面,丙、丁排在氢后;由将丁
投入丙的硝酸盐溶液中,丁的表面有丙析出,说明丁排在丙的前面,所以,四种金属的活动性顺
序为乙>甲>丁>丙。
答案:D
4.向一定量的铁粉中逐滴加入稀硫酸至过量,如图是反应过程中某种物质的质量Y随加入稀
硫酸的质量变化的关系,则Y不可能表示( )
A.消耗铁粉的质量
B.生成硫酸亚铁的质量
C.溶液的总质量
D.生成氢气的质量
解析:向一定量的铁粉中逐滴加入稀硫酸至过量,铁粉将会被全部消耗尽,即消耗铁粉的质量
逐渐增多,最后不变,故A正确;铁可以与硫酸反应生成硫酸亚铁和氢气,铁粉消耗尽时,硫酸亚
铁的质量不再改变,故B正确;随着硫酸的加入,溶液质量不断增加,当铁粉消耗尽时,随着硫酸
的不断滴加,溶液的质量继续增加,故C错误;随着铁的消耗,氢气的质量不断增加,当铁粉消耗
尽时,氢气的质量不再改变,故D正确。
答案:C
5.根据以下铁钉生锈实验的设计,得出的结论不正确的是( )A.对比甲、丙,说明铁生锈一定要有水参加
B.对比乙、丙,说明铁生锈一定要有氧气参加
C.对比甲、乙,说明铁生锈一定要有氧气参加
D.对比丙、丁,说明铁在水面附近生锈的速度较快
解析:A项,对比甲、丙,甲中没有水不生锈,丙中有水生锈,说明铁生锈一定要有水参加,正确;B
项,对比乙、丙,乙中铁钉没有接触氧气不生锈,丙中接触氧气生锈,说明铁生锈一定要有氧气
参加,正确;C项,对比甲、乙,乙中有水,而甲中没有水,变量不唯一,不能说明铁生锈一定要有氧
气参加,错误;D项,对比丙、丁,说明铁在水面附近生锈的速度较快,正确。
答案:C
6.某溶液含有Cu(NO ) 和AgNO,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液
3 2 3
中金属离子种类的关系(如图所示)。下列说法不正确的是( )
A.a~b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+
B.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
C.当参加反应的锌的质量为m 时,溶液中金属离子为Zn2+
3
D.当参加反应的锌的质量分别为m、m 时,溶液中Cu(NO ) 的质量分数相等
1 2 3 2
解析:锌粉加入Cu(NO ) 和AgNO 的混合液中,锌粉会先与AgNO 发生反应,后与Cu(NO )
3 2 3 3 3 2
发生反应。通过坐标可以看出,a~b间溶液中有三种离子,锌参与置换反应,溶液中有Zn2+、
Ag+未反应完全,所以溶液中的离子是Zn2+、Ag+、Cu2+,A项正确;通过坐标可以看出,c~d间溶
液中有两种离子,说明锌与硝酸银完全反应,所以溶液中的离子是Zn2+、Cu2+,B项正确;当参加
反应的锌的质量为m 时,溶液中含有的离子有一种,说明锌与硝酸铜、硝酸银完全反应,溶液
3
中的离子是Zn2+,C项正确;当参加反应的锌的质量分别为m 、m 时,溶液中Cu(NO ) 的质量
1 2 3 2
不变,但加入的锌的质量m 、m 不相等,置换出的银的质量不相等,所以溶液的质量也不相等,
1 2
溶液中Cu(NO ) 的质量分数就不会相等,D项错误。
3 2
答案:D
7.金属材料与人类的生产和生活密切相关。请回答:
(1)下列用品中,主要利用金属导电性的是 (填字母)。
A.铂金饰品
B.铁锅
C.铝导线
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是(填序号)。
①将铝、银分别浸入到硫酸铜溶液中
[来源:学科网ZXXK]
②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中
④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液。
①滤液中一定含有的溶质是 (填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤
渣中一定含有的物质是 (填化学式)。
(4)某钢铁厂每天需消耗4 900 t含Fe O 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁
2 3
的质量是 t。
解析:(1)在常见的金属材料用品中,铝导线主要利用金属导电性;(2)①铝与硫酸铜反应,可验
证铝的活动性比铜的强。银与硫酸铜不反应,可知银的活动性比铜的弱,可验证铝、铜、银三种
金属的活动性顺序,故①是可行的方案;②银与硫酸铝、硫酸铜都不发生反应,可验证铝、铜的
活动性比银的强。但不能验证铝、铜的活动性,不可验证铝、铜、银三种金属的活动性顺序,故
②是不可行的方案;③铜、银与硫酸铝都不反应,可验证铝的活动性比铜、银的强。但不能验证
铜、银的活动性,不可验证铝、铜、银三种金属的活动性顺序,故③是不可行的方案;④铜与硫酸
铝不反应,可知铜的活动性比铝的弱;铜与硝酸银反应,可验证铜的活动性比银的强,可验证铝、
铜、银三种金属的活动性顺序,故④是可行的方案;(3)在氯化铜和氯化亚铁的混合溶液中加入
一定量的镁粉,充分反应后过滤,得到滤渣和滤液,①由于镁的活动性强于铜和铁的,镁能与氯
化铜和氯化亚铁反应,则滤液中一定含有的溶质是MgCl ,不能确定氯化铜和氯化亚铁的存在;
2
②若向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是Fe,还有置换出的Cu,Mg
不能确定是否存在;(4)设日产含Fe 98%的生铁的质量为x,
Fe O+3CO 2Fe+3CO
2 3 2
160 112
4 900 t×76% x×98%
解得x=2 660 t
[来源:学科网ZXXK]
答案:(1)C
(2)①④
(3)①MgCl ②Cu、Fe
2
(4)2 660
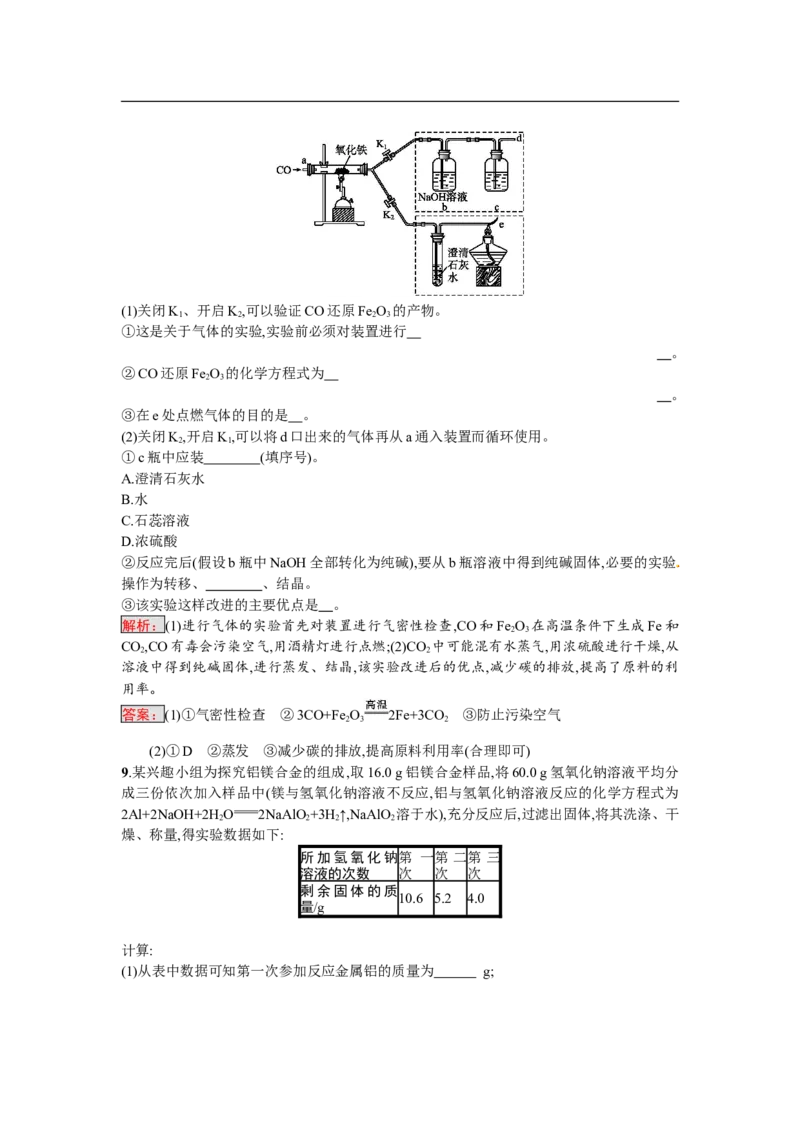
8.某校化学兴趣小组的同学,对课本中一氧化碳还原氧化铁实验作了绿色化改进后制取单质
铁(K 、K 是活塞):
1 2(1)关闭K、开启K,可以验证CO还原Fe O 的产物。
1 2 2 3
①这是关于气体的实验,实验前必须对装置进行
。
②CO还原Fe O 的化学方程式为
2 3
。
③在e处点燃气体的目的是 。
(2)关闭K,开启K,可以将d口出来的气体再从a通入装置而循环使用。
2 1
①c瓶中应装 (填序号)。
A.澄清石灰水
B.水
C.石蕊溶液
D.浓硫酸
②反应完后(假设b瓶中NaOH全部转化为纯碱),要从b瓶溶液中得到纯碱固体,必要的实验
操作为转移、 、结晶。
③该实验这样改进的主要优点是 。
解析:(1)进行气体的实验首先对装置进行气密性检查,CO和Fe O 在高温条件下生成Fe和
2 3
CO,CO有毒会污染空气,用酒精灯进行点燃;(2)CO 中可能混有水蒸气,用浓硫酸进行干燥,从
2 2
溶液中得到纯碱固体,进行蒸发、结晶,该实验改进后的优点,减少碳的排放,提高了原料的利
用率。
答案:(1)①气密性检查 ②3CO+Fe O 2Fe+3CO ③防止污染空气
2 3 2
(2)①D ②蒸发 ③减少碳的排放,提高原料利用率(合理即可)
9.某兴趣小组为探究铝镁合金的组成,取16.0 g铝镁合金样品,将60.0 g氢氧化钠溶液平均分
成三份依次加入样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应的化学方程式为
2Al+2NaOH+2H O 2NaAlO +3H ↑,NaAlO 溶于水),充分反应后,过滤出固体,将其洗涤、干
2 2 2 2
燥、称量,得实验数据如下:
所加氢氧化钠第 一第 二第 三
溶液的次数 次 次 次
剩余固体的质
10.6 5.2 4.0
量/g
计算:
(1)从表中数据可知第一次参加反应金属铝的质量为 g;(2)该合金中金属镁的质量分数;
(3)所用氢氧化钠溶液溶质的质量分数。
解析:(1)根据“镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应”,结合第一次加入氢氧化
钠溶液所得的数据可知,参加反应金属铝的质量为16.0 g-10.6 g=5.4 g;(2)根据第一次或第二
次所加入氢氧化钠溶液的实验数据,通过反应消耗铝的质量,根据反应的化学方程式,计算所
加氢氧化钠溶液中的氢氧化钠的质量,而得出所用氢氧化钠溶液中溶质的质量分数。
答案:(1)5.4
(2)该合金中金属镁的质量分数为 ×100%=25.0%
(3)第一次所加20.0 g氢氧化钠溶液能反应的铝的质量为:16.0 g-10.6 g=5.4 g,
设20.0 g氢氧化钠溶液中溶质的质量为x。
2Al+2NaOH+2H O 2NaAlO +3H ↑
2 2 2
54 80
5.4 g x
解得x=8.0 g
所用氢氧化钠溶液中溶质的质量分数= ×100%=40.0%