文档内容
第8讲 盐 化学肥料
1.初步认识常见的复分解反应,能用于解释日常生活中的一些化学现
象。
考试说明 2.了解食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途。
3.知道一些常用化肥的名称和作用。
4.完成基础的学生实验:粗盐中难溶性杂质的去除。
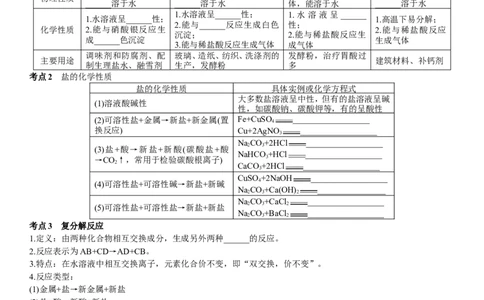
考点1 常见的盐
化学名称 氯化钠 碳酸钠 碳酸氢钠 碳酸钙
俗名 食盐 纯碱或苏打 小苏打
化学式 NaCl NaCO NaHCO CaCO
2 3 3 3
______ 色 晶 体 , ______ 色 粉 末 状 固 体 , ______色粉末状固 ______ 色 固 体 ,
物理性质
______溶于水 ______溶于水 体,能溶于水 ______溶于水
1.水溶液呈______性; 1.水溶液呈 ______
1.水溶液呈______性; 1.高温下易分解;
2.能与______反应生成白色 性;
化学性质 2.能与硝酸银反应生 2.能与稀盐酸反应
沉淀; 2.能与稀盐酸反应生
成______色沉淀 生成气体
3.能与稀盐酸反应生成气体 成气体
调味剂和防腐剂、配 玻璃、造纸、纺织、洗涤剂的 发酵粉,治疗胃酸过
主要用途 建筑材料、补钙剂
制生理盐水、融雪剂 生产,发酵粉 多
考点2 盐的化学性质
盐的化学性质 具体实例或化学方程式
大多数盐溶液呈中性,但有的盐溶液呈碱
(1)溶液酸碱性
性,如碳酸钠、碳酸钾等,有的呈酸性
(2)可溶性盐+金属→新盐+新金属(置 Fe+CuSO __________________
4
换反应) Cu+2AgNO __________________
3
NaCO+2HCl __________________
(3)盐+酸→新盐+新酸(碳酸盐+酸 2 3
NaHCO +HCl __________________
→CO↑,常用于检验碳酸根离子) 3
2
CaCO +2HCl __________________
3
CuSO +2NaOH __________________
(4)可溶性盐+可溶性碱→新盐+新碱 4
NaCO+Ca(OH) ________________
2 3 2
NaCO+CaCl __________________
(5)可溶性盐+可溶性盐→新盐+新盐 2 3 2
NaCO+BaCl __________________
2 3 2
考点3 复分解反应
1.定义:由两种化合物相互交换成分,生成另外两种______的反应。
2.反应表示为AB+CD→AD+CB。
3.特点:在水溶液中相互交换离子,元素化合价不变,即“双交换,价不变”。
4.反应类型:
(1)金属+盐→新金属+新盐
(2)盐+酸→新酸+新盐
(3)盐+碱→新碱+新盐
(4)盐+盐→新盐+新盐
(5)酸+金属氧化物→盐+水
5.反应条件:只有当两种化合物交换成分后有______或有______或有______生成时,复分解反应才可以发生。
考点4 化学肥料
1.化肥的种类
化肥种类 性质 作用 举例
多呈白色固体,但也有液体, 尿素、氨水、碳酸氢
促进植树的______及______的
氮肥 并都有一定的气味,都含有氮 铵、硝酸钠、硝酸铵、
进行十分重要
元素 氯化铵等多是白色的固体,都含有磷元 促进______,同时______、 磷矿粉、钙镁磷肥、
磷肥
素 ______ 过磷酸钙
促进______,增强______及
钾肥 多是白色固体,并含有钾元素 硫酸钾、氯化钾
______的作用
能同时供给作物几种养分,发
复合
含有______以上营养元素 挥营养元素间的作用,有效成 硝酸钾
肥
分高,且能根据实际需要配制
【温馨提示】铵态氮肥遇到碱性物质会放出氨气,使肥效降低。因此化肥要合理使用;另外,要根据土壤的情况和农作
物的种类,要注意化学肥料和农家肥料的合理配用。
2.化肥的简易鉴别
氮肥 钾肥 磷肥
看外观 色晶体 灰白色粉末
加水溶解 溶于水 溶于水
加熟石灰 放出具有刺激 无具有刺激性气
研磨 性气味的氨气 味的氨气放出
命题点1 常见的盐
草木灰是农家肥料,主要含钾盐。请回答相关问题。
【分离提纯】
(1)在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌。浸出溶液中主要含有的金属阳离子是________。
(2) 把 烧 杯 中 的 草 木 灰 连 同 浸 出 液 一 起 过 滤 。 如 果 滤 液 仍 然 浑 浊 , 处 理 的 方 法 是
________________________________。
(3)把滤液倒入蒸发皿里,加热,用玻璃棒搅拌。当蒸发到____________时,停止加热。
【成分探究】
取(3)所得的晶体少量溶于水,分到两支试管中。
(4)第一支:滴加盐酸,产生能使澄清的石灰水变浑浊的气体。请写出化学方程式:
①加盐酸:________________________________________________________________________;
②产生浑浊:________________________________________________________________________。
(5)第二支:滴加酚酞溶液后,溶液变为________色,说明溶液呈碱性。为证明溶液呈碱性是由CO引起的,再向
试管中加入________[可供选择试剂:澄清石灰水、KCl溶液(呈中性)、CaCl 溶液(呈中性)],此时发生反应的方程式为
2
________________________________,当看到________________________________时即可证明。因此,草木灰
________(填“能”或“不能”)与铵态氮肥混合施用。
思路点拨:(1)草木灰主要成分为KCO,溶液中阳离子为K+;(2)过滤一次后滤液浑浊,要重新过滤;(3)蒸发滤液
2 3
时要用玻璃棒不断搅拌,当出现较多量固体或剩余少量液体时停止加热;(4)向碳酸钾中加入稀盐酸时,会反应产生
二氧化碳气体,二氧化碳能使澄清石灰水变浑浊,其反应的化学方程式为KCO +2HCl===2KCl+CO↑+HO;
2 3 2 2
Ca(OH) +CO===CaCO ↓+HO;(5)碳酸钾溶液显碱性,滴加酚酞溶液后,溶液变红,为证明溶液的碱性是由CO引
2 2 3 2
起的,可以加入中性CaCl 溶液来除去,可以观察到溶液的红色消失,产生沉淀;由于碳酸钾显碱性,会与铵态氮肥反
2
应放出氨气,降低肥效,所以不能与铵态氮肥混合施用。
1.酸、碱、盐在工农业生产和日常生活中应用广泛。下列做法错误的是( )
A.用石灰乳与硫酸铜溶液配制农药波尔多液
B.用稀盐酸除去铁制品表面的铁锈
C.用食盐水除去水壶中的水垢
D.施用复合肥硝酸钾能使作物枝叶繁茂,并增加抗倒伏能力
2.NaCO 的水溶液呈碱性,下列说法错误的是( )
2 3
A.碳酸钠在水中会电离出OH-
B.往碳酸钠溶液中加稀硫酸后溶液的pH降低C.碳酸钠溶液中存在OH-
D.往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色
命题点2 盐的化学性质
烧杯中装有一定量的NaCO 溶液,向其中加入一定量的CaCl 溶液,充分反应后过滤,得到滤渣和滤液,
2 3 2
现对滤液中溶质的成分进行探究:
【提出猜想】
猜想1:滤液中的溶质为NaCl;
猜想2:滤液中的溶质为NaCl、CaCl ;
2
猜想3:滤液中的溶质为________________;
猜想4:滤液中的溶质为NaCl、CaCl 、NaCO。
2 2 3
(1)完成猜想3。
(2)同学们一致认为,猜想4有明显的错误,其原因是____________________________________________。
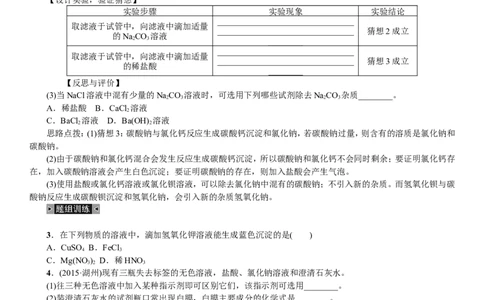
【设计实验,验证猜想】
实验步骤 实验现象 实验结论
________________________________
取滤液于试管中,向滤液中滴加适量
________________________________ 猜想2成立
的NaCO 溶液
2 3 ________
________________________________
取滤液于试管中,向滤液中滴加适量
________________________________ 猜想3成立
的稀盐酸
________
【反思与评价】
(3)当NaCl溶液中混有少量的NaCO 溶液时,可选用下列哪些试剂除去NaCO 杂质________。
2 3 2 3
A.稀盐酸 B.CaCl 溶液
2
C.BaCl 溶液 D.Ba(OH) 溶液
2 2
思路点拨:(1)猜想3:碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,若碳酸钠过量,则含有的溶质是氯化钠和
碳酸钠。
(2)由于碳酸钠和氯化钙混合会发生反应生成碳酸钙沉淀,所以碳酸钠和氯化钙不会同时剩余;要证明氯化钙存
在,加入碳酸钠溶液会产生白色沉淀;要证明碳酸钠的存在,则加入盐酸会产生气泡。
(3)使用盐酸或氯化钙溶液或氯化钡溶液,可以除去氯化钠中混有的碳酸钠;不引入新的杂质。而氢氧化钡与碳
酸钠反应生成碳酸钡沉淀和氢氧化钠,会引入新的杂质氢氧化钠。
3.在下列物质的溶液中,滴加氢氧化钾溶液能生成蓝色沉淀的是( )
A.CuSO B.FeCl
4 3
C.Mg(NO) D.稀HNO
3 2 3
4.(2015·湖州)现有三瓶失去标签的无色溶液,盐酸、氯化钠溶液和澄清石灰水。
(1)往三种无色溶液中加入某种指示剂即可区别它们,该指示剂可选用________。
(2)装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是________。
(3)上述溶液中,属于盐溶液的是__________。
命题点3 复分解反应及条件
下列离子在水溶液中无色且能大量共存的一组是( )
A.Ca2+、K+、Cl-、NO
B.Na+、Cu2+、NO、SO
C.Fe3+、Na+、OH-、NO
D.K+、H+、SO、CO
思路点拨:根据已知需要满足两个条件:①四种离子在水溶液中都无色,②四种离子间不会结合成沉淀或水或气
体。A中四种离子可以共存,形成的是无色溶液,正确;B中Cu2+在水溶液中显蓝色,不正确;C中铁离子能与氢氧根
离子结合生成沉淀,所以C不正确;D中氢离子能与碳酸根离子结合生成水和二氧化碳,所以D不正确。5.下列反应不能一步实现的是( )
A.Zn→ZnSO B.Fe O→FeCl
4 2 3 3
C.BaCl →Ba(OH) D.CH→HO
2 2 4 2
命题点4 化学肥料
下列有关化肥和农药的说法错误的是( )
A.氯化钾可用作钾肥
B.化肥能有效提高农作物产量
C.农药施用后,不会通过农作物转移到人体
D.农药应根据农作物、虫害和农药的特点合理施用
思路点拨:氯化钾(KCl)中含有钾元素,属于钾肥,A正确;化肥和农药是农业稳产、增产的重要因素,但是任意施
用化肥和农药会造成土壤、水体污染,同时,农药在农作物体内残留,会通过人类食物链转移到人体内部,对人体健
康产生危害,所以B、D正确,C错误。
6.过多的植物营养物质如尿素CO(NH) 等进入水体会导致“水华”现象。下列说法不正确的是( )
2 2
A.尿素由四种元素组成
B.尿素属于氮肥
C.尿素属于复合肥
D.使用无磷洗衣粉可以减少“水华”现象的发生
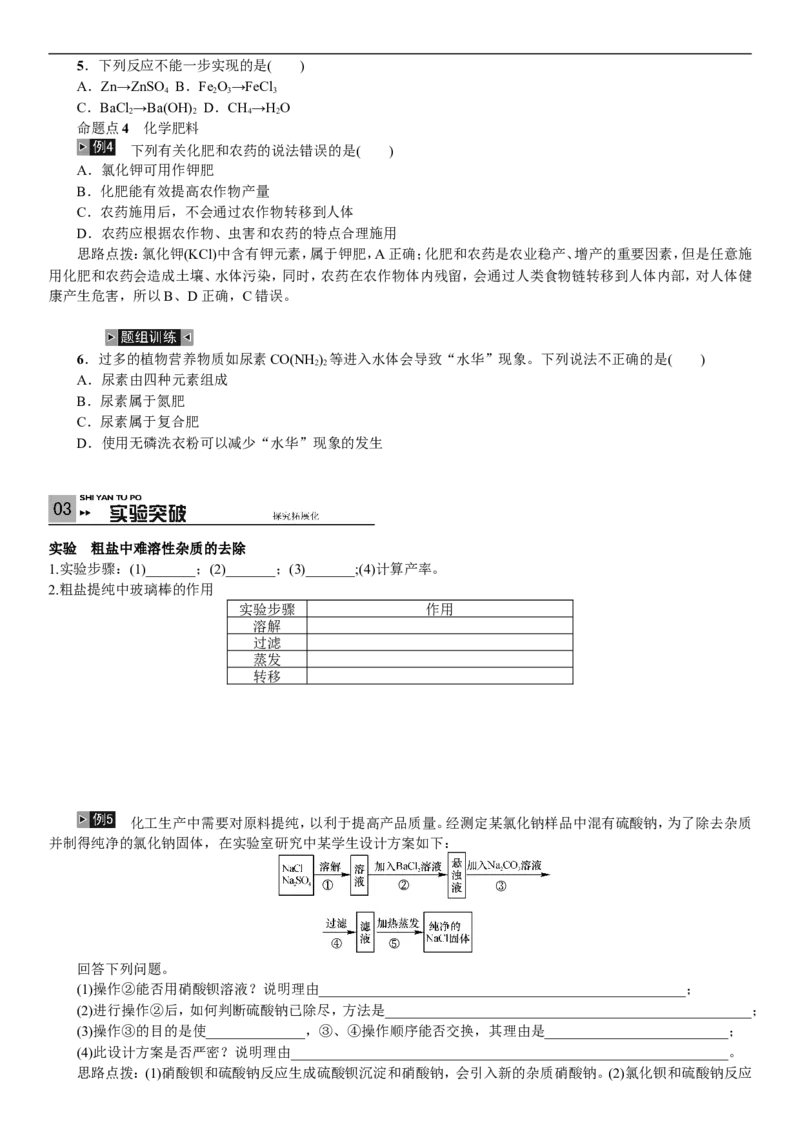
实验 粗盐中难溶性杂质的去除
1.实验步骤:(1)_______;(2)_______;(3)_______;(4)计算产率。
2.粗盐提纯中玻璃棒的作用
实验步骤 作用
溶解
过滤
蒸发
转移
化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除去杂质
并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:
回答下列问题。
(1)操作②能否用硝酸钡溶液?说明理由____________________________________________________;
(2)进行操作②后,如何判断硫酸钠已除尽,方法是____________________________________________________;
(3)操作③的目的是使______________,③、④操作顺序能否交换,其理由是__________________________;
(4)此设计方案是否严密?说明理由______________________________________________________________。
思路点拨:(1)硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,会引入新的杂质硝酸钠。(2)氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,向上层清液中滴加氯化钡溶液,看是否有沉淀生成,可判断硫酸钠是否除尽。(3)碳酸钠和
氯化钡反应生成碳酸钡沉淀和氯化钠,操作③的目的是使钡离子完全沉淀,③、④操作顺序不能交换,否则得不到滤
液。(4)此设计方案不严密,因为最后过量的碳酸钠没有除去。
除杂质问题在解答时要遵循“不增、不减、易于分离”的原则,即不增加新的杂质,不减少原有物质,同时原物
质便于分离出来。本题中为了除尽可溶性杂质,加入的试剂都是过量的,因此必须考虑过量试剂在后面操作中能否除
去,这就需要正确选择加入试剂的顺序,才能成功达到实验目的。
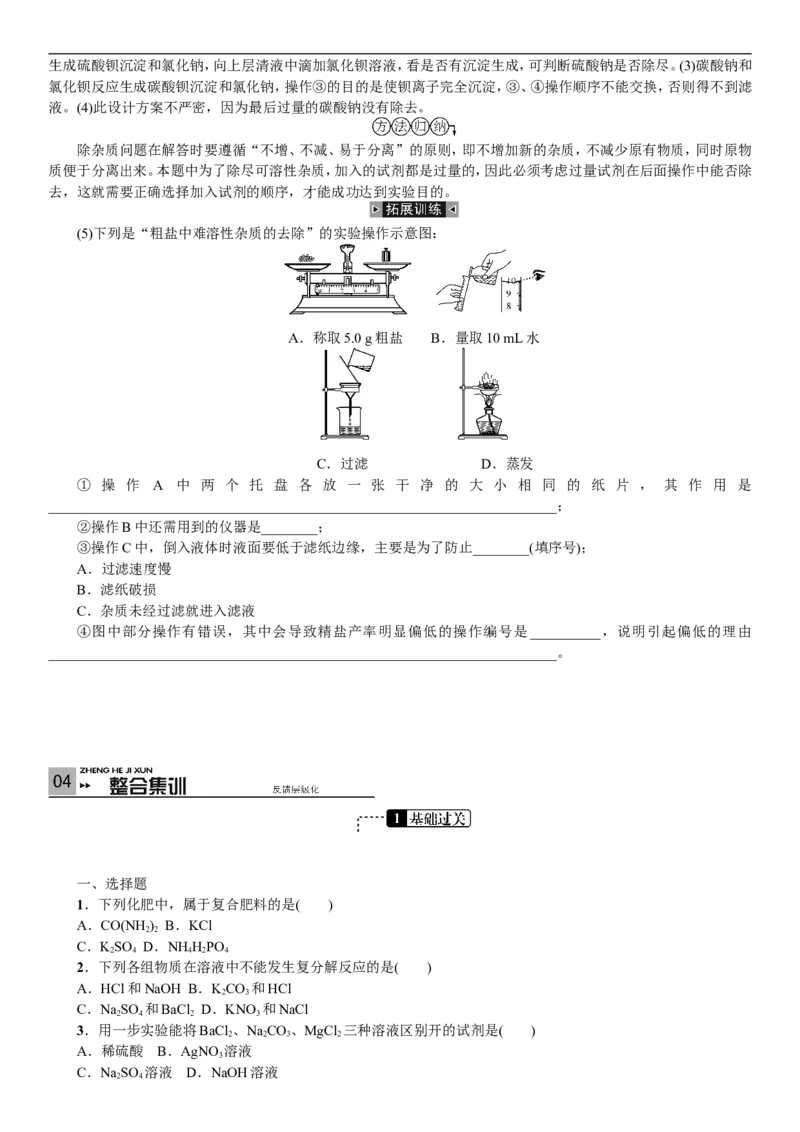
(5)下列是“粗盐中难溶性杂质的去除”的实验操作示意图:
A.称取5.0 g粗盐 B.量取10 mL水
C.过滤 D.蒸发
① 操 作 A 中 两 个 托 盘 各 放 一 张 干 净 的 大 小 相 同 的 纸 片 , 其 作 用 是
________________________________________________________________________;
②操作B中还需用到的仪器是________;
③操作C中,倒入液体时液面要低于滤纸边缘,主要是为了防止________(填序号);
A.过滤速度慢
B.滤纸破损
C.杂质未经过滤就进入滤液
④图中部分操作有错误,其中会导致精盐产率明显偏低的操作编号是__________,说明引起偏低的理由
________________________________________________________________________。
一、选择题
1.下列化肥中,属于复合肥料的是( )
A.CO(NH) B.KCl
2 2
C.KSO D.NH HPO
2 4 4 2 4
2.下列各组物质在溶液中不能发生复分解反应的是( )
A.HCl和NaOH B.KCO 和HCl
2 3
C.NaSO 和BaCl D.KNO 和NaCl
2 4 2 3
3.用一步实验能将BaCl 、NaCO、MgCl 三种溶液区别开的试剂是( )
2 2 3 2
A.稀硫酸 B.AgNO 溶液
3
C.NaSO 溶液 D.NaOH溶液
2 44.粗盐初步提纯的操作步骤如图所示,相关说法错误的是( )
A.溶解时玻璃棒用于搅拌
B.过滤时玻璃棒用于引流
C.蒸发至滤液被蒸干后再移去酒精灯
D.图中“操作1”是称量
5.草木灰是常见的农家肥料,有效成分是KCO,其水溶液呈碱性,下列化肥不能与草木灰混合施用的是( )
2 3
A.尿素 B.磷矿粉
C.硝酸铵 D.硝酸钾
6.生活中有许多盐,小苏打是其中一种,下列小苏打的化学式正确的是( )
A.NaCO B.NaHCO
2 3 3
C.NaCl D.NaOH
7 . 氨 碱 法 生 产 纯 碱 的 主 要 反 应 原 理 如 下 : (1)NaCl + NH + CO + HO===NaHCO + NH Cl
3 2 2 3 4
(2)2NaHCO =====NaCO+HO+CO↑
3 2 3 2 2
对上述信息的有关理解不正确的是( )
A.用食盐制纯碱需要含碳、氧元素的物质
B.(1)中析出晶体后剩余溶液中只有一种溶质
C.氨盐水比食盐水更易吸收二氧化碳
D.碳酸氢钠比碳酸钠受热更易分解
8.按下表进行实验,有关说法及分析错误的是( )
向少量BaCl 溶液中滴加
向少量NaOH溶液中滴加CuSO 溶液 2
4 CuSO 溶液
4
现象 ① 白色沉淀
化学方程式 CuSO +2NaOH===Cu(OH) ↓+NaSO ②
4 2 2 4
A.①有蓝色沉淀
B.②反应的化学方程式为:CuSO +BaCl ===BaSO ↓+CuCl
4 2 4 2
C.两个反应都属于复分解反应
D.只要有沉淀生成的反应就属于复分解反应
9.向一定质量CaCl 和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的NaCO 溶液。反应过程中加入的
2 2 3
NaCO 溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法不正确的是( )
2 3
A.C点溶液中溶质有2种
B.图中OA段表示生成沉淀的过程
C.整个反应过程中,氯离子个数不变
D.x值为106.0
10.下列图像能正确反映其对应操作中各量变化关系的是( )
A.用一定质量的高锰酸钾加热制氧气
B.向一定质量的石灰石中加入过量的稀盐酸
C.向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体D.分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
二、填空及简答题
11.(1)土豆等农作物的生长需要化肥。下列化肥中属于氮肥的是________。
A.NH Cl B.KCO
4 2 3
C.CO(NH) D.Ca (PO )
2 2 3 4 2
(2)(2013·遵义)KNO 可用作化肥,属于________肥(填“氮”“磷”“钾”或“复合”)。
3
12.同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中
“→”表示物质间的转化)。已知A、H为固体,通常均可在食品包装袋中用于保存食品。人体胃酸中有大量M存在。
A、B、C含有两种相同的元素。请回答下列问题:
(1)A的化学式为________;F的固体俗称________;
(2)G与M溶液反应的化学方程式为:________________________________;
(3)在B溶液中加入一定量D溶液,过滤后取滤液,滴入过量M溶液,无明显现象,则滤液中的溶质可能存在的
是________________________________________________________________________;
(4)已知金属铝可与 E 溶液反应生成偏铝酸钠(NaAlO )和一种最轻的气体,写出该反应的化学方程式
2
______________________________________。
三、实验探究题
13.某同学在学习溶液的酸碱性时发现盐溶液NaCl呈中性,NaCO 溶液呈碱性,该同学认为有可能有的盐溶液
2 3
会呈酸性,上网查资料发现(NH )SO ,FeCl 溶液呈酸性。该同学来兴趣了,写出如下的学习小结,请你做一做:
4 2 4 3
(1)盐溶液的pH可能为(将你的假设填入空格中):①________,②________,③pH=7。
(2)要测定该溶液的酸碱性用__________,如要知道该溶液的酸碱度可用________,操作方法
________________________________________________________________________。
(3)“庄稼一枝花,全靠肥当家。”(NH )SO 是一种氮肥,能促进农作物的茎、叶生长茂盛,能使紫色石蕊试液变
4 2 4
________色。
(4)铵态氮肥的检测方法是:_________________________________________________。
(5) 该 同 学 加 热 FeCl 溶 液 发 现 有 红 褐 色 沉 淀 生 成 , 请 写 出 化 学 方 程 式 :
3
__________________________________[提示:Cu(OH) 等难溶性碱在pH>5的盐酸中不溶解]。
2
一、选择题
1.小明家的芹菜茎秆细弱,施钾肥可免其倒伏。他应施加的化肥是( )
A.KOH B.Ca (PO )
3 3 2
C.KClO D.CO(NH)
3 2 2
2.能在同一溶液中大量共存,且溶液为无色透明的一组物质是( )
A.KSO ,NaNO ,NH Cl
2 4 3 4
B.BaCl ,NaSO ,NaOH
2 2 4
C.CaCl ,NaCO,AgNO
2 2 3 3
D.FeCl ,CuSO ,NaCl
3 4
3.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.向某固体物质中加入稀盐酸,生成无色无味气体,证明该物质一定是碳酸盐
B.向碳酸钠溶液中滴加无色酚酞试剂,溶液变成红色,说明碳酸钠属碱类
C.某有机物在空气中燃烧生成二氧化碳和水,证明该有机物一定含有碳、氢、氧三种元素
D.某化肥与碱混合研磨,产生刺激性气味的气体,证明该化肥是铵态化肥
二、填空及简答题4.工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如图所示,请回答:
(1)石灰石、生石灰、熟石灰均能与下列________(填字母)发生化学反应。
A.水 B.盐酸 C.二氧化碳
(2)步骤④发生反应的化学方程式是______________________________。
(3)某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了一种酸溶液,乙同学
选择了一种碱溶液,丙同学也选择了一种溶液,该溶液中溶质与甲、乙同学所用溶液中溶质的物质类别不同,他们都
能达到检验目的。你认为丙同学所选溶液中的溶质可能是
________________________________________________________________________
(填一种物质的化学式)。
三、实验探究题
5.“五一”节后,小红返回了学校,当她来到实验室时,意外地发现实验桌上有一瓶敞口放置的NaOH溶液,由
此便激发了她的探究欲望。
【提出问题】这瓶NaOH溶液一定变质了,其变质的程度如何呢?
【猜想与假设】小红的猜想:NaOH溶液部分变质。
你的不同猜想:______________________。
【收集资料】小红知道,NaOH 敞口放置会变质的原因是 NaOH 与空气中的 CO 反应,化学方程式为
2
____________________________。
【实验探究】小红设计如下实验验证自己的猜想,请根据表中内容填写小红实验时的现象。
实验步骤 现象 结论
第一步:取少量NaOH溶液于试管中,
①____________ NaOH溶液
滴加足量的CaCl 溶液
2 部分变质
第二步:向上述试管中再滴加酚酞溶液 ②____________
假设你的猜想正确,并按小红的实验方案进行实验,则你观察到的现象是③____________;④________________。
【实验反思】保存NaOH溶液的方法是________。
四、计算题
6.著名化学家侯德榜发明了联合制碱法,为我国化学工业的发展做出杰出贡献。某实验小组取仅含有氯化钠杂
质的纯碱样品14.4 g,加入到盛有100 g稀盐酸的烧杯中,恰好完全反应。此时烧杯内各物质的总质量为110 g。试计
算:
(1)反应生成二氧化碳________克。
(2)所用稀盐酸的质量分数。参考答案
考点解读
考点1 白 易 白 易 白 白 不 中 白 碱 Ca(OH) Ba(OH) 、CaCl 、BaCl 碱
2 2 2 2
考点 2 FeSO +Cu 2Ag+Cu(NO ) 2NaCl+HO+CO↑ NaCl+HO+CO↑ CaCl +HO+CO↑
4 3 2 2 2 2 2 2 2 2
Cu(OH) ↓+NaSO CaCO ↓+2NaOH CaCO ↓+2NaCl BaCO ↓+2NaCl
2 2 4 3 3 3
考点3 1.化合物 5.气体 沉淀 水
考点4 1.生长发育 光合作用 农作物生长 增强农作物抗寒、抗旱能力 生长 抗病虫害 抗倒伏 两种
或两种 2.白 全部 大多不溶于水或部分
各个击破
例 1 (1)K+ (2)重新过滤(或再过滤一次) 出现大量固体 (4)①KCO +2HCl===2KCl+CO↑+HO
2 3 2 2
②Ca(OH) +CO===CaCO ↓+HO (5)红 CaCl 溶液 KCO +CaCl ===CaCO ↓+2KCl 红色褪去(或消失),
2 2 3 2 2 2 3 2 3
产生白色沉淀 不能 例2 【提出猜想】NaCl、NaCO 【设计实验,验证猜想】有白色沉淀产生 有气泡产生
2 3
【反思与评价】ABC
例3 A 例4 C
题组训练 1.C 2.A 3.A 4.(1)石蕊试液 (2)CaCO (3)氯化钠溶液 5.C 6.C
3
实验突破
实验 1.(1)溶解 过滤 蒸发 2.搅拌,加快粗盐的溶解速率 引流 搅拌液体,防止液体局部温度过高,造成
液滴飞溅 转移固体
例5 (1)不能用硝酸钡溶液,会引入新的硝酸钠杂质而无法除去 (2)向上层清液中滴加氯化钡溶液,看是否有
沉淀生成 (3)钡离子完全沉淀 (4)不能,得不到滤液 不严密,过量的碳酸钠没有除去
拓展训练 防止药品腐蚀托盘;使称量更准确 胶头滴管 C D 未用玻璃棒搅拌,会导致液体外溅,损失部
分氯化钠
整合集训基础过关
1.D 2.D 3.A 4.C 5.C 6.B 7.B 8.D 9.B 10.D 11.(1)AC (2)复合 12.(1)CaO 干冰 (2)Fe O +
2 3
6HCl===2FeCl +3HO (3)NaOH或NaOH和Ca(OH) (4)2Al+2NaOH+2HO=====2NaAlO +3H↑ 13.(1)pH
3 2 2 2 2 2
>7 pH<7 (2)酸碱指示剂 pH试纸 用玻璃棒蘸取待测液涂在pH试纸上,把显示的颜色与标准比色卡对照即
可 (3)红 (4)与熟石灰混合研磨,观察是否有刺激性的气味产生 (5)FeCl +3HO===Fe(OH) ↓+3HCl
3 2 3
能力提升
1.C 2.A 3.D 4.(1)B (2)Ca(OH) +NaCO===CaCO ↓+2NaOH (3)CaCl 或 Ca(NO ) 或 BaCl 或
2 2 3 3 2 3 2 2
Ba(NO ) 5.NaOH溶液全部变质 2NaOH+CO===Na CO +HO 产生白色沉淀 溶液变红色 产生白色沉淀
3 2 2 2 3 2
溶液没有变红色 密封保存
6.(1)4.4 设所用稀盐酸中溶质的质量为x。
NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2
73 44
x 4.4 g
= x=7.3 g
所用稀盐酸的质量分数是×100%=7.3%
答:所用稀盐酸的质量分数是7.3%。