文档内容
第二节 分子晶体与共价晶体
第1课时 分子晶体
基础过关练
题组一 分子晶体及其结构
1.下列有关分子晶体的说法中正确的是( )
A.分子内均存在共价键
B.分子间一定存在范德华力
C.分子间一定存在氢键
D.其结构一定为分子密堆积
2.下列各组物质各自形成晶体,均属于分子晶体的化合物是( )
A.NH 、HD、C H B.PCl 、CO 、H SO
3 10 8 3 2 2 4
C.SO 、SiO 、P O D.CCl 、Na S、H O
2 2 2 5 4 2 2 2
3.下列各物质所形成的晶体中,属于分子晶体且分子内只含极性共价键的是( )
A.CO B.O C.NH Cl D.Ar
2 2 4
4.(2020河南郑州外国语学校高二月考)在海洋深处的沉积物中含有大量可燃冰,其主要成分是甲烷水
合物。甲烷水合物的结构可以看成是甲烷分子装在由水分子形成的“笼子”里。下列说法正确的是(
)
A.甲烷分子和水分子的VSEPR模型都是正四面体形
B.甲烷分子通过氢键与构成“笼子”的水分子相结合
C.可燃冰属于分子晶体
D.水分子的键角大于甲烷分子的键角
5.干冰晶胞如图所示,若干冰的晶胞棱长为a,则每个CO 分子周围与其相距❑√2a的CO 分子有( )
2 2
2
A.4个 B.8个 C.12个 D.6个
6.下图为冰晶体的结构模型,大球代表O,小球代表H。下列有关说法正确的是( )A.冰晶体中每个水分子与另外四个水分子形成四面体结构
B.冰晶体具有空间网状结构,是共价晶体
C.水分子间通过H—O键形成冰晶体
D.冰融化后,水分子之间的空隙增大
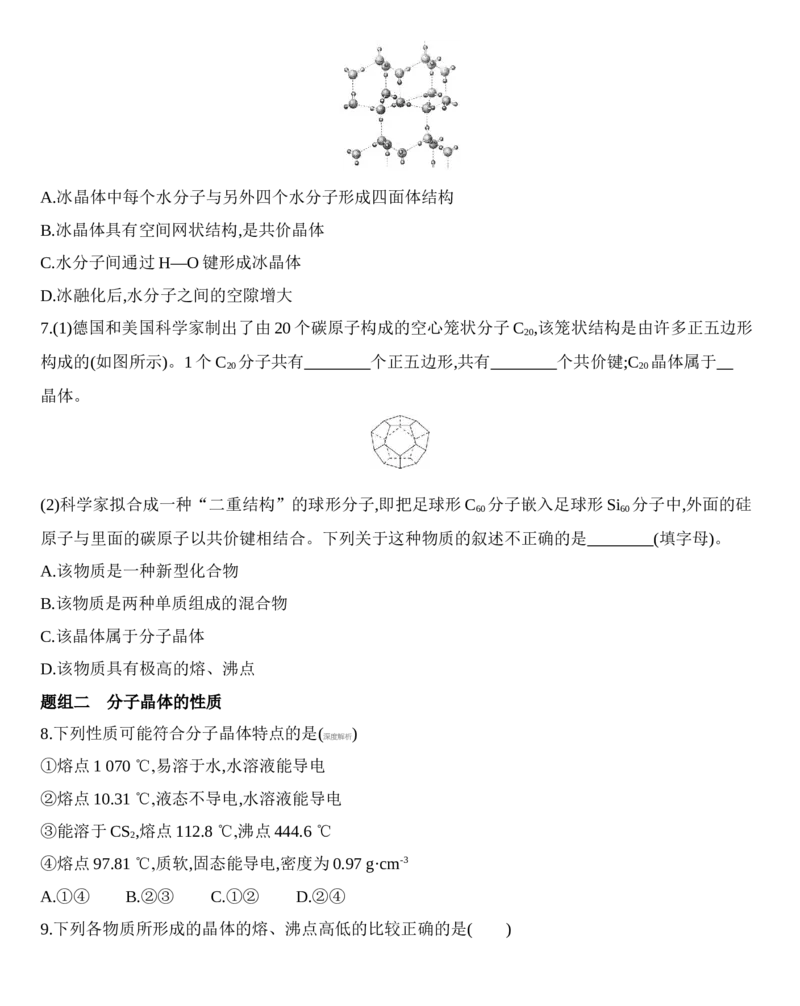
7.(1)德国和美国科学家制出了由20个碳原子构成的空心笼状分子C ,该笼状结构是由许多正五边形
20
构成的(如图所示)。1个C 分子共有 个正五边形,共有 个共价键;C 晶体属于
20 20
晶体。
(2)科学家拟合成一种“二重结构”的球形分子,即把足球形C 分子嵌入足球形Si 分子中,外面的硅
60 60
原子与里面的碳原子以共价键相结合。下列关于这种物质的叙述不正确的是 (填字母)。
A.该物质是一种新型化合物
B.该物质是两种单质组成的混合物
C.该晶体属于分子晶体
D.该物质具有极高的熔、沸点
题组二 分子晶体的性质
8.下列性质可能符合分子晶体特点的是( )
深度解析
①熔点1 070 ℃,易溶于水,水溶液能导电
②熔点10.31 ℃,液态不导电,水溶液能导电
③能溶于CS ,熔点112.8 ℃,沸点444.6 ℃
2
④熔点97.81 ℃,质软,固态能导电,密度为0.97 g·cm-3
A.①④ B.②③ C.①② D.②④
9.下列各物质所形成的晶体的熔、沸点高低的比较正确的是( )A.H >N >O
2 2 2
B.NH >AsH >PH
3 3 3
C.Cl >Br >I
2 2 2
D.C(CH ) >(CH ) CHCH CH >CH CH CH CH CH
3 4 3 2 2 3 3 2 2 2 3
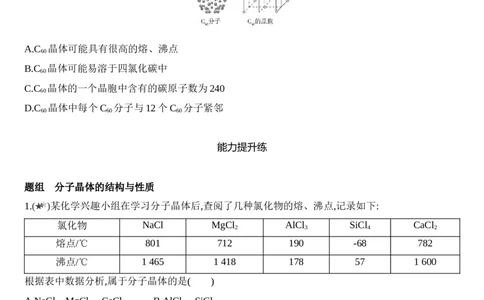
10.C 分子和C 晶胞示意图如图所示。下列关于C 晶体的说法中不正确的是( )
60 60 60
A.C 晶体可能具有很高的熔、沸点
60
B.C 晶体可能易溶于四氯化碳中
60
C.C 晶体的一个晶胞中含有的碳原子数为240
60
D.C 晶体中每个C 分子与12个C 分子紧邻
60 60 60
能力提升练
题组 分子晶体的结构与性质
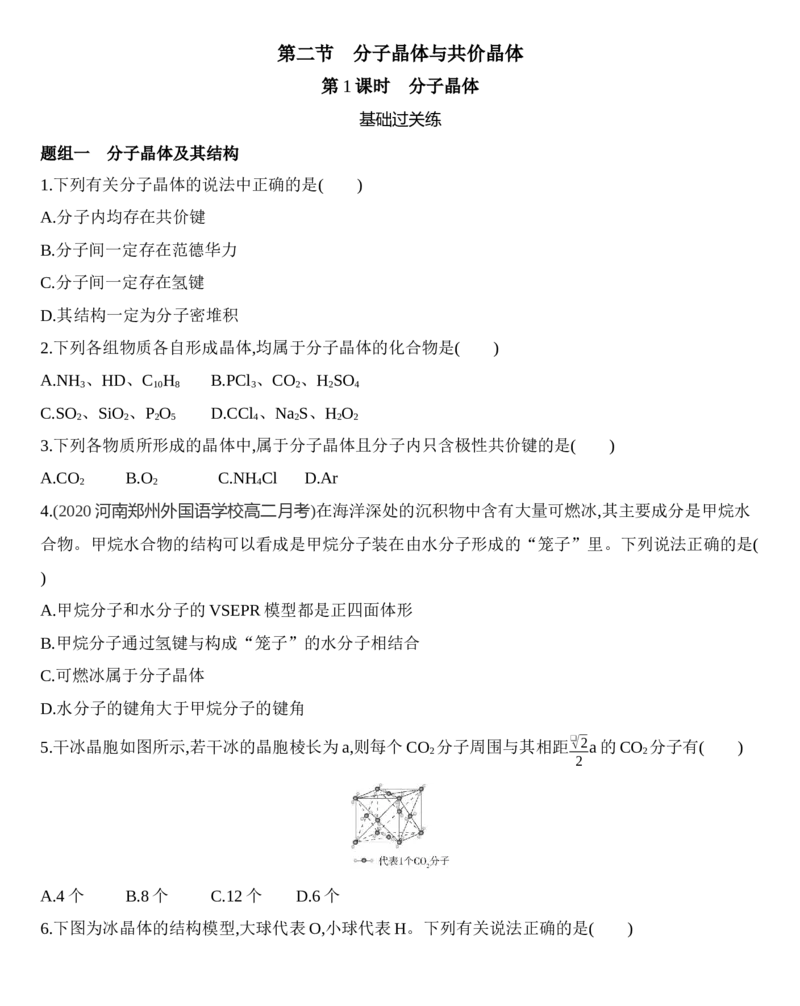
1.( )某化学兴趣小组在学习分子晶体后,查阅了几种氯化物的熔、沸点,记录如下:
氯化物 NaCl MgCl AlCl SiCl CaCl
2 3 4 2
熔点/℃ 801 712 190 -68 782
沸点/℃ 1 465 1 418 178 57 1 600
根据表中数据分析,属于分子晶体的是( )
A.NaCl、MgCl 、CaCl B.AlCl 、SiCl
2 2 3 4
C.NaCl、CaCl D.全部
2
2.(双选)( )常温下硫单质主要以S 形式存在,加热时S 会转化为S 、S 、S 等,当温度达到750 ℃时
8 8 6 4 2
主要以S 形式存在,下列说法正确的是( )
2
A.S 转化为S 、S 、S 属于物理变化
8 6 4 2
B.无论哪种硫分子,在空气中完全燃烧时都生成SO
2C.常温条件下单质硫为分子晶体
D.把硫单质在空气中加热到750 ℃即得S
2
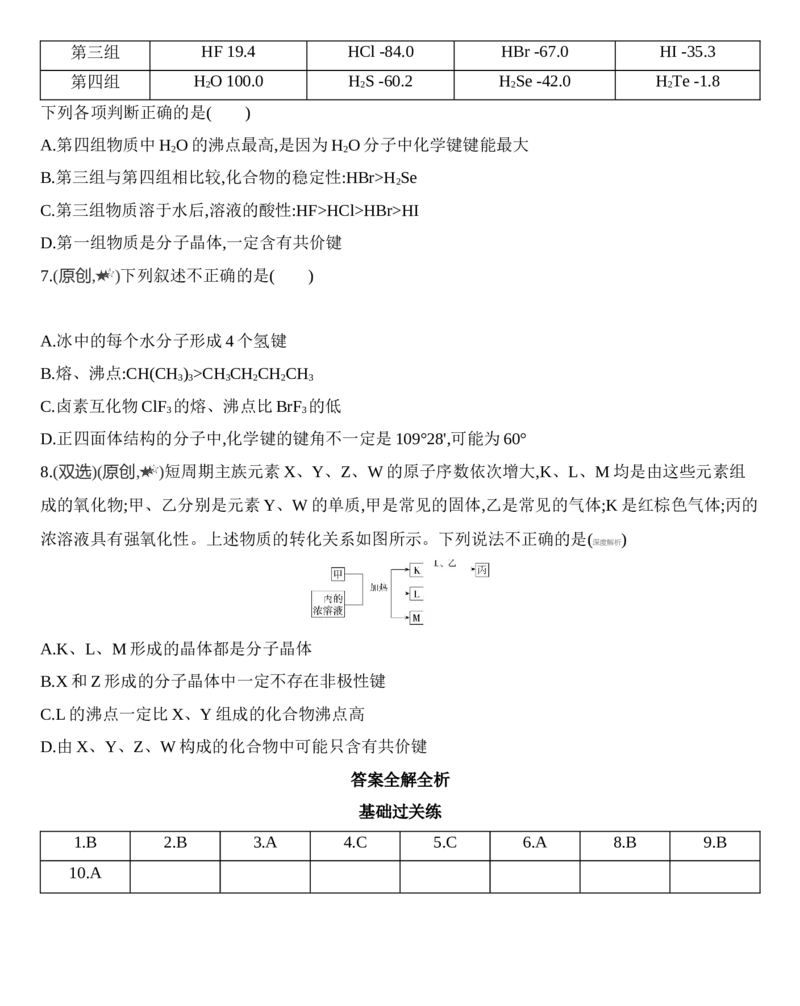
3.( )近年来,科学家合成了一些具有独特化学性质的氢铝化合物(AlH ) 。已知,最简单的氢铝化合物
3 n
的化学式为Al H ,它的熔点为150 ℃,燃烧时放出大量的热量。Al H 的结构如下图。下列说法肯定错
2 6 2 6
误的是 ( )
A.Al H 在固态时所形成的晶体是分子晶体
2 6
B.氢铝化合物可能成为未来的储氢材料和火箭燃料
C.Al H 在空气中完全燃烧,产物为氧化铝和水
2 6
D.Al H 中含有离子键和极性共价键
2 6
4.( )冰晶胞中水分子的空间排列方式与金刚石晶胞类似,其晶胞结构如图所示。下列有关说法正确
的是( )
A.冰晶胞内水分子间以共价键结合
B.每个冰晶胞平均含有4个水分子
C.水分子间的氢键具有方向性和饱和性,也是σ键的一种
D.冰变成水,氢键部分被破坏
5.( )下列说法正确的是( )
A.范德华力普遍存在于分子之间,如液态水中因范德华力的存在使水分子发生缔合
B.H SO 为强电解质,硫酸晶体是能导电的
2 4
C.冰中1个H O分子可通过氢键与4个水分子相连,所以冰中H O分子与氢键的数目之比为1∶4
2 2
D.氢键有饱和性和方向性,所以液态水结成冰时体积会变大
6.( )有四组同一族元素所形成的不同物质,在101 kPa时测定它们的沸点(℃)如下表所示:
第一组 A -268.8 B -249.5 C -185.8 D -151.7
第二组 F -187.0 Cl -33.6 Br 58.7 I 184.0
2 2 2 2第三组 HF 19.4 HCl -84.0 HBr -67.0 HI -35.3
第四组 H O 100.0 H S -60.2 H Se -42.0 H Te -1.8
2 2 2 2
下列各项判断正确的是( )
A.第四组物质中H O的沸点最高,是因为H O分子中化学键键能最大
2 2
B.第三组与第四组相比较,化合物的稳定性:HBr>H Se
2
C.第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI
D.第一组物质是分子晶体,一定含有共价键
7.(原创, )下列叙述不正确的是( )
A.冰中的每个水分子形成4个氢键
B.熔、沸点:CH(CH ) >CH CH CH CH
3 3 3 2 2 3
C.卤素互化物ClF 的熔、沸点比BrF 的低
3 3
D.正四面体结构的分子中,化学键的键角不一定是109°28',可能为60°
8.(双选)(原创, )短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组
成的氧化物;甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体;K是红棕色气体;丙的
浓溶液具有强氧化性。上述物质的转化关系如图所示。下列说法不正确的是( )
深度解析
A.K、L、M形成的晶体都是分子晶体
B.X和Z形成的分子晶体中一定不存在非极性键
C.L的沸点一定比X、Y组成的化合物沸点高
D.由X、Y、Z、W构成的化合物中可能只含有共价键
答案全解全析
基础过关练
1.B 2.B 3.A 4.C 5.C 6.A 8.B 9.B
10.A1.B 稀有气体组成的晶体中,其分子内不存在任何化学键,A项错误;分子间作用力包括范德华力和氢
键,所有的分子晶体中都存在范德华力,但只有部分分子晶体的分子间存在氢键,B项正确,C项错误;存
在氢键的分子晶体不采取分子密堆积的方式,D项错误。
2.B A项,HD属于单质;C项,SiO 属于共价晶体;D项,Na S中含有离子键。
2 2
3.A 固体CO (干冰)是分子晶体,分子内只有极性键。O 、Ar形成的晶体都属于分子晶体,但O 中只
2 2 2
有非极性共价键,Ar原子间没有共价键。NH Cl由NH+和Cl-组成,是离子化合物,其形成的晶体不属于
4 4
分子晶体。
4.C CH 的VSEPR模型为正四面体形,H O的VSEPR模型是四面体形,A项错误;甲烷分子与构成
4 2
“笼子”的水分子间不能形成氢键,B项错误;可燃冰属于分子晶体,C项正确;H O的键角为105°,CH
2 4
的键角为 109°28',D项错误。
5.C 以顶点CO 分子为研究对象,若干冰的晶胞棱长为a,该CO 分子周围与其相距❑√2a的CO 分子处
2 2 2
2
于共用这个顶点的面的面心,由于顶点CO 分子为8个晶胞共有,则每个CO 分子周围与其相距❑√2a的
2 2
2
CO 分子有8×3=12个,故选C。
2
2
6.A 冰晶体属于分子晶体,冰晶体中的水分子主要是靠氢键结合在一起,氢键不是化学键,而是一种分
子间作用力,故B、C两项均错误。每个水分子可以与4个水分子形成氢键,从而形成四面体结构,A项
正确。冰晶体中形成的氢键具有方向性和饱和性,故水分子间由氢键连接后,分子间空隙变大,因此冰
融化成水后,体积减小,水分子之间空隙减小,D项错误。
7.答案 (1)12 30 分子 (2)BD
解析 (1)根据题给信息可判断C 晶体属于分子晶体。根据其结构可知每个碳原子形成3个C—C键,
20
每个共价键被2个碳原子共用,所以1个C 分子含有的共价键数是20×3=30。因为每个共价键被2个
20
2
正五边形共用,所以平均每个正五边形含有的共价键数是5=2.5,故1个C 分子共有 30 =12个正五边
20
2 2.5
形。(2)该物质是一种“二重结构”的球形分子,故A项正确;该物质中碳原子和硅原子间形成共价键,它是化合物,故B项错误;该晶体是由分子构成的,属于分子晶体,故C项正确;该晶体属于分子晶体,熔、
沸点较低,故D项错误。
8.B 本题考查分子晶体的性质。分子晶体中分子之间是以分子间作用力相结合的,分子晶体具有低
熔点、易升华、硬度小等性质。①熔点高,不是分子晶体的性质;④固态能导电,不是分子晶体的性质,
故选②③。
归纳总结 在分子晶体中,相邻分子靠分子间作用力相互吸引。由于分子间作用力较弱,分子晶体熔
化时,只需克服分子间作用力,不破坏化学键,所以分子晶体一般具有较低的熔、沸点。此外,还具有硬
度小、易升华、有较强的挥发性、一般不导电等特点。
9.B 一般组成和结构相似的分子晶体的熔、沸点随相对分子质量的增大而升高,即熔、沸
点:H AsH >PH ,B项正确;相对分子质量相同的烷烃,其支链越多,熔、沸点越低,即熔、沸
3 3 3
点:C(CH ) <(CH ) CHCH CH H Se,B正确;第三组物质溶于水后,HF溶液的酸
2
性最弱,C不正确;第一组物质是分子晶体,但分子中不一定含有共价键,如稀有气体分子中无共价键,D
不正确。
7.B 冰中每个水分子形成4个氢键,A项正确;相对分子质量相同的烷烃,其支链越多,熔、沸点越低,
即熔、沸点:CH(CH )