文档内容
A、氧化物 B、酸 C、碱 D、盐
附参考答案
初三年级化学第7单元检测(酸碱)
10.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是
(满分:70分,时间:60分钟) A.烧碱 B.石灰水 C.浓盐酸 D.氯化钾
12.15 11.下列物质的用途,是利用其物理性质的是
一、选择题(每题2分,共30分) A.干冰用于人工降雨 B.盐酸用于除铁锈
1.硫代硫酸钠晶体是一种恒温保温瓶的填充物,硫代硫酸钠(NaSO)属于 C.氧气用于医疗急救 D.熟石灰用于改良土壤酸性
2 2 3
A.氧化物 B.酸 C.碱 D.盐 12.由Mg(OH) 和MgO组成的混合物,测得其中含镁元素的质量分数为48%。取该混合物10g,将其投
2
2.下列操作中,不正确的是 入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为 ( )
A.用胶头滴管向试管中滴加液体时,把滴管伸入试管内 A.12g B.24g C.36g D.48g
B.把氢氧化钠固体放在天平左盘的玻璃器皿中称量 13.下列实验能利用厨房中的食盐、食醋、纯碱三种物质做成功的是
C.在实验室里制取CO 气体时,应先检查装置气密性 ①检验自来水中是否含有氯离子;②检验鸡蛋壳能否溶于酸;③除去热水瓶中的水垢。
2
D.浓硫酸沾到皮肤上,要立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液 A.①②③ B.②③ C.①③ D.①②
3. 铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应 14.现有四组物质的溶液,仅用酚酞试液及同组物质之间相互反应就能鉴别出来的是 ( )
关系如图3所示,图中两圆相交部分(A、B、C、D)表示物质间反应的 A.NaOH Ba(OH) HCl B.NaOH HCl NaCl
2
主要实验现象,其中描述正确的是 石灰水 A 稀盐酸 C.NaOH H C1 HNO D.HSO NaCl NaSO
3 2 4 2 4
A.有气泡产生 B.无明显现象
B D
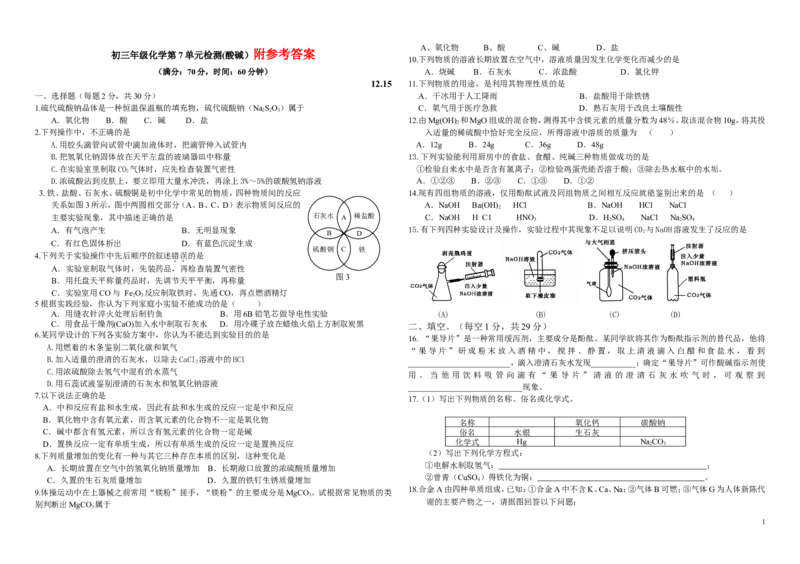
15.有下列四种实验设计及操作,实验过程中其现象不足以说明C0
2
与Na0H溶液发生了反应的是
C.有红色固体析出 D.有蓝色沉淀生成
硫酸铜 C 铁
4.下列关于实验操作中先后顺序的叙述错误的是
A.实验室制取气体时,先装药品,再检查装置气密性
图3
B.用托盘天平称量药品时,先调节天平平衡,再称量
C.实验室用CO与 Fe O 反应制取铁时,先通CO,再点燃酒精灯
2 3
5根据实践经验,你认为下列家庭小实验不能成功的是( )
A.用缝衣针淬火处理后制钓鱼 B.用6B铅笔芯做导电性实验 (A) (B) (C) (D)
C.用食品干燥剂(CaO)加入水中制取石灰水 D.用冷碟子放在蜡烛火焰上方制取炭黑 二、填空。(每空1分,共29分)
6.某同学设计的下列各实验方案中,你认为不能达到实验目的的是
16. “果导片”是一种常用缓泻剂,主要成分是酚酞。某同学欲将其作为酚酞指示剂的替代品,他将
A.用燃着的木条鉴别二氧化碳和氧气
“果导片”研成粉末放入酒精中,搅拌、静置,取上清液滴入白醋和食盐水,看到
B.加入适量的澄清的石灰水,以除去CaCl 溶液中的HCl
2 _________________________,滴入澄清石灰水发现___________;确定“果导片”可作酸碱指示剂使
C.用浓硫酸除去氢气中混有的水蒸气
用 。 当 他 用 饮 料 吸 管 向 滴 有 “ 果 导 片 ” 清 液 的 澄 清 石 灰 水 吹 气 时 , 可 观 察 到
D.用石蕊试液鉴别澄清的石灰水和氢氧化钠溶液
____________________________现象。
7.以下说法正确的是
17.(1)写出下列物质的名称、俗名或化学式。
A.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
B.氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物
名称 氧化钙 碳酸钠
C.碱中都含有氢元素,所以含有氢元素的化合物一定是碱 俗名 水银 生石灰
D.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应 化学式 Hg Na 2 CO 3
(2)写出下列化学方程式:
8.下列质量增加的变化有一种与其它三种存在本质的区别,这种变化是
①电解水制取氢气: ;
A.长期放置在空气中的氢氧化钠质量增加 B.长期敞口放置的浓硫酸质量增加
②曾青(CuSO )得铁化为铜: 。
C.久置的生石灰质量增加 D.久置的铁钉生锈质量增加 4
18.合金A由四种单质组成,已知:①合金A中不含K、Ca、Na;②气体B可燃;③气体G为人体新陈代
9.体操运动中在上器械之前常用“镁粉”搓手,“镁粉”的主要成分是MgCO 。试根据常见物质的类
3
谢的主要产物之一,请据图回答以下问题:
别判断出MgCO 属于
3
1。
(2)实验a中产生的气体,可用 法收集。
(3)同学们对实验a中产生的气体的组成看法不一,提出了以下几种假设:
①该气体是CO; ②该气体是H。
2
请你推测该气体还可能是 (写化学式)。
三、计算。(1,2小题,每题3分,第3小题5分)
22.成都市近年来常常发生“毒奶粉”事件。劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质的
(1)合金A由哪些单质组成(用化学式表示): 、 、 、 ; 含量,导致食用这种奶粉的众多婴幼儿严重营养不良乃至死亡。
(2)写出反应①的化学方程式: ; 为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白
(3)写出反应②的化学方程式: 。 质中的氮元素完全转化为氨气(化学式为 NH ),再用稀硫酸吸收氨气,反应的化学方程式为:2
3
19.锅炉发生爆炸,可能是由于锅炉内水垢过厚或缺水造成的。为了防止锅炉爆炸,常采用下列措施: NH +H SO = (NH ) SO 现取该奶粉样品100g,用“盖尔达法”分解其中的蛋白质,产生的氨气用
3 2 4 4 2 4。
(1)锅炉使用软水。生活中区别软水和硬水常用的物质是 。 7.5g溶质质量分数为19.6%的稀硫酸恰好完全吸收。
(2)通过锅炉水位计指示情况,及时向锅炉内补充水。水位计应用了 原理。 计算并回答下列问题:(1)产生氨气的质量是多少?(计算结果精确到0.01,下同)
(3)定期清洗锅炉。水垢的主要成分是碳酸钙和氢氧化镁,请写出用稀盐酸清洗水垢的化学方程 (2)含氮元素的质量多少?
式(写一个即可) 。 (3) 该奶粉中氮的含量是否达到了国家规定的标准。(奶粉中蛋白质的含量国家标准为:每100g婴幼
20.请根据图示回答下列问题:
儿奶粉中含12g~25g。蛋白质含氮元素的质量分数为16%)
初三年级化学第7单元检测参考答案
一、选择题(每题2分,共30分)
1—5:DACAA 6—10:DBBDB 11—15:ABBBB
二、填空。(每空1分,共29分)
(1
)写出图中标号的仪器名称:① ,② ;
16.无明显变化 变红色 溶液浑浊,颜色变浅(或消失)
(2)实验室欲用高锰酸钾制取氧气,应选择的气体发生装置是 ,产生氧气的化学方 17..(1)汞 CaO 纯碱等(合理即可) (2)2HO 2H↑+O ↑ Fe+CuSO=FeSO+Cu
2 2 2 4 4
程式为 ;
18.(1)Fe、Cu、C、Mg (2)2Al+3FeCl =3Fe+2AlCl (2分)(3)CuO+HSO =CuSO +H O(2分)
2 3 2 4 4 2
(3)已知过氧化钠(NaO)是一种淡黄色固体,常温下可与水反应生成氢氧化钠和氧气。如果在实
2 2 9.(1)肥皂水(选用其他合理的物质也可给分) (2)连通器
验室中用A装置作气体发生装置,用过氧化钠和水反应来制取一瓶干燥的氧气,所选装置的正确
连接顺序是(填写管口字母) a → 。若只改变A装置中的药品,仍采
(3)CaCO
3
+2HCl== CaCl
2
+H
2
O+CO
2
↑ 或Mg(OH)
2
+2HCl== MgCl
2
+2H
2
O
用已连接的整套装置,还可以用来制取的气体是 。 20.(1)①锥形瓶,②酒精灯;(2)B,2KMnO
△
K MnO +MnO+O ↑;
4 2 4 2 2
(4)通过上述两种制取氧气的方法所选用发生装置的对比,你觉得选择气体发生装置应考虑的因
(3)g→f→i。CO;(4)药品的状态和反应条件;
素是 ; 2
(5)装置A和C都可以作为实验室制取同种气体的发生装置,A和C相比,具有哪些优点?(只答
(5)可随时加液体反应物,并通过滴加液体的快慢,控制反应的速率。
出一条即可) 。 21.(7分)(1)钠、氧 质量守恒定律 (2)排水 (3)O
2
21.某淡黄色的颗粒状固体,其化学性质比较活泼,在通常状况下能跟许多物质发生化学反应。例如:它 三、计算。22. (1)0.51g (2)0.42g (3)不达标
与CO 反应时,只生成了NaCO 和O,它与稀盐酸反应时,只生成了NaCl、HO和O。上课时,老师做
2 2 3 2 2 2
了如下实验:
a.取少量的淡黄色的颗粒状固体投入到盛有少量水的试管中,可观察到产生了一种无色无味的气体;
b.再向试管中滴加几滴酚酞试液,可观察到烧杯中溶液变红。
根据实验现象,回答下列问题:
(1)淡黄色的颗粒状固体中一定含有 元素。你做出这个判断的理由是
2