文档内容
第三章 铁 金属材料
过关测试 基础卷
(时间:90分钟)
一、选择题(每小题3分,共48分)
1.下列说法中不正确的是( )
A.生铁是铁的一种合金
B.合金是混合物
C.一般地说合金的熔点比它的各成分金属的熔点都高
D.铝制餐具不宜用来蒸煮或长期存放酸性或碱性食物
2.下列说法错误的是( )
A.铝合金大量用于高铁建设
B.“玉兔二号”钛合金筛网轮的主要成分是非金属材料
C.制饭勺、饭盒,高压锅等的不锈钢是合金
D.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品
3.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮
及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
A.无水硫酸铜、蔗糖B.硅胶、食盐 C.食盐、硫酸亚铁 D.生石灰、硫酸亚铁
4.实验室用 FeCl 溶液与烧碱制备 Fe(OH) ,为了使生成的产物不容易被氧化, 下列说法中不正确的是
2 2
A.配制 FeCl 溶液和烧碱溶液所用的蒸馏水通常要煮沸
2
B.可在 FeCl 溶液的上面加一层植物油,以隔绝空气
2
C.向 FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入试管内
2
D.产生 Fe(OH) 沉淀后,不能振荡试管
2
5.在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.
B.
C.
D.
6.制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得。用以上两
种方法都可制得的氯化物是( )
A.AlCl B.FeCl C.FeCl D.CuCl
3 3 2 2
7.类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是( )
A.已知:将Fe加入CuSO 溶液中 Fe+ Cu2+= Cu + Fe2+
4类推:将 Na加入 到CuSO 溶液中2Na + Cu2+= Cu+2Na+
4
B.已知:稀硫酸与Ba(OH ) 溶液反应至中性2H+ + SO 2-+ Ba2++ 2OH- = BaSO↓+ 2H O
2 4 4 2
类推:NaHSO 溶液与Ba(OH) 溶液反应至中性2H+ + SO 2-+ Ba2++ 2OH- = BaSO↓+ 2H O
4 2 4 4 2
C.已知:铁和氯气反应2Fe + 3Cl 2FeCl
2 3
类推:铁和碘单质反应2Fe + 3I 2FeI
2 3
D.已知:向Ca(ClO) 溶液中通入少量CO:Ca2+ + 2ClO-+ CO+ H O= CaCO ↓+2HClO
2 2 2 2 3
类推:向 Ca(ClO) 溶液中通入少量SO :Ca2+ + 2ClO-+ SO + H O= CaSO ↓+2HClO
2 2 2 2 3
8.等质量的两份铝分别与适量的稀HSO 和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀HSO
2 4 2 4
与NaOH溶液的物质的量浓度之比为( )
A.3∶2 B.2∶3 C.2∶1 D.1∶2
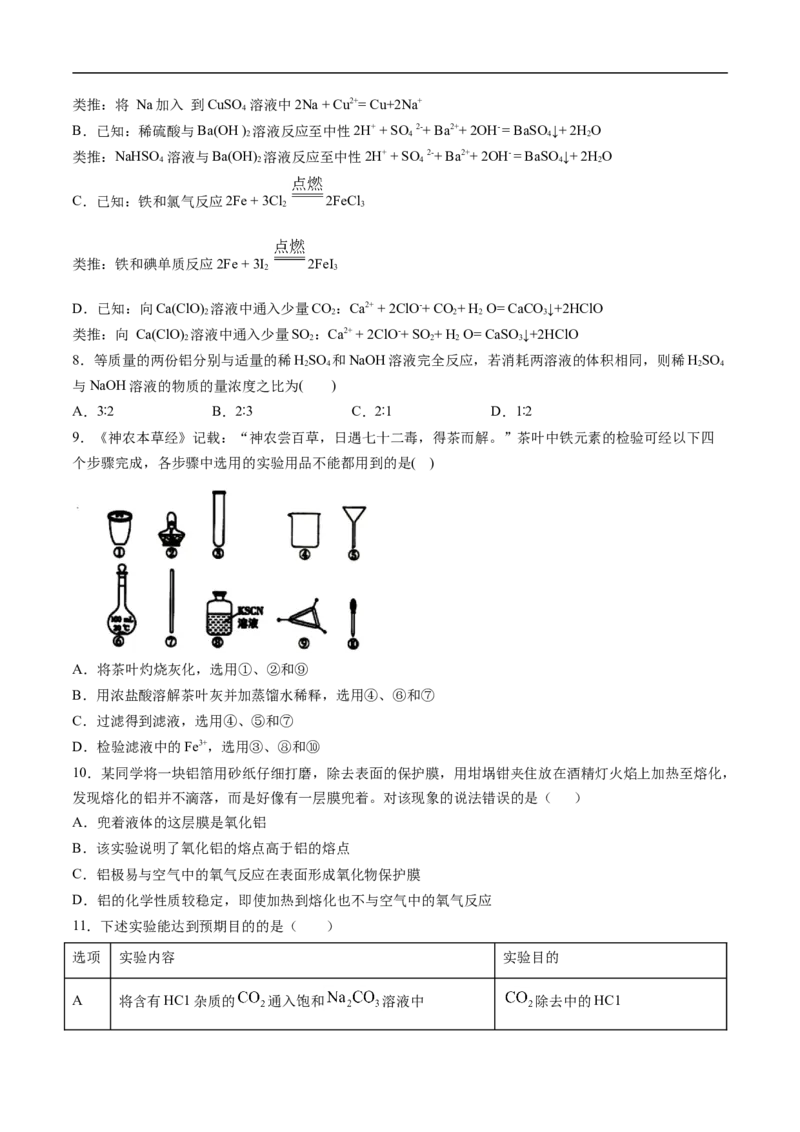
9.《神农本草经》记载:“神农尝百草,日遇七十二毒,得茶而解。”茶叶中铁元素的检验可经以下四
个步骤完成,各步骤中选用的实验用品不能都用到的是( )
A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+,选用③、⑧和⑩
10.某同学将一块铝箔用砂纸仔细打磨,除去表面的保护膜,用坩埚钳夹住放在酒精灯火焰上加热至熔化,
发现熔化的铝并不滴落,而是好像有一层膜兜着。对该现象的说法错误的是( )
A.兜着液体的这层膜是氧化铝
B.该实验说明了氧化铝的熔点高于铝的熔点
C.铝极易与空气中的氧气反应在表面形成氧化物保护膜
D.铝的化学性质较稳定,即使加热到熔化也不与空气中的氧气反应
11.下述实验能达到预期目的的是( )
选项 实验内容 实验目的
A 将含有HC1杂质的 通入饱和 溶液中 除去中的HC1B 向含氯化铁杂质的氯化铵溶液中加入氢氧化钠溶液,过滤 除去氯化铵中的氯化铁
C 向含 杂质的 溶液中加入铁粉 除去 溶液中的
D 向含 杂质的 溶液中加入 溶液 除去 溶液中的
12.下列金属①铁、②镁、③锰、④矾、⑤铬,可用铝热法制备的有( )
A.①②④ B.①②③⑤
C.①③④⑤ D.①②③④⑤
13.设N 为阿伏加德罗常数,下列有关说法正确的是( )
A
A.100mL12mol/L浓盐酸与足量的MnO 加热充分反应生成Cl 分子数为0.3N
2 2 A
B.5.4g铝粉与足量的氢氧化钠溶液充分反应生成H 分子数为0.3N
2 A
C.向FeI 溶液中通入适量Cl,当有1 mol Fe2+被氧化时,转移的电子的数目为N
2 2 A
D.18gH O在标准状况下所占体积约为22.4L
2
14.在CuCl 溶液中加入一定量的Zn、Fe充分反应,得到一些固体,过滤,向固体中加入少量稀盐酸,有
2
气体产生。对上述固体的叙述正确的是( )
①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe ⑥可能含有Cu
A.②③④ B.①②③ C.③④⑤ D.①②⑥
15.下列各项操作中,不产生“先生成沉淀,然后沉淀又溶解”现象的是( )
A.向饱和 溶液中通入过量的
B.向澄清石灰水中持续通入
C.向 溶液中逐滴加入过量的稀 溶液
D.向 胶体中逐滴加入过量的稀盐酸
16.向某溶液中加入铝粉能放出 ,下列各组离子一定不能在该溶液中大量共存的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
二、非选择题(共52分)
17.(8分)铝是一种重要金属:
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:___。
(2)铝还用于冶炼熔点较高的金属如钒、铬、锰等,请配平下列用铝冶炼金属钒的化学反应方程式:
___VO+___Al ___Al O+___V
2 5 2 3
该反应中氧化剂是___,要得到1mol金属钒,需要纯铝的质量___g。
18.(10分)铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:(1)FeCl 溶液呈黄色,FeCl 溶液的分散质是_______,分散剂是_______。
3 3
(2)Fe(OH) 是难溶于水的固体,那么分离Fe(OH) 与水的悬浊液常用的方法是________
3 3
(3)Fe(OH) 胶体呈红褐色,具有良好的净水效果。由饱和FeCl 溶液制备 Fe(OH) 胶体的化学方程式是
3 3 3
________。
(4)鉴别FeCl 溶液和Fe(OH) 胶体,除了可通过观察颜色以外,还有的方法是_______。
3 3
(5)下列关于Fe(OH) 胶体和Fe(OH) 悬浊液的描述,正确的是_______
3 3
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠 有多种方法,其
2 4
中一种方法的原理可用离子方程式表示为 3ClO-+2Fe3++10OH-=2FeO +3Cl-+5HO,则NaFeO 中铁元
2 2 4
素的化合价为_______,该离子反应中氧化剂与还原剂的个数比为_______,生成1个高铁酸钠转移
_______个电子。
19.(10分)根据你学过的有关金属的知识,回答下列问题(已知:铜、锌能与硝酸反应,而金不反应):
(1)铜钱在我国历史上曾经是一种广泛流通的货币,如图所示,铜常用于制造货币的原因可能是
______________(填字母)。
A.铜的熔点不是太高,易于冶炼,易于铸造成型
B.铜的性质不活没,不易被腐蚀
C.我国较早地掌握了湿法冶炼铜的技术
D.自然界有大量的游离态的铜
(2)铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是________________________(填化学式,
下同),常见的铁的氧化物还有__________________、__________________。
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏,若使氧化铝与氢氧
化钠溶液作用,反应的化学方程式为_____________________________________________。
(4)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的货币,这肯定是_______________币,黑色物质
是___________________(填名称),形成这种物质的化学方程式为____________________,绿色物质是
___________________(填化学式),这枚金属币的真面目为________________色。另外一枚是闪闪发光的黄
色金属币,它肯定是__________币,表面一直未被氧化的原因是
________________________________________________________。
20.(12分)某研究小组对市售某种补铁口服液(标签如图所示)的成分进行探究。根据名称猜测该糖浆中
含有 ,设计方案进行验证。Ⅰ.设计方案如下:
方案 试剂X 预期现象
i
ii 酸性 溶液
iii 依次加入5滴KSCN溶液、1mL新制氯水
(1)方案i的预期现象是产生白色沉淀,逐渐变为灰绿色,最终变为红褐色。产生白色沉淀的离子方程式是
_________________________,由白色沉淀变为红褐色沉淀的化学方程式是_____________________。
(2)方案ⅱ的预期现象是__________________________。
(3)方案ⅲ的预期现象是___________________。氯水参与反应的离子方程式是______________________。
Ⅱ.由Ⅰ中设计方案得到的实际现象如下:
方案 实际现象 是否与预期现象相同
i 产生灰绿色浑浊,长时间不变红褐色
ii 酸性 溶液褪色
iii 自始至终无明显现象
(4)为探究实际现象与预期现象不同的原因,该小组同学查看说明书,得知该补铁口服液的成分如下:
结合资料对实际现象与预期现象不同的原因进行猜想:_____________________;为验证该猜想,在方案
ⅲ的基础上继续加入过量的新制氯水,得到了预期现象。
(5)实验反思;方案ⅱ中预期现象与实验现象相同,并不能证明补铁口服液中一定含有 ,理由是
____________________________________________________。
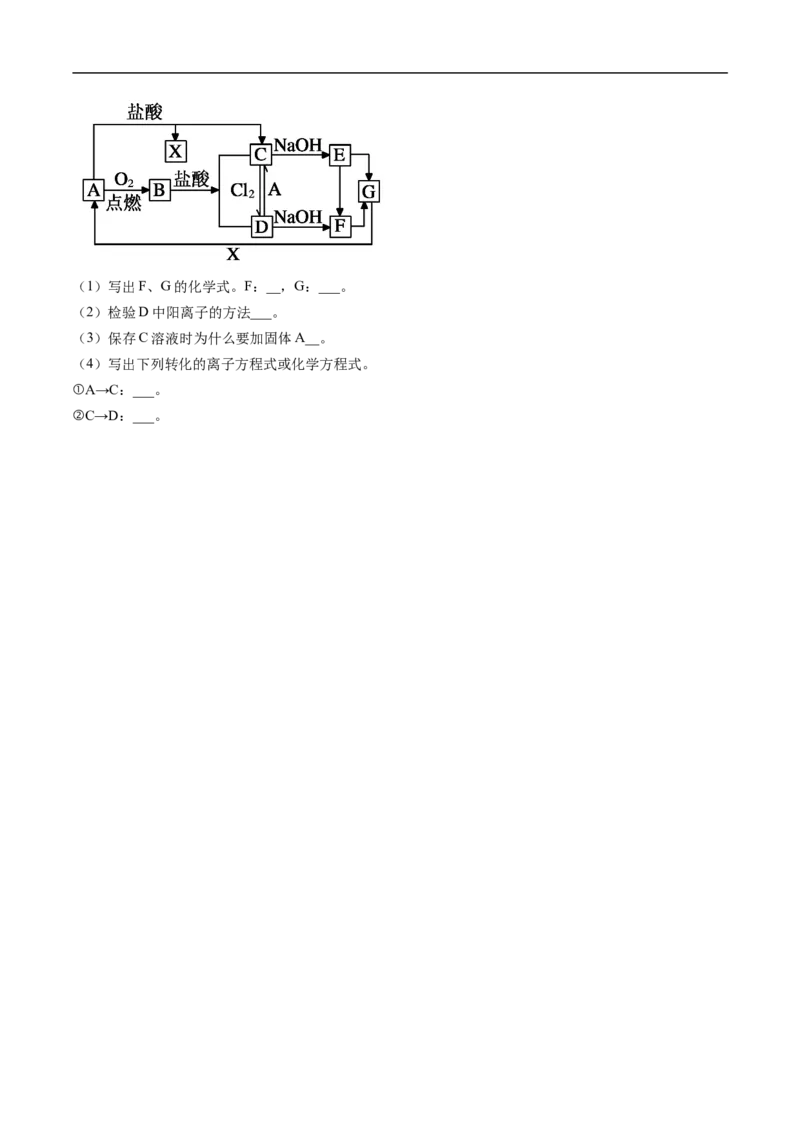
21.(10分)已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。(1)写出F、G的化学式。F:__,G:___。
(2)检验D中阳离子的方法___。
(3)保存C溶液时为什么要加固体A__。
(4)写出下列转化的离子方程式或化学方程式。
①A→C:___。
②C→D:___。