文档内容
课后达标训练/训练·提升作业
【基础达标】
1.下列有关物质的化学式、名称、俗名不完全对应的是( )
A.NaCl 氯化钠 食盐
B.CaO 氧化钙 熟石灰
C.Na CO 碳酸钠 纯碱
2 3
D.NaOH 氢氧化钠 烧碱
2.下列说法不正确的是( )
A.纯碱属于碱类,可用于玻璃、造纸、纺织、洗涤剂的生产
B.小苏打是制造发酵粉的主要成分之一,还可以治疗胃酸过多症
C.大理石、石灰石的主要成分相同,都是重要的建筑材料
D.胃酸中含有适量的盐酸,帮助消化,增加食欲
3.如图是实验室里一瓶标签破损的白色粉末状固体。小明同学取出
少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明
溶液,继续加入少量盐酸,有无色无味的气体产生。该固体可能是(
)
A.Na SO B.NaCl C.NaHCO D.NaOH
2 4 3
4.下列溶液混合后,不发生复分解反应的一组是( )
A.HCl和NaOH B.Na CO 和H SO
2 3 2 4
C.KNO 和NaCl D.NaOH和FeCl
3 3
5.下列物质分别能与稀盐酸、稀硫酸、氯化铜溶液反应并能观察到不同实验现象
的是( )
1A.氯化钾溶液 B.碳酸钠溶液
C.硝酸钡溶液 D.氢氧化钡溶液
6.下列各组离子在溶液中一定能大量共存的是( )
A.H+、OH-、Na+
B.Ca2+、OH-、CO 2-
3
C.Na+、K+、Cl-
D.H+、NO -、CO 2-
3 3
7.已知甲、乙、丙、丁四种溶液分别是Ba(OH) 溶液、MgSO 溶液、Na CO 溶液和稀
2 4 2 3
盐酸中的一种。甲、乙混合有白色沉淀出现;乙、丙按一定比例混合后所得液体的
导电性几乎为零。则甲、乙、丙、丁四种溶液可能是( )
A.Ba(OH) 、MgSO 、Na CO 、HCl
2 4 2 3
B.Na CO 、Ba(OH) 、MgSO 、HCl
2 3 2 4
C.HCl、MgSO 、Ba(OH) 、Na CO
4 2 2 3
D.Ba(OH) 、Na CO 、HCl、MgSO
2 2 3 4
8.在下列物质中:a.食盐b.纯碱c.碳酸氢钠d.碳酸钙
(1)“侯德榜制碱法”中的“碱”指的是____________(填字母,下同)。
(2)可用作调味剂的是______________。
(3)可用作补钙剂和牙膏填充剂的是______________。
(4)可用作发酵粉和治疗胃酸过多症的是_______________。
(5)既是钙盐又是碳酸盐的是_______________。
9.复分解反应是我们学过的化学基本反应类型之一。
(1)写出下列反应的化学方程式。
2①氯化钡溶液与硫酸钠溶液混合:
___________________________________________________________________;
②碳酸钠溶液与稀盐酸混合:
___________________________________________________________________;
③氢氧化钡溶液与稀硝酸混合:
___________________________________________________________________。
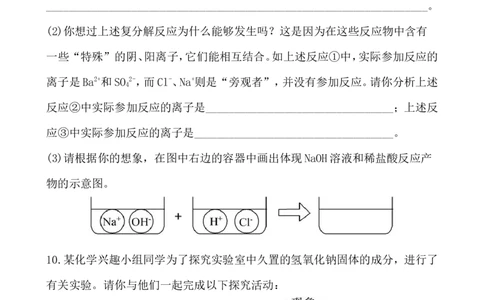
(2)你想过上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有
一些“特殊”的阴、阳离子,它们能相互结合。如上述反应①中,实际参加反应的
离子是Ba2+和SO 2-,而Cl-、Na+则是“旁观者”,并没有参加反应。请你分析上述
4
反应②中实际参加反应的离子是_________________________________;上述反
应③中实际参加反应的离子是___________________________________。
(3)请根据你的想象,在图中右边的容器中画出体现NaOH溶液和稀盐酸反应产
物的示意图。
10.某化学兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了
有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na CO ;
2 3
3猜想Ⅲ:是NaOH和Na CO 的混合物
2 3
【实验和推断】
(1)若现象a为有气泡产生,则加入的A溶液是_______________,说明氢氧化钠
已经变质,有气泡产生的反应的化学方程式是__________________________
___________________________________________________________________。
(2)若A是Ca(OH) 溶液,现象a为有白色沉淀,现象b为无色酚酞溶液变红色,
2
则白色沉淀为_______________(填化学式),该实验_______________(填“能”
或“不能”)说明样品中有NaOH。
(3)若A是CaCl 溶液,当实验现象a为_________________________,现象b为
2
_________________________________________,则猜想Ⅱ成立。
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)________________
___________________________________________________________________。
【知能提升】
1.在蔬菜生长过程中,常喷洒农药防治病虫害。据研究,用碱性溶液或清水浸泡,
可使残留在蔬菜上的农药的毒性降低。因此,买来的蔬菜在食用前最好用稀碱水
或清水浸泡一段时间。浸泡蔬菜时应加入适量( )
A.纯碱 B.白酒 C.白糖 D.食醋
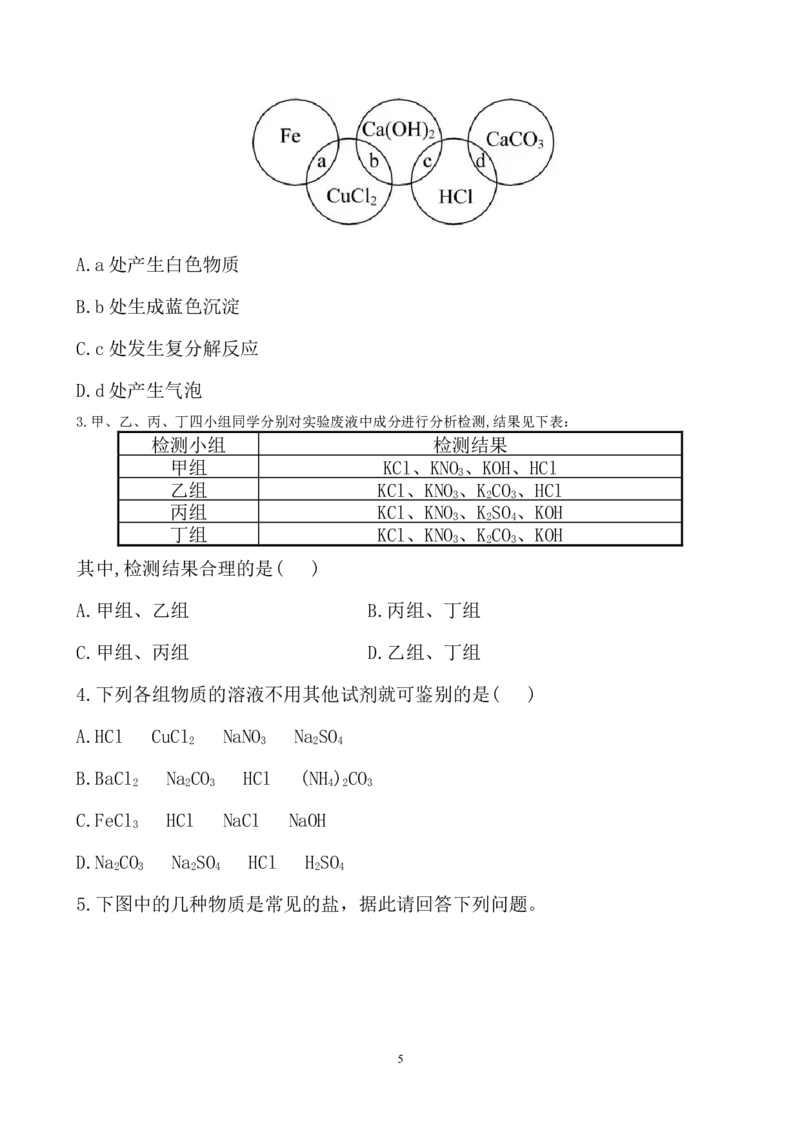
2.铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交
部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是(
)
4A.a处产生白色物质
B.b处生成蓝色沉淀
C.c处发生复分解反应
D.d处产生气泡
3.甲、乙、丙、丁四小组同学分别对实验废液中成分进行分析检测,结果见下表:
检测小组 检测结果
甲组 KCl、KNO 、KOH、HCl
3
乙组 KCl、KNO 、K CO 、HCl
3 2 3
丙组 KCl、KNO 、K SO 、KOH
3 2 4
丁组 KCl、KNO 、K CO 、KOH
3 2 3
其中,检测结果合理的是( )
A.甲组、乙组 B.丙组、丁组
C.甲组、丙组 D.乙组、丁组
4.下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuCl NaNO Na SO
2 3 2 4
B.BaCl Na CO HCl (NH ) CO
2 2 3 4 2 3
C.FeCl HCl NaCl NaOH
3
D.Na CO Na SO HCl H SO
2 3 2 4 2 4
5.下图中的几种物质是常见的盐,据此请回答下列问题。
5(1)在碳酸钠溶液中滴入氯化钙溶液,现象是________________。
(2)碳酸钙、碳酸钠均能与稀盐酸反应生成CO ,是因为碳酸钙、碳酸钠中均含有
2
________________ (写离子符号)。
(3)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的化学方程式为__________
___________________________________________________________________;
硫酸铜溶液与氯化钠溶液不能反应,其理由是____________________________
___________________________________________________________________。
6.某同学欲测定草木灰中碳酸钾的含量,称取69 g试样于烧杯中,加入29.2 g
稀盐酸恰好完全反应,充分反应后,称得混合物的总质量为93.8 g(忽略二氧化
碳的溶解对质量的影响)。请计算:
(1)反应过程中产生的二氧化碳质量为________________g。
(2)该草木灰试样中碳酸钾的质量分数。
【探究创新】
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对
反应后锥形瓶中残留废液进行了探究。
6【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na CO 和HCl。
2 3
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是_______________________________________。
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是__________________
___________________________________________________________________。
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产
生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验
________________(填“能”或“不能”)验证猜想(二)的正确性,原因是
____________________________________________________________________
__________________________________________________________________。
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应
的化学方程式为____________________________________________________
___________________________________________________________________。
7(3)若验证猜想(四)是否正确,下列试剂中可选用的有_____________(填序号)。
①氢氧化钠溶液 ②氯化钙溶液
③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进
行____________________操作即可从废液中得到NaCl固体。此方法的缺点是
____________________________________________________________________
________________________________________________________。
答案解析
【基础达标】
1.【解析】选B。氧化钙俗称生石灰,氢氧化钙俗称熟石灰,所以B不正确。
2.【解析】选A。纯碱是碳酸钠的俗称,其水溶液呈碱性,但其属于盐类。
3.【解析】选C。本题考查酸、碱、盐的性质。四种固体都能溶于水形成无色溶液,
但只有碳酸氢钠与盐酸反应会产生无色、无味的二氧化碳气体。
84.【解析】选C。HCl和NaOH反应生成氯化钠和水;Na CO 和H SO 反应生成硫酸钠、
2 3 2 4
水和二氧化碳气体;KNO 和NaCl不反应;NaOH和FeCl 反应生成氢氧化铁沉淀和
3 3
氯化钠。
【拓展延伸】复分解反应的判断
(1)生成物:有沉淀或气体或水生成时,复分解反应才可以发生。
反应物:有酸酸必溶,无酸碱盐溶。
(2)由于初中常见的酸是可溶性的,因此:
金属氧化物+酸→盐+水,
碱+酸→盐+水,
RHCO /RCO +酸→另一种盐+CO ↑+H O,
3 3 2 2
这三种复分解反应一定能发生。
5.【解析】选D。氯化钾与稀盐酸、稀硫酸、氯化铜都不反应,故A不符合题意;碳
酸钠与稀盐酸、稀硫酸反应都有气体生成,与氯化铜溶液反应生成沉淀,故B不
符合题意;硝酸钡溶液能与稀硫酸反应生成白色沉淀,与稀盐酸、氯化铜不反应,
没有现象,故C不符合题意;氢氧化钡溶液与稀盐酸反应没有明显现象,与稀硫
酸反应生成白色沉淀,与氯化铜溶液反应生成蓝色沉淀,故D符合题意。
6.【解析】选C。结合复分解反应发生的条件,A中H+与OH-结合生成水不能共存;B
中Ca2+与CO 2-结合生成碳酸钙沉淀,不能共存;C中各离子相互之间不反应能共
3
存;D中H+与CO 2-结合生成水与二氧化碳,不能共存。
3
7.【解析】选B。根据乙与丙按一定比例混合后所得液体的导电性几乎为零,可知
反应后溶液中不存在自由移动的离子,应该是MgSO 与Ba(OH) 的反应,故A、D错
4 2
误,又根据甲、乙混合有白色沉淀出现,而盐酸与MgSO 不反应,故可排除C选项,
4
故B正确。
8.【解析】“侯德榜制碱法”中的“碱”指的是纯碱;食盐有咸味,可食用,常用
作调味剂;碳酸钙含有钙元素,可用作补钙剂和牙膏填充剂;碳酸氢钠可用作发
酵粉和治疗胃酸过多症的药剂;盐可以根据所含的金属元素分类也可以根据所
含的酸根分类,碳酸钙既是钙盐又是碳酸盐。
答案:(1)b (2)a (3)d (4)c (5)d
9.【解析】按照复分解反应的规律,两种化合物相互交换成分生成两种新的化合
物,可写出有关的化学方程式。根据复分解反应的条件,在溶液中两种离子相互
结合生成了气体、沉淀或水。碳酸钠溶液与稀盐酸混合,实际参加反应的离子是
H+和CO 2-,结合生成了H O与CO ,氢氧化钡溶液与稀硝酸混合,实际参加反应的
3 2 2
离子是H+和OH-,结合生成了H O。
2
答案:(1)①BaCl +Na SO ====BaSO ↓+2NaCl
2 2 4 4
②Na CO +2HCl====2NaCl+H O+CO ↑
2 3 2 2
③Ba(OH) +2HNO ====Ba(NO ) +2H O
2 3 3 2 2
(2)H+和CO 2- H+和OH-
3
(3)
10.【解析】(1)Na CO 能与酸反应生成二氧化碳,若现象a为有气泡产生,则加入
2 3
的A溶液是盐酸或稀硫酸等酸。(2)Ca(OH) 与Na CO 反应生成白色沉淀CaCO 和
2 2 3 3
9NaOH,滴加无色酚酞溶液后变红色,该实验不能说明样品中有NaOH。(3)CaCl 溶
2
液与Na CO 溶液反应生成白色沉淀CaCO 和溶液显中性的氯化钠。所以当实验现
2 3 3
象a为有白色沉淀产生,现象b为无色酚酞溶液不变红色,则猜想Ⅱ成立。
答案:【实验和推断】
(1)盐酸 Na CO +2HCl====2NaCl+H O+CO ↑
2 3 2 2
(或稀硫酸等酸及其对应的化学方程式)
(2)CaCO 不能
3
(3)有白色沉淀产生无色酚酞溶液不变红色
【反思】CO +2NaOH====Na CO +H O
2 2 3 2
【知能提升】
1.【解析】选A。纯碱是碳酸钠的俗称,其水溶液呈碱性,因此浸泡蔬菜时可加入
适量的纯碱。
2.【解析】选A。Fe与CuCl 溶液反应的现象为铁丝表面覆盖一层红色物质。CuCl
2 2
与Ca(OH) 反应生成蓝色Cu(OH) 沉淀。所以A错,B、C、D均正确。
2 2
3.【解析】选B。甲组氢氧化钾和稀盐酸反应生成氯化钾和水,不能共存。乙组碳
酸钾和稀盐酸反应生成氯化钾和水还有二氧化碳气体,乙组不能共存。丙组相互
之间不反应能共存。丁组也能共存。故选B。
4.【解析】选C。根据溶液的颜色,可以鉴别出黄色的FeCl 溶液,再取FeCl 溶液
3 3
于三支试管,将剩余的三种溶液分别滴入FeCl 溶液中,产生红褐色沉淀的是
3
NaOH溶液;再将剩余的两种溶液滴入沉淀中,能使沉淀溶解的是HCl溶液。
5.【解析】(1)碳酸钠和氯化钙反应生成难溶于水的白色沉淀碳酸钙;(2)CO 2-会
3
和H+结合成水和二氧化碳;(3)硫酸铜与氯化钠反应的生成物中没有沉淀或气体
或水,不符合复分解反应的条件,所以不能发生复分解反应。
答案:(1)产生白色沉淀
(2)CO 2-
3
(3)CuSO +2NaOH====Cu(OH) ↓+Na SO
4 2 2 4
生成物中没有沉淀或气体或水
6.【解析】(1)由质量守恒定律可知,反应过程中产生的二氧化碳质量为69 g+
29.2 g-93.8 g=4.4 g。
(2)设试样中K CO 的质量为x。
2 3
K CO +2HCl====2KCl+H O+CO ↑
2 3 2 2
138 44
x 4.4 g
138 44
x 4.4 g
解得:x=13.8 g
试样中K CO 的质量分数=13.8 g ×100%=20%
2 3
69 g
答案:(1)4.4 (2)20%
【探究创新】
【解析】Na CO 与HCl反应生成NaCl、H O和CO ,当Na CO 过量时,废液中的溶质
2 3 2 2 2 3
还可能是Na CO 和NaCl;在溶液中Na CO 和HCl不能共存,所以猜想(一)废液中
2 3 2 3
10的溶质可能是NaCl、Na CO 和HCl肯定是错误的;溶液中若有HCl,滴加AgNO 溶
2 3 3
液也能产生不溶于稀硝酸的白色沉淀,所以滴入AgNO 溶液,产生白色沉淀,滴加
3
稀硝酸沉淀不溶解,不能证明只有NaCl;大理石的主要成分是CaCO ,能与盐酸
3
反应生成二氧化碳气体;要证明是否含有Na CO 可以滴加氯化钙溶液看是否有
2 3
沉淀生成,也可以滴加稀盐酸看是否有气体生成。
答案:【猜想与假设】Na CO 和NaCl
2 3
【讨论与交流】在溶液中Na CO 和HCl不能共存
2 3
【实验与结论】(1)不能溶液中若有HCl,遇AgNO 溶液也能产生不溶于稀硝酸的
3
白色沉淀
(2)CaCO +2HCl====CaCl +H O+CO ↑
3 2 2 2
(3)②、③
【拓展与应用】蒸发 挥发出的HCl会污染空气
11