文档内容
扬州市江都区2013年九年级化学模拟试卷
2013.04.
(满分:100分 考试时间:100分钟)
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求:
1.本试卷共6页,包含选择题(第1题~第20题,共40分)、非选择题(第21题~第26题,共
60分)两部分。本次考试时间为100分钟,满分100分。考试结束后,请将答题纸交回。
2.答题前,请考生务必将自己的学校、班级、姓名、准考证号用0.5毫米的黑色签字笔写在答题
纸上相应的位置。请在答题纸指定区域作答,在试卷或草稿纸上作答一律无效。
你可能用到的相对原子质量:H:1 C:12 O:16 Na:23 Fe:56
一、选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.下列行为中,不符合“绿V客(Green Week)”环保活动主题的是
A.缩短城市景观灯亮灯时间 B.周末呆在家里上网看电视
C.尽量使用可降解方便袋 D.步行或骑单车上下班
2.下列变化属于物理变化的是
A.玻璃破碎 B.燃气燃烧 C.钢铁锈蚀 D.光合作用
3.下列属于人体必需微量元素的是
A.H B.Zn C.Ca D.O
4.二氧化氯(ClO )是一种新型杀菌消毒剂,其中Cl元素的化合价是
2
A.—1 B.0 C.+4 D.+5
5.草木灰的主要成分是KCO,KCO 属于
2 3 2 3
A.氧化物 B.酸 C.碱 D.盐
6.空气成分中,体积分数最大的是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
7.下列关于用微粒知识解释生活中现象的说法,不正确的是
A.酒香不怕巷子深 —— 微粒在不停运动
B.1滴水中含有1.7×1021个HO分子 —— 微粒是很小的
2
C.等体积的大米和绿豆混合后总体积减小 —— 微粒间有间隙
D.食盐溶液能导电 —— 溶液中存在能自由移动的离子
8.下列物质加入水中能形成溶液的是
1A.粉笔灰 B.植物油 C.蔗糖 D.生铁
9.在化学反应:4HgS + 4CaO = 4Hg + 3CaS + X中,X的化学式为
A. SO B.SO C.CaSO D.CaSO
2 3 3 4
10.下列有关实验现象的描述,正确的是
A.白磷在空气中燃烧产生大量白雾
B.NaOH溶于水时,吸收热量,温度降低
C.细铁丝在氧气中燃烧,火星四射,生成红棕固体
D.电解水正极得到的气体能使带火星的木条复燃
11.用灯帽盖灭酒精灯的原理是
A.隔离可燃物 B.隔绝空气
C.降低酒精的着火点 D.降低温度至酒精的着火点以下
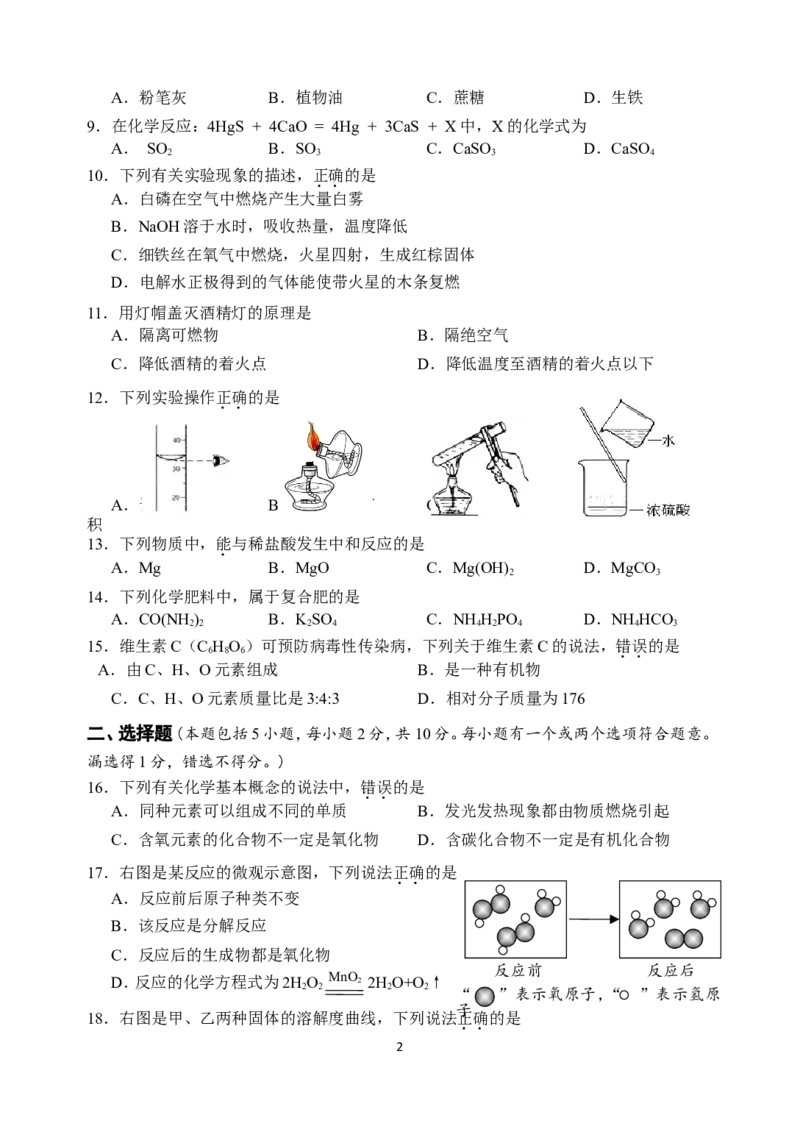
12.下列实验操作正确的是
A.读取液体体 B.点燃酒精灯 C.加热液体 D.稀释浓硫酸
积
13.下列物质中,能与稀盐酸发生中和反应的是
A.Mg B.MgO C.Mg(OH) D.MgCO
2 3
14.下列化学肥料中,属于复合肥的是
A.CO(NH) B.KSO C.NH HPO D.NH HCO
2 2 2 4 4 2 4 4 3
15.维生素C(C HO)可预防病毒性传染病,下列关于维生素C的说法,错误的是
6 8 6
A.由C、H、O元素组成 B.是一种有机物
C.C、H、O元素质量比是3:4:3 D.相对分子质量为176
二、选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。
漏选得1分,错选不得分。)
16.下列有关化学基本概念的说法中,错误的是
A.同种元素可以组成不同的单质 B.发光发热现象都由物质燃烧引起
C.含氧元素的化合物不一定是氧化物 D.含碳化合物不一定是有机化合物
17.右图是某反应的微观示意图,下列说法正确的是
A.反应前后原子种类不变
B.该反应是分解反应
C.反应后的生成物都是氧化物
反应前 反应后
D.反应的化学方程式为2H
2
O
2
M n O 2 2H
2
O+O
2
↑
“ ”表示氧原子,“ ”表示氢原
子
18.右图是甲、乙两种固体的溶解度曲线,下列说法正确的是
2A.甲的溶解度大于乙的溶解度
B.10℃时,等质量的甲乙饱和溶液中溶质质量相等
C.20℃时,将10g甲物质加入50g水中,得到60g溶液
D.30℃时,甲物质饱和溶液中,溶质质量分数最大为60%
19.下列物质的除杂实验中,所选用的试剂、方法及反应类型均正确的是
选项 物质(括号内为杂质) 试剂、方法 反应类型
A. CaO(CaCO) 高温 分解反应
3
B. Fe(Fe O) 足量CO 置换反应
2 3
C. CO(CO) 足量O 化合反应
2 2
D. CaCl 溶液(HCl) 足量CaCO 复分解反应
2 3
20.某钢铁厂用800吨(Fe%=75%)FeO、Fe O、Fe O 的混合铁矿石炼铁,炼得生铁(非铁
2 3 3 4
元素含量<8%)的质量可能是(生铁中C%为2% ~ 4.3%)
A.600吨 B.608吨 C.625吨 D.676.5吨
三、(
本题包括4小题,每空1分,共27分
)
21.(4分)(1)用化学用语填空:
3个氧分子 ▲ ;沼气的主要成分 ▲ ;+5价的P元素 ▲ ;地壳中含量最多
的金属元素 ▲ 。
22.(6分)用字母序号填空:
a.CO b.Ca(OH) c.CaO d.NaHCO e.NaCl f.O
2 2 3 2
常用作食品干燥剂的是 ▲ ;可改良酸性土壤的是 ▲ ;用于运动饮料生产的气体
是 ▲ ;可作调味品的是 ▲ ;用于焙制糕点的是 ▲ ;可供给呼吸的是 ▲ 。
23.(9分)材料在生活中应用很广泛。
(1)下列生活物品属于无机材料的是 ▲ ;
A.玻璃杯 B.铁锅 C.塑料桶 D.玻璃钢转椅
(2)现行流通的硬币材质均为金属材料,如一元硬币是钢芯镀镍(Ni),伍角硬币是钢芯镀
铜,一角硬币是铝合金或不锈钢。
①选择铸造硬币的材料不需要考虑的因素是 ▲ (填序号);
A.金属的导电性 B.金属的耐腐蚀性
C.金属的硬度 D.金属价格与硬币面值的吻合度
②五角硬币镀铜是因为常温下,铜的化学性质 ▲ (填“稳定”或“活泼”);
③钢是一种含碳量为 ▲ (填数值)的铁合金,其硬度比铁 ▲ (填“大”或
“小”);
④在一定条件下,镍在空气中会形成致密的氧化膜(NiO),反应的
化学方程式为 ▲ 。镍和稀硫酸反应会生成硫酸镍(NiSO )和
4
3
镍原子一种可燃性气体单质,反应化学方程式为 ▲ ;
⑤根据右图镍原子的结构示意图回答:镍原子的原子序数是 ▲ ,在化学变化中易
▲ 电子(填“得到”或“失去”)。
24.(8分)关注碳排放。
(1)化石燃料属于 ▲ (填“可再生”或“不可再生”)能源,请你推荐一种新型绿色的
能源 ▲ ;
(2)下列做法不符合“低碳”生活理念的是 ▲ ;
A.使用一次性木筷和纸巾 B.推广电热水器 C.逐步淘汰白炽灯
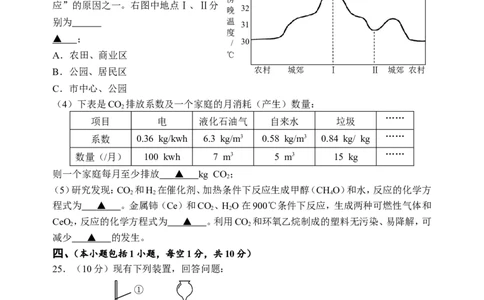
(3)CO 过多排放是城市“热岛效
2 33
傍
应”的原因之一。右图中地点Ⅰ、Ⅱ分
晚 32
别为 温
31
度
▲ ;
/ 30
A.农田、商业区 ℃
B.公园、居民区 农村 城郊 Ⅰ Ⅱ 城郊 农村
C.市中心、公园
(4)下表是CO 排放系数及一个家庭的月消耗(产生)数量:
2
……
项目 电 液化石油气 自来水 垃圾
系数 0.36 kg/kwh 6.3 kg/m3 0.58 kg/m3 0.84 kg/ kg ……
数量(/月) 100 kwh 7 m3 5 m3 15 kg ……
则一个家庭每月至少排放 ▲ kg CO;
2
(5)研究发现:CO 和H 在催化剂、加热条件下反应生成甲醇(CHO)和水,反应的化学方
2 2 4
程式为 ▲ 。金属铈(Ce)和CO、HO在900℃条件下反应,生成两种可燃性气体和
2 2
CeO,反应的化学方程式为 ▲ 。利用CO 和环氧乙烷制成的塑料无污染、易降解,可
2 2
减少 ▲ 的发生。
四、(本小题包括1小题,每空1分,共10分)
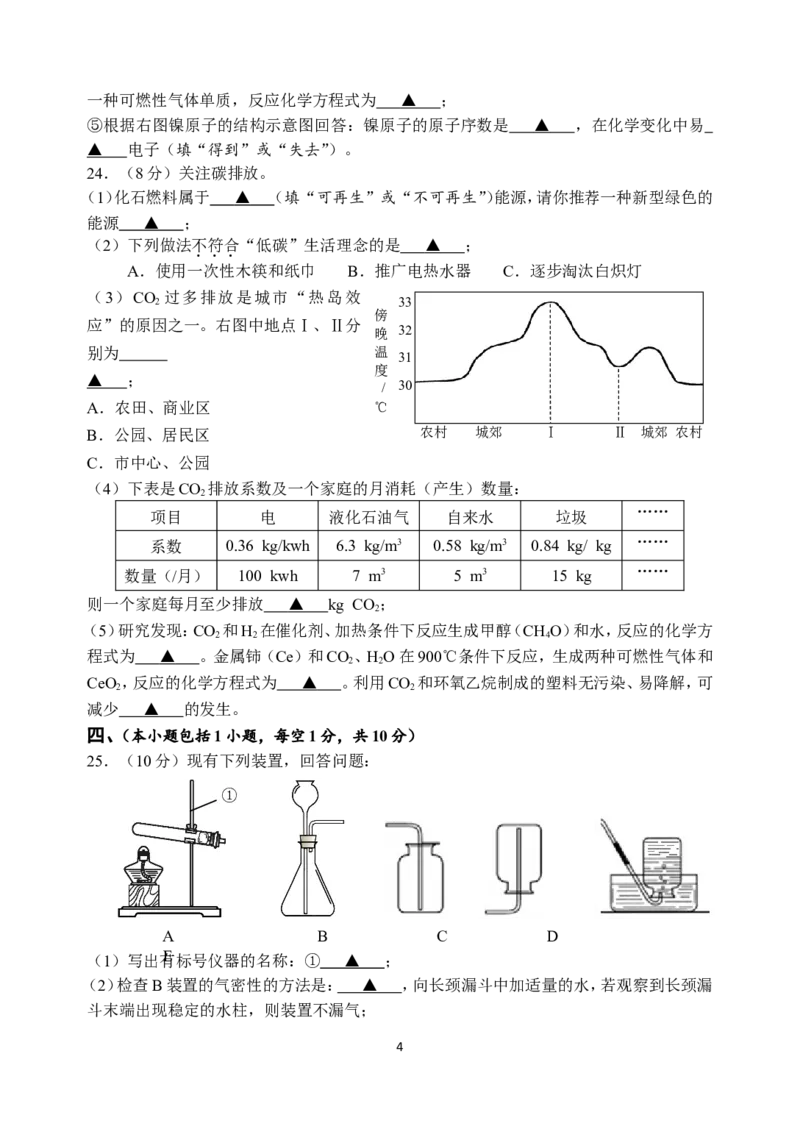
25.(10分)现有下列装置,回答问题:
①
A B C D
(1)写出有E标 号仪器的名称:① ▲ ;
(2)检查B装置的气密性的方法是: ▲ ,向长颈漏斗中加适量的水,若观察到长颈漏
斗末端出现稳定的水柱,则装置不漏气;
4(3)实验室制取H 的反应化学方程式为 ▲ ,发生装置为 ▲ ;
2
(4)实验发现:用40%的硫酸制取H 效果最好。现欲配制30mL 40%(密度为1.30g·mL—1)
2
的硫酸,需要98%(密度为1.84g·mL—1)的浓硫酸 ▲ mL(精确到小数点后一位),需
要水 ▲ mL(精确到小数点后一位)。量取浓硫酸时,若仰视读数(其他操作均正确),
则所配硫酸的质量分数 ▲ 40%(填“>”或“=”或“<”),配制过程不需要的仪
器是 ▲ ;
A.托盘天平 B.量筒 C.烧杯 D.玻璃棒 E.胶头滴管 F.铁架台
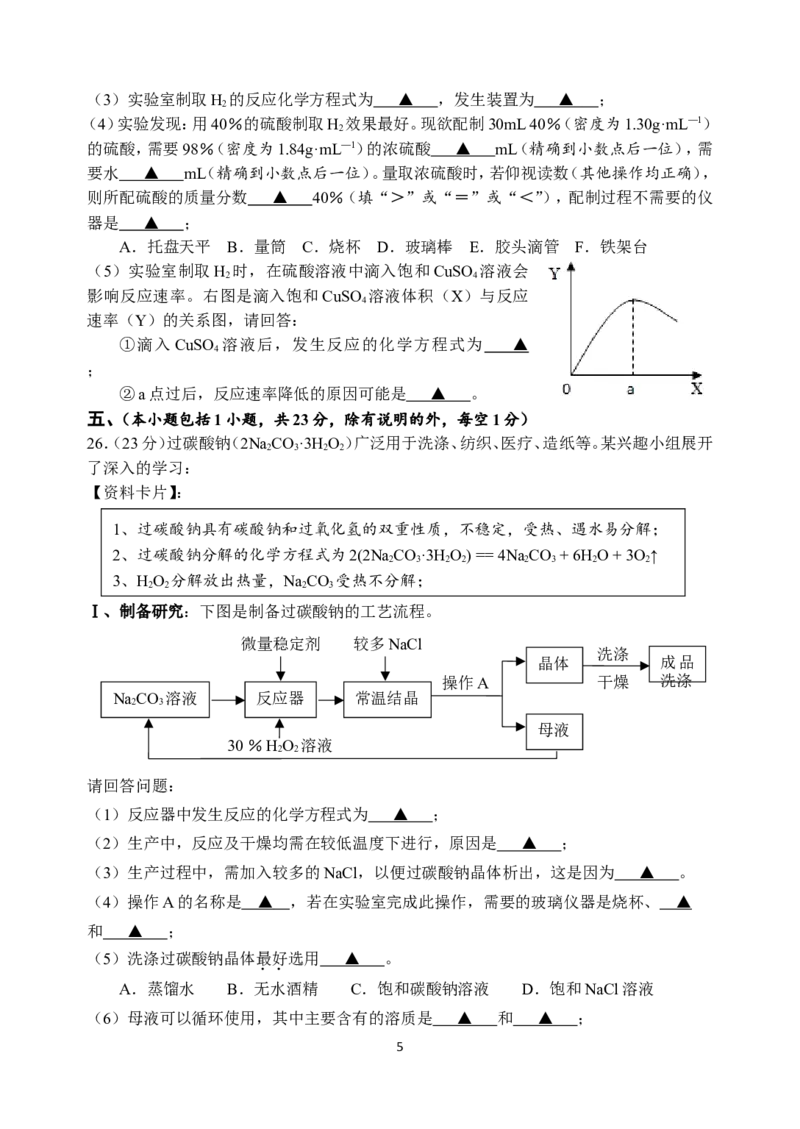
(5)实验室制取H 时,在硫酸溶液中滴入饱和CuSO 溶液会
2 4
影响反应速率。右图是滴入饱和CuSO 溶液体积(X)与反应
4
速率(Y)的关系图,请回答:
①滴入 CuSO 溶液后,发生反应的化学方程式为 ▲
4
;
②a点过后,反应速率降低的原因可能是 ▲ 。
五、(本小题包括1小题,共23分,除有说明的外,每空1分)
26.(23分)过碳酸钠(2NaCO·3H O)广泛用于洗涤、纺织、医疗、造纸等。某兴趣小组展开
2 3 2 2
了深入的学习:
【资料卡片】:
1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解;
2、过碳酸钠分解的化学方程式为2(2NaCO·3H O) == 4NaCO + 6HO + 3O↑
2 3 2 2 2 3 2 2
3、HO 分解放出热量,NaCO 受热不分解;
2 2 2 3
Ⅰ、制备研究:下图是制备过碳酸钠的工艺流程。
微量稳定剂 较多NaCl
洗涤
晶体 成品
操作A 干燥 洗涤
Na CO 溶液 反应器 常温结晶
2 3
母液
30%H O 溶液
2 2
请回答问题:
(1)反应器中发生反应的化学方程式为 ▲ ;
(2)生产中,反应及干燥均需在较低温度下进行,原因是 ▲ ;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 ▲ 。
(4)操作A的名称是 ▲ ,若在实验室完成此操作,需要的玻璃仪器是烧杯、 ▲
和 ▲ ;
(5)洗涤过碳酸钠晶体最好选用 ▲ 。
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是 ▲ 和 ▲ ;
5Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2NaCO·3H O 的质量分数。
2 3 2 2
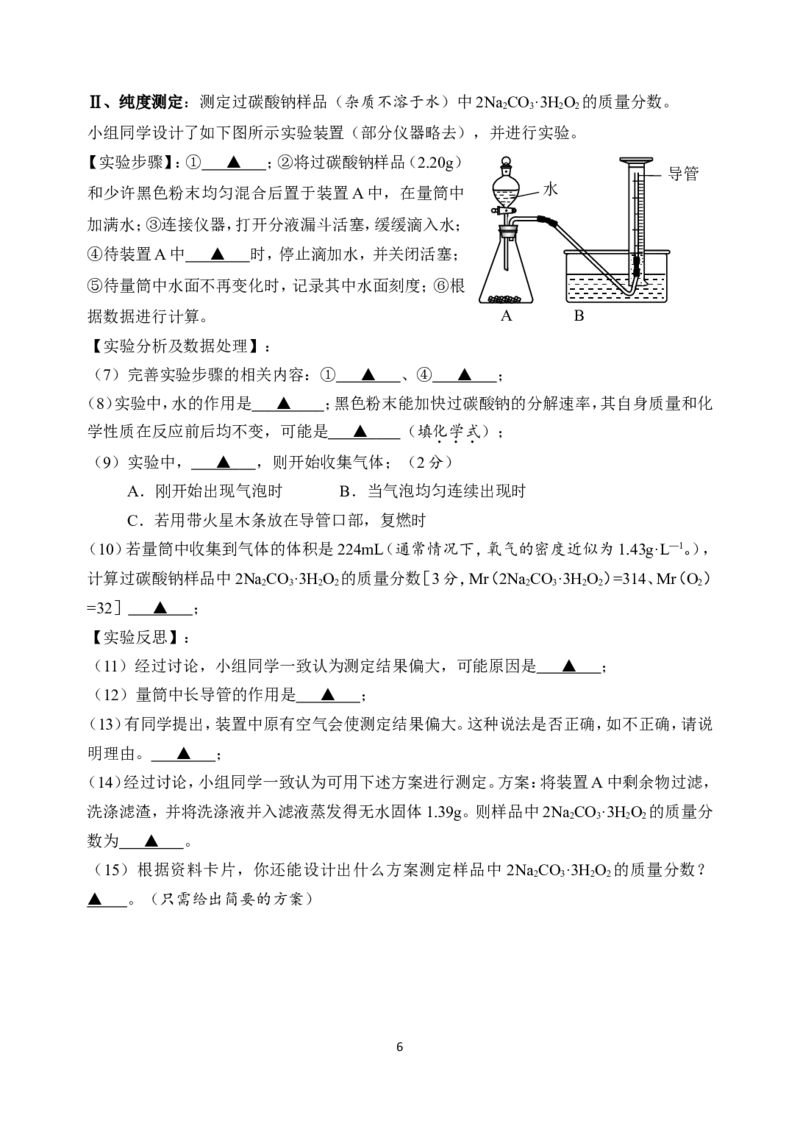
小组同学设计了如下图所示实验装置(部分仪器略去),并进行实验。
【实验步骤】:① ▲ ;②将过碳酸钠样品(2.20g)
导管
和少许黑色粉末均匀混合后置于装置A中,在量筒中 水
加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;
④待装置A中 ▲ 时,停止滴加水,并关闭活塞;
⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根
据数据进行计算。 A B
【实验分析及数据处理】:
(7)完善实验步骤的相关内容:① ▲ 、④ ▲ ;
(8)实验中,水的作用是 ▲ ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化
学性质在反应前后均不变,可能是 ▲ (填化学式);
(9)实验中, ▲ ,则开始收集气体;(2分)
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g·L—1。),
计算过碳酸钠样品中2NaCO·3H O 的质量分数[3分,M(r 2NaCO·3H O)=314、M(r O)
2 3 2 2 2 3 2 2 2
=32] ▲ ;
【实验反思】:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 ▲ ;
(12)量筒中长导管的作用是 ▲ ;
(13)有同学提出,装置中原有空气会使测定结果偏大。这种说法是否正确,如不正确,请说
明理由。 ▲ ;
(14)经过讨论,小组同学一致认为可用下述方案进行测定。方案:将装置A中剩余物过滤,
洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g。则样品中2NaCO·3H O 的质量分
2 3 2 2
数为 ▲ 。
(15)根据资料卡片,你还能设计出什么方案测定样品中 2NaCO·3H O 的质量分数?
2 3 2 2
▲ 。(只需给出简要的方案)
6参考答案及评分标准
【评卷说明】
1、 所有专业术语、化学用语(符号、化学式等)错误均不给分。
2、 化学方程式中反应物或生成物书写错误、未配平不给分。
3、 文字表达只要答到关键词即可得分。
4、 答题中其它合理的说法和解法均可得分。
一 二、选择题(本题包括20小题,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 B A B C D A C C D D
题号 11 12 13 14 15 16 17 18 19 20
答案 B A C C C B AB BC AD C
三、(本题包括4小题,每空1分,共27分)
21.(4分)3O CH + A5l
2 4
P
22.(6分)c b a e d f
23.(9分)(1)AB (共1分,全对得1分) (2)①A ②稳定 ③0.03% ~ 2% 大
④2Ni + O == 2NiO Ni + H SO == NiSO + H ↑ ⑤28 失去
2 2 4 4 2
24.(8分)(1)不可再生 太阳能等 (2)AB (3)C (4)95.6
催化剂
(5)CO + 3H ====== CH O + HO Ce + CO + H O ==9=0=0℃ CeO + CO + H 白色污染
2 2 4 2 2 2 2 2
加热
四、(本题包括1小题,每空1分,共10分)
25.(10分)(1)铁架台 (2)堵住右侧导气管 (3)Zn + H SO == ZnSO + H ↑ (或
2 4 4 2
Zn+2HCl=ZnCl2+ H ↑) B (4)8.7 23.0(或23.1) > AF (共1分,全对得1分)
2
(5)①Zn + CuSO == ZnSO + Cu ②生成的Cu覆盖在Zn表面,阻止反应进一步进行(或
4 4
硫酸浓度变小,使反应速率降低)
五、(本题包括1小题,共23分,除有说明的外,每空1分)
26.(1)2NaCO + 3H O == 2NaCO·3H O (2)防止过碳酸钠分解,影响产量和产率
2 3 2 2 2 3 2 2
(3)过碳酸钠在NaCl溶液中溶解度较小,易析出晶体
(4)过滤 玻璃棒 漏斗 (5)B (6)NaCl NaCO(或HO)
2 3 2 2
7(7)检查气密性 不再产生气体时 (8)溶解过碳酸钠,利于其分解 MnO(或CuO)
2
(9)A(2分)
(10)过碳酸钠分解产生氧气质量为224mL ×10—3×1.43g·L—1 = 0.32g ……………… 1分
2(2Na CO·3H O) ~ 3O ↑
2 3 2 2 2
314×2 32×3
X 0.32g
解得X=2.09g ……………………………………………………………… 1分
2.09g
则样品中,2NaCO·3H O 的质量分数为: 1000 95.00 (或95.2%)… 1分
2 3 2 2 2.20g 0 0
(11)滴入的水占据了锥形瓶内的体积,使得O 体积偏大
2
(12)起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸)
(13)不正确,装置中原有空气和生成的O 等体积代换 (注:理由叙述不正确不给分 )
2
(14)93.6%(或93.5%)
(15)想方法测出过碳酸钠和酸反应生成CO 的体积或质量,进而进行计算(或过碳酸钠
2
和氯化钙、氯化钡等溶液生成沉淀质量进行测定)(其他合理答案也可得分)
8