文档内容
第三课时 不同价态含硫物质的转化
[明确学习目标] 1.了解硫元素在自然界中的存在形态及转化。2.了解硫元
素不同价态间的转化及反应条件的控制。
学生自主学习
1.硫元素在自然界中的存在
(1)游离态:存在于 □ 火山口 附近或 □ 地壳的岩层 中。
(2)化合态
2.不同价态含硫物质的转化
(1)硫元素的常见化合价有 □ - 2 、 0 、+ 4 和+ 6 。
(2)硫元素每种价态对应的物质:
-2价:H S、Na S、CuFeS 、KHS等
2 2 2
0价:S等
+4价:SO 、H SO 、Na SO 等
2 2 3 2 3
+6价:SO 、H SO 、K SO 、CuSO ·5H O等
3 2 4 2 4 4 2
上面的各步转化中,含硫物质表现氧化性的有 □ ②④⑥ ,表现还原性的有
□ ①③⑤ 。
FeS 和CuFeS 中硫元素的化合价相同吗?
2 2
提示:不相同;FeS 中S的化合价是-1价,CuFeS 中S的化合价是-2价。
2 2课堂互动探究
一、不同价态硫元素的转化关系
二、实验室里研究不同价态硫元素间的转化
1.方法导引
2.第一步:确定研究物质
提供药品:
Na S溶液、浓硫酸、酸性KMnO 溶液、Na SO 溶液、氯水、铜片、品红溶
2 4 2 3
液、NaOH溶液
第二步:设计实验并讨论其可行性
对-2、+4、+6价含硫物质的化学性质做出大胆预测,怎样实现它们之间
的转化?小组讨论寻找尽可能多的方案,并对方案的可行性进行判断。
实验方案和记录第三步:实验步骤及现象
S ((((\a\vs4\al(S) ((((S ((((S
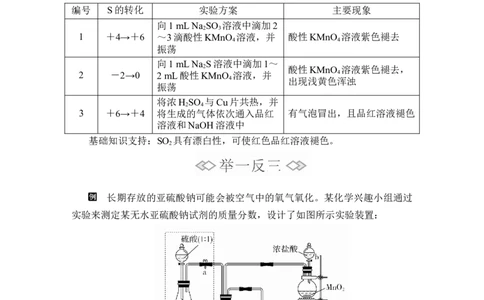
编号 S的转化 实验方案 主要现象
向1 mL Na SO 溶液中滴加2
2 3
1 +4→+6 ~3滴酸性KMnO 溶液,并 酸性KMnO 溶液紫色褪去
4 4
振荡
向1 mL Na S溶液中滴加1~
2 酸性KMnO 溶液紫色褪去,
2 -2→0 2 mL酸性KMnO 溶液,并 4
4 出现浅黄色浑浊
振荡
将浓H SO 与Cu片共热,并
2 4
3 +6→+4 将生成的气体依次通入品红 有气泡冒出,且品红溶液褪色
溶液和NaOH溶液中
基础知识支持:SO 具有漂白性,可使红色品红溶液褪色。
2
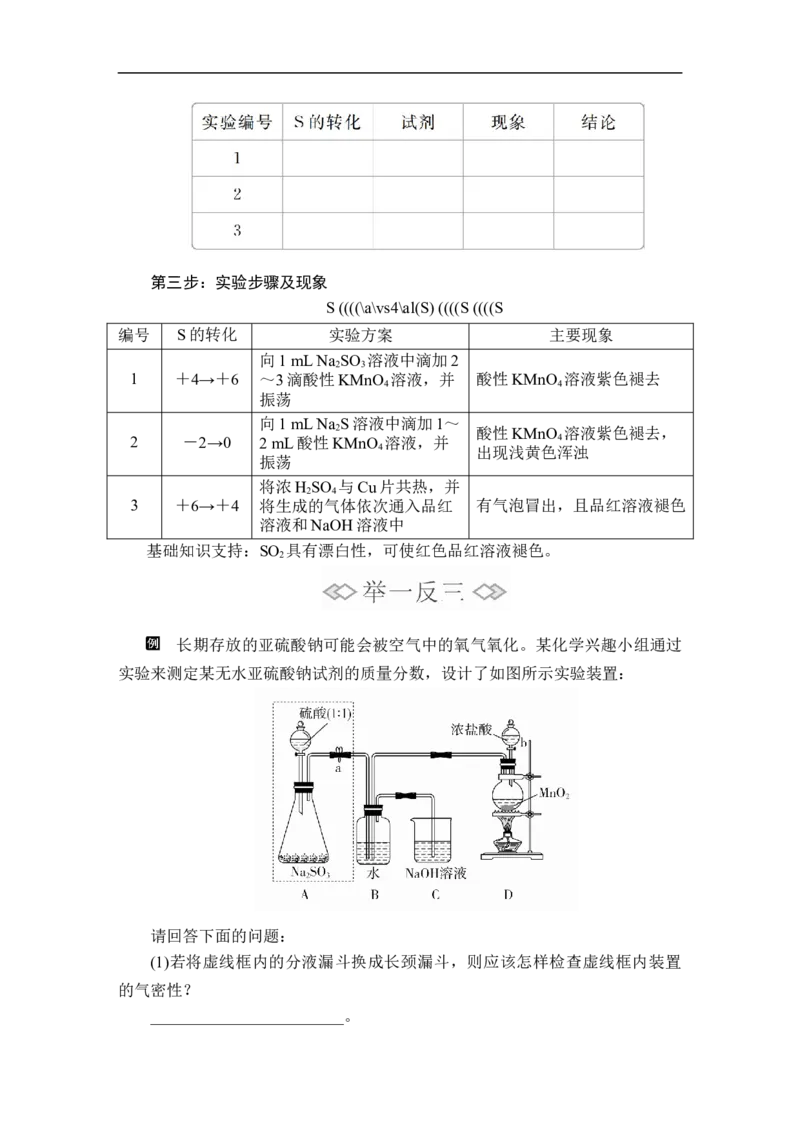
长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过
实验来测定某无水亚硫酸钠试剂的质量分数,设计了如图所示实验装置:
请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置
的气密性?
________________________。(2)D装置中反应的化学方程式为_____________________。
B装置中反应的离子方程式为_________________________。
(3)称量a g Na SO 样品放入锥形瓶中,向B装置反应后的溶液中加入足量的
2 3
BaCl 溶液充分反应,过滤、洗涤、干燥,得白色沉淀b g,原样品中Na SO 的
2 2 3
质量分数为__________________。
(4)C装置的作用为__________________。
[批注点拨][答案] (1)关闭弹簧夹(或止水夹)a,由长颈漏斗向锥形瓶内加水至漏斗内液
面高于锥形瓶内液面,过一段时间观察液面是否变化,若不变,说明气密性良好,
否则,说明装置漏气
(2)MnO +4HCl(浓)=====MnCl +Cl ↑+2H O
2 2 2 2
Cl +SO +2H O===4H++2Cl-+SO
2 2 2
(3)×100%
(4)吸收尾气,防止污染空气
[练1] 现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl 溶液、Ba(NO ) 溶
2 3 2液,请从中选择合适试剂,设计一种实验方法测定部分变质的无水亚硫酸钠的质
量分数:_______________________。
答案 称取一定质量的样品置于烧杯中,加水溶解,依次加入足量盐酸和
BaCl 溶液充分反应,过滤,洗涤,干燥,称量沉淀物的质量,计算出被氧化的
2
Na SO 的质量,即可求出部分变质的无水亚硫酸钠的质量分数(其他合理答案也
2 3
可)
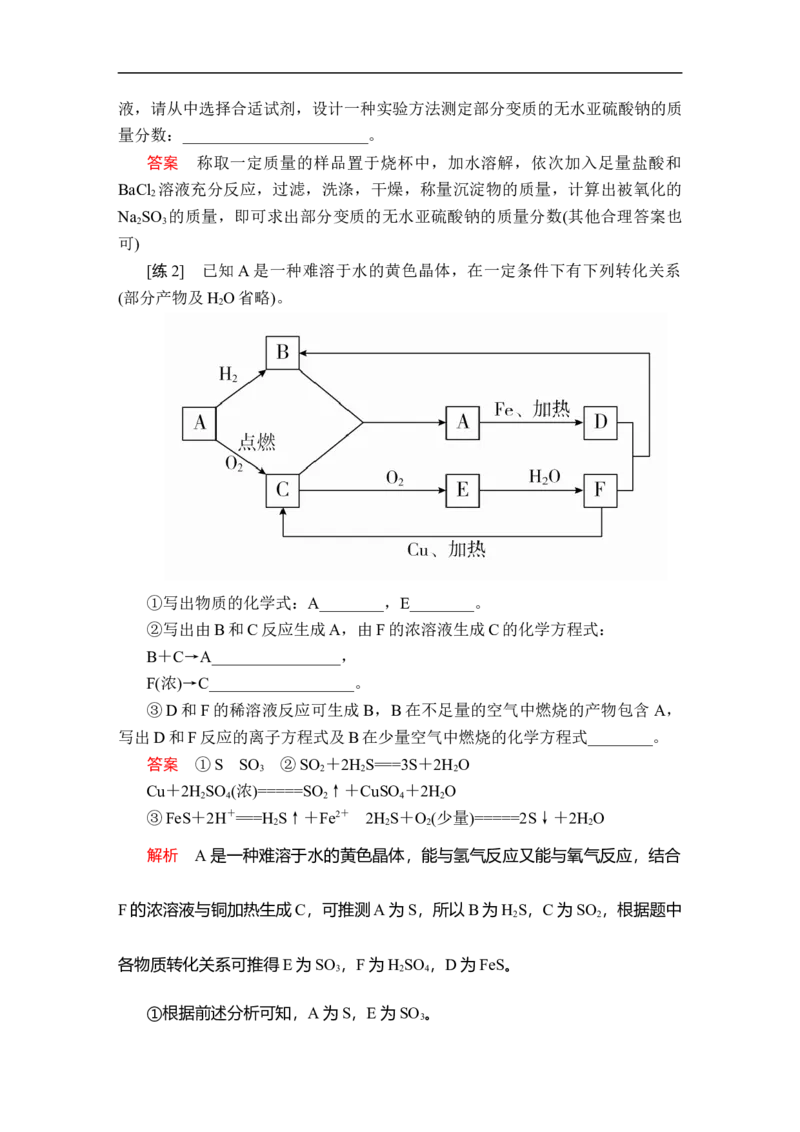
[练2] 已知A是一种难溶于水的黄色晶体,在一定条件下有下列转化关系
(部分产物及H O省略)。
2
①写出物质的化学式:A________,E________。
②写出由B和C反应生成A,由F的浓溶液生成C的化学方程式:
B+C→A________________,
F(浓)→C__________________。
③D和F的稀溶液反应可生成B,B在不足量的空气中燃烧的产物包含 A,
写出D和F反应的离子方程式及B在少量空气中燃烧的化学方程式________。
答案 ①S SO ②SO +2H S===3S+2H O
3 2 2 2
Cu+2H SO (浓)=====SO ↑+CuSO +2H O
2 4 2 4 2
③FeS+2H+===H S↑+Fe2+ 2H S+O (少量)=====2S↓+2H O
2 2 2 2
解析 A是一种难溶于水的黄色晶体,能与氢气反应又能与氧气反应,结合
F的浓溶液与铜加热生成C,可推测A为S,所以B为H S,C为SO ,根据题中
2 2
各物质转化关系可推得E为SO ,F为H SO ,D为FeS。
3 2 4
①根据前述分析可知,A为S,E为SO 。
3②B+C→A的化学方程式为 SO +2H S===3S+2H O,F(浓)→C的化学方
2 2 2
程式为Cu+2H SO (浓)=====SO ↑+CuSO +2H O。
2 4 2 4 2
③D和F的稀溶液反应可生成 B的离子方程式:FeS+2H+===H S↑+Fe2
2
+,B在少量空气中燃烧的化学方程式:2H S+O (少量)=====2S↓+2H O。
2 2 2
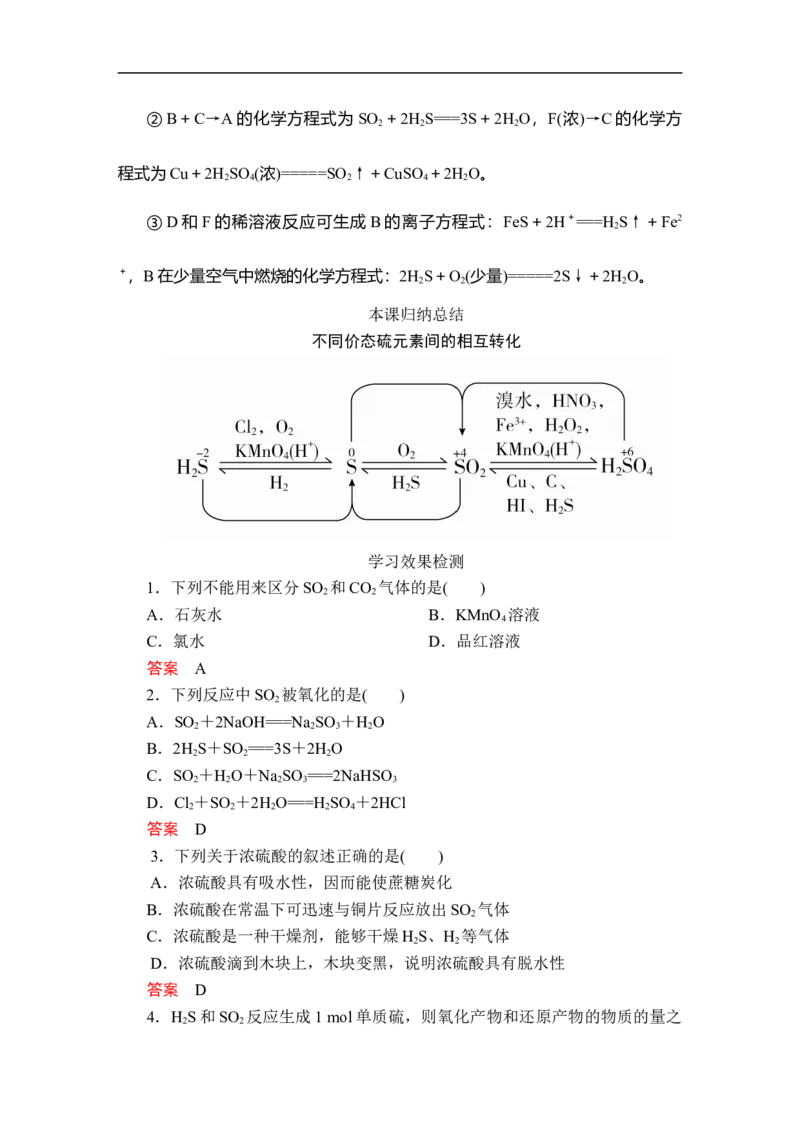
本课归纳总结
不同价态硫元素间的相互转化
学习效果检测
1.下列不能用来区分SO 和CO 气体的是( )
2 2
A.石灰水 B.KMnO 溶液
4
C.氯水 D.品红溶液
答案 A
2.下列反应中SO 被氧化的是( )
2
A.SO +2NaOH===Na SO +H O
2 2 3 2
B.2H S+SO ===3S+2H O
2 2 2
C.SO +H O+Na SO ===2NaHSO
2 2 2 3 3
D.Cl +SO +2H O===H SO +2HCl
2 2 2 2 4
答案 D
3.下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出SO 气体
2
C.浓硫酸是一种干燥剂,能够干燥H S、H 等气体
2 2
D.浓硫酸滴到木块上,木块变黑,说明浓硫酸具有脱水性
答案 D
4.H S和SO 反应生成1 mol单质硫,则氧化产物和还原产物的物质的量之
2 2比为( )
A.1∶2 B.2∶1 C.1∶1 D.1∶3
答案 B
5.Cl 和SO 都有漂白作用,能使品红溶液褪色,若将等物质的量的 Cl 和
2 2 2
SO 混合后再通入品红与BaCl 的混合溶液中,能观察到的现象是( )
2 2
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③ C.②③ D.②④
答案 C
解析 Cl +SO +2H O===H SO +2HCl,Cl 和SO 按1∶1发生上述反应后
2 2 2 2 4 2 2
生成物不具有漂白性,且因H SO +BaCl ===BaSO ↓+2HCl,而在溶液中生成
2 4 2 4
沉淀,故答案为C。
6.分别向盛有①紫色石蕊溶液 ② NaOH 溶液 ③品红溶液 ④酸性
KMnO 溶液的试管中通入SO 气体
4 2
(1)试管①中现象____________。发生反应的化学方程式为___________。
(2)试管②中发生反应的化学方程式为_______________。
(3)试管③中现象:_____________,如果将吸收SO 后的溶液加热,现象:
2
____________________。
(4)上述实验中,SO 表现出酸性氧化物性质的是________(填标号,下同),
2
SO 表现出漂白性的是________,SO 表现出还原性的是__________。
2 2
答案 (1)溶液变为红色 SO +H OH SO
2 2 2 3
(2)SO +2NaOH===Na SO +H O
2 2 3 2
(3)溶液变为无色 无色溶液变为红色
(4)①② ③ ④