文档内容
2014 年中考模拟考试化学试卷
注意事项:本试卷共6页,考试时间:100分钟;试卷满分:100分.
选用的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cu-64 Ca-40
一、选择题(本题包括15小题,每小题2分,共30分.每小题只有1个选项符合题意)
1.下列变化中,属于物理变化的是
A.火箭发射 B.煤的燃烧 C.风力发电 D.酸雨侵蚀
2.下列物质中,属于纯净物的是
A.蒸馏水 B.洁净的空气 C.鲜橙汁 D.澄清石灰水
3. 下列日常生活用品,用有机合成材料制作的是
A.瓷花瓶 B.食品保鲜膜 C.剔骨刀 D.玻璃钢餐桌
4.下列物质,其名称、俗名、化学式一致的是
A.铁、生铁、Fe B.碳酸钠、纯碱、Na CO
2 3
C.冰、干冰、CO D.氢氧化钙、石灰石、Ca(OH)
2 2
5.下列实验操作错误的是
A.测溶液的pH B.取用粉末状固体 C.闻气体气味 D.点燃酒精灯
6.水是生命之源,也是重要的溶剂,下列说法正确的是
A. 常温下将1gCaO投入到99g水中,溶质的质量分数1%
B. 天然河水经沉降、过滤操作后,可作人们的生活饮用水
C. 将NaCl、蔗糖溶于水后,溶质均以分子形式存在
D. 溶质在溶解于水的过程中,有的放出热量,有的吸收热量
7.下列对有关主题知识的归纳不正确的一组是
A. 物质鉴别 B. 元素与人体健康
蚕丝布料和化纤布料:点燃、闻气味 蛋白质摄入过少:使人生长发育迟缓等
葡萄糖和淀粉:碘酒、观察颜色变化 适量补充钙元素:预防骨质疏松
C.安全常识 D.资源与环境
海鲜防腐:甲醛溶液浸泡 减轻水污染:合理使用农药与化肥
被困于火灾区:蹲下或匍匐前行逃生 回收废旧金属:节约资源、减少环境污染
8.下图为某反应的微观示意图,不同的球代表不同元素的原子,下列说法正确的是
1A.该反应属于置换反应 B.1个X分子中有3个原子
C.反应物分子的个数比为1:1 D.反应前后元素的化合价不改变
9.下列说法错误的是
A.人体为了补钙,可以长期饮用含钙较多的硬水
B.用水能区分NH NO 和NaOH固体
4 3
C.用灼烧的方法能区别棉花和羊毛
D.用饱和硫酸铵溶液能区分淀粉和蛋白质溶液
10.下列实验数据或现象合理的是
①用托盘天平称取15.6g氧化铜粉末; ②用广泛pH试纸测得某溶液的pH为3.52;
③铁丝在空气中燃烧,火星四射; ④用10mL量筒量取某溶液6.6mL;
A.①②③④ B.②③④ C.③④ D.①④
11.下列化学方程式符合题意且书写正确的是
点燃
A.用点燃的方法除去二氧化碳中少量的一氧化碳: 2CO+O2 2CO2
B.证明铜的活动性比银强:Fe+2 AgCl FeCl2+2 Ag
C.医疗上用氢氧化铝中和过多胃酸:2 Al(OH)
3
+ 3 H2SO4 Al
2
(SO
4
)
3
+ 6 H2O
D.用一氧化碳还原氧化铁:Fe2O3+3CO 高 温 2Fe+3CO2
12.60℃时,分别向盛有10g水的A、B两支试管中,加入等质量的甲、乙两种固体物质,使其充
分溶解,可观察到如右图1所示的现象.下列说法错误的是
A.60℃时,B试管中的溶液可能是饱和溶液
B.图2中可表示甲物质的溶解度曲线的是a
C.A中剩余的固体继续溶解可采用加水或加热的方法
D.测得a曲线表示的物质溶液的质量分数为37.5%,
则在40℃时该溶液一定饱和
13.为贮存运输的方便,工业上将H O 转化为固态的过碳酸钠晶体,该晶体具有Na CO 和
2 2 2 3
H2O2 的双重性质(化学式2 Na
2
CO
3.
3 H
2
O
2
),下列物质不会使晶体较快失效的是
A.二氧化锰 B.硫酸钠 C.稀硫酸 D.澄清石灰水
14.下列各组转化中,一定条件下均能一步实现的组合是
CuO CaCO 3 Na 2 CO 3
Cu(OH) Cu CaO Ca(OH) Na SO NaOH
2 2 2 4
① ② ③
2A.①② B.①③ C.②③ D.①②③
15.某甲醛(HCHO)的水溶液中,氢元素的质量分数为10%,则该溶液中甲醛的质量分数为
A.10% B.12% C.30% D. 25%
二、选择题(本题包括5小题,每小题2分,共10分.每小题有1—2个选项符合题意按题意选
对给2分;错选、多选不给分;少选且选对给1分)
16.从反应原理和产物纯度两个角度考虑,下列制取Fe (SO ) 溶液的方案中最佳的是
2 4 3
A.过量的Fe O 与稀硫酸反应,过滤 B.过量的稀硫酸与Fe O 反应,过滤
2 3 2 3
C.过量的铁粉与稀硫酸反应,过滤 D.过量的铁粉与硫酸铜溶液反应,过滤
17.除去下列各组物质中的杂质,所用试剂和方法均正确的是
物质 杂质 除杂所用试剂和方法
A O HCl气体 先通过NaOH溶液,再通过浓硫酸
2
B NaOH溶液 Ca(OH) 溶液 先加入过量NaCO 的溶液,再过滤
2 2 3
C NaCl NaCO 加入澄清的石灰水,过滤
2 3
D CaO CaCO 加入适量的稀盐酸,蒸发
3
18.不用其他试剂,通过观察及组内相互反应的方法,就能将它们一一鉴别出来的是
A.NaCl、BaCl 、CuSO 、NaOH、KNO B.Ba(NO ) 、NaCl、Na SO 、H SO 、HCl
2 4 3 3 2 2 4 2 4
C.NaOH、FeCl 、MgSO 、BaCl 、KCl D.AgNO 、HCl、Na CO 、KCl、CaCl
3 4 2 3 2 3 2
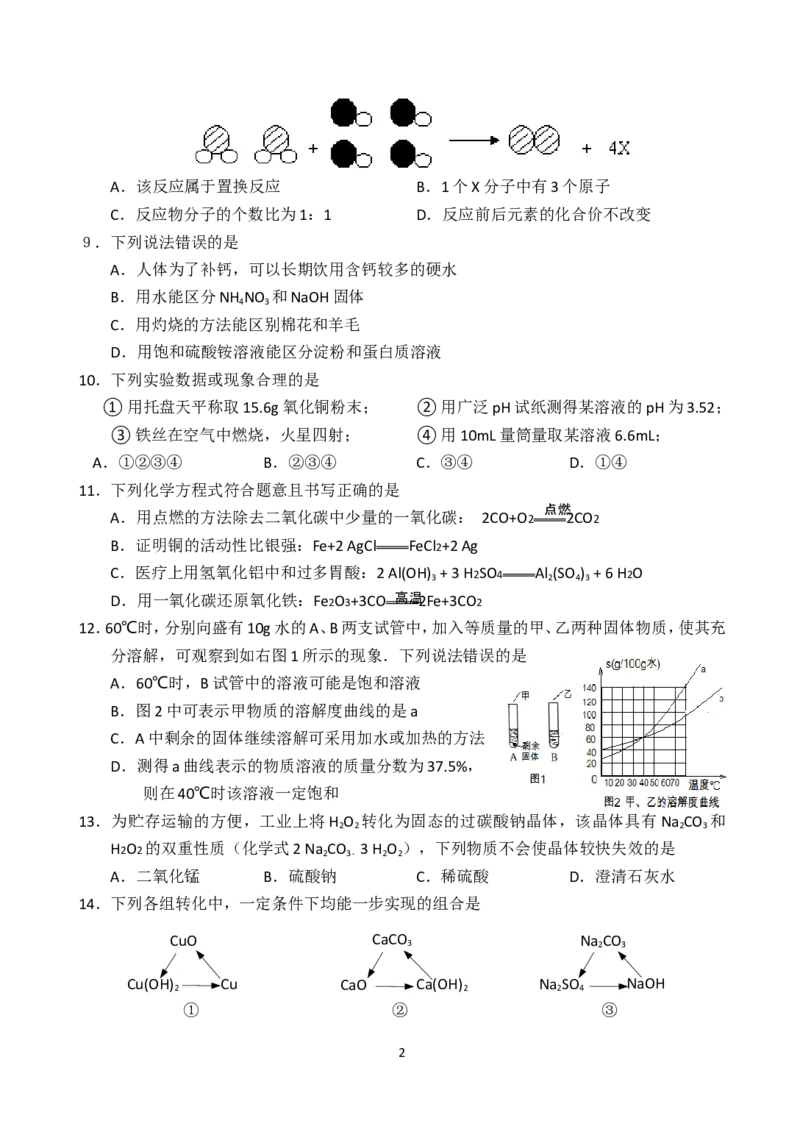
19.探究中和反应是否发生的方法有多种.小华同学进行了以下四个实验,并用图像分别
描述了实验过程中的现象.其中,依据图示现象不能判断中和反应一定发生的是
A.在稀盐酸中加入氯化铜,然后向其中逐滴加入NaOH溶液
B.在NaOH溶液中加入CaCO ,然后向其中逐滴加入稀盐酸
3
C.在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
D.在NaOH溶液中加入Ba(NO ) ,然后向其中逐滴加入稀硫酸
3 2
20.二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋
“捕捉”空气中的CO2 (如下图).则关于该方法的叙述正确的是
A.该方法中包含复分解反应、分解反应、置换反应 等
3B.物质①是NaOH溶液
C.操作①是蒸发浓缩、降温结晶
D.该方法可制得纯净的CO
2
第II卷(非选择题 共60分)
三、填空题(本题包括5小题,共17分)
21.(4分)用化学用语填空:
⑴3个铁离子 ▲ ; ⑵人体缺乏 ▲ 元素严重时会得侏儒症;
⑶4个甲烷分子 ▲ ; ⑷氢氧化镁中镁元素的化合价 ▲ .
22.(6分)用序号填空: A稀盐酸、B小苏打、C钛合金、D蔗糖、E过磷酸钙、F氯化钠
(1) 用于做糕点发酵粉的是 ▲ ; (2)在医疗上配制“生理盐水”的是 ▲ ;
(3) 用于金属表面除锈的是 ▲ ; (4) 用于制造人造骨的是 ▲ ;
(5) 常用作磷肥的是 ▲ ; (6)白糖、冰糖的主要成分 ▲ .
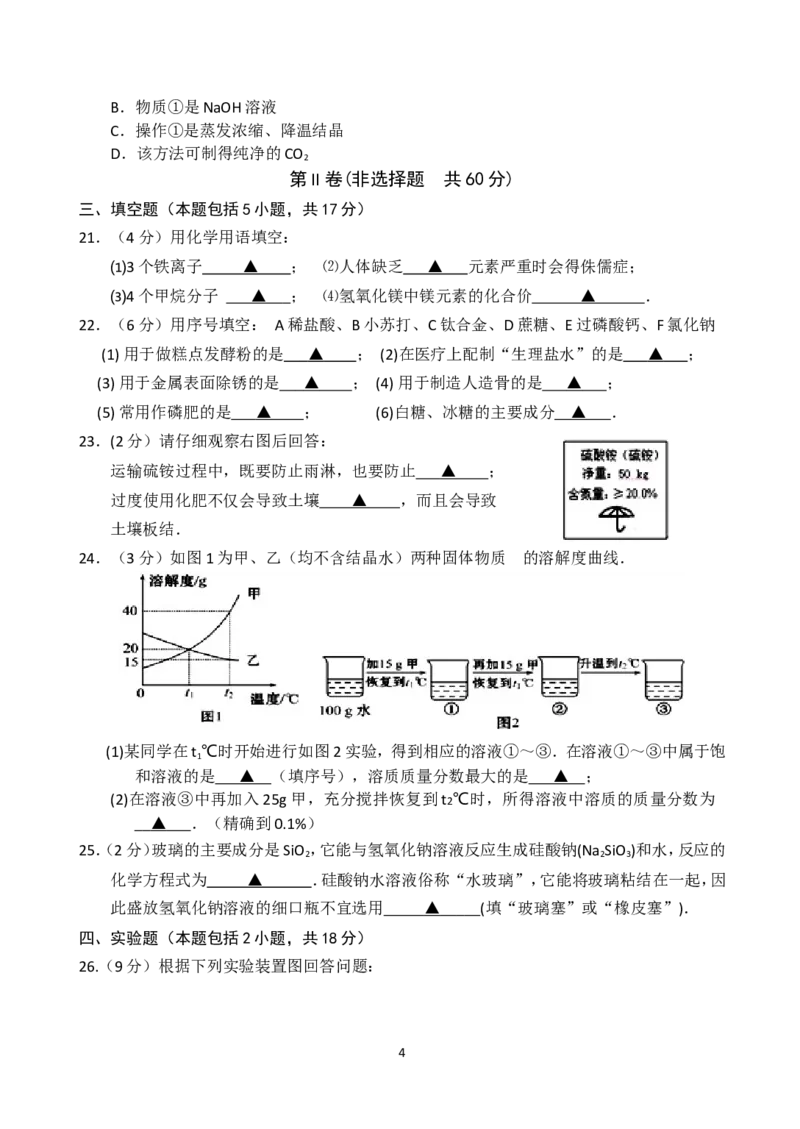
23.(2分)请仔细观察右图后回答:
运输硫铵过程中,既要防止雨淋,也要防止 ▲ ;
过度使用化肥不仅会导致土壤 ▲ ,而且会导致
土壤板结.
24.(3分)如图1为甲、乙(均不含结晶水)两种固体物质 的溶解度曲线.
(1)某同学在t ℃时开始进行如图2实验,得到相应的溶液①~③.在溶液①~③中属于饱
1
和溶液的是 ▲ (填序号),溶质质量分数最大的是 ▲ ;
(2)在溶液③中再加入25g甲,充分搅拌恢复到t2℃时,所得溶液中溶质的质量分数为
▲ .(精确到0.1%)
25.(2分)玻璃的主要成分是SiO ,它能与氢氧化钠溶液反应生成硅酸钠(Na SiO )和水,反应的
2 2 3
化学方程式为 ▲ .硅酸钠水溶液俗称“水玻璃”,它能将玻璃粘结在一起,因
此盛放氢氧化钠溶液的细口瓶不宜选用 ▲ (填“玻璃塞”或“橡皮塞”).
四、实验题(本题包括2小题,共18分)
26.(9分)根据下列实验装置图回答问题:
4(1)写出图中①②的仪器名称:① ▲ ,② ▲ .
(2)用A装置制取氧气,反应的化学方程式 ▲ ,开始的气泡不宜收集,
当 ▲ 时才收集.
(3)装置B和C可用于制取多种气体,若导管口a连接b,可用来制取 ▲ 气体,反应的
化学方程式为 ▲ ;若导管口a连接c,可用来制取 ▲ 气体.
(4)检查B装置气密性的方法:打开旋塞,从长颈漏斗管口注水至 ▲ ,关闭旋塞继续注
水,使长颈漏斗内的液面高于锥形瓶内的液面,静置后 ▲ ,说明气密性良好.
27.( 9分)某化学兴趣小组的同学学习“灭火器原理”后,设计了如图甲所示实验,并对反应
后瓶中残留废液进行探究.
【提出问题】废液中所含溶质是什么?
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na CO 和HCl.猜想2:废液中的溶质只有NaCl.
2 3
猜想3:废液中的溶质是NaCl和HCl.猜想4:废液中的溶质是 ▲ .
【讨论与交流】小明认为猜想1无需验证就知道是错误的,他的理由是 ▲ .
【实验与结论】
(1)小亮同学为验证猜想2,取少量废液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不
变色,于是小亮认为猜想2正确.你认为他的结论 ▲ (填“正确”或“错
误”),理由是 ▲ .
(2)小美为验证猜想3,用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=4,
她认为猜想3正确.对她的操作方法、测量结果及结论的评价,正确的是 ▲ .
A.方法不正确,结果偏小,结论正确 B.方法不正确,结果偏大,结论正确
C.方法正确,结果偏大,结论正确 D.方法正确,结果偏小,结论不正确
【拓展与应用】
(1)若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行
5▲ 操作即可从废液中得到NaCl固体.此方法的缺点是 ▲ .
(2)向一定质量CaCl 和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na CO 溶液.
2 2 3
反应过程中加入的Na CO 溶液的质量与产生沉淀或气体的质量关系如图乙,回答下
2 3
列问题:①c点对应的溶液中溶质为 ▲ ;②x值为 ▲ g.
五、推断题(本题包括2小题,共12分)
28.(6分)在一次自主探究实验中,教师为同学们提供下列药品:CuSO 溶液、Na CO 溶液、
4 2 3
Ba(NO ) 溶液、NaOH溶液、稀盐酸.A、B、C三组同学任选药品相互混合进行探究.探究时
3 2
发现:CuSO 溶液与Na CO 溶液混合时产生的沉淀不是白色的.实验后在集中清理废液时
4 2 3
发现:
(1)A组废液中有蓝色沉淀;B组废液中无沉淀;C组废液中有白色沉淀.
(2)先将A组废液倒入废液桶中,然后依次倒入B、C组废液.倒入B组废液时,沉淀全部溶
解;再倒入C组废液,观察到有气泡产生.测得混合溶液pH<7.由此可以推断:
A组同学在实验中一定使用的一种药品是 ▲ ,一定未使用的一种药品是 ▲ .
B组同学在实验中一定使用了的一种药品是 ▲ .
C组同学实验使用的药品中一定含有 ▲ 、 ▲ .
三组废液混合后,废液中含有的沉淀是 ▲ .
29(. 6分)右图为某些物质间转化关系(部分反应条件省略).其中A为黑色固体氧化物,E为绿
色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y为常见无色气
体;X是常见的红色金属.请回答下列问题:
(1)X的化学式是 ▲ ;
(2)反应①中A的作用 ▲ ;
(3)在自然界中普遍存在反应⑤,其名称为 ▲ ;
(4)在生活中为防止反应②的发生,可采取的措施是 ▲ (写一点即可);
(5)反应①、③的化学方程式是:① ▲ ;③ ▲ .
六、综合题(本小题1题,共13分)
30.叠氮化钠(NaN )被广泛应用于汽车安全气囊,某化学小组同学对其进行研究.
3
【资料在线】①NaN 受撞击会生成Na、N .
3 2
6②NaN 遇盐酸、H SO 溶液无气体生成.
3 2 4
③碱石灰是CaO和 NaOH的混合物.④NaN 与可溶性的钙盐、钡盐不反应.
3
【问题探究】
(1)NaN 的制备方法是:将金属钠与液态氨反应制得NaNH ,再将NaNH 与N O反应可生
3 2 2 2
成NaN 、NaOH和气体X,该反应的化学方程式为2NaNH +N O = NaN +NaOH+X;则
3 2 2 3
X的化学式为 ▲ ,实验室检验X气体的方法是 ▲ .
(2)工业级NaN 中常含有少量的Na CO ,其原因是(用化学方程式表示) ▲ .
3 2 3
【Na CO 纯度测定】
2 3
(3)为测定某工业级NaN 样品中含有Na CO 的质量分数,化学小组同学设计了如下实验.
3 2 3
①小明同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定
Na CO 的纯度,小组内同学通过讨论认为不可以,其理由可能是 ▲ .
2 3
②小刚同学在大家讨论的基础上,设计了装置II.请分析:装置II中A的作用是 ▲ ;
若无装置C,对测定结果造成的影响是 ▲ (填“偏大”、“偏小”或“无影响”)
装置E的作用是 ▲ .
③小静同学认为取少量NaN 样品溶于水,滴加过量的Ba(NO ) 溶液也可以测定Na CO 的
3 3 2 2 3
质量分数,则如何判断滴加的试剂已过量 ▲ .
【NaN 纯度测定】
3
精确称量0.140 g NaN 样品,设计如下右图装置测定其纯度.
3
已知2 NaN → 3N2(NaN 中的N全部转化为N ,其他产物略),反应中放出大量的热.
3 3 2
(4)使小试管中的NaN3样品与M溶液接触的操作是: ▲ .
(5)使用冷水冷凝的目的是: ▲ .
反应前应将液面调节到量气管的“0”刻度,并使两边液面相
平,反应后读数时,还需要进行的操作是 ▲ .
(6)常温下测得量气管读数为67.2 mL(N 的密度为1.25 g/L),
2
则实验中选用的量气管规格合适的是 ▲ (填字母序号).
A. 100 mL B. 1 L C. 2 L
(7)计算NaN 样品的纯度 ▲ .(精确到0.1%)
3
72014 年中考模拟考试化学试卷答题纸
题 号 一 二 三 四 五 六 总 分
得 分
一、二、选择题(1-15 题只有一个选项符合题意、16-
20 有 1—2 个正确选项)
题号 1 2 3 4 5 6 7 8 9 10
答案
题号 11 12 13 14 15 16 17 18 19 20
答案
三、填空题(本题包括5小题,共17分)
21.(4分)用化学用语表示:
(1) ;(2) ;(3) ;(4) .
22.(6分)用序号填空::
(1) ;(2) ;(3) ;(4) ;(5) ;(6) .
23.(2分)
既要防止雨淋,也要防止 ;过度使用化肥不仅会导致土壤 .
24.(3分)
(1)在溶液①~③中属于饱和溶液的是 (填序号)、溶质质量分数最大的是 ;
(2)充分搅拌恢复到t2℃时,所得溶液中溶质的质量分数为 .
25.(2分)该反应的化学方程式为: ,
不宜选用 (填“玻璃塞”或“橡皮塞”).
四、实验题(本题包括2小题,共18分)
26.(9分)
(1)仪器名称:① ,② .
(2)用A制取氧气的化学方程式 ,
当 时才收集.
8(3)若a连接b,可用来制取 气体,化学方程式为 ;
若a连接c,可用来制取 气体.
(4)从长颈漏斗管口注水至 ,
静置后 ,说明气密性良好.
27.(9分)
【猜想与假设】猜想4:废液中的溶质是 .
【讨论与交流】他的理由是 ;
【实验与结论】
(1)小亮认为猜想2正确.你认为他的结论 (填“正确”或“错误”),
理由是 .
(2)对她的操作方法、测量结果及结论的评价,正确的是 .
【拓展与应用】
只要对废液进行 操作即可从废液中得到NaCl固体.此方法的缺点是 .
(4)①c点对应的溶液中溶质为 ;②x值为 g.
五、推断题(本题包括2小题,共12分)
28.(6分)
A组同学一定使用的一种药品是 ,一定未使用的一种药品是 .
B组同学在实验中一定使用了的一种药品是 .
C组同学实验使用的药品中一定含有 、 .
三组废液混合后,废液中含有的沉淀是 .
29.(6分)
(1)X的化学式是 ;
(2)反应①中A的作用 ;
(3)在自然界中普遍存在反应⑤,其名称为 ;
(4)在生活中为防止反应②的发生,可采取的措施是 (写一点即可);
(5)反应①、③的化学方程式是:
① ;③ .
六、综合题(本题1小题,共13分)
30.(1)则X的化学式为 ,实验室检验X气体的方法是 .
(2)其原因是(用化学方程式表示) .
(3)①其理由可能是 .
②装置II中A的作用是 .
若无装置C的影响是 ;装置E的作用是 .
③则如何判断滴加的试剂已过量 .
(4)使小试管中的NaN 样品与M溶液接触的操作是 .
3
9(5)使用冷水冷凝的目的是: .
还需要进行的操作是 .
(6)则实验中选用的量气管规格合适的是 .
(7)计算NaN 样品的纯度 .
3
102014 年中考模拟考试化学试卷参考答案
一、二、选择题(1-15 题只有一个选项符合题意、16-
20 有 1~2 个正确选项)
题号 1 2 3 4 5 6 7 8 9 10
答案 C A B B D D C B A D
题号 11 12 13 14 15 16 17 18 19 20
答案 D B B C D A A CD D BD
三、填空题(本题包括5小题,共17分,每空1分)
+2
21.(4分)3Fe3+ Zn 4CH Mg(OH)
4 2
22.(6分)(1) B (2)F (3) A (4) C (5) E (6) D
23.(2分)高温 或 曝晒 (合理即可) 土壤酸化
24.( 3分)(1)② ③ (2)28.6%
25.(2分)2NaOH+SiO =Na SiO +H O 玻璃塞
2 2 3 2
四、实验题(本题包括2小题,共18分每空1分,)
△
26.(9分)(1)试管 集气瓶(2)2KMnO ===K MnO +MnO +O ↑ 当气泡连续均匀
4 2 4 2 2
(3) O
2
(或CO
2
)、 2H
2
O
2
== 催 == 化 2 剂 H
2
O+O
2
↑(或CaCO
3
+2HCl=CaCl
2
+H
2
O+CO
2
↑) H
2
(4)长颈漏斗下端 液面不下降 或 水注不回落
27.(6分)【猜想与假设】猜想4: Na CO 和NaCl
2 3
【讨论与交流】在溶液中NaCO 和HCl不能共存(或意思正确,或写化学方程式均可给分)
2 3
【实验与结论】
(1)错误 酚酞溶液滴入猜想3中也不变色(或酚酞溶液遇到HCl溶液也不变色)(2)B
【拓展与应用】(1)蒸发 挥发出的HCl气体会污染空气(2)①NaCl、Na2CO3 ②106
五、推断题(本题包括2小题,共12分,每空1分)
28.(6分)(1)CuSO Ba(NO ) (2)稀HCl (3)Na CO Ba(NO ) BaSO
4 3 2 2 3 3 2 4
29.(6分,每空1分)
(1)Cu (2)催化作用或催化剂 (3)光合作用(4)涂油或刷漆(合理即可)
CuO
(5)2H O === 2H O +O ↑ Cu (OH) CO + 4HCl ====2CuCl +CO ↑+3H O
2 2 2 2 2 2 3 2 2 2
六、综合题(本题1小题,共13分,每空1分)
30.(1)NH 使湿润的红色石蕊试纸变蓝 (2)2NaOH+CO═NaCO+HO
3 2 2 3 2
(3)①浓盐酸有挥发性,挥发出的氯化氢气体会被氢氧化钠溶液吸收,带来实验误差
②除去空气中的水和二氧化碳 偏大
证明生成的二氧化碳在B中已全部吸收(或防止空气中的二氧化碳进入B,干扰实验)
③继续滴加Ba(NO ) 溶液,无白色沉淀生成
3 2
11(4)倾斜锥形瓶,使样品与M溶液接触(5)防止生成的气体受热膨胀(或使水蒸气液化);调
节两边液面平衡 (6)A (7)92.9%
12