文档内容
第三课时 硝酸
[明确学习目标] 1.通过硝酸与不活泼金属、非金属反应,认识硝酸的强氧
化性。2.通过比较浓硝酸与稀硝酸性质的差异,认识浓度、反应条件对反应产物
的影响。3.知道氮的氧化物(NO ),硫的氧化物(SO )是主要的大气污染物及防治
2 2
措施。
学生自主学习
硝酸的性质
1.硝酸是 □ 无 色, □ 易 挥发,有 □ 刺激性 气味的液体。
2.浓硝酸的不稳定性,用化学方程式表示为:□4HNO =====4NO ↑+O ↑
3 2 2
+2H O。
2
3.稀硝酸的强氧化性
稀硝酸与Cu发生反应:□8HNO (稀)+3Cu===3Cu(NO ) +2NO↑+4H O,
3 3 2 2
离子方程式为□2NO+3Cu+8H+===3Cu2++2NO↑+4H O。
2
4.浓硝酸的强氧化性
(1)常温下Fe、Al遇浓硝酸钝化,因此可用铝制或铁质的容器贮存浓硝酸。
(2)浓硝酸与Cu发生反应:□4HNO (浓)+Cu===Cu(NO ) +2NO ↑+2H O,
3 3 2 2 2
离子方程式为□2NO+Cu+4H+===Cu2++2NO ↑+2H O。
2 2
5.王水
由 □ 浓硝酸 和 □ 浓盐酸 组成的混合物,体积比为 □ 1 ∶ 3 。能使不溶于硝酸的金
属如 □ 金 、 □ 铂 等溶解。
6.硝酸的用途
是制炸药、染料、塑料的原料,也是化学实验室的必备试剂。
酸雨及防治
1.SO 与NO 的主要来源
2 2
(1)SO :主要来源于 □ 煤、石油 和某些含硫的金属矿物的燃烧或冶炼。
2
(2)NO :主要来自于汽车尾气。
2
2.危害
(1)引起大气污染,直接危害人体健康。
(2)溶于水形成 □ 酸雨 。
3.酸雨(1)概念: □ pH<5.6 的降雨。
(2)成因: □ 二氧化硫、氮氧化物以及它们在大气中发生反应后的生成物 溶于
雨水形成的。
(3)危害
①直接破坏农作物、森林、草原,使 □ 土壤、湖泊 酸化。
②加速 □ 建筑物、桥梁、工业设备、运输工具 及电信电缆的腐蚀。
分析铜与浓硝酸、稀硝酸的反应,思考硝酸的浓度对还原产物有何影响?
提示:反应中,浓硝酸的还原产物是 NO ,稀硝酸的还原产物是NO,一般
2
地硝酸的浓度越低,还原产物的价态越低。
课堂互动探究
知识点一 硝酸的性质
1.硝酸的物理性质
颜色 状态 气味 溶解性 挥发性
无色 液态 刺激性气味 易溶于水 有挥发性
硝酸浓度越大越易挥发。
2.硝酸的不稳定性
HNO 在光照或加热条件下会分解,硝酸浓度越大越容易分解。反应方程式
3
为4HNO =====4NO ↑+O ↑+2H O。所以HNO 应盛放在棕色细口试剂瓶中,
3 2 2 2 3
且放在阴凉处;浓硝酸呈黄色是由于溶有NO 的缘故。
2
3.硝酸的强氧化性
(1)本质
HNO 中的+5价氮元素具有很强的得电子能力。
3
(2)规律
①硝酸的浓度越大,反应温度越高,其氧化性越强。
②还原剂一般被氧化成最高价态。
(3)具体表现
①硝酸与金属的反应
a.除Au、Pt等少数金属外,硝酸几乎可以氧化所有的金属。如3Ag+4HNO (稀)===3AgNO +NO↑+2H O。
3 3 2
b.活泼金属与HNO 反应不生成H ,HNO 的浓度不同,还原产物不同。
3 2 3
c.常温下浓硝酸、浓H SO 能使Fe、Al钝化。
2 4
②硝酸与非金属的反应
反应规律:非金属单质+浓硝酸―→最高价氧化物或其含氧酸+NO ↑+
2
H O
2
如:C+4HNO (浓)=====CO ↑+4NO ↑+2H O
3 2 2 2
③硝酸与还原性化合物的反应
硝酸的强氧化性还表现在可以氧化具有还原性的化合物或离子,如 HI、
HBr、SO 、Fe2+、FeO、Br-、I-、S2-、SO等均能被HNO 氧化。
2 3
1 某稀溶液中 HNO 和 H SO 的物质的量浓度分别为 3.0 mol/L 和 2.0
3 2 4
mol/L。取该溶液20 mL,加入3.2 g铜粉,充分反应后,产生的气体在标准状况
下的体积约是( )
A.0.75 L B.0.336 L C.1.5 L D.0.448 L
[批注点拨]
[解析] 20 mL 溶液中:n(H+)=0.14 mol,n(NO)=0.06 mol,n(Cu)=0.05
mol。依据离子方程式计算:3Cu + 8H+ + 2NO===3Cu2++2NO↑+4H O
2
3 8 2 2×22.4 L
0.05 mol 0.14 mol 0.06 mol V(NO)
三者反应时,H+与NO均过量,依据Cu的物质的量可得V(NO)≈0.75 L。
[答案] A
[练1] 将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的
是( )
A.反应剧烈程度:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
答案 B
解析 相同质量的铜分别和过量浓硝酸、稀硝酸反应时,浓硝酸参与的反应
更剧烈,A 错;铜和浓硝酸、稀硝酸反应的方程式分别为① 4HNO (浓)+
3
Cu===Cu(NO ) +2NO ↑+2H O,②8HNO (稀)+3Cu===3Cu(NO ) +2NO↑+
3 2 2 2 3 3 2
4H O。①产生红棕色气体,②产生无色气体,C错误;由于参加反应的铜的质
2
量相同,且两反应中还原剂都是铜,反应后铜的价态又相同,所以反应中转移的
电子总数相等,D错;1 mol Cu和浓硝酸反应消耗4 mol硝酸,1 mol Cu和稀硝
酸反应消耗 mol硝酸,同质量的铜和过量浓硝酸、稀硝酸反应时,消耗的浓硝
酸多,B正确。
[练2] 9.7 g Cu和Zn的合金与足量的稀硝酸反应,还原产物只有NO气体,
其体积在标准状况下为2.24 L。将溶液稀释为1 L,测得溶液的c(H+)=0.1 mol·L
-1,此时溶液中NO的浓度为( )
A.0.3 mol·L-1 B.0.4 mol·L-1C.0.2 mol·L-1 D.0.6 mol·L-1
答案 B
解析 n(NO)=0.1 mol,转移电子的物质的量为 0.1 mol×3=0.3 mol,n(Cu
+Zn)=0.3 mol÷2=0.15 mol,n[Cu(NO ) ]+n[Zn(NO ) ]=0.15 mol,其中所含
3 2 3 2
n(NO)=0.3 mol,溶液的 c(HNO )=c(H+)=0.1 mol·L-1,其中含 n(NO)=0.1
3
mol,溶液中NO的总浓度为0.4 mol·L-1。
知识点二 酸雨及防治
1.SO 和氮的氧化物的吸收
2
(1)NaOH溶液吸收
SO +2NaOH===Na SO +H O
2 2 3 2
NO +NO+2NaOH===2NaNO +H O
2 2 2
2NO +2NaOH===NaNO +NaNO +H O
2 2 3 2
(2)氨气吸收
2NH +H O+SO ===(NH ) SO
3 2 2 4 2 3
NH +H O+SO (多)===NH HSO
3 2 2 4 3
8NH +6NO =====7N +12H O
3 2 2 2
4NH +6NO=====5N +6H O
3 2 2
2.酸雨类型
(1)硫酸型:SO →H SO →H SO
2 2 3 2 4
SO +H OH SO 2H SO +O ===2H SO
2 2 2 3, 2 3 2 2 4
(2)硝酸型:NO →HNO
2 3
3NO +H O===2HNO +NO
2 2 3
3.防治措施
(1)调整能源结构,发展清洁能源。
(2)研究原煤的脱硫技术,改进燃烧技术,减少二氧化硫和氮氧化物的排放,
如用石灰法,对煤燃烧后的烟气脱硫。
(3)加强工厂废气的回收处理。(4)改进汽车尾气的处理技术,控制尾气排放。
2 汽车尾气(含CO、SO 和NO等)是城市空气污染源之一,治理的方法
2
之一是在汽车的排放管上装一个“催化转化器”,它能使CO跟NO反应生成可
参与大气生态循环的无毒气体,并促进二氧化硫的转化。
(1)汽车尾气中导致酸雨形成的主要物质是________________。
(2)写出在催化剂的作用下CO跟NO反应的化学方程式:
________________________________________。
(3)使用“催化转化器”的缺点是在一定程度上提高了排放废气的酸度,有可
能促进了酸雨的形成,其原因是______________________________。
[批注点拨]
[解析] (2)从题目叙述中“它能使CO跟NO反应生成可参与大气生态循环
的无毒气体”,可推出该反应为2CO+2NO=====N +2CO 。
2 2
(3)使用“催化转化器”促进 SO 转化为 SO ,而 SO 与 H O 化合生成
2 3 3 2H SO ,提高了空气的酸度,促进了酸雨的形成。
2 4
[答案] (1)SO 、NO
2
(2)2CO+2NO=====N +2CO
2 2
(3)由于促进了SO 的转化,生成的SO 增多,SO +H O===H SO 提高了空
2 3 3 2 2 4
气的酸度
[练3] 以下非金属氧化物与其引起的环境问题及主要来源对应正确的是(
)
氧化物 环境问题 主要来源
A CO 破坏臭氧层 化石燃料的燃烧
2
B SO 温室效应 汽车尾气的排放
2
C NO 光化学烟雾 工厂废气的排放
2
D CO 酸雨 汽车尾气和化石燃料的不完全燃烧
答案 C
解析 CO 不会破坏臭氧层,A错误;SO 主要引起酸雨,来源于煤的燃烧,
2 2
B错误;CO不会引起酸雨,D错误。
[练4] 下列有关环境污染的说法正确的是( )
A.煤燃烧时加入适量石灰石,可减少SO 的排放
2
B.光化学烟雾的形成主要与CO 有关
2
C.pH在5.6~7之间的降水通常称为酸雨
D.含磷洗涤剂易于被细菌分解,故不会导致水体污染
答案 A
解析 燃烧时加入石灰石,发生的反应有CaCO =====CaO+CO ↑、CaO+
3 2
SO =====CaSO 、2CaSO +O ===2CaSO (炉渣),因此能减少SO 的排放,A正
2 3 3 2 4 2
确;光化学烟雾主要是由氮氧化物和碳氢化合物导致的,B错误;pH<5.6的雨
水被称为酸雨,C错误;含磷洗涤剂会造成水体富营养化而引起赤潮、水华等现象,D错误。
规律方法
(1)引起温室效应的气体除CO 之外,还有CH 等。
2 4
(2)酸雨、光化学烟雾、臭氧空洞均与氮氧化物有关。
(3)CO 不属于空气污染物。
2
本课归纳总结
1.浓硝酸在加热或光照条件下易分解,其分解生成的NO 溶于其中,是浓
2
HNO 通常显黄色的原因。
3
2.稀HNO 的还原产物为NO:
3
3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O,
3 3 2 2
浓HNO 的还原产物为NO :
3 2
Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O。
3 3 2 2 2
3.铁、铝在常温下,遇到浓H SO 或浓HNO 发生钝化,这都体现了二者的
2 4 3
强氧化性。
4.pH<5.6的降雨称为酸雨,酸雨分为硫酸型和硝酸型。前者由SO 引起,
2
后者由NO 引起。
x
学习效果检测
1.对于硫酸和硝酸的比较中,下列叙述中不正确的是( )
A.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装
B.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性
C.浓硫酸和稀硝酸都具有氧化性
D.硫酸和硝酸都是重要的化工原料
答案 B
2.下列关于浓HNO 与浓H SO 的叙述正确的是( )
3 2 4
A.常温下都不能用铁制容器贮存
B.常温下都能与铜较快反应
C.露置于空气中,溶液质量均减轻
D.露置于空气中,溶液浓度均降低
答案 D解析 浓HNO 易挥发,浓 H SO 具有吸水性,露置于空气中,浓 HNO 的
3 2 4 3
质量减轻,浓H SO 的质量增加,但二者的浓度均降低。
2 4
3.下列反应中,硝酸只表现氧化性的是( )
A.Zn+HNO (稀)―→
3
B.Mg(OH) +HNO (稀)―→
2 3
C.C+HNO (浓)―→
3
D.Cu+HNO (浓)―→
3
答案 C
解析 A项,锌与稀硝酸反应生成 NO和硝酸锌和水,表现了硝酸的氧化性
和酸性;B项,Mg(OH) 与硝酸反应生成硝酸镁,只体现了硝酸的酸性;C项,
2
C与浓硝酸反应生成CO 、NO 和水,只体现了硝酸的氧化性;D项,铜与浓硝
2 2
酸反应生成硝酸铜、NO 和水,硝酸既表现氧化性又表现酸性。
2
4.下列关于硝酸的认识中,正确的是( )
A.浓硝酸和稀硝酸都具有氧化性
B.浓硝酸与金属反应不产生氢气,而稀硝酸与金属反应可置换出氢气
C.因常温下铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器
中
D.硝酸与金属反应时,只表现出氧化性
答案 A
解析 浓、稀硝酸都有氧化性,与金属反应不产生氢气;在与金属反应时,
硝酸既表现氧化性又表现酸性;浓硝酸可盛放在铝制或铁制容器中,因为铝和铁
在冷浓硝酸中钝化。
5.在通风橱中进行下列实验:下列说法中不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为2NO+O ===2NO
2 2
B.Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO 的氧化性强于浓HNO
3 3
D.红棕色气体的成分是NO
2
答案 C
解析 Ⅰ中由于稀硝酸有强的氧化性,与铁发生氧化还原反应,硝酸得到电
子被还原变为 NO,气体为无色,当遇到空气时,发生反应:2NO+
O ===2NO ,气体变为红棕色的NO ,A、D正确;在Ⅱ中浓硝酸有强氧化性,
2 2 2
在室温下遇铁、铝会使金属表面氧化产生一层氧化物薄膜,对内层金属起保护作
用,从而防止金属的进一步反应,即发生钝化现象,因此不能进一步反应,这恰
好说明浓硝酸的氧化性比稀硝酸强,B正确,C错误。
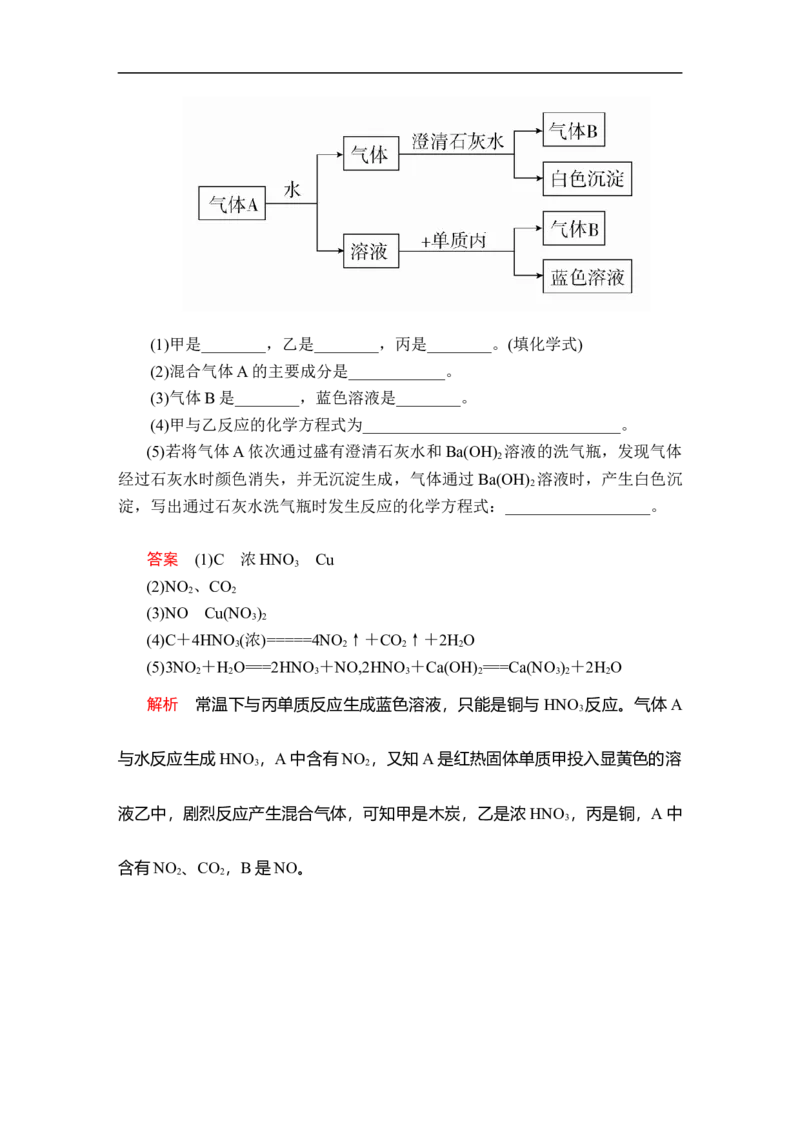
6.将红热固体单质甲投入显黄色的溶液乙中,剧烈反应产生混合气体 A,
A在常温下不与空气反应,根据下图所示的变化关系填空。(1)甲是________,乙是________,丙是________。(填化学式)
(2)混合气体A的主要成分是____________。
(3)气体B是________,蓝色溶液是________。
(4)甲与乙反应的化学方程式为________________________________。
(5)若将气体A依次通过盛有澄清石灰水和Ba(OH) 溶液的洗气瓶,发现气体
2
经过石灰水时颜色消失,并无沉淀生成,气体通过Ba(OH) 溶液时,产生白色沉
2
淀,写出通过石灰水洗气瓶时发生反应的化学方程式:__________________。
答案 (1)C 浓HNO Cu
3
(2)NO 、CO
2 2
(3)NO Cu(NO )
3 2
(4)C+4HNO (浓)=====4NO ↑+CO ↑+2H O
3 2 2 2
(5)3NO +H O===2HNO +NO,2HNO +Ca(OH) ===Ca(NO ) +2H O
2 2 3 3 2 3 2 2
解析 常温下与丙单质反应生成蓝色溶液,只能是铜与 HNO 反应。气体A
3
与水反应生成HNO ,A中含有NO ,又知A是红热固体单质甲投入显黄色的溶
3 2
液乙中,剧烈反应产生混合气体,可知甲是木炭,乙是浓HNO ,丙是铜,A中
3
含有NO 、CO ,B是NO。
2 2