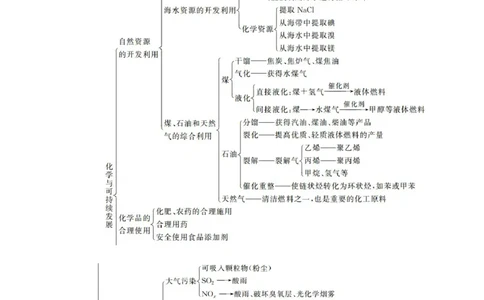
文档内容
\s\up17(知识网络建构)\s\up17(热点专题突破)
专题 无机化工生产流程综合分析
1.问题设置与考查知识点
有关无机化工生产试题的考查内容归纳起来主要有六个方面:
(1)将原料转化为产品的生产原理:考查“复分解反应、氧化还原反应、水解
反应”等原理。
(2)除去所有杂质并分离提纯产品:考查“物质分离与提纯的实验操作”。
(3)提高产量与产率(转化率):考查“化学反应速率和化学平衡”。
(4)减少污染:考查“绿色化学”生产。
(5)原料的来源:考查物质的来源及成本问题。
(6)生产设备简单,生产工艺简便可行等工艺生产问题:要准确、顺利解答
无机化工生产流程题,除了要掌握物质的性质和物质之间相互作用的基本知识以
及除杂、分离提纯物质的基本技能外,还要具备分析工艺生产流程的能力。
2.解答无机化工生产流程题的程序
(1)基本步骤
①从题干中获取有用信息,了解生产的产品。
②整体阅读流程图,辨别出预处理、反应、提纯、分离等阶段。
③分析流程中的每一个步骤,从几个方面了解流程:反应物是什么;发生了
什么反应;该反应造成了什么后果;对制造产品有什么作用。抓住一个关键点:
一切反应或操作都是为获得产品而服务。
④从问题中获取信息,帮助解题。
(2)解题思路
明确整个流程及每一步的目的→仔细分析每步反应发生的条件以及得到的产
物的物理或化学性质→结合基础理论与实际问题思考→注意答题的模式与要点。
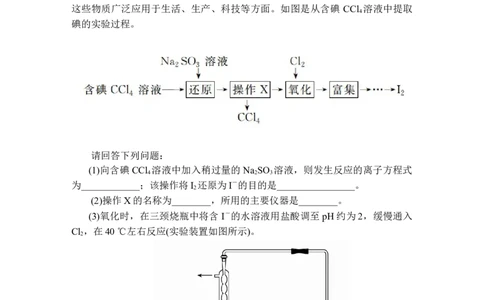
3.解题模板海水是一种丰富的资源,工业生产可以从海水中提取许多有用的物质,
这些物质广泛应用于生活、生产、科技等方面。如图是从含碘 CCl 溶液中提取
4
碘的实验过程。
请回答下列问题:
(1)向含碘CCl 溶液中加入稍过量的 Na SO 溶液,则发生反应的离子方程式
4 2 3
为____________;该操作将I 还原为I-的目的是________________。
2
(2)操作X的名称为________,所用的主要仪器是________。
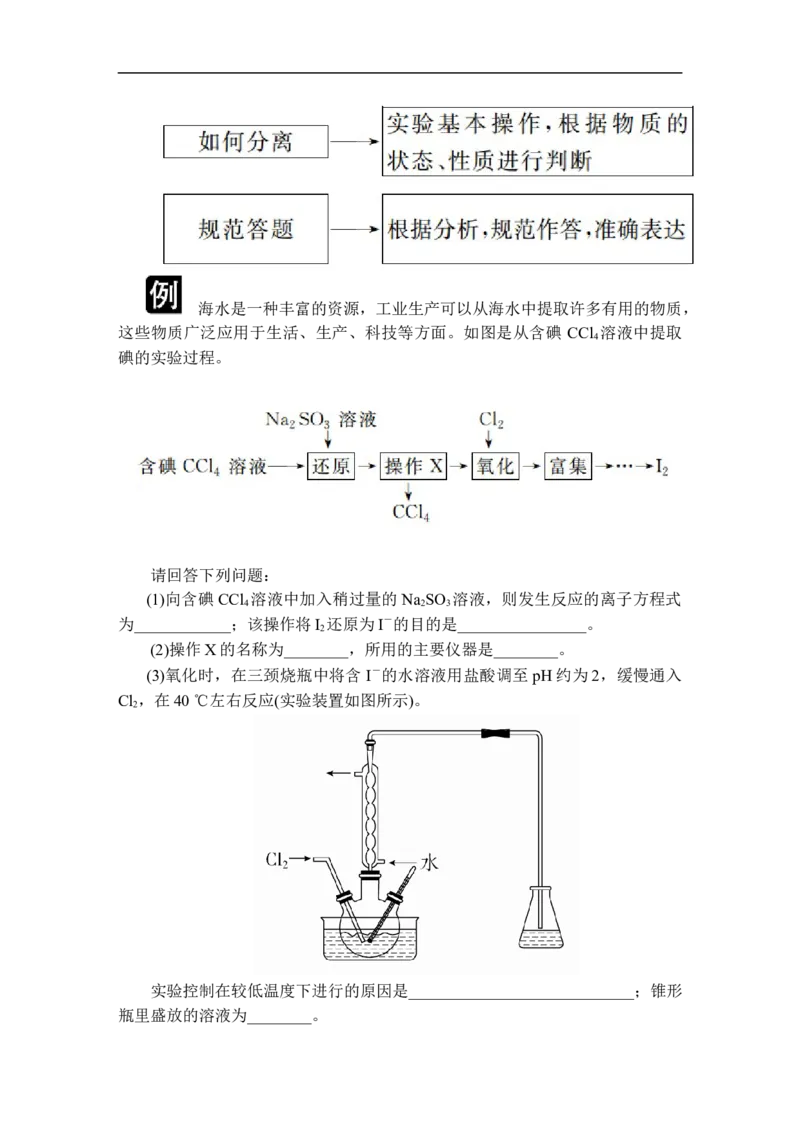
(3)氧化时,在三颈烧瓶中将含 I-的水溶液用盐酸调至 pH约为2,缓慢通入
Cl ,在40 ℃左右反应(实验装置如图所示)。
2
实验控制在较低温度下进行的原因是____________________________;锥形
瓶里盛放的溶液为________。(4)已知:5SO+2IO+2H+===I +5SO+H O,某含碘溶液(pH约为8)中一定
2 2
存在I ,可能存在I-、IO中的一种或两种。请补充完整检验含碘溶液中是否同
2
时含有I-、IO的实验方案:
____________________________。
实验中可供选择的试剂:CCl 、稀盐酸、淀粉溶液。
4[解析] (1)碘能将SO氧化为SO,自身被还原为I-,其发生反应的离子方程
式为SO+I +H O===2I-+SO+2H+;将碘还原为I-,目的是使四氯化碳中的
2 2
碘单质转化为I-进入水溶液,以便利用分液法分离出四氯化碳。
(2)分离互不相溶的液体可采用分液法,四氯化碳和水溶液互不相溶,所以操作X为分液;使用的主要仪器是分液漏斗。
(3)碘不稳定,易升华,且温度高时气体难溶解,所以实验控制在较低温度
下的原因是防止碘升华、增大氯气溶解度;氯气能和强碱溶液反应,所以锥形瓶
中的液体是NaOH溶液。
(4)根据题给反应方程式可知,在酸性环境中,IO有强氧化性,故可推断,
在酸性环境中,IO能将I-氧化。因此,检验含碘溶液中是否同时含有 I-和IO,
可先用四氯化碳多次萃取含碘溶液,然后分液,水层用淀粉溶液检验,当水层不
含碘时,取少量水层溶液,加入淀粉溶液,再加盐酸酸化,如果同时含有 I-和
IO,二者发生氧化还原反应生成I 使溶液变蓝色,否则不同时含有I-和IO。
2
[答案] (1)SO+I +H O===2I-+SO+2H+ 使四氯化碳中的碘单质转化为
2 2
碘离子进入水溶液
(2)分液 分液漏斗
(3)防止碘升华、增大氯气溶解度 NaOH溶液
(4)取少量含碘溶液用四氯化碳多次萃取、分液;水层用淀粉溶液检验,当水
层不含碘单质时,取少量水层溶液,加入1~2 mL淀粉溶液,加盐酸酸化,若
溶液变蓝,说明溶液中同时含有 I-和IO;如果溶液不变蓝,说明不同时含有 I-
和IO