文档内容
第一节 自然资源的开发利用
第一课时 金属矿物及海水资源的开发利用
[明确学习目标] 1.了解金属在自然界中的存在形式及金属的冶炼方法。2.
了解铝热反应的原理,了解金属回收和资源保护的意义。3.了解海水资源、海水
淡化的方法。4.了解海水化学资源的开发和利用,即海水制盐、海水提溴、海带
提碘。5.了解海水综合利用的重要方向。
学生自主学习
金属矿物的开发利用
1.金属在自然界中的存在形态
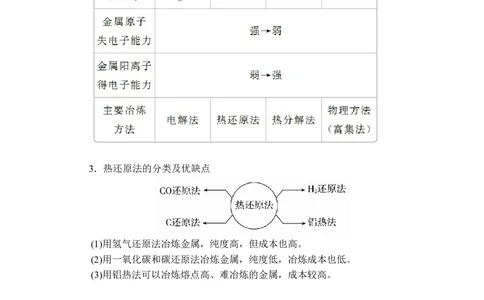
2.金属的冶炼方法3.金属资源的合理开发利用
(1)合理开发利用金属资源
金属的冶炼需要消耗大量的资源和能源,还会造成环境污染,地球上的金属
资源是有限的,是不可再生的,因此金属资源应合理开发和利用。
(2)有效利用金属资源的途径
①提高金属矿物的利用率,开发环保高效的金属冶炼方法;
②加强废旧金属的回收和再利用;
③使用其他材料代替金属材料。
海水资源的开发利用
(一)海水中的水资源
1.海水中水的储量约占地球上总水量的 □ 97% 。
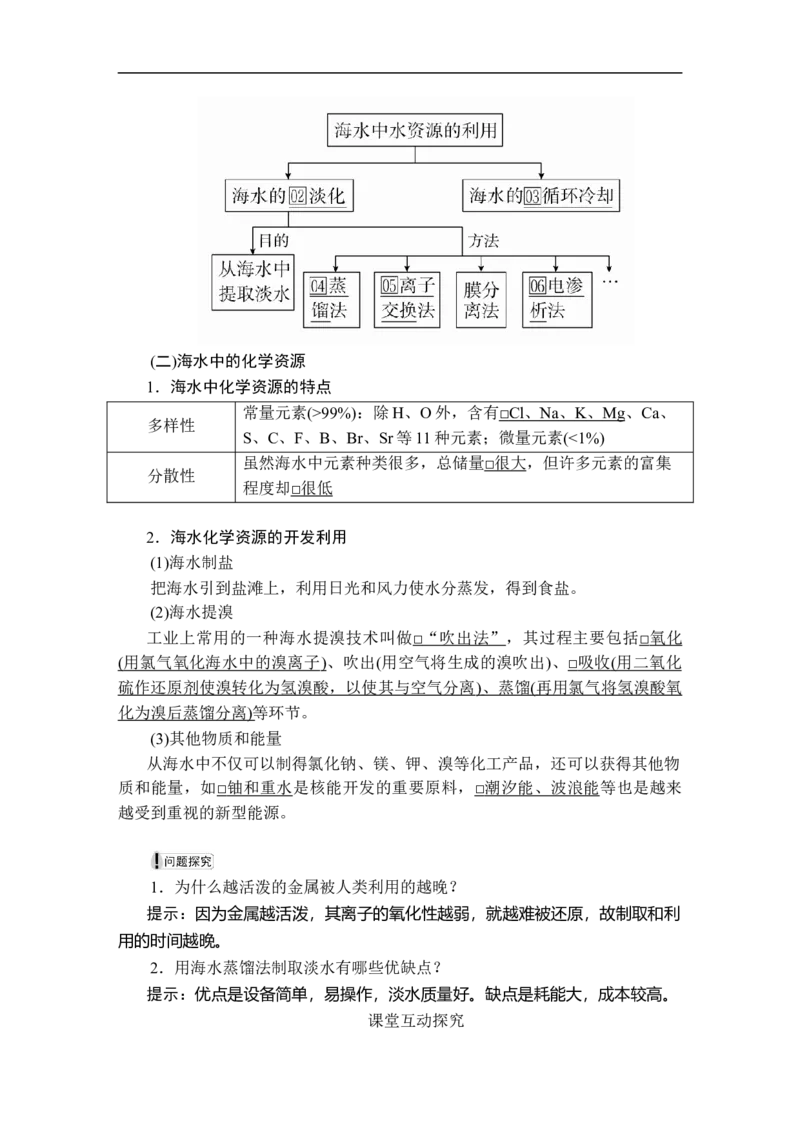
2.海水中水资源的利用(二)海水中的化学资源
1.海水中化学资源的特点
常量元素(>99%):除H、O外,含有 □ Cl 、 Na 、 K 、 Mg 、Ca、
多样性
S、C、F、B、Br、Sr等11种元素;微量元素(<1%)
虽然海水中元素种类很多,总储量 □ 很大 ,但许多元素的富集
分散性
程度却 □ 很低
2.海水化学资源的开发利用
(1)海水制盐
把海水引到盐滩上,利用日光和风力使水分蒸发,得到食盐。
(2)海水提溴
工业上常用的一种海水提溴技术叫做 □ “ 吹出法 ” ,其过程主要包括 □ 氧化
( 用氯气氧化海水中的溴离子 ) 、吹出(用空气将生成的溴吹出)、 □ 吸收 ( 用二氧化
硫作还原剂使溴转化为氢溴酸,以使其与空气分离 ) 、蒸馏 ( 再用氯气将氢溴酸氧
化为溴后蒸馏分离 )等环节。
(3)其他物质和能量
从海水中不仅可以制得氯化钠、镁、钾、溴等化工产品,还可以获得其他物
质和能量,如 □ 铀和重水 是核能开发的重要原料, □ 潮汐能、波浪能 等也是越来
越受到重视的新型能源。
1.为什么越活泼的金属被人类利用的越晚?
提示:因为金属越活泼,其离子的氧化性越弱,就越难被还原,故制取和利
用的时间越晚。
2.用海水蒸馏法制取淡水有哪些优缺点?
提示:优点是设备简单,易操作,淡水质量好。缺点是耗能大,成本较高。
课堂互动探究知识点一 金属矿物的开发利用
1.金属的冶炼原理
金属冶炼的实质是使金属化合物中的金属阳离子得到电子被还原为金属单质
的过程,即:Mn++ne-===M。
2.金属活动性顺序与金属冶炼方法的关系
3.热还原法的分类及优缺点
(1)用氢气还原法冶炼金属,纯度高,但成本也高。
(2)用一氧化碳和碳还原法冶炼金属,纯度低,冶炼成本也低。
(3)用铝热法可以冶炼熔点高、难冶炼的金属,成本较高。
1.铝热反应的实验探究2.铝热反应的原理及特点1 下表中金属的冶炼原理与方法不完全正确的是( )
选项 冶炼原理 方法
A 2HgO=====2Hg+O ↑ 热分解法
2
B 2Al O (熔融)=====4Al+3O ↑ 电解法
2 3 2
C Cu S+O =====2Cu+SO 热分解法
2 2 2
D Fe O +2Al=====2Fe+Al O 热还原法
2 3 2 3
[批注点拨][解析] 活泼金属 K、Ca、Na、Mg、Al 等用电解法冶炼,中等活泼金属
Zn、Fe、Sn、Pb、Cu等用热还原法冶炼,不活泼金属Hg、Ag利用热分解法冶
炼,故A、B、D正确;C项为火法炼铜,错误。
[答案] C
[练1] 冶炼金属一般有下列4种方法:①焦炭法;②水煤气(或氢气、一氧
化碳)法;③活泼金属置换法;④电解法。这4种方法在工业上均有应用。古代
有:Ⅰ.火烧孔雀石炼铜;Ⅱ.湿法炼铜。现代有:Ⅲ.铝热法炼铬;Ⅳ.从光卤石
(MgCl ·6H O)中炼镁。对它们的冶炼方法的分类,不正确的是( )
2 2
A.Ⅰ,① B.Ⅱ,② C.Ⅲ,③ D.Ⅳ,④
答案 B
解析 金属冶炼方法的选择与金属在自然界中存在的状态、金属活动性等有
关,需要在理解的基础上加以记忆。Ⅰ、Ⅱ、Ⅲ、Ⅳ发生的反应分别是:
Ⅰ.Cu (OH) CO =====2CuO+CO ↑+H O
2 2 3 2 2
C+2CuO=====2Cu+CO ↑
2
Ⅱ.Fe+CuSO ===FeSO +Cu
4 4
Ⅲ.2Al+Cr O =====Al O +2Cr
2 3 2 3
Ⅳ.先从光卤石中提取MgCl ,再电解熔融的MgCl :
2 2
MgCl (熔融)=====Mg+Cl ↑
2 2
则Ⅰ属于方法①,Ⅱ属于方法③,Ⅲ属于方法③,Ⅳ属于方法④。综上分析,
B选项不正确。
[练2] (1)Al与Fe O 发生铝热反应的化学方程式为____________________,
3 4
该反应中氧化剂是__________,还原剂是________。
(2)工业上电解冶炼铝的化学方程式为____________________,若电路中通过1 mol电子,可以得到Al________ g。
答 案 (1)8Al + 3Fe O =====4Al O + 9Fe Fe O Al (2)2Al O ( 熔
3 4 2 3 3 4 2 3
融)=====4Al+3O ↑ 9
2
解析 铝热反应中铝失电子作还原剂,Fe O 得电子化合价降低作氧化剂。
3 4
工业制铝用电解熔融Al O 的方法,冰晶石降低Al O 熔点,作助熔剂。由方程
2 3 2 3
式知转移12 mol e-得到铝4×27 g,转移1 mol e-得到铝9 g。
规律方法
利用铝热反应推断混合物的组成,根据得失电子守恒即可计算转移1 mol电
子可以还原的金属元素的质量,用极端假设法和平均值原理判断。
知识点二 海水资源的开发利用
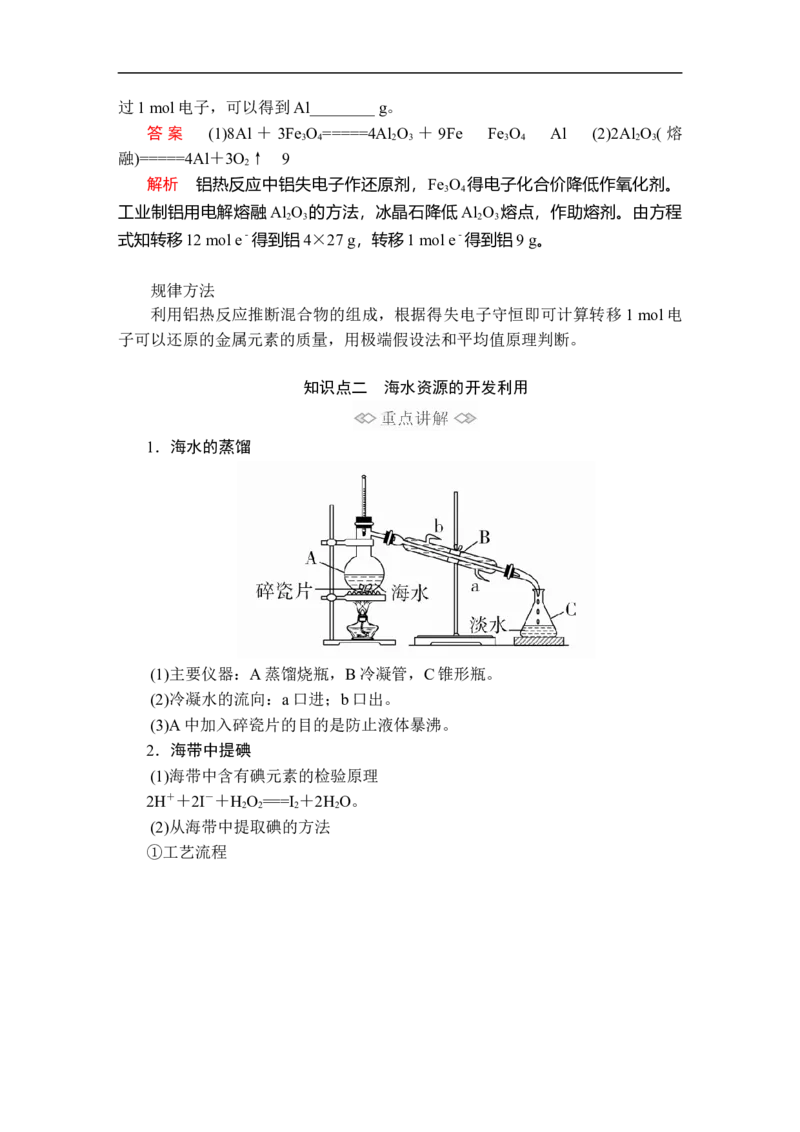
1.海水的蒸馏
(1)主要仪器:A蒸馏烧瓶,B冷凝管,C锥形瓶。
(2)冷凝水的流向:a口进;b口出。
(3)A中加入碎瓷片的目的是防止液体暴沸。
2.海带中提碘
(1)海带中含有碘元素的检验原理
2H++2I-+H O ===I +2H O。
2 2 2 2
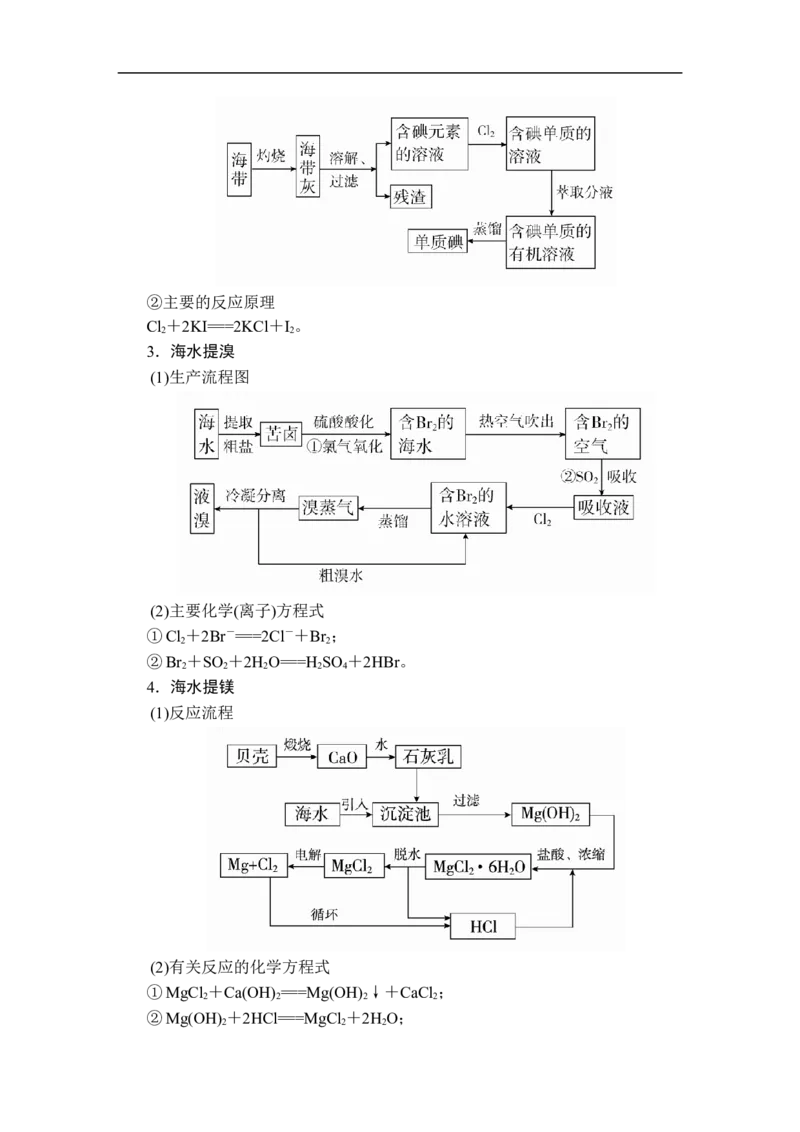
(2)从海带中提取碘的方法
①工艺流程②主要的反应原理
Cl +2KI===2KCl+I 。
2 2
3.海水提溴
(1)生产流程图
(2)主要化学(离子)方程式
①Cl +2Br-===2Cl-+Br ;
2 2
②Br +SO +2H O===H SO +2HBr。
2 2 2 2 4
4.海水提镁
(1)反应流程
(2)有关反应的化学方程式
①MgCl +Ca(OH) ===Mg(OH) ↓+CaCl ;
2 2 2 2
②Mg(OH) +2HCl===MgCl +2H O;
2 2 2③MgCl ·6H O=====MgCl +6H O;
2 2 2 2
④MgCl (熔融)=====Mg+Cl ↑。
2 2
2 从苦卤中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用Na SO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl ===2Cl-+Br
2 2
C.从溴的浓溶液中提取单质溴,可以用乙醇进行萃取
D.步骤Ⅳ包含萃取、分液和蒸馏
[批注点拨]
[解析] A项,X试剂应选用还原性物质,可用Na SO 饱和溶液;B项步骤
2 3
Ⅲ的离子反应为2Br-+Cl ===2Cl-+Br ;C项由于乙醇和水互溶,故不能作为
2 2
从溴水中提取溴的萃取剂,错误;D项步骤Ⅳ是将Br 的浓溶液中的溴提取出来,
2
因此过程包含萃取、分液和蒸馏。[答案] C
[练3] 下列方法中,不能实现海水淡化的是( )
A.蒸馏法 B.电渗析法
C.过滤法 D.离子交换法
答案 C
解析 海水淡化常用的方法有蒸馏法、电渗析法和离子交换法。
[练4] 下列说法正确的是( )
A.海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水
资源,不必节约
B.海水淡化的主要方法有蒸馏法、电渗析法、膜分离法和离子交换法
C.海水淡化的各种方法中,蒸馏法的成本最低
D.以上说法都正确
答案 B
解析 地球表面咸水多,淡水少,许多国家面临着淡水资源的危机,故不可
以随意浪费水资源,A错误;海水淡化的方法中蒸馏法的成本较高,C错误。本课归纳总结
1.金属冶炼的实质是金属化合物中的金属阳离子得到电子被还原为金属单质。
2.常见金属的冶炼方法:K、Ca、Na、Mg、Al―→电解法,Zn~Cu―→热
还原法,Hg、Ag―→热分解法。
3.必记七反应
(1)2HgO=====2Hg+O ↑。
2
(2)2Ag O=====4Ag+O ↑。
2 2
(3)MgCl (熔融)=====Mg+Cl ↑。
2 2
(4)2Al O (熔融)=====4Al+3O ↑。
2 3 2
(5)2NaCl(熔融)=====2Na+Cl ↑。
2
(6)Fe O +2Al=====2Fe+Al O 。
2 3 2 3
(7)Fe O +3CO=====2Fe+3CO 。
2 3 2
4.海水淡化的主要方法有蒸馏法、电渗析法、离子交换法等。
5.海水提溴
(1)工艺流程:海水――→Br ――→溴蒸气――→HBr――→Br 蒸馏,液溴。
2 2
(2)反应原理:Cl +2Br-===Br +2Cl-。
2 2
学习效果检测
1.从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平,
下图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于
( )
A.金属的导电性强弱
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的活动性大小
答案 D
解析 金属的冶炼就是使化合态的金属阳离子被还原为游离态的金属单质,
金属越活泼,对应离子得电子能力越弱,越难被还原,冶炼时所需条件越高。从
题给图示可以归纳出越不活泼的金属(如铜)越早被开发利用,故选D。
2.下列关于金属的冶炼方法的叙述不正确的是( )
A.热分解法适用于制备不活泼金属
B.热还原法常用的还原剂是C、H 、CO、Al等
2C.电解法适用于制备不活泼金属
D.水溶液中置换法适用于用活泼金属制备不活泼金属
答案 C
解析 电解法适用于制备活泼性强的金属,如Na、Mg、Al。
3.若将海水淡化作饮用水使用,下列方法在原理上完全不可行的是 ( )
A.加明矾使海水中的盐沉淀而淡化
B.利用太阳能使海水蒸馏淡化
C.将海水缓慢凝固以获取淡化的饮用水
D.将海水通过离子交换树脂,以除去所含离子
答案 A
解析 明矾净水是利用Al3+反应生成的Al(OH) 胶体的吸附作用而除去水中
3
的一些泥沙,并不能除去海水中的阴、阳离子而使海水淡化。利用太阳能使海水
蒸馏淡化,是有研究价值的一种淡化途径。海水缓慢凝固后可结成冰,在这个过
程中可以除去海水中的离子而淡化。将海水通过离子交换树脂使海水淡化是一种
已被应用的海水淡化方法。
4.从海水中提取的溴约占世界溴年产量的,从海水中提取溴的主要步骤可
表示为( )
A.氧化→吸收→吹出 B.氧化→吹出→吸收
C.吹出→氧化→吸收 D.吹出→吸收→氧化
答案 B
解析 从海水中提取溴,先用氧化剂将溴离子氧化为溴单质,再用热空气吹
出后用二氧化硫水溶液吸收。
5.NaCl是从海水中提取出来的一种重要物质,除食用外,它还是一种工业
原料。下列以NaCl为原料可制取的产品(或物质)是( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸 ⑥漂白粉
A.全是 B.只有①②③④
C.只有①②③⑤ D.只有①②④⑤⑥
答案 A
解析 从海水中制得的氯化钠,可作化工产品,工业上用电解饱和 NaCl溶
液的方法来制取NaOH、Cl 和H ,并以它们为原料生产一系列化工产品,如盐
2 2
酸、漂白粉等;电解熔融的 NaCl可得金属钠和氯气,以 NaCl为原料,也可制
取Na CO 。
2 3
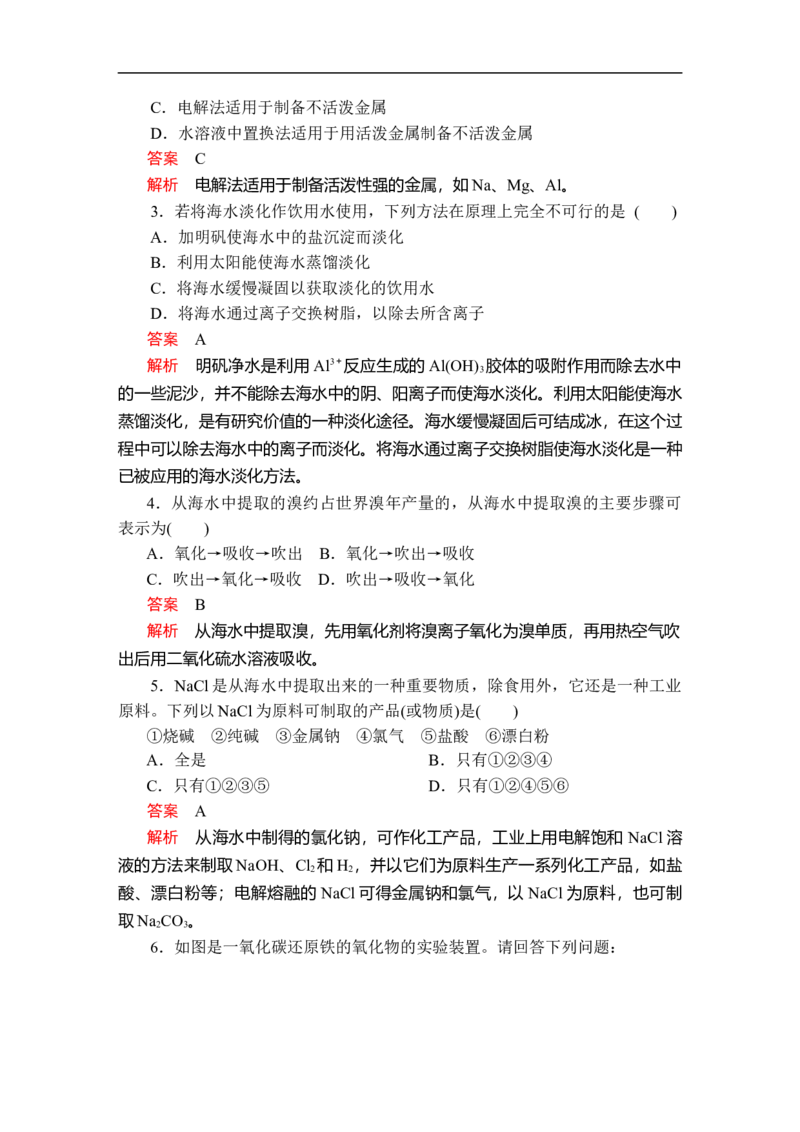
6.如图是一氧化碳还原铁的氧化物的实验装置。请回答下列问题:(1)判断硬质玻璃管中已开始发生反应的现象是__________________;反应
过程中产生的现象是________________________。
(2)在A处点燃可见淡蓝色火焰的原因是_____________________________
_________________________________________________________________。
(3)实验结束时正确的操作是________。
①先停止通入CO
②先熄灭酒精灯,并继续通入CO
③熄灭酒精灯,同时停止通入CO
④先熄灭酒精灯,继续通入CO,并点燃排出的CO气体
答案 (1)B中澄清石灰水变浑浊 玻璃管里的粉末由红棕色逐渐变黑,B中
澄清石灰水变浑浊
(2)从A导管逸出的尾气中有未反应的CO,而CO燃烧时,火焰呈淡蓝色
(3)④
解析 (1)硬质玻璃管中发生反应:3CO+Fe O =====2Fe+3CO ,故硬质玻
2 3 2
璃管中红棕色固体变黑。
(2)通过硬质玻璃管时,CO不完全反应,在A处点燃,有未反应的CO燃烧,
火焰呈淡蓝色。
(3)实验过程中若先停止通CO,则生成的铁可能被氧化,而且可能发生倒吸
现象,故应先熄灭酒精灯,继续通 CO至玻璃管冷却,CO为有害气体,需进行
点燃处理。