文档内容
第六章 章末测试(基础)
一、单选题(本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题
给出的四个选项中,只有一项是符合题目要求的。)
1.(2021·甘肃·武威十八中高一期中)已知空气—锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO+H O;
2
碳棒: O+H O+2e- =2OH- ,据此判断,锌片是
2 2
A.负极,被氧化 B.正极,被氧化
C.负极,被还原 D.正极,被还原
2.(2021·四川省绵阳南山中学高一阶段练习)对于敞口容器中的反应:
,下列叙述不正确的是( )
A. 和 的总能量大于 和 的总能量
B.反应过程中能量关系可用图表示
C.若将该反应设计成原电池,则 为负极
D.若将该反应设计成原电池,当有65g锌溶解时,正极放出11.2L气体(标准状况)
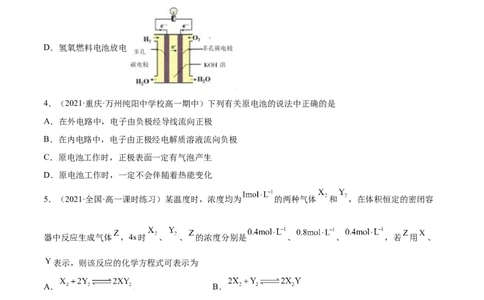
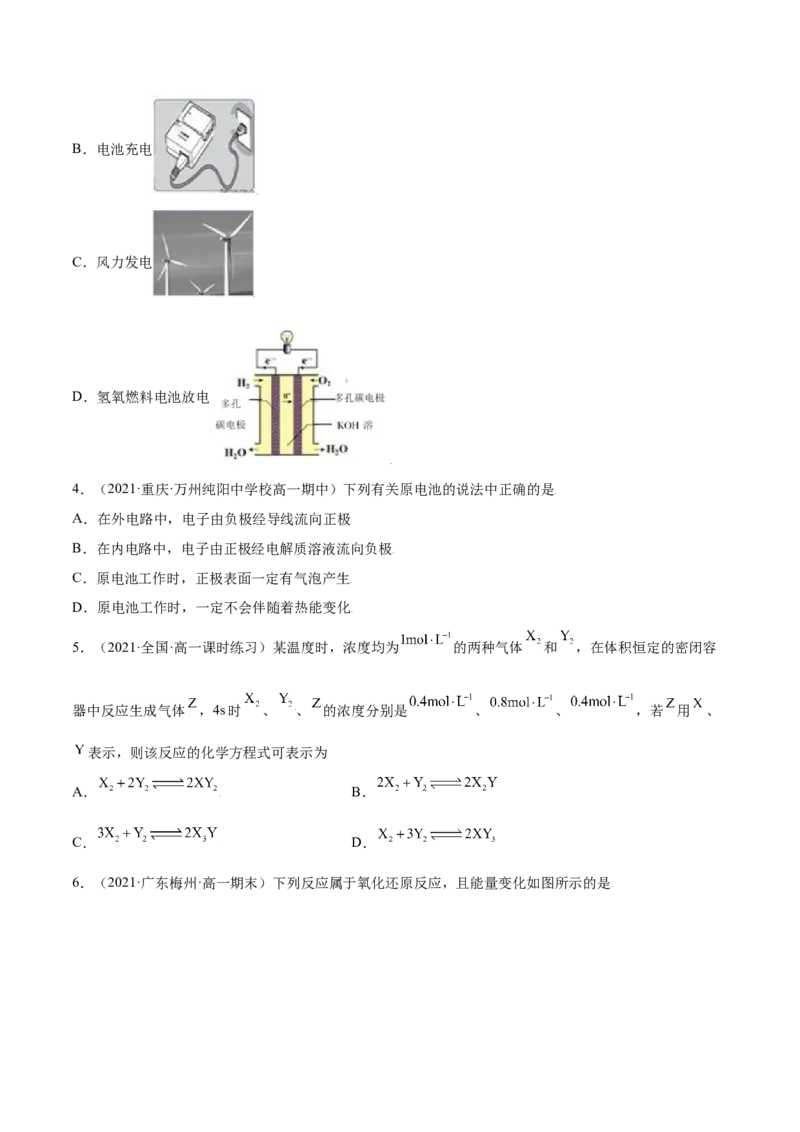
3.(2021·河南·新乡县高中高一阶段练习)下列选项描述的过程能实现化学能转化为电能的是
A.太阳能发电B.电池充电
C.风力发电
D.氢氧燃料电池放电
4.(2021·重庆·万州纯阳中学校高一期中)下列有关原电池的说法中正确的是
A.在外电路中,电子由负极经导线流向正极
B.在内电路中,电子由正极经电解质溶液流向负极
C.原电池工作时,正极表面一定有气泡产生
D.原电池工作时,一定不会伴随着热能变化
5.(2021·全国·高一课时练习)某温度时,浓度均为 的两种气体 和 ,在体积恒定的密闭容
器中反应生成气体 ,4s时 、 、 的浓度分别是 、 、 ,若 用 、
表示,则该反应的化学方程式可表示为
A. B.
C. D.
6.(2021·广东梅州·高一期末)下列反应属于氧化还原反应,且能量变化如图所示的是A.锌粒和稀硫酸反应
B.灼热的木炭与CO 反应
2
C.甲烷在空气中燃烧的反应
D.Ba(OH)·8HO晶体与NH Cl晶体的反应
2 2 4
7.(2021·福建省福州外国语学校高一期中)下列有关化学反应速率的说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.10.0mL2mol﹒L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO 的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
2
D.汽车尾气中的NO和CO可以缓慢反应生成N 和CO,减小压强,反应速率减慢
2 2
8.(2021·全国·高一课时练习)可使反应C(s)+CO(g)=2CO(g)的反应速率增大的措施是:①增大压强 ②增
2
加碳的用量 ③通入CO ④恒压下充入N ⑤恒容下充入N ⑥通入CO
2 2 2
A.①③⑤ B.②④⑥ C.①③⑥ D.③⑤⑥
9.(2021·全国·高一课时练习)C、CO、 和 是常用的燃料,1 mol上述物质分别完全燃烧生
成 及 时,放出的热量依次为393.5 kJ、283.0 kJ、890.3 kJ和1366.8 kJ。相同质量的这4种燃
料完全燃烧,放出热量最多的是。
A.C B.CO C. D.
10.(2021·浙江浙江·高一阶段练习)用NaFeO 溶液氧化废水中的还原性污染物M,为研究降解效果.设
2 4
计如下对比实验探究温度、浓度、pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系
如图所示,下列说法不正确的是( )实验编号 温度°C pH
① 25 1
② 45 1
③ 25 7
④ 25 1
A.实验①在15min内M的降解速率为1.33×10-5mol/(L·min)
B.若其他条件相同,实验①②说明升高温度,M降解速率增大
C.若其他条件相同,实验①③证明pH越高,越不利于M的降解
D.实验①④说明M的浓度越小,降解的速率越快
11.(2020·全国·高一课时练习)在一定温度下的密闭容器中,可逆反应 N + 3H 2NH 达到平衡状
2 2 3
态的标志是
A.N、H、NH 在容器中共存
2 2 3
B.混合气体的总物质的量不再发生变化
C.单位时间内生成 n mol N ,同时生成 3n mol H
2 2
D.单位时间内消耗 n mol N ,同时消耗 n mol NH
2 3
12.(2021·江西·上高二中高一阶段练习)有一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷达到一定
浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其
中的固体电解质是YO—NaO,O2-可以在其中自由移动。下列有关叙述正确的是( )
2 3 2A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B.电极b是正极,O2-由电极a流向电极b
C.电极a的反应式为:CH+5O2--8e-=CO +2H O
4 2
D.当固体电解质中有1molO2-通过时,电子转移4mol
13.(2020·全国·高一课时练习)在带有活塞的密闭容器中发生反应: ,采取
下列措施不能改变反应速率的是( )
A.增加 的量 B.保持容器体积不变,增加 的量
C.充入 ,保持容器内压强不变 D.充入 ,保持容器体积不变
14.(2021·湖北·武汉市钢城第四中学高一期中)已知反应 ,在不同条件下,
用不同物质表示其反应速率,分别为
①
②
③
④
则此反应在不同条件下进行最快的是
A.②③ B.①③ C.②④ D.②
15.(2021·山东·临沂二十四中高一期中)将过量的等质量的两份锌粉a、b,分别加入相同质量、相同浓
度的稀硫酸,同时向a中加少量CuSO 溶液,图中产生H 的体积V(L)与时间t(min)的关系,其中正确的是
4 2
A. B.C. D.
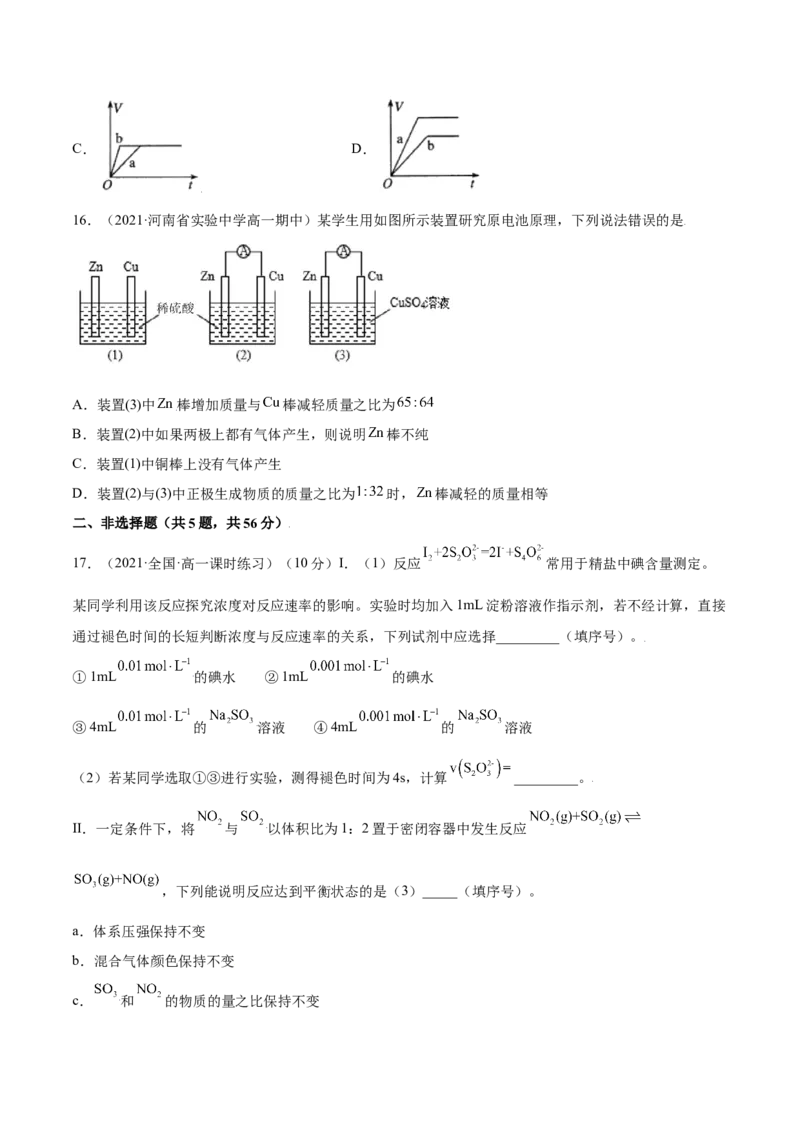
16.(2021·河南省实验中学高一期中)某学生用如图所示装置研究原电池原理,下列说法错误的是
A.装置(3)中 棒增加质量与 棒减轻质量之比为
B.装置(2)中如果两极上都有气体产生,则说明 棒不纯
C.装置(1)中铜棒上没有气体产生
D.装置(2)与(3)中正极生成物质的质量之比为 时, 棒减轻的质量相等
二、非选择题(共5题,共56分)
17.(2021·全国·高一课时练习)(10分)Ⅰ.(1)反应 常用于精盐中碘含量测定。
某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液作指示剂,若不经计算,直接
通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择_________(填序号)。
①1mL 的碘水 ②1mL 的碘水
③4mL 的 溶液 ④4mL 的 溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算 _________。
Ⅱ.一定条件下,将 与 以体积比为1:2置于密闭容器中发生反应
,下列能说明反应达到平衡状态的是(3)_____(填序号)。
a.体系压强保持不变
b.混合气体颜色保持不变
c. 和 的物质的量之比保持不变d.每消耗1mol 的同时生成1mol
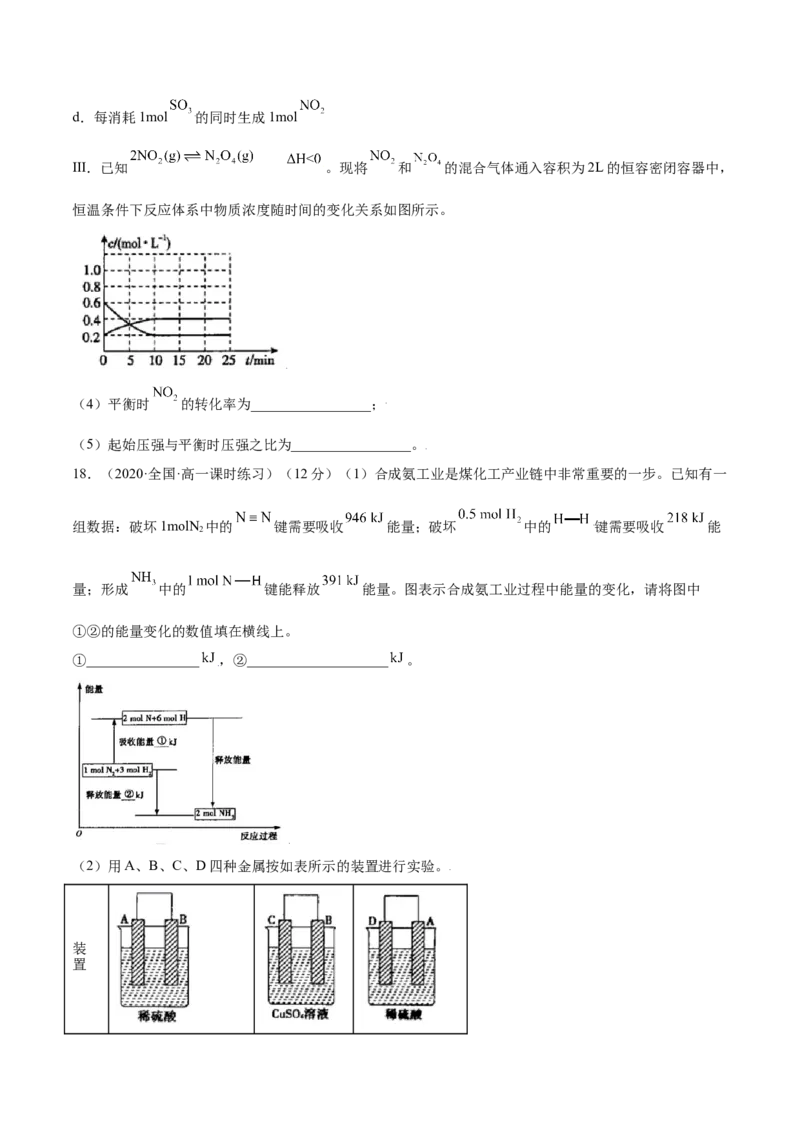
Ⅲ.已知 。现将 和 的混合气体通入容积为2L的恒容密闭容器中,
恒温条件下反应体系中物质浓度随时间的变化关系如图所示。
(4)平衡时 的转化率为_________________;
(5)起始压强与平衡时压强之比为_________________。
18.(2020·全国·高一课时练习)(12分)(1)合成氨工业是煤化工产业链中非常重要的一步。已知有一
组数据:破坏1molN 中的 键需要吸收 能量;破坏 中的 键需要吸收 能
2
量;形成 中的 键能释放 能量。图表示合成氨工业过程中能量的变化,请将图中
①②的能量变化的数值填在横线上。
①________________ ,②____________________ 。
(2)用A、B、C、D四种金属按如表所示的装置进行实验。
装
置甲 乙
丙
现
二价金属A不断溶解 C的质量增加 A上有气体产生
象
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为__________________。
②装置乙中正极的电极反应式为________________。
③装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是________。
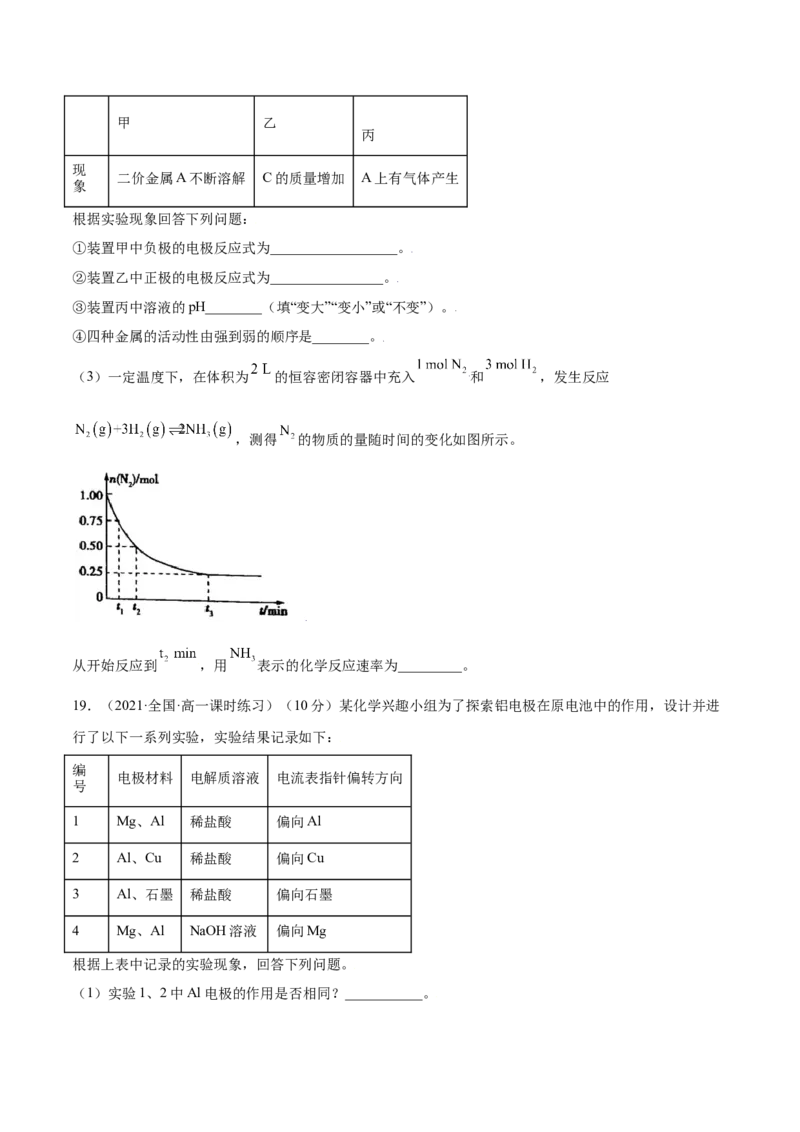
(3)一定温度下,在体积为 的恒容密闭容器中充入 和 ,发生反应
,测得 的物质的量随时间的变化如图所示。
从开始反应到 ,用 表示的化学反应速率为_________。
19.(2021·全国·高一课时练习)(10分)某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进
行了以下一系列实验,实验结果记录如下:
编
电极材料 电解质溶液 电流表指针偏转方向
号
1 Mg、Al 稀盐酸 偏向Al
2 Al、Cu 稀盐酸 偏向Cu
3 Al、石墨 稀盐酸 偏向石墨
4 Mg、Al NaOH溶液 偏向Mg
根据上表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同?___________。(2)实验3中铝为___________极,电极反应式为 ;石墨为___________极,电极反应式为
;电池总反应式为___________。
(3)实验4中的铝为___________极,原因是___________。写出铝电极的电极反应式:___________。
(4)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响___________?
20.(2021·全国·高一课时练习)(10分)某同学为了探究锌与盐酸反应过程中的速率变化,他在100 mL
稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况下的体积),实
验记录如下(累计值):
时间/min 1 2 3 4 5
氢气体积/mL 50 120 232 290 310
(1)反应速率最大的时间段是___________(填“0~1 min”“1~2 min”“2~3 min”“3~4 min”或“4~5 min”),原因是
___________。
(2)反应速率最小的时间段是___________(填“0~1 min”“1~2 min”“2~3 min”“3~4 min“或“4~5min”),原因是
___________。
(3)2~3 min时间段内,以盐酸的浓度变化表示该反应的速率为___________。
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列
液体,你认为可行的是___________(填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D. 溶液
21.(2021·四川仁寿·)(14分)在2 L的某恒容密闭容器中发生反应:CO(g)+3H(g) CHOH(g)+
2 2 3
HO(g) H。已知反应中化学键数据如下表:
2
化学键 △ H-H C-O C=O H-O C-H
E/(kJ/mol) 436 351 745 463 413
回答下列问题:
(1)△H___________(填“>”“<”或“=”)0。
(2)某温度下,向该容器中充入0.3 mol CO 、0.9 mol H,发生上述反应,5 min末,反应达到平衡,此
2 2
时测得HO(g)的物质的量分数为25%。
2
①0~5 min内,H 平均速率v(H )=___________mol·L-1·min-1。
2 2
②每生成0.15 mol CH OH,转移的电子数为___________N 。
3 A
③反应前后的总压强之比为___________。(3)工业上有一种方法是用CO 来生产燃料甲醇(化学式:CHOH,常温下为无色液体),可以将CO 变废
2 3 2
为宝。在体积为2 L的密闭容器中,充入2 mol CO 和6 mol H ,一定条件下发生反应:CO(g)
2 2 2
+3H (g) CHOH(g)+H O(g),测得CO(g)和CHOH(g)的浓度随时间变化如图所示:
2 3 2 2 3
⇌
①从开始到平衡,CHOH的平均反应速率v(CHOH)=_______;H 的转化率a(H)=_______;
3 3 2 2
②若反应CO(g)+3H(g) CHOH(g)+H O(g),在四种不同情况下的反应速率分别为:
2 2 3 2
a.v(CO
2
)=0.15 mol∙L-1∙m⇌in-1 b.v(H
2
)=0.01 mol∙L-1∙min-1
c.v(CHOH)=0.2 mol∙L-1∙min-1 d.v(H O)=0.45 mol∙L-1∙min-1
3 2
该反应进行最快的是____________(填字母)。
③以下结论可以作为CO(g)+3H(g) CHOH(g)+H O(g)已达平衡的标志的是_________。
2 2 3 2
a.v(H 2 ) 正 =v(CH 3 OH) 逆 ⇌
b.c(CO):c(H):c(CHOH):c(HO)=1:3:1:1
2 2 3 2
c.容器内压强不再变化
d.单位时间内,每生成1 mol CH OH,同时消耗3 mol H
3 2
e.容器内混合气体的密度不再变化
f.H 的体积分数不再变化
2倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育