文档内容
2017-2018 学年河北省邯郸市馆陶县九年级(上)期中化学试卷
一、选择题(共20小题,每小题2分,满分40分)
1.我们生活在多姿多彩的物质世界里,下列关于化学物质的说法正确的是
( )
A.垃圾是“放错了地方的资源”,蕴藏着巨大的能量
B.大量使用化肥和农药是粮食增产的主要方法
C.某饮料中绝对不含化学物质
D.气功可以使铝变成金
2.下列说法不属于氮气用途的是( )
A.制氮肥 B.做霓虹灯光源 C.做灯泡填充气 D.做瓜果保护气
3.下了没有涉及化学变化的是( )
A.
烧制陶瓷 B.
干冰升华C.
粮食酿酒 D.
蜡烛燃烧
4.下到有关水的说法不正确的是( )
A.水是由水分子构成的
B.电解水的实验中,得到的氢气与氧气体积比为1:2
C.过滤、吸附、蒸馏、消毒等都是常用的净水方法
第1页(共30页)D.地球上的水储量是丰富的,但可供利用的淡水资源是有限的
5.近年来,我国采取了汽车限行等多种措施减少雾霾的产生,下列措施不利于改
善环境的是( )
A.乘坐公共交通工具、低碳出行
B.参与植树造林,扩大植被面积
C.经常使用一次性筷子、塑料袋等方便生活
D.提倡使用太阳能等清洁能源
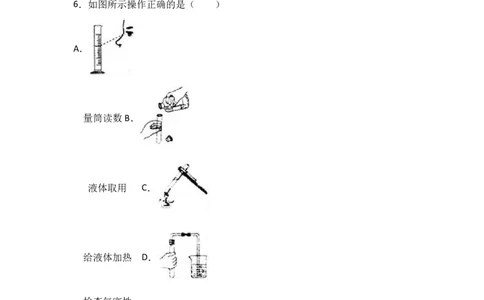
6.如图所示操作正确的是( )
A.
量筒读数B.
液体取用 C.
给液体加热 D.
检查气密性
7.关于催化剂的说法正确的是( )
A.反应前后催化剂的化学性质通常会发生改变
B.催化剂可改变化学反应速率
C.用过氧化氢制取氧气时,加入催化剂可使生成氧气的质量增加
D.制取氧气时必须加入催化剂,否则反应不能发生
8.用排水法收集一瓶人体呼出的气体的操作顺序为( )
第2页(共30页)①将饮水管小心地插入集气瓶内,并向集气瓶内缓缓吹气,直到集气瓶充满呼出
的气体;
②把盛满水的集气瓶连同玻璃片一起倒立在水槽内;
③将集气瓶盛满水,用玻璃片先盖住瓶口的一部分,然后推动玻璃片将瓶口全部
盖住;
④在水下立即用玻璃片将集气瓶的瓶口盖好,然后取出集气瓶放在桌上.
A.①②③④B.②③①④C.③②①④D.④③②①
9.下列生活中的变化不属于缓慢氧化的是( )
A.木柴的燃烧 B.菜刀生锈
C.人在长跑时急促呼吸D.农家肥料的腐熟
10.三瓶无色气体分别是氧气、空气、二氧化碳,下列区分的方法正确的是( )
A.用带火星的木条B.用燃着的木条
C.用澄清石灰水 D.用紫色的石蕊试液
11.下列是四位同学对氧气的描述,你认为不正确的是( )
A.出现高原反应要及时吸氧,因为氧气能够供给呼吸
B.用含有氧元素的物质反应才有可能产生氧气
C.在压强101kPa,氧气在﹣183℃变为无色的液体
D.氧气是性质比较活泼的气体,具有氧化性
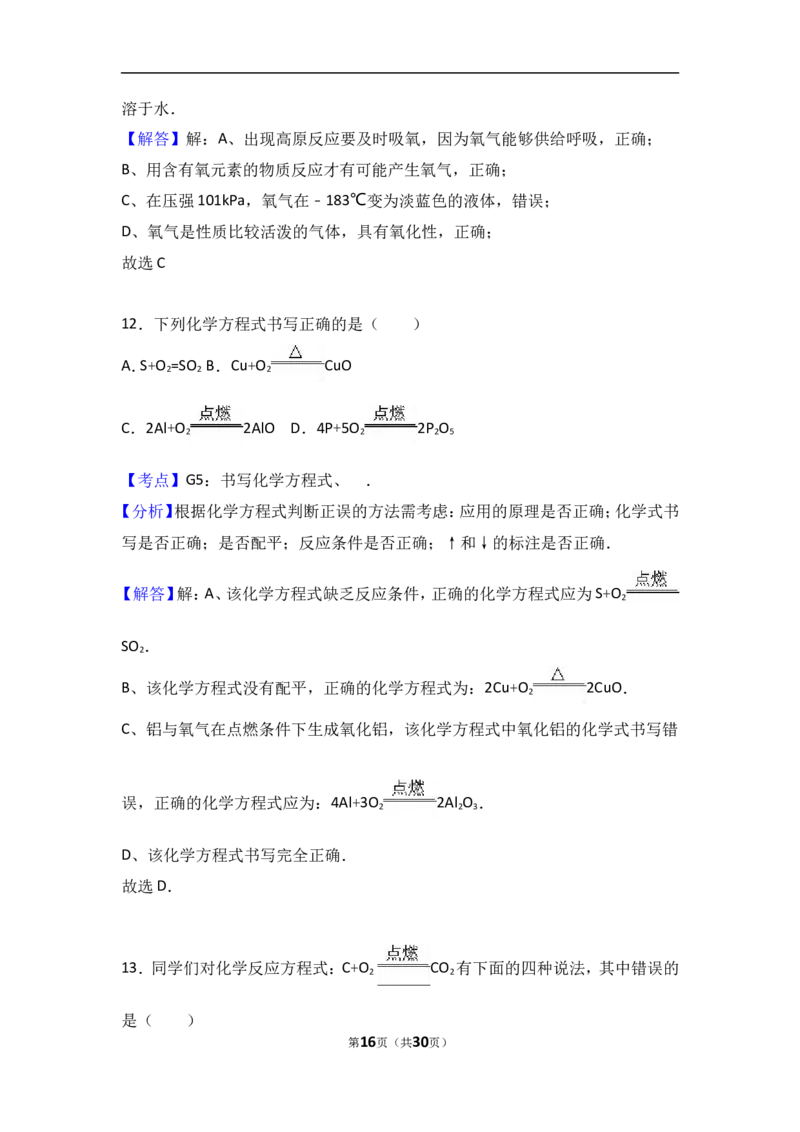
12.下列化学方程式书写正确的是( )
A.S+O =SO B.Cu+O CuO
2 2 2
C.2Al+O 2AlO D.4P+5O 2P O
2 2 2 5
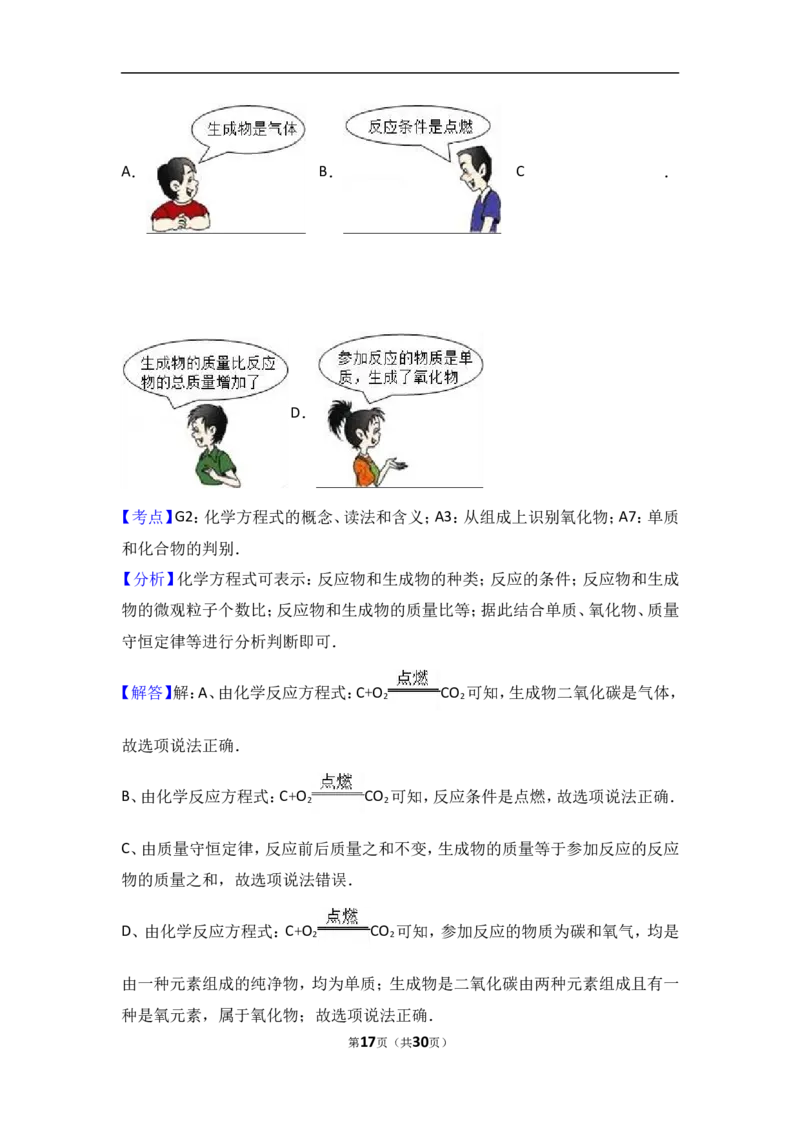
13.同学们对化学反应方程式:C+O CO 有下面的四种说法,其中错误的
2 2
是( )
第3页(共30页)A. B. C .
D.
14.化学反应遵守质量守恒定律的原因是( )
A.物质的种类没有改变
B.分子的种类没有改变
C.分子的数目没有改变
D.原子的种类、数目、质量都没改变
15.2017年8月8日晚,四川九寨沟发生7.0级地震,震后当地水质发生变化,为
了饮用安全,下列做法错误的是( )
A.可以用活性炭去除水中的异味
B.用过滤的方法净化后可以直接饮用
C.家庭生活中加热煮沸后再饮用
D.要对饮用水进行适当的消毒杀菌
16.下列各项,在化学变化前后,肯定没有变化的是( )
①原子数目 ②分子数目 ③元素种类 ④物质的总质量 ⑤物质的种类.
A.①④B.①③④ C.①③⑤ D.①③④⑤
17.下列现象能用质量守恒定律解释的是( )
A.水结冰前后质量不变
B.1升芝麻和1升大米混合,总体积小于2升
第4页(共30页)C.在加压降温的条件下,氧气变为淡蓝色液体
D.氧化钙与水反应生成氢氧化钙,反应前后物质的总质量不变
18.下列物质中含有氧气的是( )
A.水 B.氯酸钾 C.液态空气D.过氧化氢
19.科学家发现,在液晶电视等制造过程中使用的三氟化氮(NF )的温室效应是
3
二氧化碳的1.7万倍.NF 中氟元素为﹣1价,则氮元素的化合价是( )
3
A.﹣3 B.0C.+1 D.+3
20.奶奶在小商贩那里买到一个银手镯,小红认为它可能是假的,准备先拿磁铁
来吸一下.就拿磁铁来吸一下这一过程而言,属于科学探索中的( )
A.假设B.实验 C.观察D.做出结论
二、填空题(共7小题,每小题4分,满分35分)
21.用化学用语填空:
(1)一个氢原子 ;(2)二个氮气分子 ;
(3)三个钠离子 ;(4)四氧化三铁 .
22.改正下列有错误的元素符号.
镁MG ,铁F ,铝AL ,硅Sl ,氢N ,铜Ca
.
23.生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水.
(1)检查洲河水是硬水还是软水,可用的物质是 ;
(2)生活中硬水软化的方法是 ;
(3)活性炭能除去洲河水中有颜色,有异味的物质,这是利用活性炭的 性;
(4)自来水生产过程中,分离不溶物的操作方法是 ;
(5)为保护水资源,请你提出一条防水污染的建议: .
(6)下列“水”中,属于纯净物的是 (填序号)
a、海水 b、河水 c、蒸馏水 d、井水.
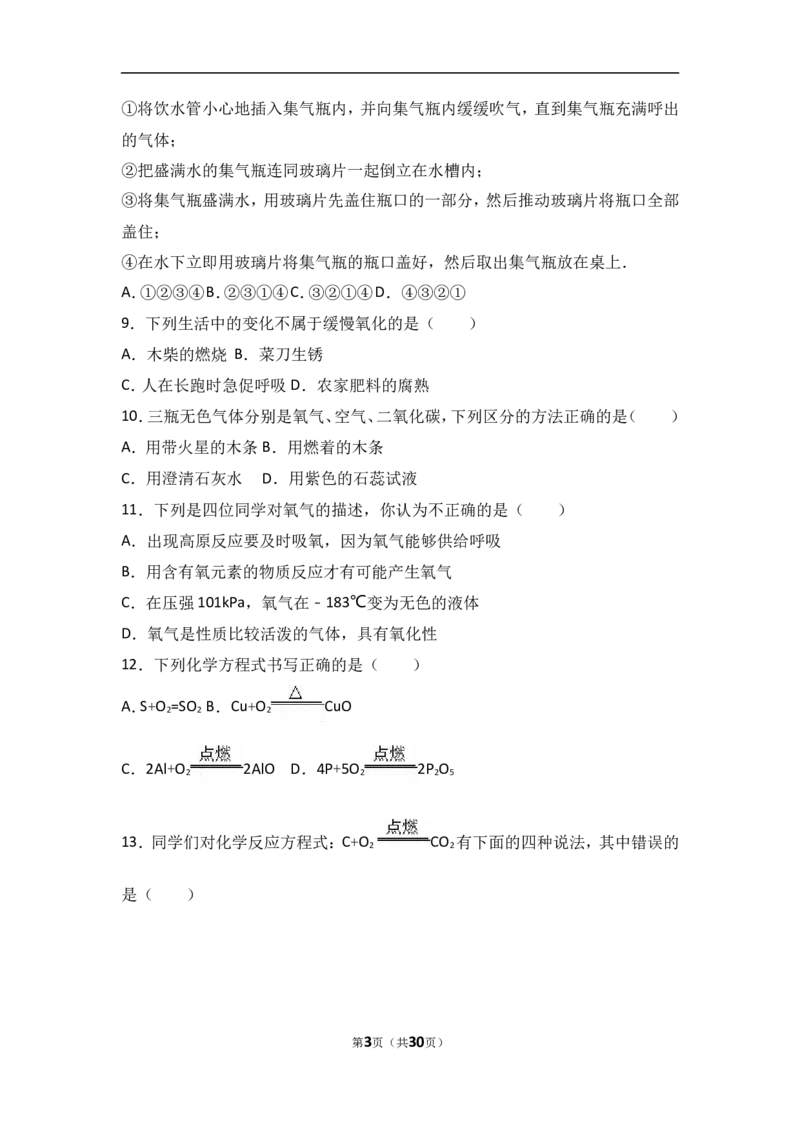
24.水是一种重要的资源.
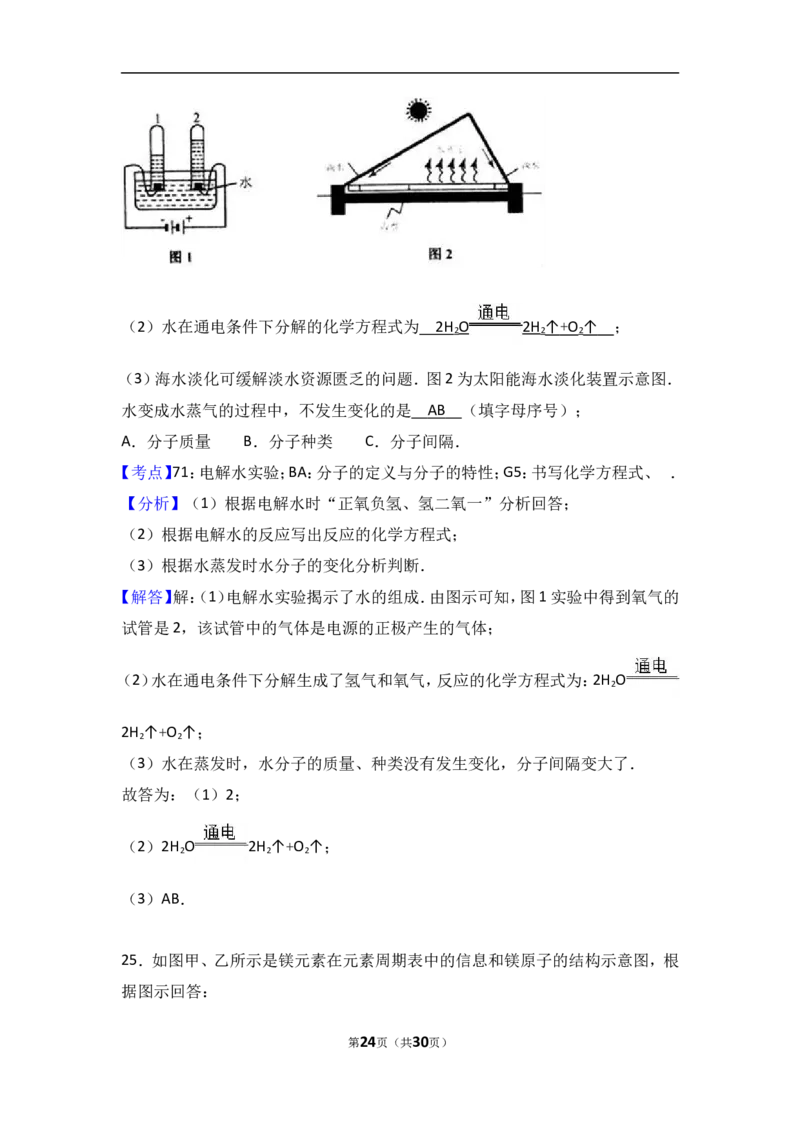
(1)电解水实验揭示了水的组成.图1实验中得到氧气的试管是 (填“1”
或“2”);
第5页(共30页)(2)水在通电条件下分解的化学方程式为 ;
(3)海水淡化可缓解淡水资源匮乏的问题.图2为太阳能海水淡化装置示意图.
水变成水蒸气的过程中,不发生变化的是 (填字母序号);
A.分子质量 B.分子种类 C.分子间隔.
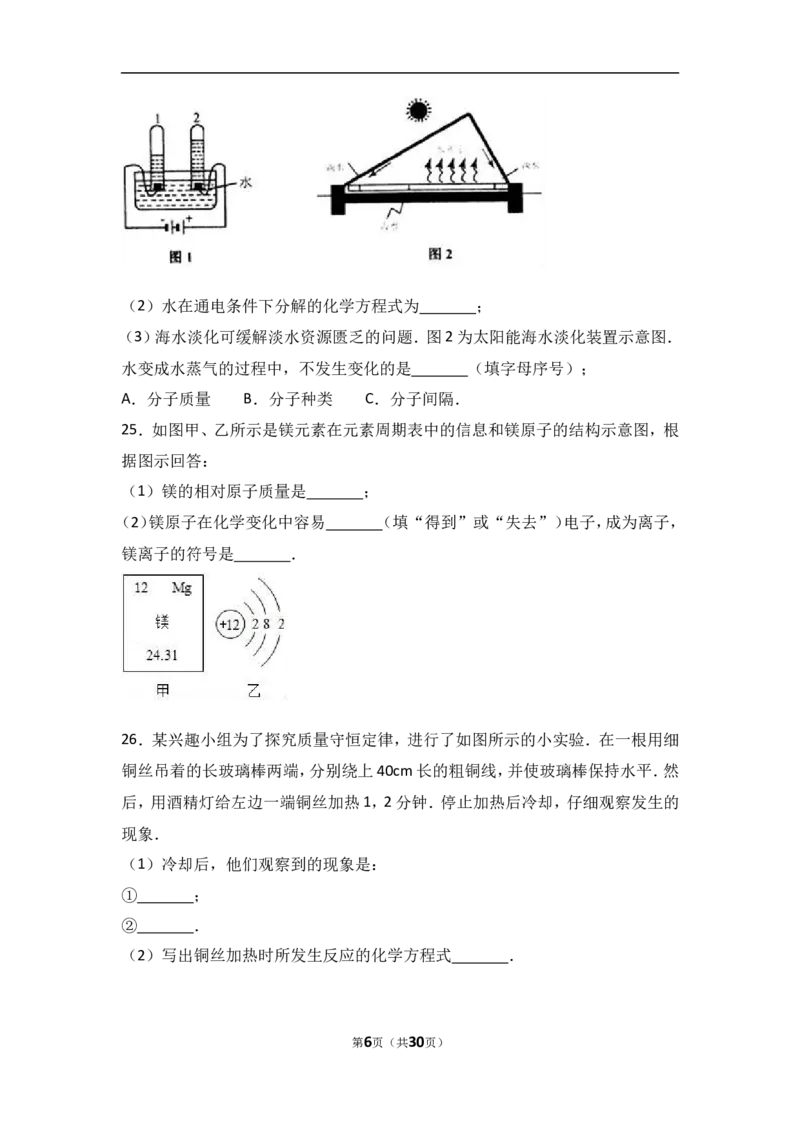
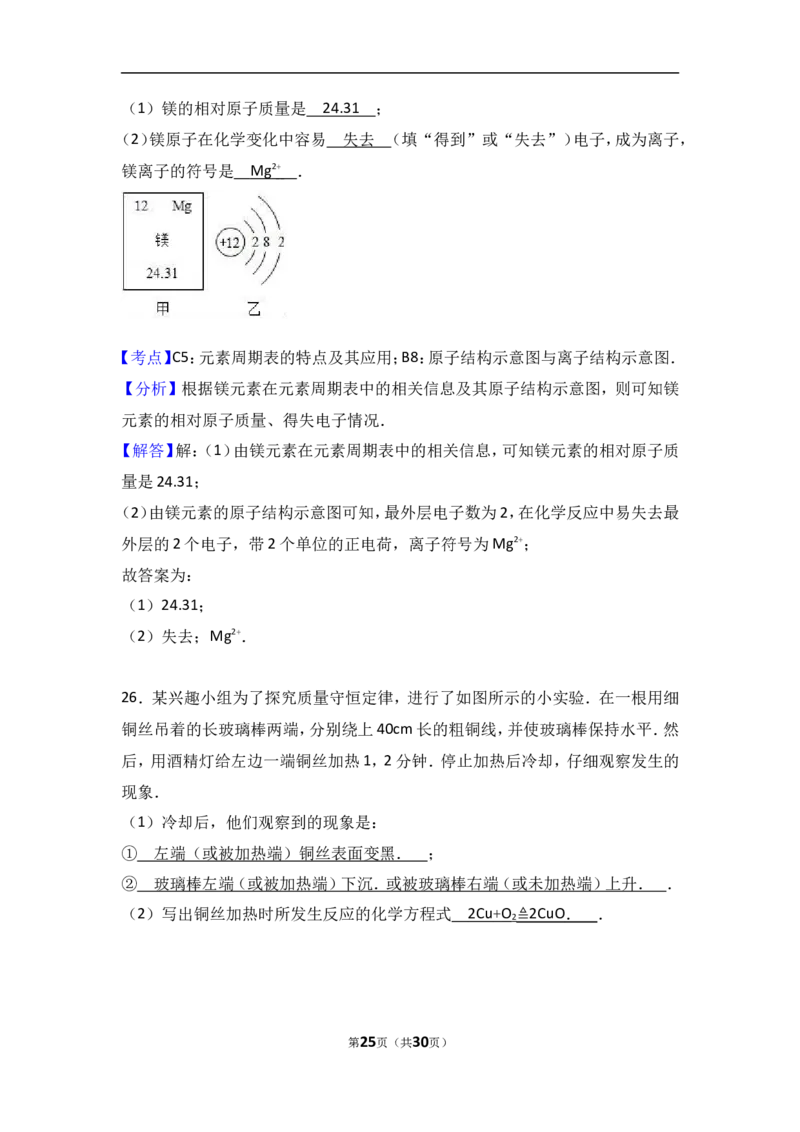
25.如图甲、乙所示是镁元素在元素周期表中的信息和镁原子的结构示意图,根
据图示回答:
(1)镁的相对原子质量是 ;
(2)镁原子在化学变化中容易 (填“得到”或“失去”)电子,成为离子,
镁离子的符号是 .
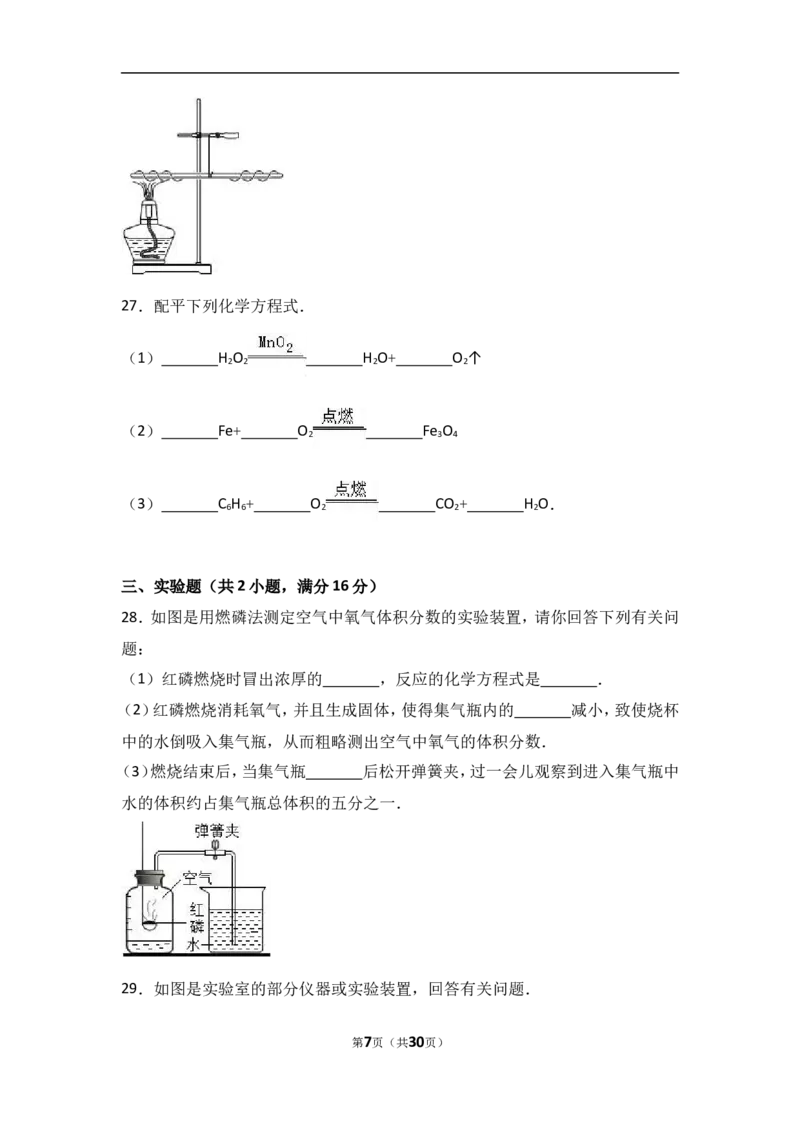
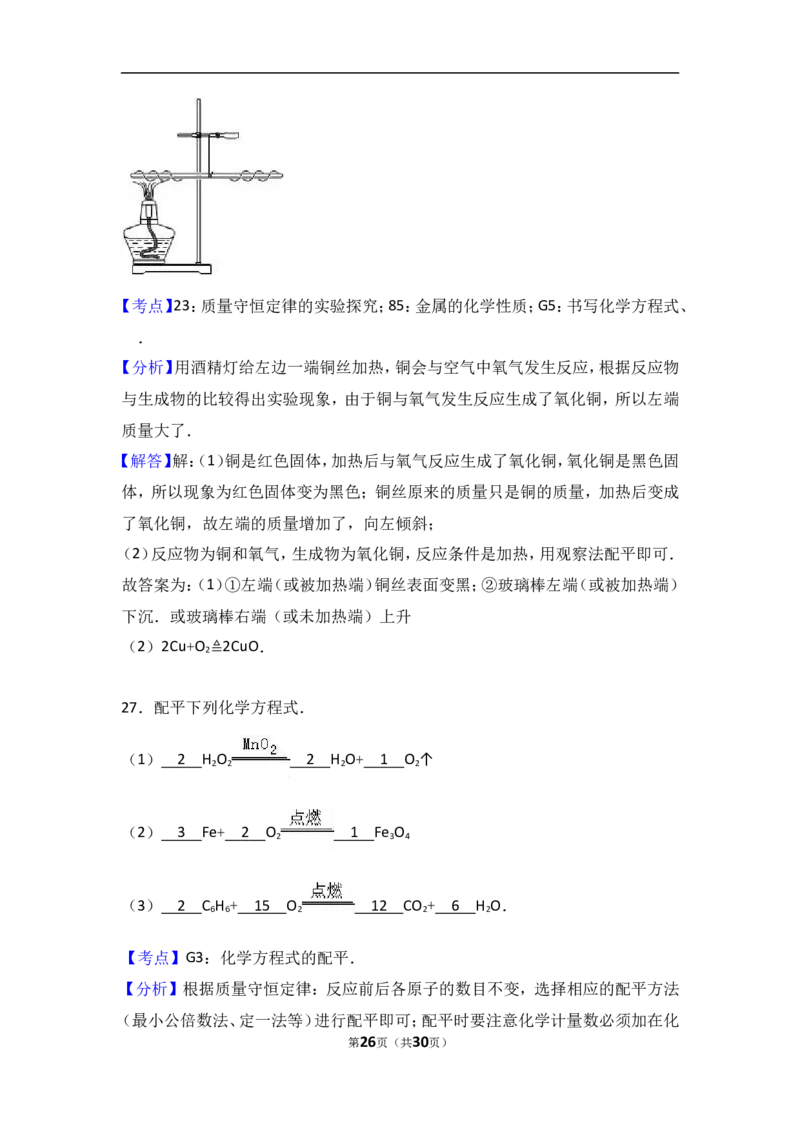
26.某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根用细
铜丝吊着的长玻璃棒两端,分别绕上40cm长的粗铜线,并使玻璃棒保持水平.然
后,用酒精灯给左边一端铜丝加热1,2分钟.停止加热后冷却,仔细观察发生的
现象.
(1)冷却后,他们观察到的现象是:
① ;
② .
(2)写出铜丝加热时所发生反应的化学方程式 .
第6页(共30页)27.配平下列化学方程式.
(1) H O H O+ O ↑
2 2 2 2
(2) Fe+ O Fe O
2 3 4
(3) C H + O CO + H O.
6 6 2 2 2
三、实验题(共2小题,满分16分)
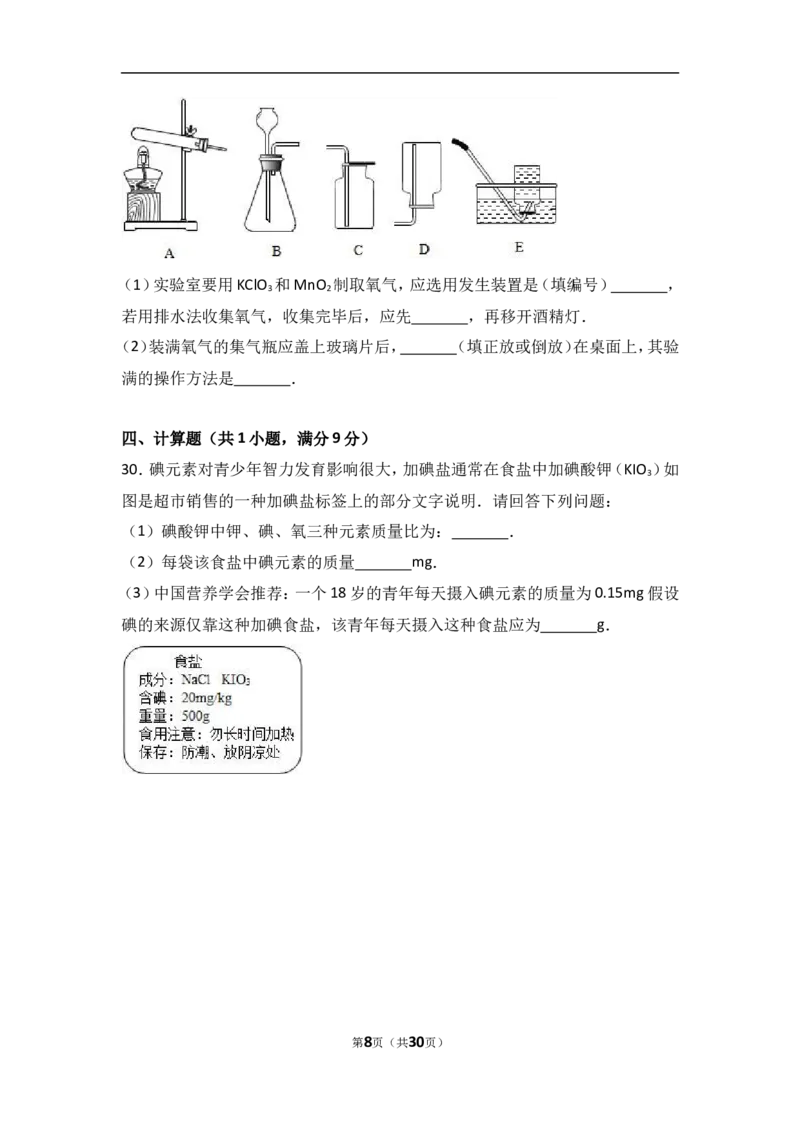
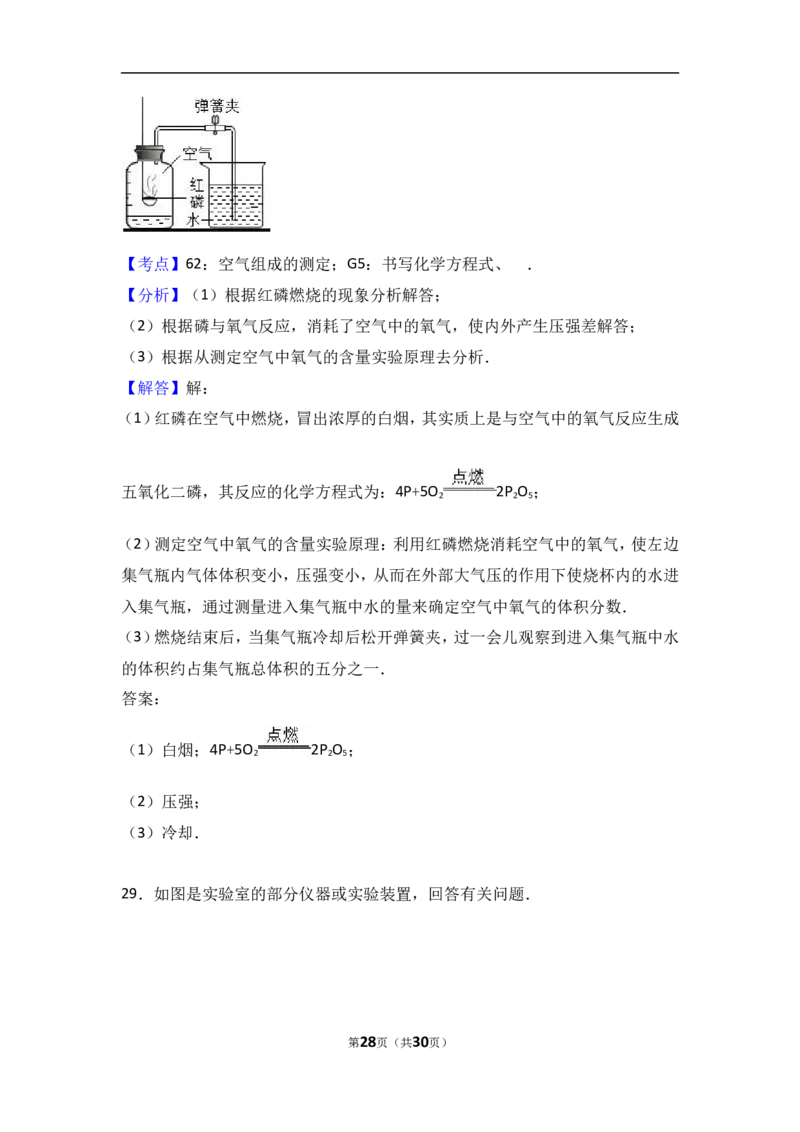
28.如图是用燃磷法测定空气中氧气体积分数的实验装置,请你回答下列有关问
题:
(1)红磷燃烧时冒出浓厚的 ,反应的化学方程式是 .
(2)红磷燃烧消耗氧气,并且生成固体,使得集气瓶内的 减小,致使烧杯
中的水倒吸入集气瓶,从而粗略测出空气中氧气的体积分数.
(3)燃烧结束后,当集气瓶 后松开弹簧夹,过一会儿观察到进入集气瓶中
水的体积约占集气瓶总体积的五分之一.
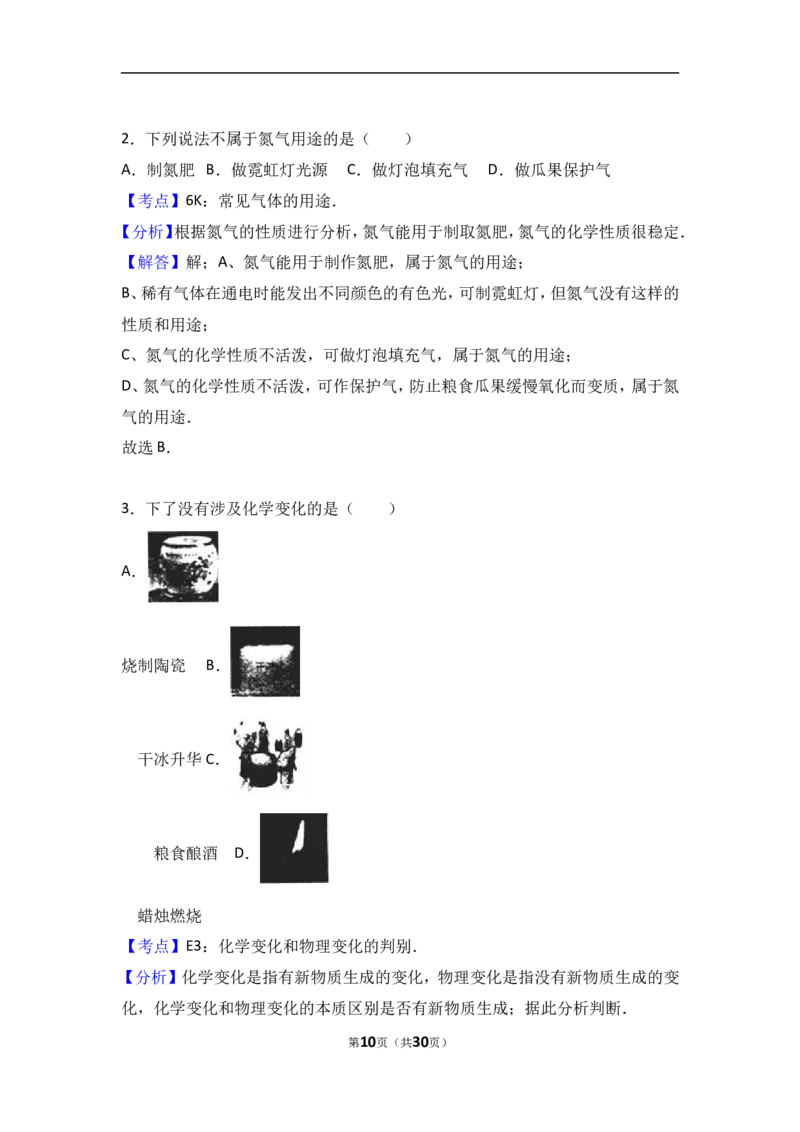
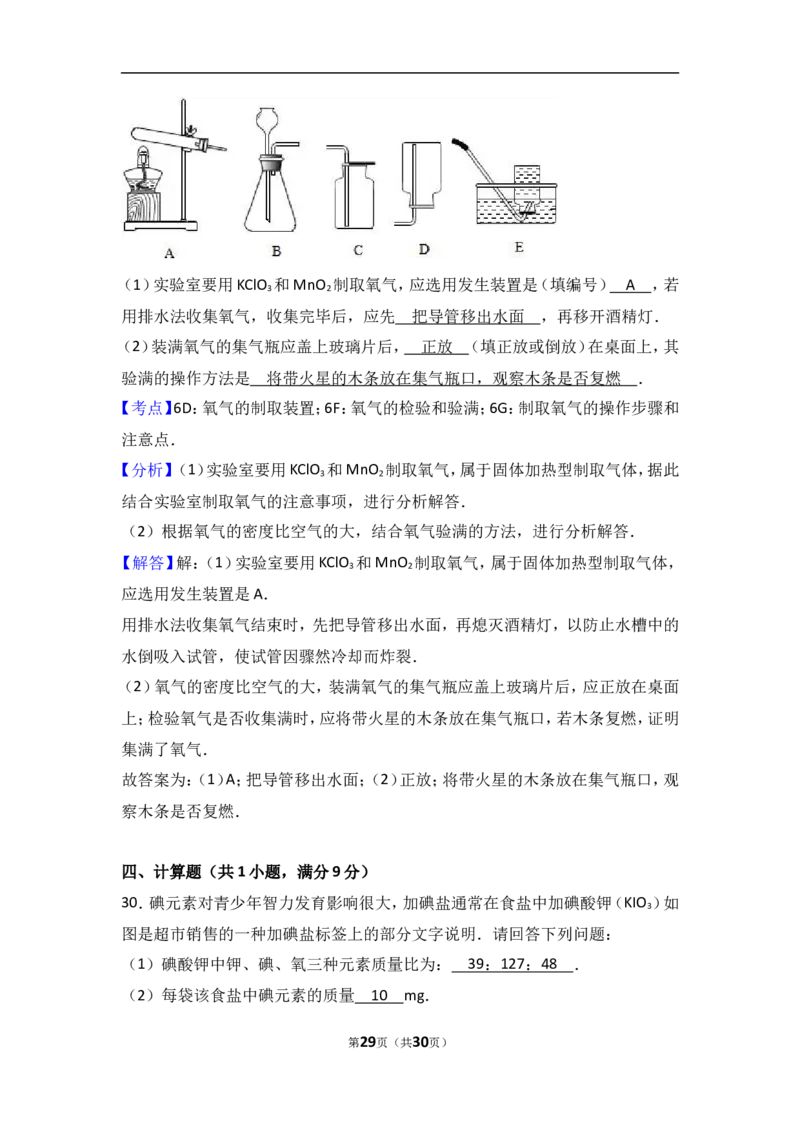
29.如图是实验室的部分仪器或实验装置,回答有关问题.
第7页(共30页)(1)实验室要用KClO 和MnO 制取氧气,应选用发生装置是(填编号) ,
3 2
若用排水法收集氧气,收集完毕后,应先 ,再移开酒精灯.
(2)装满氧气的集气瓶应盖上玻璃片后, (填正放或倒放)在桌面上,其验
满的操作方法是 .
四、计算题(共1小题,满分9分)
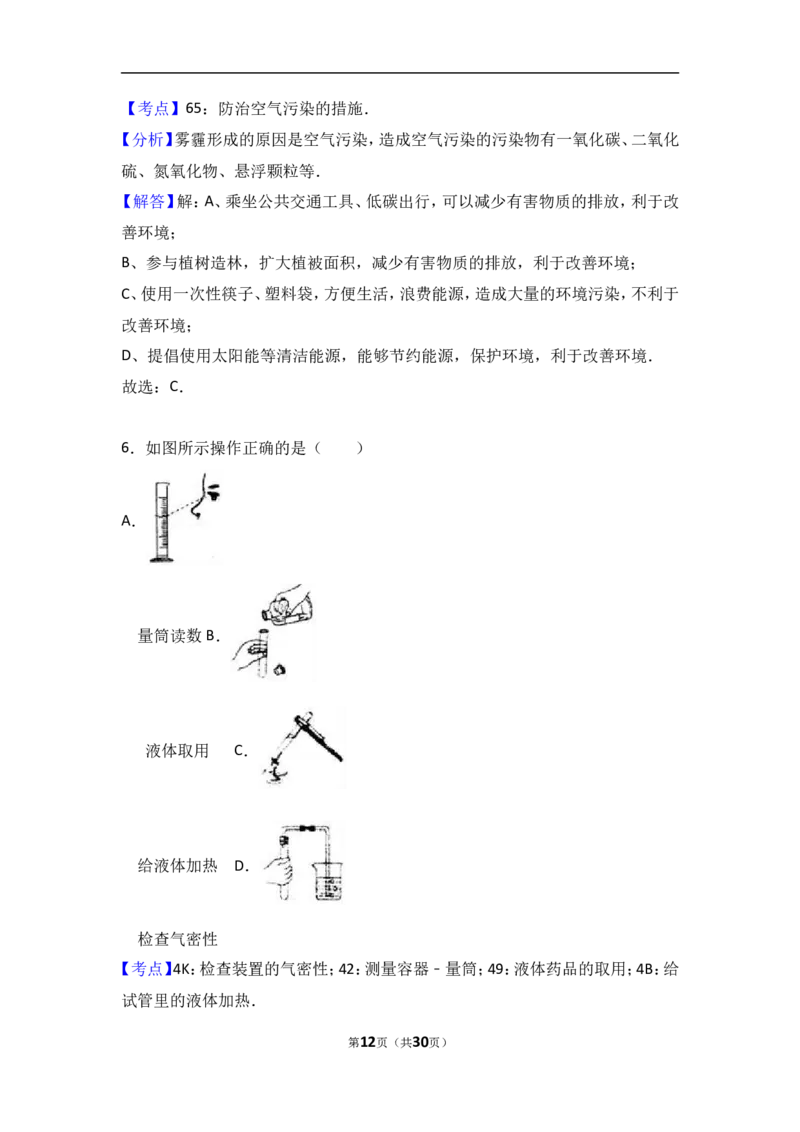
30.碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO )如
3
图是超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题:
(1)碘酸钾中钾、碘、氧三种元素质量比为: .
(2)每袋该食盐中碘元素的质量 mg.
(3)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg假设
碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为 g.
第8页(共30页)2017-2018 学年河北省邯郸市馆陶县九年级(上)期中化
学试卷
参考答案与试题解析
一、选择题(共20小题,每小题2分,满分40分)
1.我们生活在多姿多彩的物质世界里,下列关于化学物质的说法正确的是
( )
A.垃圾是“放错了地方的资源”,蕴藏着巨大的能量
B.大量使用化肥和农药是粮食增产的主要方法
C.某饮料中绝对不含化学物质
D.气功可以使铝变成金
【考点】G1:质量守恒定律及其应用;K6:合理使用化肥、农药对保护环境的重要
意义.
【分析】A、根据垃圾回收再利用的情况回答;
B、大量使用化肥和农药会造成水资源的污染;
C、自然界中的任何物质都可以说由化学物质组成;
D、根据质量守恒定律进行分析.
【解答】解:A、现在垃圾回收利用的方法很多,如焚烧垃圾发电等,垃圾回收再利
用,不但可保护环境,而且还节约资源,所以说“垃圾是放错了地方的资源”,故
正确;
B、大量使用化肥和农药会造成水资源的污染,所以应该适量使用化肥和农药以
使粮食增产,故错误;
C、本饮料中绝对不含化学物质,说法错误,因为任何物质都可以说由化学物质组
成,故错误;
D、气功可以使铝变成金,说法错误,因为铝由铝元素组成,金由金元素组成,根据
质量守恒定律可知,二者不能相互转化,故错误.
故选A.
第9页(共30页)2.下列说法不属于氮气用途的是( )
A.制氮肥 B.做霓虹灯光源 C.做灯泡填充气 D.做瓜果保护气
【考点】6K:常见气体的用途.
【分析】根据氮气的性质进行分析,氮气能用于制取氮肥,氮气的化学性质很稳定.
【解答】解;A、氮气能用于制作氮肥,属于氮气的用途;
B、稀有气体在通电时能发出不同颜色的有色光,可制霓虹灯,但氮气没有这样的
性质和用途;
C、氮气的化学性质不活泼,可做灯泡填充气,属于氮气的用途;
D、氮气的化学性质不活泼,可作保护气,防止粮食瓜果缓慢氧化而变质,属于氮
气的用途.
故选B.
3.下了没有涉及化学变化的是( )
A.
烧制陶瓷 B.
干冰升华C.
粮食酿酒 D.
蜡烛燃烧
【考点】E3:化学变化和物理变化的判别.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
第10页(共30页)【解答】解:A、烧制陶瓷过程中有新物质生成,属于化学变化.
B、干冰升华过程中只是状态发生改变,没有新物质生成,属于物理变化.
C、粮食酿酒过程中有新物质酒精生成,属于化学变化.
D、蜡烛燃烧过程中有新物质二氧化碳生成,属于化学变化.
故选B.
4.下到有关水的说法不正确的是( )
A.水是由水分子构成的
B.电解水的实验中,得到的氢气与氧气体积比为1:2
C.过滤、吸附、蒸馏、消毒等都是常用的净水方法
D.地球上的水储量是丰富的,但可供利用的淡水资源是有限的
【考点】71:电解水实验;75:水的净化;78:水资源状况;B2:分子、原子、离子、元
素与物质之间的关系.
【分析】A、根据水的构成进行解答;
B、根据电解水的实验中,得到的氢气与氧气体积比为2:1进行解答;
C、根据常用的净水方法进行解答;
D、根据水资源的分布进行解答.
【解答】解:A、水是由水分子构成的,故A正确;
B、电解水的实验中,得到的氢气与氧气体积比为2:1,而不是1:2,故B错误;
C、常用的净水方法:过滤、吸附、蒸馏、消毒,故C正确;
D、地球上的水储量是丰富的,但可供利用的淡水资源是有限的,且分布不均,所
以我们要节约用水,故D正确.
故选:B.
5.近年来,我国采取了汽车限行等多种措施减少雾霾的产生,下列措施不利于改
善环境的是( )
A.乘坐公共交通工具、低碳出行
B.参与植树造林,扩大植被面积
C.经常使用一次性筷子、塑料袋等方便生活
D.提倡使用太阳能等清洁能源
第11页(共30页)【考点】65:防治空气污染的措施.
【分析】雾霾形成的原因是空气污染,造成空气污染的污染物有一氧化碳、二氧化
硫、氮氧化物、悬浮颗粒等.
【解答】解:A、乘坐公共交通工具、低碳出行,可以减少有害物质的排放,利于改
善环境;
B、参与植树造林,扩大植被面积,减少有害物质的排放,利于改善环境;
C、使用一次性筷子、塑料袋,方便生活,浪费能源,造成大量的环境污染,不利于
改善环境;
D、提倡使用太阳能等清洁能源,能够节约能源,保护环境,利于改善环境.
故选:C.
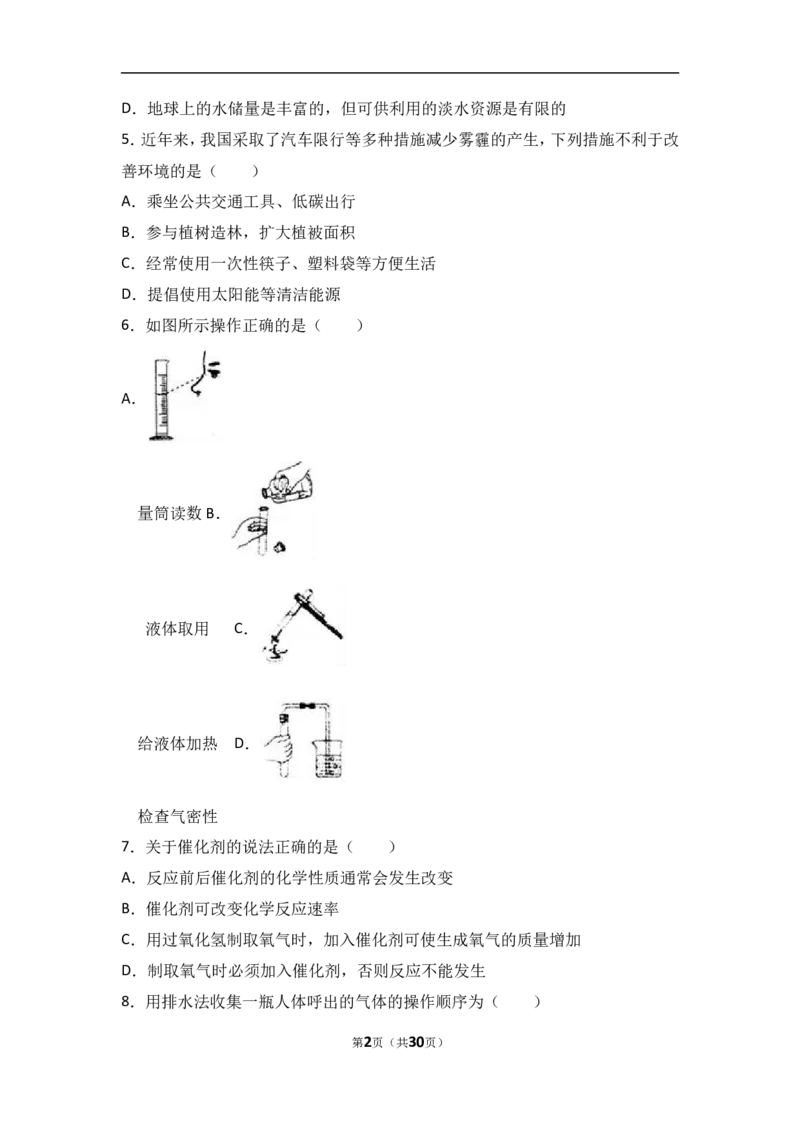
6.如图所示操作正确的是( )
A.
量筒读数B.
液体取用 C.
给液体加热 D.
检查气密性
【考点】4K:检查装置的气密性;42:测量容器﹣量筒;49:液体药品的取用;4B:给
试管里的液体加热.
第12页(共30页)【分析】A、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断;
B、根据液体药品的取用方法进行分析判断;
C、根据给试管中的液体加热的方法进行分析判断;
D、根据检查装置气密性的方法进行分析判断.
【解答】解:A、量取液体时,视线与液体的凹液面最低处保持水平,图中所示操作
错误;
B、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示
操作错误;
C、给液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管
容积的 ,图中所示操作错误;
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导
管口有气泡冒出,装置不漏气,图中所示操作正确.
故选:D.
7.关于催化剂的说法正确的是( )
A.反应前后催化剂的化学性质通常会发生改变
B.催化剂可改变化学反应速率
C.用过氧化氢制取氧气时,加入催化剂可使生成氧气的质量增加
D.制取氧气时必须加入催化剂,否则反应不能发生
【考点】6J:催化剂的特点与催化作用.
【分析】在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性
质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点可
以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化
学性质在化学反应前后保持不变.
【解答】解:A、反应前后催化剂的化学性质不会发生改变,故选项错误.
B、催化剂能改变其他物质的化学反应速率,催化剂能加快化学反应速率,但本身
的化学性质不变,故选项说法正确.
C、催化剂只能改变化学反应速率,对生成物的质量无影响,使用催化剂不能增加
生成物的质量,故选项说法错误.
第13页(共30页)D、制取氧气时不是必须加入催化剂,如过氧化氢常温下就能分解制取氧气,故选
项说法错误.
故选:B.
8.用排水法收集一瓶人体呼出的气体的操作顺序为( )
①将饮水管小心地插入集气瓶内,并向集气瓶内缓缓吹气,直到集气瓶充满呼出
的气体;
②把盛满水的集气瓶连同玻璃片一起倒立在水槽内;
③将集气瓶盛满水,用玻璃片先盖住瓶口的一部分,然后推动玻璃片将瓶口全部
盖住;
④在水下立即用玻璃片将集气瓶的瓶口盖好,然后取出集气瓶放在桌上.
A.①②③④B.②③①④C.③②①④D.④③②①
【考点】56:吸入空气与呼出气体的比较.
【分析】根据排水法收集人体呼出的气体的操作方法,进行分析判断即可.
【解答】解:用排水法收集一瓶人体呼出的气体时,首先将集气瓶装满水,用玻璃
片先盖住瓶口的一小部分,然后推动玻璃片将瓶口全部盖住,然后把盛满水的集
气瓶连同玻璃片倒放在水槽中,将饮料管小心地插入集气瓶内,并向集气瓶内缓
缓吹气,直到集气瓶内充满呼出的气体,然后在水下立即用玻璃片将集气瓶的瓶
口盖好,取出集气瓶正放在桌上即可.故操作顺序为③②①④.
故选:C.
9.下列生活中的变化不属于缓慢氧化的是( )
A.木柴的燃烧 B.菜刀生锈
C.人在长跑时急促呼吸D.农家肥料的腐熟
【考点】H6:燃烧、爆炸、缓慢氧化与自燃.
【分析】根据缓慢氧化的概念进行分析解答,缓慢氧化是指反应进行的很缓慢,甚
至不容易被察觉的氧化反应.
【解答】解:A、木柴的燃烧是剧烈的氧化反应,不属于缓慢氧化,故选项正确.
B、菜刀生锈,实际是金属与空气中的氧气和水等共同作用,发生缓慢氧化所致,
故选项错误.
第14页(共30页)C、人在长跑时急促呼吸的过程反应缓慢,不容易察觉,属于缓慢氧化,故选项错
误.
D、农家肥料的腐熟,是肥料与空气中的氧气发生的不容易察觉的缓慢氧化,故选
项错误.
故选:A.
10.三瓶无色气体分别是氧气、空气、二氧化碳,下列区分的方法正确的是( )
A.用带火星的木条B.用燃着的木条
C.用澄清石灰水 D.用紫色的石蕊试液
【考点】4Q:常见气体的检验与除杂方法.
【分析】区别空气、氧气和二氧化碳三瓶无色气体,要求根据三种气体性质差别,
所设计的方案能出现三种明显不同的实验现象,达到鉴别气体的目的.
【解答】解:A、用带火星的木条,只能检验出氧气,不能检验出空气、二氧化碳,故
A错误;
B、燃着的木条分别放入瓶中,燃烧无明显变化的气体为空气;燃烧更旺的气体为
氧气;燃烧熄灭的气体为二氧化碳;故B正确;
C、倒入澄清石灰水,石灰水变浑浊的气体为二氧化碳,无明显现象的为空气或氧
气.无法区别三种气体,故C错误;
D、倒入紫色石蕊试液,使溶液变红的气体为二氧化碳,无明显现象的为空气或氧
气.无法区别三种气体,故D错误;
故选B.
11.下列是四位同学对氧气的描述,你认为不正确的是( )
A.出现高原反应要及时吸氧,因为氧气能够供给呼吸
B.用含有氧元素的物质反应才有可能产生氧气
C.在压强101kPa,氧气在﹣183℃变为无色的液体
D.氧气是性质比较活泼的气体,具有氧化性
【考点】68:氧气的化学性质;67:氧气的物理性质;69:氧气的用途.
【分析】常情况下,氧气是一种无色、无味的气体,常压下,熔点为﹣183℃,液氧是
淡蓝色液体;氧气的化学性质很活泼,在一定条件下,能与很多物质反应;氧气难
第15页(共30页)溶于水.
【解答】解:A、出现高原反应要及时吸氧,因为氧气能够供给呼吸,正确;
B、用含有氧元素的物质反应才有可能产生氧气,正确;
C、在压强101kPa,氧气在﹣183℃变为淡蓝色的液体,错误;
D、氧气是性质比较活泼的气体,具有氧化性,正确;
故选C
12.下列化学方程式书写正确的是( )
A.S+O =SO B.Cu+O CuO
2 2 2
C.2Al+O 2AlO D.4P+5O 2P O
2 2 2 5
【考点】G5:书写化学方程式、 .
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书
写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】解:A、该化学方程式缺乏反应条件,正确的化学方程式应为S+O
2
SO .
2
B、该化学方程式没有配平,正确的化学方程式为:2Cu+O 2CuO.
2
C、铝与氧气在点燃条件下生成氧化铝,该化学方程式中氧化铝的化学式书写错
误,正确的化学方程式应为:4Al+3O 2Al O .
2 2 3
D、该化学方程式书写完全正确.
故选D.
13.同学们对化学反应方程式:C+O CO 有下面的四种说法,其中错误的
2 2
是( )
第16页(共30页)A. B. C .
D.
【考点】G2:化学方程式的概念、读法和含义;A3:从组成上识别氧化物;A7:单质
和化合物的判别.
【分析】化学方程式可表示:反应物和生成物的种类;反应的条件;反应物和生成
物的微观粒子个数比;反应物和生成物的质量比等;据此结合单质、氧化物、质量
守恒定律等进行分析判断即可.
【解答】解:A、由化学反应方程式:C+O CO 可知,生成物二氧化碳是气体,
2 2
故选项说法正确.
B、由化学反应方程式:C+O CO 可知,反应条件是点燃,故选项说法正确.
2 2
C、由质量守恒定律,反应前后质量之和不变,生成物的质量等于参加反应的反应
物的质量之和,故选项说法错误.
D、由化学反应方程式:C+O CO 可知,参加反应的物质为碳和氧气,均是
2 2
由一种元素组成的纯净物,均为单质;生成物是二氧化碳由两种元素组成且有一
种是氧元素,属于氧化物;故选项说法正确.
第17页(共30页)故选C.
14.化学反应遵守质量守恒定律的原因是( )
A.物质的种类没有改变
B.分子的种类没有改变
C.分子的数目没有改变
D.原子的种类、数目、质量都没改变
【考点】G1:质量守恒定律及其应用.
【分析】从化学反应的实质入手,化学变化的实质是分子分成原子,原子再重新组
合成新的分子,所以反应前后原子的种类、数目、质量都不变.
【解答】解:A、如果物质种类没有改变的话,就不能是化学变化了,所以物质的种
类一定变;
B、如果分子的种类没有改变的话,也不属于化学变化了,所以分子的种类也一定
变;
C、分子的数目可能变,可能不变,所以C是错误的.
D、化学反应前后六个不变:原子的种类、数目、质量、元素种类、质量、物质总质
量.所以D是正确的.
故选D.
15.2017年8月8日晚,四川九寨沟发生7.0级地震,震后当地水质发生变化,为
了饮用安全,下列做法错误的是( )
A.可以用活性炭去除水中的异味
B.用过滤的方法净化后可以直接饮用
C.家庭生活中加热煮沸后再饮用
D.要对饮用水进行适当的消毒杀菌
【考点】77:硬水与软水;4G:过滤的原理、方法及其应用.
【分析】A、根据活性炭的吸附作用进行分析;
B、根据过滤的原理进行分析;
C、根据煮沸的过程中除了杀菌、消毒外还能起到降低水的硬度进行分析;
D、根据水的成分进行分析.
第18页(共30页)【解答】解:A、活性炭具有吸附性,能吸附色素和异味,用活性炭可除去水中的色
素和异味,故A正确;
B、过滤是分离不溶性固体和液体的一种方法,用过滤的方法不能除去水中可溶
的钙、镁化合物以及重金属离子,故B不正确;
C、水在烧开、煮沸的过程中除了杀菌、消毒外还能起到降低水的硬度的作用,故C
正确;
D、饮用水中含有有害细菌或病毒等,要对饮用水进行适当的消毒杀菌,故D正确
故选B.
16.下列各项,在化学变化前后,肯定没有变化的是( )
①原子数目 ②分子数目 ③元素种类 ④物质的总质量 ⑤物质的种类.
A.①④B.①③④ C.①③⑤ D.①③④⑤
【考点】G1:质量守恒定律及其应用.
【分析】根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反
应后生成各物质的质量总和.化学反应的过程,就是参加反应的各物质(反应物)
的原子,重新组合而生成其他物质的过程.在化学反应中,反应前后原子的种类
没有改变,数目没有增减,原子的质量也没有改变.
【解答】解:分子分成原子所以分子种类一定发生了变化,分子种类变了,物质的
种类也就发生了变化,原子进行重新组合,所以原子的种类、数目、质量都没有发
生变化,原子的种类不变,元素的种类也不会发生变化,由于分子种类发生了变
化,分子的数目可能变了,可能没变.
故选:B.
17.下列现象能用质量守恒定律解释的是( )
A.水结冰前后质量不变
B.1升芝麻和1升大米混合,总体积小于2升
C.在加压降温的条件下,氧气变为淡蓝色液体
D.氧化钙与水反应生成氢氧化钙,反应前后物质的总质量不变
【考点】G1:质量守恒定律及其应用.
【分析】根据质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用
第19页(共30页)于化学变化;物质发生物理变化,则不适用于质量守恒定律来解释进行分析.
【解答】解:A、水结成冰后质量不变,没有新物质生成,属于物理变化,不能用质
量守恒定律解释,故A错误;
B、1升芝麻和1升大米混合,总体积小于2升,是由芝麻和大米的间隔不同,不属
于化学变化,不能用质量守恒定律解释,故B错误;
C、在降温加压条件下,氧气变为淡蓝色液体,属于物理变化,不能用质量守恒定
律解释,故C错误;
D、氧化钙与水反应生成氢氧化钙属于化学变化,能用质量守恒定律来解释,故D
正确.
故选:D.
18.下列物质中含有氧气的是( )
A.水 B.氯酸钾 C.液态空气D.过氧化氢
【考点】61:空气的成分及各成分的体积分数;A5:纯净物和混合物的判别.
【分析】化合物中含有的是氧元素,含有氧气的物质中还含有其它物质,属于混合
物.
【解答】解:A、水中含有氢元素和氧元素,不含有氧气,故A错;
B、氯酸钾中含有氯元素、钾元素、氧元素,不含有氧气,故B错;
C、液态空气中含有氧气、氮气、二氧化碳等物质,属于混合物,故C正确;
D、过氧化氢中含有氢元素和氧元素,不含有氧气,故D错.
故选C.
19.科学家发现,在液晶电视等制造过程中使用的三氟化氮(NF )的温室效应是
3
二氧化碳的1.7万倍.NF 中氟元素为﹣1价,则氮元素的化合价是( )
3
A.﹣3 B.0C.+1 D.+3
【考点】D6:有关元素化合价的计算.
【分析】根据在化合物中正负化合价代数和为零,结合三氟化氮的化学式进行解
答本题.
【解答】解:氟元素显﹣1价,设氮元素的化合价是x,根据在化合物中正负化合价
代数和为零,可得:x+(﹣1)×3=0,则x=+3.
第20页(共30页)故选D.
20.奶奶在小商贩那里买到一个银手镯,小红认为它可能是假的,准备先拿磁铁
来吸一下.就拿磁铁来吸一下这一过程而言,属于科学探索中的( )
A.假设B.实验 C.观察D.做出结论
【考点】14:科学探究的基本环节.
【分析】科学探究的主要环节有提出问题→猜想与假设→制定计划(或设计方案)
→进行实验→收集证据→解释与结论→反思与评价→拓展与迁移,据此结合题意
进行分析判断.
【解答】解:A、“拿磁铁来吸一下”这一过程,属于科学探究中的实验,而不是假
设,故选项错误.
B、“拿磁铁来吸一下”这一过程,属于科学探究中的实验,故选项正确.
C、“拿磁铁来吸一下”这一过程,属于科学探究中的实验,而不是观察,故选项
错误.
D、“拿磁铁来吸一下”这一过程,属于科学探究中的实验,而不是做出结论,故
选项错误.
故选:B.
二、填空题(共7小题,每小题4分,满分35分)
21.用化学用语填空:
(1)一个氢原子 H ;(2)二个氮气分子 2N ;
2
(3)三个钠离子 3N a + ;(4)四氧化三铁 F e O .
3 4
【考点】DF:化学符号及其周围数字的意义.
【分析】书写元素符号时,第一个字母要大写,第二个字母要小写;化学符号周围
的数字表示不同的意义:符号前面的数字,表示原子、分子或离子的个数;右上角
的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;
元素正上方的数字表示元素的化合价.一个氢原子表示为H,二个氮气分子表示
为2N ,三个钠离子表示为3Na+,四氧化三铁表示为Fe O .
2 3 4
【解答】解:(1)符号前面的数字,表示原子、分子或离子的个数;一个氢原子表示
为H,故答案为:H;
第21页(共30页)(2)符号前面的数字,表示原子、分子或离子的个数;二个氮气分子表示为2N ,
2
故答案为:2N ;
2
(3)符号前面的数字,表示原子、分子或离子的个数;右上角的数字表示一个离子
所带的电荷数,三个钠离子表示为3Na+,故答案为:3Na+;
(4)书写元素符号时,第一个字母要大写,第二个字母要小写;四氧化三铁表示为
Fe O ,故答案为:Fe O ;
3 4 3 4
22.改正下列有错误的元素符号.
镁MG M g ,铁F F e ,铝AL A l ,硅Sl S i ,氢N H ,铜Ca Cu .
【考点】C3:元素的符号及其意义.
【分析】根据元素符号的书写进行分析,元素符号书写时第一个字母大写,第二个
字母小写,据此解答.
【解答】解:镁的元素符号是Mg,铁的元素符号是Fe,铝的元素符号是Al,硅的元
素符号是Si,氢的元素符号是H,铜的元素符号是Cu.
答案:Mg,Fe,Al,Si,H,Cu.
23.生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水.
(1)检查洲河水是硬水还是软水,可用的物质是 肥皂水 ;
(2)生活中硬水软化的方法是 煮沸 ;
(3)活性炭能除去洲河水中有颜色,有异味的物质,这是利用活性炭的 吸附
性;
(4)自来水生产过程中,分离不溶物的操作方法是 过滤 ;
(5)为保护水资源,请你提出一条防水污染的建议: 污水经处理达标后排放 .
(6)下列“水”中,属于纯净物的是 c (填序号)
a、海水 b、河水 c、蒸馏水 d、井水.
【考点】77:硬水与软水;79:水资源的污染与防治;A5:纯净物和混合物的判别;
C6:碳单质的物理性质及用途.
【分析】(1)根据用肥皂水可以鉴别硬水和软水解答;
(2)根据硬水软化的方法是蒸馏或煮沸,生活中常用的硬水软化的方法是加热煮
沸解答;
第22页(共30页)(3)根据活性炭具有吸附性解答;
(4)根据水中不溶性杂质可用过滤的方法除去;
(5)应从污水治理、文明习惯等方面入手;
(6)根据纯净物的概念进行分析;
【解答】解:
(1)用肥皂水可以鉴别硬水和软水,泡沫多的是软水,泡沫少的是硬水;
(2)硬水软化的方法是蒸馏或煮沸,生活中常用的硬水软化的方法是加热煮沸;
(3)活性炭能除去洲河水中有颜色,有异味的物质,这是利用活性炭的吸附性;
(4)来水生产过程中,分离不溶物的操作方法是过滤;
(5)护好太湖水合理的建议:污水经处理达标后排放;养成文明习惯,不往河里乱
丢垃圾;
(6)a、海水中含有水、氯化钠等物质,属于混合物.故选项错误;
b、河水中含有水和一些可溶性的物质,属于混合物,故选项错误;
c、蒸馏水是由一种物质组成的,属于纯净物.故选项正确;
d、井水中含有水和一些可溶性的物质,属于混合物,故选项错误.
故选c.
故答案为:
(1)肥皂水;
(2)加热煮沸;
(3)吸附;
(4)过滤;
(5)污水经处理达标后排放;
(6)c.
24.水是一种重要的资源.
(1)电解水实验揭示了水的组成.图1实验中得到氧气的试管是 2 (填“1”或
“2”);
第23页(共30页)(2)水在通电条件下分解的化学方程式为 2H O 2H ↑ + O ↑ ;
2 2 2
(3)海水淡化可缓解淡水资源匮乏的问题.图2为太阳能海水淡化装置示意图.
水变成水蒸气的过程中,不发生变化的是 AB (填字母序号);
A.分子质量 B.分子种类 C.分子间隔.
【考点】71:电解水实验;BA:分子的定义与分子的特性;G5:书写化学方程式、 .
【分析】(1)根据电解水时“正氧负氢、氢二氧一”分析回答;
(2)根据电解水的反应写出反应的化学方程式;
(3)根据水蒸发时水分子的变化分析判断.
【解答】解:(1)电解水实验揭示了水的组成.由图示可知,图1实验中得到氧气的
试管是2,该试管中的气体是电源的正极产生的气体;
(2)水在通电条件下分解生成了氢气和氧气,反应的化学方程式为:2H O
2
2H ↑+O ↑;
2 2
(3)水在蒸发时,水分子的质量、种类没有发生变化,分子间隔变大了.
故答为:(1)2;
(2)2H O 2H ↑+O ↑;
2 2 2
(3)AB.
25.如图甲、乙所示是镁元素在元素周期表中的信息和镁原子的结构示意图,根
据图示回答:
第24页(共30页)(1)镁的相对原子质量是 24.31 ;
(2)镁原子在化学变化中容易 失去 (填“得到”或“失去”)电子,成为离子,
镁离子的符号是 M g 2 + .
【考点】C5:元素周期表的特点及其应用;B8:原子结构示意图与离子结构示意图.
【分析】根据镁元素在元素周期表中的相关信息及其原子结构示意图,则可知镁
元素的相对原子质量、得失电子情况.
【解答】解:(1)由镁元素在元素周期表中的相关信息,可知镁元素的相对原子质
量是24.31;
(2)由镁元素的原子结构示意图可知,最外层电子数为2,在化学反应中易失去最
外层的2个电子,带2个单位的正电荷,离子符号为Mg2+;
故答案为:
(1)24.31;
(2)失去;Mg2+.
26.某兴趣小组为了探究质量守恒定律,进行了如图所示的小实验.在一根用细
铜丝吊着的长玻璃棒两端,分别绕上40cm长的粗铜线,并使玻璃棒保持水平.然
后,用酒精灯给左边一端铜丝加热1,2分钟.停止加热后冷却,仔细观察发生的
现象.
(1)冷却后,他们观察到的现象是:
① 左端(或被加热端)铜丝表面变黑. ;
② 玻璃棒左端(或被加热端)下沉.或被玻璃棒右端(或未加热端)上升. .
(2)写出铜丝加热时所发生反应的化学方程式 2Cu + O
2
≜2CuO . .
第25页(共30页)【考点】23:质量守恒定律的实验探究;85:金属的化学性质;G5:书写化学方程式、
.
【分析】用酒精灯给左边一端铜丝加热,铜会与空气中氧气发生反应,根据反应物
与生成物的比较得出实验现象,由于铜与氧气发生反应生成了氧化铜,所以左端
质量大了.
【解答】解:(1)铜是红色固体,加热后与氧气反应生成了氧化铜,氧化铜是黑色固
体,所以现象为红色固体变为黑色;铜丝原来的质量只是铜的质量,加热后变成
了氧化铜,故左端的质量增加了,向左倾斜;
(2)反应物为铜和氧气,生成物为氧化铜,反应条件是加热,用观察法配平即可.
故答案为:(1)①左端(或被加热端)铜丝表面变黑;②玻璃棒左端(或被加热端)
下沉.或玻璃棒右端(或未加热端)上升
(2)2Cu+O 2≜2CuO.
27.配平下列化学方程式.
(1) 2 H O 2 H O+ 1 O ↑
2 2 2 2
(2) 3 Fe+ 2 O 1 Fe O
2 3 4
(3) 2 C H + 1 5 O 1 2 CO + 6 H O.
6 6 2 2 2
【考点】G3:化学方程式的配平.
【分析】根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法
(最小公倍数法、定一法等)进行配平即可;配平时要注意化学计量数必须加在化
第26页(共30页)学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整
数.
【解答】解:(1)本题可利用“定一法”进行配平,把H O 的化学计量数定为1,则
2 2
H O、O 前面的化学计量数分别为:1、 ,同时扩大2倍,则H O 、H O、O 前面的
2 2 2 2 2 2
化学计量数分别为2、2、1.
(2)利用最小公倍数法进行配平,以氧原子作为配平的起点,O 、Fe O 前面的化
2 3 4
学计量数分别为:2、1,最后调整Fe前面的化学计量数为3.
(3)本题可利用“定一法”进行配平,把C H 的化学计量数定为1,则O 、CO 、
6 6 2 2
H O前面的化学计量数分别为: 、6、3,同时扩大2倍,则C H 、O 、CO 、H O前
2 6 6 2 2 2
面的化学计量数分别为2、15、12、6.
故答案为:
(1)2、2、1;
(2)3、2、1;
(3)2、15、12、6.
三、实验题(共2小题,满分16分)
28.如图是用燃磷法测定空气中氧气体积分数的实验装置,请你回答下列有关问
题:
(1)红磷燃烧时冒出浓厚的 白烟 ,反应的化学方程式是 4P + 5O
2
2P O .
2 5
(2)红磷燃烧消耗氧气,并且生成固体,使得集气瓶内的 压强 减小,致使烧杯
中的水倒吸入集气瓶,从而粗略测出空气中氧气的体积分数.
(3)燃烧结束后,当集气瓶 冷却 后松开弹簧夹,过一会儿观察到进入集气瓶
中水的体积约占集气瓶总体积的五分之一.
第27页(共30页)【考点】62:空气组成的测定;G5:书写化学方程式、 .
【分析】(1)根据红磷燃烧的现象分析解答;
(2)根据磷与氧气反应,消耗了空气中的氧气,使内外产生压强差解答;
(3)根据从测定空气中氧气的含量实验原理去分析.
【解答】解:
(1)红磷在空气中燃烧,冒出浓厚的白烟,其实质上是与空气中的氧气反应生成
五氧化二磷,其反应的化学方程式为:4P+5O 2P O ;
2 2 5
(2)测定空气中氧气的含量实验原理:利用红磷燃烧消耗空气中的氧气,使左边
集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进
入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数.
(3)燃烧结束后,当集气瓶冷却后松开弹簧夹,过一会儿观察到进入集气瓶中水
的体积约占集气瓶总体积的五分之一.
答案:
(1)白烟;4P+5O 2P O ;
2 2 5
(2)压强;
(3)冷却.
29.如图是实验室的部分仪器或实验装置,回答有关问题.
第28页(共30页)(1)实验室要用KClO 和MnO 制取氧气,应选用发生装置是(填编号) A ,若
3 2
用排水法收集氧气,收集完毕后,应先 把导管移出水面 ,再移开酒精灯.
(2)装满氧气的集气瓶应盖上玻璃片后, 正放 (填正放或倒放)在桌面上,其
验满的操作方法是 将带火星的木条放在集气瓶口,观察木条是否复燃 .
【考点】6D:氧气的制取装置;6F:氧气的检验和验满;6G:制取氧气的操作步骤和
注意点.
【分析】(1)实验室要用KClO 和MnO 制取氧气,属于固体加热型制取气体,据此
3 2
结合实验室制取氧气的注意事项,进行分析解答.
(2)根据氧气的密度比空气的大,结合氧气验满的方法,进行分析解答.
【解答】解:(1)实验室要用KClO 和MnO 制取氧气,属于固体加热型制取气体,
3 2
应选用发生装置是A.
用排水法收集氧气结束时,先把导管移出水面,再熄灭酒精灯,以防止水槽中的
水倒吸入试管,使试管因骤然冷却而炸裂.
(2)氧气的密度比空气的大,装满氧气的集气瓶应盖上玻璃片后,应正放在桌面
上;检验氧气是否收集满时,应将带火星的木条放在集气瓶口,若木条复燃,证明
集满了氧气.
故答案为:(1)A;把导管移出水面;(2)正放;将带火星的木条放在集气瓶口,观
察木条是否复燃.
四、计算题(共1小题,满分9分)
30.碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO )如
3
图是超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题:
(1)碘酸钾中钾、碘、氧三种元素质量比为: 3 9 : 12 7 : 4 8 .
(2)每袋该食盐中碘元素的质量 1 0 mg.
第29页(共30页)(3)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg假设
碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为 7. 5 g.
【考点】DE:标签上标示的物质成分及其含量;D9:元素质量比的计算.
【分析】(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之
比,进行分析解答.
(2)根据题意,含碘:20mg/kg,每袋的质量为500g,据此进行分析解答.
(3)根据题意,一个18岁的青年每天摄入碘素的质量为0.15mg,假设碘的来源仅
靠这种加碘食盐,据此进行分析解答.
【解答】解:(1)碘酸钾中钾元素、碘元素、氧元素的质量比是39:127:(16×3)
=39:127:48.
(2)含碘:20mg/kg,每袋的质量为 500g,则每袋该食盐中碘元素的质量为
20mg× =10mg.
(3)根据题意,一个18岁的青年每天摄入碘元素的质量为0.15mg,该加碘盐含碘
元素20mg/kg,该青年每天摄入这种食盐应为0.15mg÷20mg∕kg=0.0075kg=7.5g.
故答案为:(1)39:127:48;(2)10mg;(3)7.5.
第30页(共30页)