文档内容
第17讲 溶液的浓度
(满分50分,限时40分钟)
一、选择题(每小题2分,共16分)
1.将50 g 98%的浓硫酸溶于450 g水中,所得溶液中溶质的质量分数为(A)(导学号
58504335)
A.9.8% B.10.2% C.10.8% D.19.6%
2.(2017,滨州)欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液,下列
说法正确的是(D)
A.过滤时,用玻璃棒搅拌加快过滤速度
B.蒸发时,待蒸发皿中晶体全部析出后停止加热
C.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
D.配制溶液需要经过计算、称量、溶解、装瓶存放等步骤
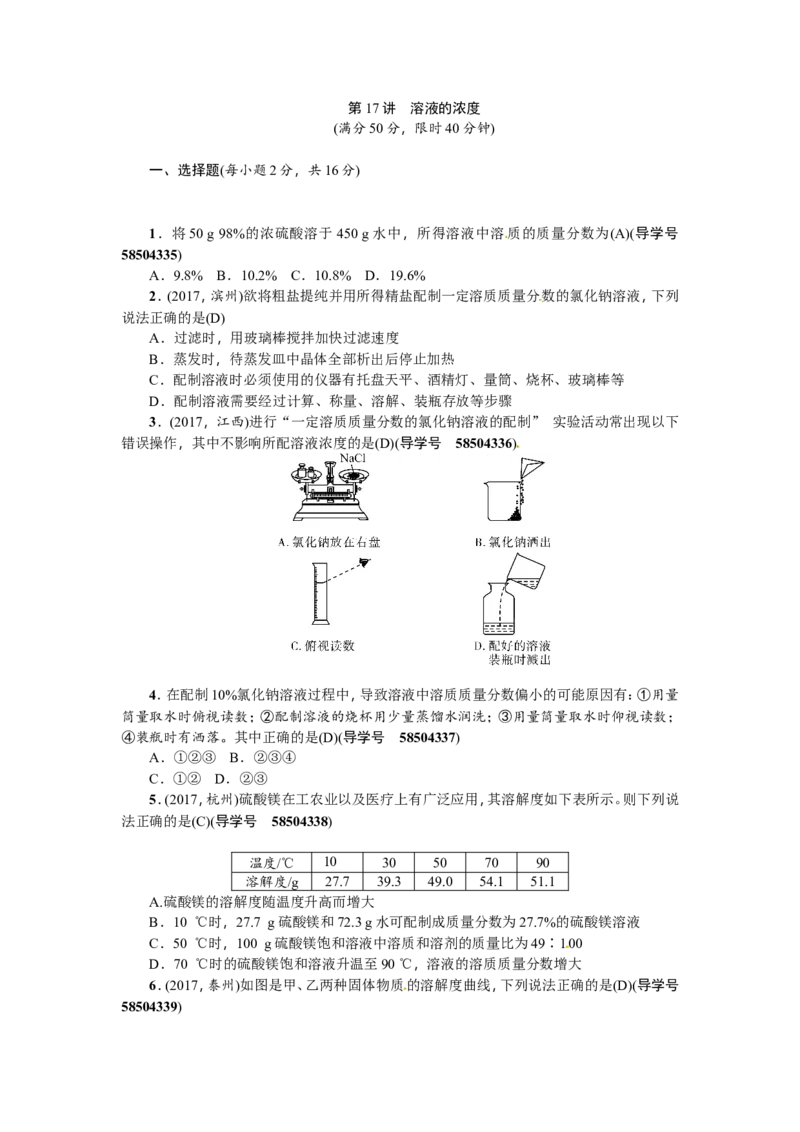
3.(2017,江西)进行“一定溶质质量分数的氯化钠溶液的配制” 实验活动常出现以下
错误操作,其中不影响所配溶液浓度的是(D)(导学号 58504336)
4.在配制10%氯化钠溶液过程中,导致溶液中溶质质量分数偏小的可能原因有:①用量
筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③用量筒量取水时仰视读数;
④装瓶时有洒落。其中正确的是(D)(导学号 58504337)
A.①②③ B.②③④
C.①② D.②③
5.(2017,杭州)硫酸镁在工农业以及医疗上有广泛应用,其溶解度如下表所示。则下列说
法正确的是(C)(导学号 58504338)
温度/℃ 10 30 50 70 90
[来源:学科网
ZXXK]
溶解度/g 27.7 39.3 49.0 54.1 51.1
A.硫酸镁的溶解度随温度升高而增大
B.10 ℃时,27.7 g硫酸镁和72.3 g水可配制成质量分数为27.7%的硫酸镁溶液
C.50 ℃时,100 g硫酸镁饱和溶液中溶质和溶剂的质量比为49∶100
D.70 ℃时的硫酸镁饱和溶液升温至90 ℃,溶液的溶质质量分数增大
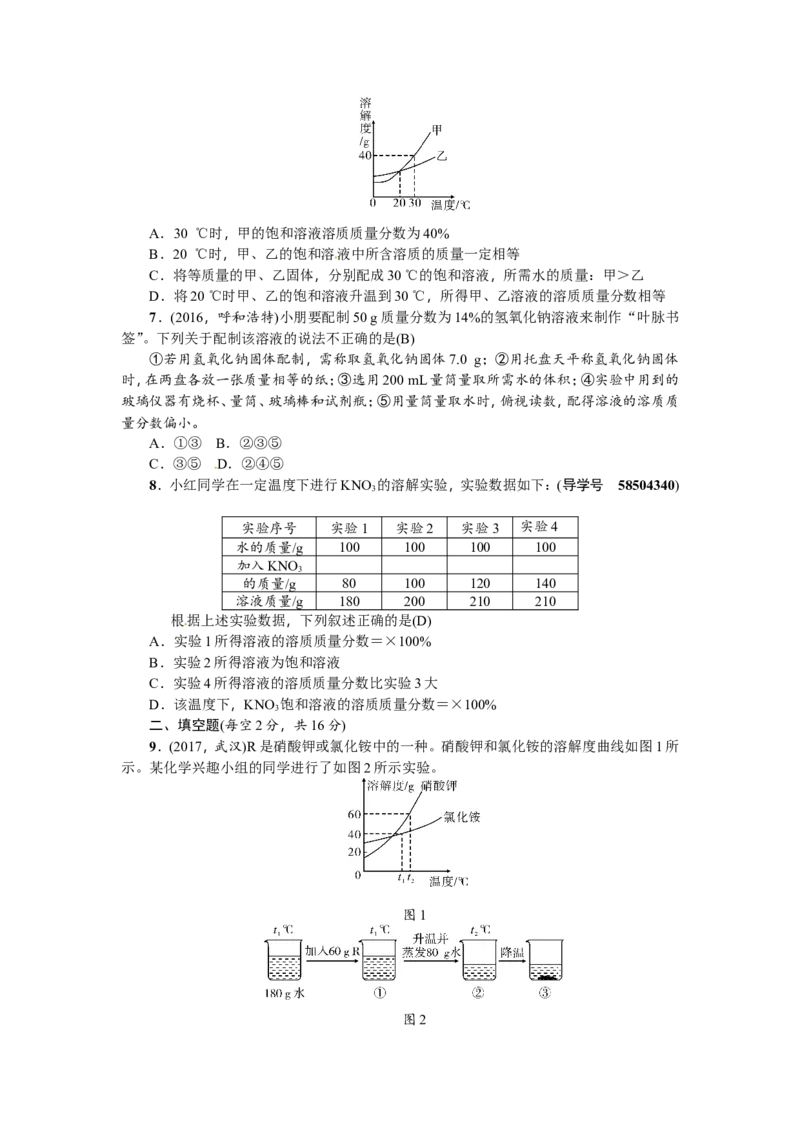
6.(2017,泰州)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是(D)(导学号
58504339)A.30 ℃时,甲的饱和溶液溶质质量分数为40%
B.20 ℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C.将等质量的甲、乙固体,分别配成30 ℃的饱和溶液,所需水的质量:甲>乙
[来源:学*科*网Z*X*X*K]
D.将20 ℃时甲、乙的饱和溶液升温到30 ℃,所得甲、乙溶液的溶质质量分数相等
7.(2016,呼和浩特)小朋要配制50 g质量分数为14%的氢氧化钠溶液来制作“叶脉书
签”。下列关于配制该溶液的说法不正确的是(B)
①若用氢氧化钠固体配制,需称取氢氧化钠固体7.0 g;②用托盘天平称氢氧化钠固体
时,在两盘各放一张质量相等的纸;③选用200 mL量筒量取所需水的体积;④实验中用到的
玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶;⑤用量筒量取水时,俯视读数,配得溶液的溶质质
量分数偏小。
A.①③ B.②③⑤
C.③⑤ D.②④⑤
8.小红同学在一定温度下进行KNO 的溶解实验,实验数据如下:(导学号 58504340)
3
实验序号 实验1 实验2 实验3 实验4
[来源:学科
网]
水的质量/g 100 100 100 100
加入KNO
3
的质量/g 80 100 120 140
溶液质量/g 180 200 210 210
根据上述实验数据,下列叙述正确的是(D)
A.实验1所得溶液的溶质质量分数=×100%
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,KNO 饱和溶液的溶质质量分数=×100%
3
二、填空题(每空2分,共16分)
9.(2017,武汉)R是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所
示。某化学兴趣小组的同学进行了如图2所示实验。
图1
图2(1)t ℃时,氯化铵的溶解度为__40__ g。
1
(2)①的溶液中溶质质量分数为__25%__。
(3)根据以上信息可推出R是__硝酸钾__(填名称或化学式)。
(4)关于图2中烧杯内的物质,以下几种说法正确的有__BC__(填字母)。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
10.(2016,天津)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。(导学号
58504341)
(1)生理盐水是医疗上常用的一种溶液,其溶质是__NaCl__ (填化学式)。
(2)在盛有水的烧杯中加入以下某种物质,形成溶液的过程中温度上升。这种物质是
__C__(填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠
(3)某同学在实验室用氯化钠固体和蒸馏水配制50 g 质量分数为6%的氯化钠溶液时,
涉及以下实验步骤:①溶解;②称量和量取;③计算;④装入试剂瓶贴好标签。配制上述溶液
正确的实验步骤顺序是__③②①④__(填序号)。
(4)某注射用药液的配制方法如下:
①把1.0 g药品溶于水配制成4.0 mL溶液a;
②取0.1 mL溶液a,加水稀释至1.0 mL,得溶液b;
③取0.1 mL溶液b,加水稀释至1.0 mL,得溶液c;
④取0.4 mL溶液c,加水稀释至1.0 mL,得溶液d。
由于在整个配制过程中药液很稀,其密度都可近似看作1 g/cm3。则最终得到的药液(溶
液d)中溶质的质量分数为__0.1%__ 。
三、实验探究题(共8分)
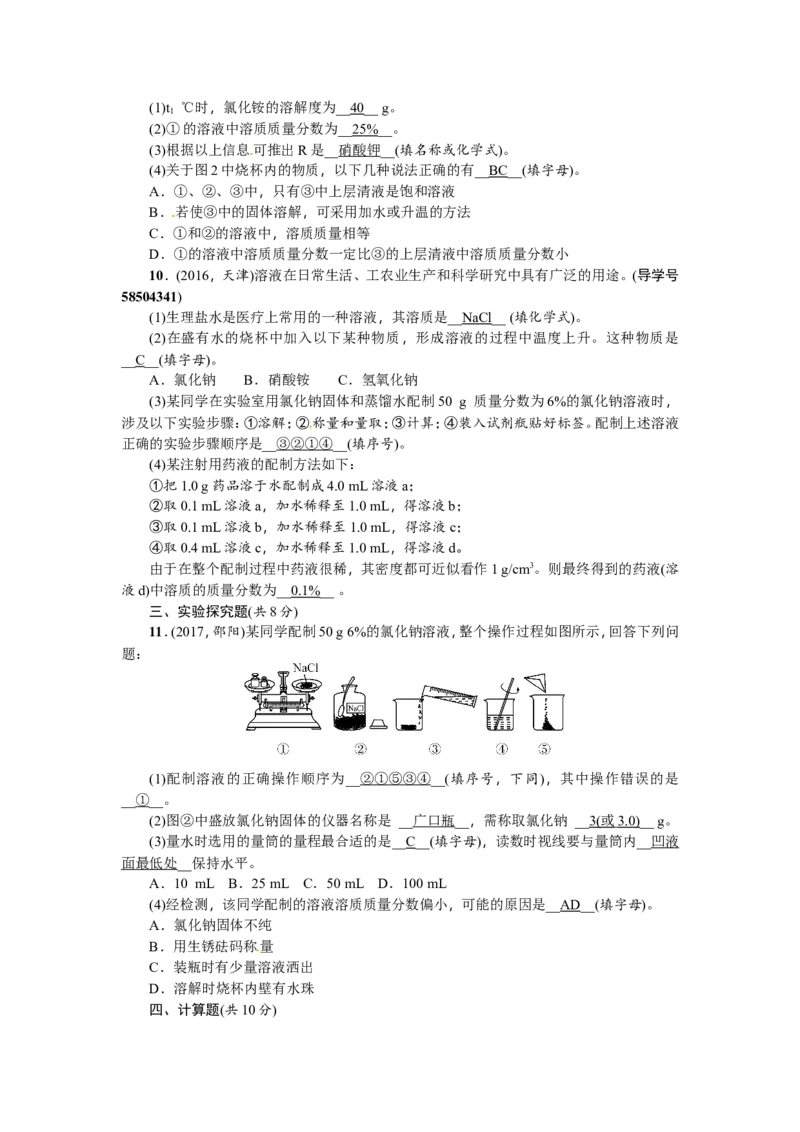
11.(2017,邵阳)某同学配制50 g 6%的氯化钠溶液,整个操作过程如图所示,回答下列问
题:
[来源:Zxxk.Com]
(1)配制溶液的正确操作顺序为__②①⑤③④__(填序号,下同),其中操作错误的是
__①__。
(2)图②中盛放氯化钠固体的仪器名称是 __广口瓶__,需称取氯化钠 __ 3( 或 3.0) __ g。
(3)量水时选用的量筒的量程最合适的是__C__(填字母),读数时视线要与量筒内__凹液
面最低处__保持水平。
A.10 mL B.25 mL C.50 mL D.100 mL
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是__AD__(填字母)。
[来源:Zxxk.Com]
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
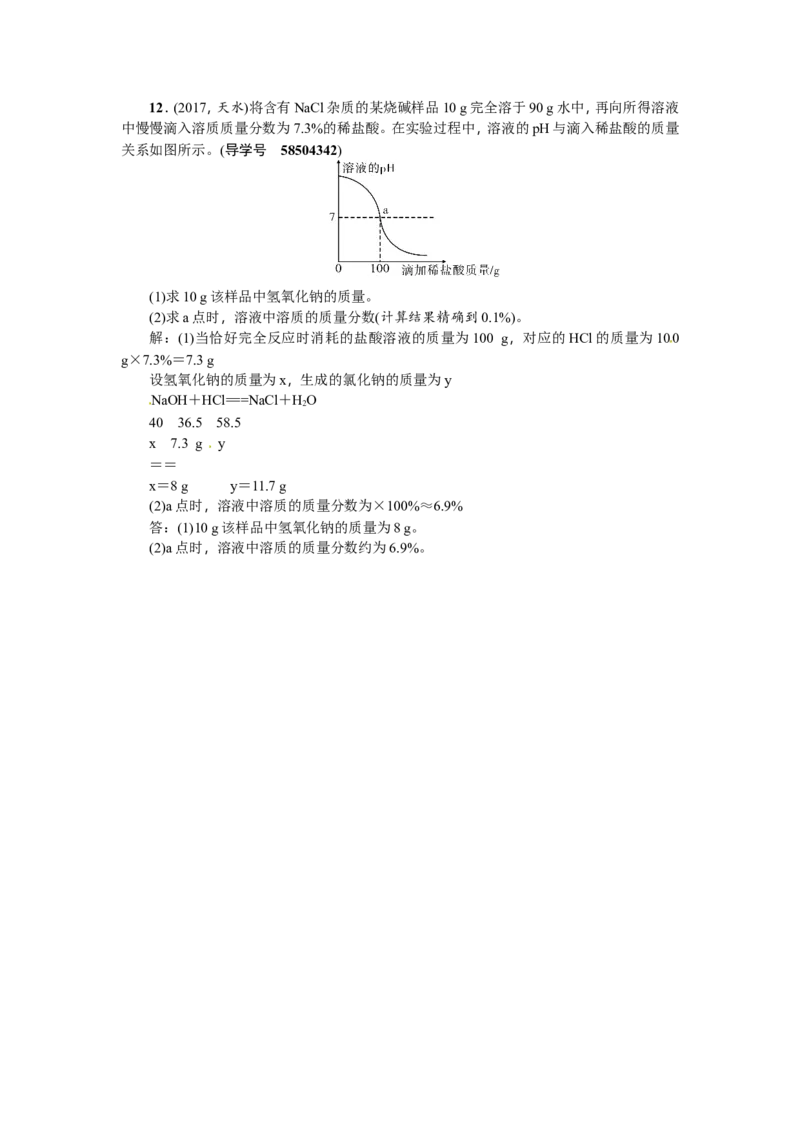
四、计算题(共10分)12.(2017,天水)将含有NaCl杂质的某烧碱样品10 g完全溶于90 g水中,再向所得溶液
中慢慢滴入溶质质量分数为7.3%的稀盐酸。在实验过程中,溶液的pH与滴入稀盐酸的质量
关系如图所示。(导学号 58504342)
(1)求10 g该样品中氢氧化钠的质量。
(2)求a点时,溶液中溶质的质量分数(计算结果精确到0.1%)。
解:(1)当恰好完全反应时消耗的盐酸溶液的质量为100 g,对应的HCl的质量为100
g×7.3%=7.3 g
设氢氧化钠的质量为x,生成的氯化钠的质量为y
NaOH+HCl===NaCl+HO
2
40 36.5 58.5
x 7.3 g y
==
x=8 g y=11.7 g
(2)a点时,溶液中溶质的质量分数为×100%≈6.9%
答:(1)10 g该样品中氢氧化钠的质量为8 g。
(2)a点时,溶液中溶质的质量分数约为6.9%。