文档内容
第4课时 溶液的浓度 溶液的配制
考点1 溶质质量分数的计算
1.某温度下,在100 g质量分数为20%的KNO 不饱和溶液甲中加入10 g KNO 固体,恰好得到饱和溶液乙,下列说
3 3
法正确的是( )
A.该温度下,KNO 的溶解度为 30 g
3
B.乙溶液的质量分数为30%[来源:Z*xx*k.Com]
C.降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
2.把200 g蔗糖溶液完全蒸干后,得到固体50 g,则原溶液中溶质的质量是________,溶剂的质量是________,溶质
的质量分数是________。
考点2 关于溶液稀释的计算[来源:Zxxk.Com]
3.现有100 g溶质质量分数为4.5%的氯化钠溶液,将它稀释成溶质质量分数为0.9%的生理盐水,需加水多少毫升
(水的密度为1 g/cm3)?
[来源:Zxxk.Com]
[来源:学,科,网]
4.100 g质量分数为10%的硝酸钾溶液,若使其质量分数变为20%,则需加入溶质多少克?蒸发溶剂多少克?
考点3 配制一定溶质质量分数的溶液
5.在“配制一定溶质质量分数的氯化钠溶液”实验中,下列操作正确的是( )
图K4-1
A.图甲表示称取7.5 g氯化钠
B.图乙表示量取42.5 mL水
C.图丙表示溶解氯化钠
D.图丁表示向试剂瓶中转移溶液
6.小莉、小晶两位同学用如下两种不同的方法,配制100 g溶质质量分数为5%的氯化钠溶液。
[小莉用固体氯化钠和水配制溶液]
(1)小莉用到的玻璃仪器有量筒、胶头滴管、烧杯、____________和试剂瓶。
(2)小莉实验时应进行的步骤是计算、称量、量取、________、装瓶并贴标签。
[小晶用溶质质量分数为20%的氯化钠溶液加水稀释](3)小晶实验时应量取水的体积是________mL (水的密度可近似看作1 g/cm3)。
(4)若小晶量取水时俯视读数,则所配溶液的溶质质量分数________(填“>”“<”或“=”)5%。
考点4 溶质质量分数与化学方程式相结合的计算
7. B某同学用自制电解器电解水,为了加快电解速率,可在水中加少许硫酸钠增强其导电性,当他在93.6 g质量分
数为5%的硫酸钠溶液中通电一段时间后,正极上产生3.2 g氧气。计算:
(1)负极上产生氢气的质量。
(2)通电后溶液中硫酸钠的质量分数。
(3)该同学认为电解速率较慢,又继续向通电后的溶液中加入硫酸钠,若要使溶液中溶质的质量分数变为10%,则需
要加入硫酸钠固体的质量是多少?
[来源:学+科+网]
1.小朋要配制50 g质量分数为14%的氢氧化钠溶液来制作“叶脉书签”。下列关于配制该溶液的说法不正确的是(
)
①若用氢氧化钠固体配制,需称取氢氧化钠固体7.0 g
②用托盘天平称氢氧化钠固体时,在两盘各放一张质量相等的纸
③选用200 mL量筒量取所需水的体积
④实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
⑤用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小[来源:Z+xx+k.Com]
A.①③ B.②③⑤
C.③⑤ D.②④⑤
2. “配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题。
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体________g。
下列实验操作与目的分析均正确的一组是______(填序号)。
选项 实验操作 目的分析
A 称量时,将取出的过量氯化钠放回原瓶 节约药品
B 溶解氯化钠时用玻璃棒搅拌 增大氯化钠的溶解度
C 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 整洁美观
量取所需水量时,视线与量筒内液体凹液面的最低处保持
D 准确读数
水平
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和
______________。
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图K4-2所示,与丙烧杯中溶液溶质
质量分数一定相同的是______(填序号)烧杯中的溶液。
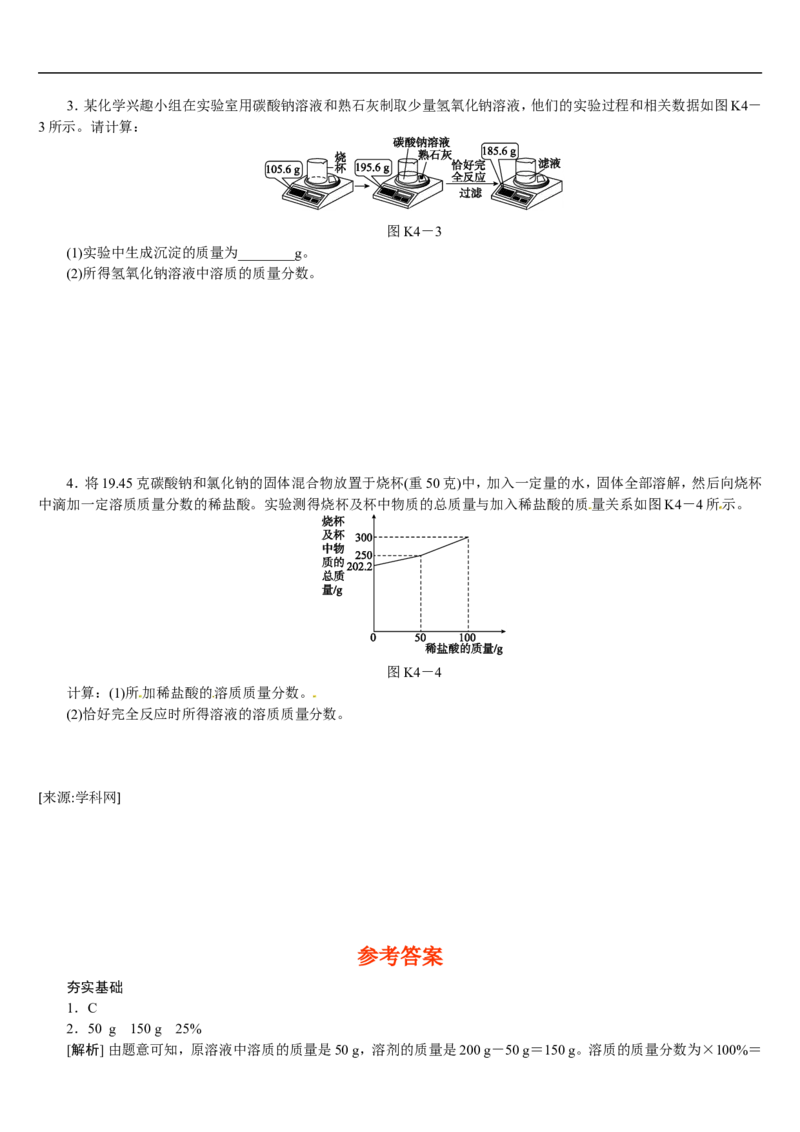
图K4-2[来源:学&科&网Z&X&X&K]3.某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液,他们的实验过程和相关数据如图K4-
3所示。请计算:
图K4-3
(1)实验中生成沉淀的质量为________g。
(2)所得氢氧化钠溶液中溶质的质量分数。
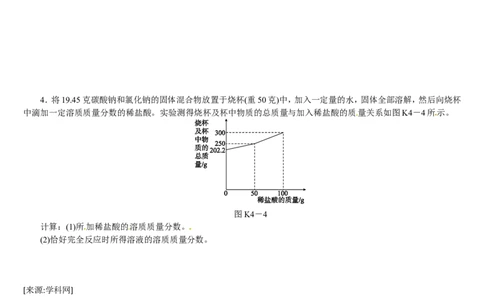
4.将19.45克碳酸钠和氯化钠的固体混合物放置于烧杯(重50克)中,加入一定量的水,固体全部溶解,然后向烧杯
中滴加一定溶质质量分数的稀盐酸。实验测得烧杯及杯中物质的总质量与加入稀盐酸的质量关系如图K4-4所示。
图K4-4
计算:(1)所加稀盐酸的溶质质量分数。
(2)恰好完全反应时所得溶液的溶质质量分数。
[来源:学科网]
参考答案
夯实基础
1.C
2.50 g 150 g 25%
[解析] 由题意可知,原溶液中溶质的质量是50 g,溶剂的质量是200 g-50 g=150 g。溶质的质量分数为×100%=25%。
3.解:设需加水的质量为x。
100 g×4.5%=(100 g+x)×0.9%
x=400 g
V=400 g÷1 g/cm3 =400 cm3=400 mL
答:需加水的体积为400 mL。
4.解:设需加入溶质质量为x,蒸发溶剂质量为y。
100 g×10%+x=(100 g+x)×20% x=12.5 g
100 g×10%=(100 g-y)×20% y=50 g
答:略。
5.C [解析] 托盘天平的使用要遵循“左物右码”的原则,图甲中所示操作砝码与药品位置放反了;量取42.5 mL
水,应使用量筒,不能使用烧杯;向试剂瓶中转移溶液时,瓶塞要倒放,烧杯尖嘴紧挨试剂瓶口。
6.(1)玻璃棒 (2)溶解 (3)75 (4)>
7.解:(1)设生成氢气的质量为x,反应的水的质量为y。
2HO=====2H↑+O↑
2 2 2
36 4 32
y x 3.2 g[来源:Zxxk.Com]
= x=0.4 g
= y=3.6 g
(2)溶液中硫酸钠的质量为93.6 g×5%=4.68 g,
电解后溶液的质量为93.6 g-3.6 g=90 g,
电解后溶液中溶质质量分数为×100%=5.2%。
(3)设需要加入硫酸钠的质量为z。
z+4.68 g=(z+90 g)×10%
z=4.8 g
答:(1)负极上产生氢气的质量是0.4 g;(2)通电后溶液中硫酸钠的质量分数为5.2%;(3)需要加入硫酸钠固体的质量
为4.8 g。
能力提升
1.B
2.(1)4.5 D (2)胶头滴管 (3)丁
[解析] (1)配制500 g溶质质量分数为0.9%的生理盐水,需氯化钠的质量为500 g×0.9%=4.5 g。对化学实验中的剩
余药品,不能放回原瓶,以免污染试剂;溶解氯化钠时用玻璃棒搅拌,可以加速溶解,不能增大氯化钠的溶解度;天平调
平后在左、右托盘中各垫一张相同的纸,并不是为了整洁美观,而是为了避免污染天平。
3.(1)10
(2)解:设生成氢氧化钠的质量为x。
NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
100 80
10 g x
= x=8 g
所得氢氧化钠溶液中溶质的质量分数为
×100%=10%。
答:所得氢氧化钠溶液中溶质的质量分数为10%。
4.解:(1)设参加反应的HCl的质量为x,NaCO 的质量为y,生成的NaCl质量为z。
2 3
生成CO 的质量为 202.2 g+50 g-250 g=2.2 g。
2
NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2106 73 117 44
y x z 2.2 g
=
x=3.65 g
=
y=5.3 g[来源:学科网]
=
z=5.85 g
所加稀盐酸的溶质质量分数为×100%=7.3%。
(2)恰好完全反应时所得溶液的溶质质量分数为×100%=10%。
答:(1)所加稀盐酸的溶质质量分数为7.3%;
(2)恰好完全反应时所得溶液的溶质质量分数为10%。